奥沙利铂联合亚叶酸钙及氟尿嘧啶化疗治疗晚期食管癌临床观察
温永胜
(夏邑县第二人民医院,河南 商丘 476400)
食管癌属于临床常见的恶性肿瘤,由于发病早期无典型的临床特征,确诊时多已处于中晚期,导致患者错过了最佳的治疗时机,因此多以化疗为主[1]。目前,临床对晚期食管癌患者的化疗多采用奥沙利铂、顺铂、亚叶酸钙、氟尿嘧啶等药物,但单一用药疗效不佳,且易复发,还可能引发诸多不良反应[2-3]。本研究采用奥沙利铂联合亚叶酸钙及氟尿嘧啶化疗方案治疗晚期食管癌,临床疗效显著。报告如下。
1 资料与方法
1.1 一般资料
选择我院2016年11月—2018年6月收治的晚期食管癌患者104 例,利用随机数表法分为观察组和对照组,每组52 例。对照组中男28 例,女24 例,年龄42~78 岁。观察组中男30 例,女22 例,年龄43~76 岁。两组一般资料对比差异无统计学意义(P>0.05),有可比性。本研究获院内医学伦理委员会同意。
1.2 纳入及排除标准
纳入标准:均经病理检查确诊为食管癌;病理分期属Ⅲ~Ⅳ期;患者均签署知情同意书。排除标准:合并自身免疫性疾病;合并血液疾病;合并心、肝、肾等功能不全;合并其他恶性肿瘤。
1.3 方法
对照组采用顺铂联合亚叶酸钙及氟尿嘧啶化疗,第1天:将20 mg/m2的顺铂注射液(云南生物谷药业股份有限公司,国药准字H20043889,规格2 mL∶10 mg)溶于500 mL生理盐水中,静脉滴注,滴注时间至少2 h。第1天至第5天:将200 mg/m2的亚叶酸钙注射液(重庆药友制药有限责任公司,国药准字H20010615,规格10 mL∶0.1 g)溶于250 mL生理盐水中,静脉滴注,滴注时间至少2 h,每日1次;静脉滴注750 mg/m2的氟尿嘧啶注射液(天津金耀药业有限公司,国药准字H12020959,规格10 mL∶0.25 g)连续滴注时间6~8 h,每日1次。观察组采用奥沙利铂联合亚叶酸钙及氟尿嘧啶化疗,第1天:将100 mg/m2奥沙利铂(深圳海王药业有限公司,国药准字H20031048,规格20 mL∶40 mg)溶于5%的葡萄糖溶液250 mL中,静脉滴注,滴注时间为2~6 h,3周后重复用药1次;亚叶酸钙与氟尿嘧啶的用法用量与对照组相同。一个周期为3周,两组共治疗2个周期。
1.4 观察指标
测定血清肿瘤标志物水平,包括癌胚抗原(CEA)、糖类抗原19-9(CA19-9)、糖类抗原125(CA125),于化疗前及化疗两个周期后采用电化学发光法测定。记录两组不良反应。
1.5 疗效评定标准
完全缓解:经胃镜检查可见病灶消失,且维持超过4周;部分缓解:经胃镜检查可见病灶缩小超过50%,且维持超过4周;稳定:经胃镜检查可见病灶未增大,无新病灶;进展:出现新病灶[4]。总缓解率=(完全缓解+部分缓解)例数/总例数×100%。
1.6 统计学方法
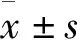
2 结 果
2.1 两组临床疗效比较
观察组总缓解率高于对照组,差异有统计学意义(χ2=4.833,P<0.05)(见表1)。
2.2 两组血清肿瘤标志物水平比较
化疗后,两组CEA,CA19-9及CA125水平均较化疗前降低,且观察组更低,差异均有统计学意义(P<0.05)(见表2)。
2.3 两组不良反应情况比较
观察组不良反应发生率低于对照组,差异有统计学意义(χ2=4.727,P<0.05)(见表3)。

表1 两组临床疗效对比 例(%)
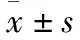
表2 两组血清肿瘤标志物水平对比

表3 两组不良反应情况比较 例(%)
3 讨 论
食管癌属于消化道常见疾病,多发于食管中下段,患者多伴有进行性吞咽障碍。临床上对于食管癌的发病机制尚不明确,多认为与生活不规律、遗传、酗酒等相关[5]。手术是目前临床上治疗早期食管癌的重要方式,但受到食管癌隐匿性特征的影响,患者确诊时多处于中晚期,因此只能通过化疗的方式进行干预。血清肿瘤标志物的变化情况与肿瘤的发生发展密切相关,CEA和CA19-9及CA125均属于常见的血清肿瘤标志物,人体处于正常状态时,组织内血清肿瘤标志物水平均较低,一旦发生肿瘤,其水平迅速升高,且处于较高水平[6]。本研究结果显示,观察组总缓解率高于对照组,血清肿瘤标志物水平低于对照组,表明采用奥沙利铂联合亚叶酸钙及氟尿嘧啶化疗方案治疗晚期食管癌患者,其临床疗效显著,且在调节血清肿瘤标志物水平方面具有重要意义。氟尿嘧啶是一种常用的抗肿瘤药物,具有良好的抗代谢作用,可有效抑制S期细胞,进而抑制胸腺嘧啶核苷酸酶合成,达到阻断肿瘤细胞DNA和RNA合成的效果[7-8]。奥沙利铂属于新型的铂类化疗药,其抗癌机制类似于其他铂类化疗药。它将DNA作为作用靶点,与DNA结合后,形成铂化DNA,进而有效抑制DNA的合成及修复,抑制肿瘤细胞发展,促进肿瘤细胞凋亡[9-10]。氟尿嘧啶与奥沙利铂联合使用可起到协同作用,增强抗癌效果。亚叶酸钙属于还原型衍生物,可增强氟尿嘧啶的抗癌效果,还可减轻患者不良反应[11]。本研究结果显示,观察组不良反应发生率低于对照组,表明此化疗方案治疗晚期食管癌安全可靠。
综上所述,采用奥沙利铂联合亚叶酸钙及氟尿嘧啶化疗方案治疗晚期食管癌患者,临床疗效显著,可有效调节血清肿瘤标志物水平,减少不良反应。

