应用于离子液体体系汽液平衡测定的液相配制、气相分析方法
谭亚龙,舒高翔,崔林芳,章连众
(浙江工业大学化工学院,浙江杭州310006)
引 言
对于汽液平衡测定而言,离子液体体系类似于传统的含盐体系,易过热、爆沸。为了获得平衡气相组成样品,汽液平衡釜通常需要有较大的气相回流。这些是实现配制液相组成的困难所在。关于汽液平衡测定文献中已有全面的讨论[1-5]。Pereiro等[6]综述了离子液体应用于共沸体系分离,涉及多种方法测定众多离子液体体系的汽液平衡数据。具体有顶空法、静态法以及应用较多的循环法。
汽液平衡测定的物理量包括温度(T)、压力(p),以及气、液相组成(x、y)。通常,顶空法[7-13]测定Txy数据,静态法[14-16]测定Tpx数据。循环法可以同时测定Tpxy数据[17-25],其中拟静态法一般测定Tpx数据[26-29]。一般而言,顶空法、静态法和拟静态法比较容易实现液相配制。本课题组采用基于气液双循环的液相配制、气相分析方法[30-32],基本思路来源于韩世钧先生研究团队发展的汽液平衡测定的拟静态法[3]和置换法[4],以及能够主动提供气化中心的沸腾器结构[5]。该方法的特点是液相配制并且同时测定Tpxy数据,因此能够避免较为烦琐的含离子液体液相的分析,能够不依赖活度系数模型获得挥发性组分的活度系数。
基于课题组前期工作[30-35],本文讨论实现液相配制、气相采样分析汽液平衡釜的基本特征,并提出改进的气相回流器和沸腾器结构。对于含任意挥发性组分和非挥发性组分体系,提出了液相组成计算方法和误差估计。面向萃取精馏应用,讨论了连续配制方法。
1 汽液平衡釜
如图1 所示,汽液平衡釜的沸腾器具有夹套结构,能够主动提供气化中心;泵式磁力搅拌提供强制液相循环;填料柱提供气液接触界面和停留时间以消除过热。三方面综合的结果保证了沸腾器稳定运行。通常,平衡温度在30 min 内波动不大于0.01 K。尤其重要的是,液相回流能够独立于气相回流。液相回流量由磁力搅拌转速调节,通常大于500 cm3/min;而气相回流量则由沸腾器加热量调节,通常稳定在2 cm3/min。气相物料离开平衡室后立即冷凝,并聚集于溢流式气相样品池。
其中,改进的气相回流器采用变径结构并增加一个球泡,有利于气相逐滴稳定回流;气液相在沸腾器底部回流,有利于釜内快速达到平衡。

图1 具有液相配制、气相采样分析特征的汽液平衡釜Fig.1 Vapor-liquid equilibrium still featuring synthetic liquid phase composition and vapor phase sampling and analysis
2 液相组成计算方法
如图2 所示,通常将汽液平衡釜中物料归类为总体、液相和气相三种。三者的总和即配制物料。首先考虑平衡釜内静态物料衡算。从平衡釜结构来看,液相物料量占比很小,组成非常接近总体物料。因此,在静态物料衡算中将液相物料并入总体物料。据此,总体物料中任意组分i的质量m是其在配制物料中的质量减去其在气相物料中的质量,即

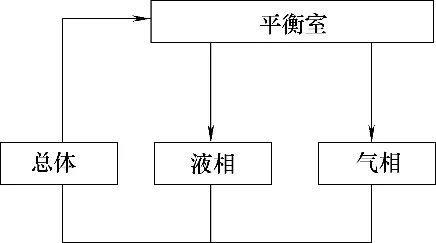
图2 双循环汽液平衡釜物料的总体、液相和气相分布Fig.2 Distribution of materials of bulk,liquid and vapor phase in a double-circulation vapor-liquid equilibrium still
其中,下标b、s、v 分别表示总体、配制和气相。对于离子液体,其在气相物料中的质量为零。对于挥发性组分,其在气相物料中的质量由气相滞留体积、气相密度和气相组成计算。气相组成由分析获得,气相密度根据气相组成估算。滞留体积包括气相样品池中样品滞留体积(2.5 cm3)和管壁样品滞留体积(估计为0.2 cm3)。根据各组分在总体物料中质量可以计算各组分的质量分数。
进一步,依据动态物料衡算计算各组分液相质量分数

其中,w为质量分数,ṁ为质量流量,下标l表示液相。定义

则

根据气相和液相回流量并考虑到气液两相密度差异,通常将β估计为0.003。式(3)~式(5)适用于任意体系的挥发性或非挥发性组分。对于离子液体,Ki=0。
最后,由各组分质量分数可以方便地计算摩尔分数,并进一步计算各组分活度系数。
由式(5)计算各组分液相组成,其相对误差为

显然,误差由两项组成。第一项是总体物料中各组分质量分数的相对误差,主要来源于加料过程中特别是含量较低组分的挥发,以及管壁样品滞留体积的估计误差。考虑到平衡釜容量为270 cm3,而且含量较低挥发性组分会最后加入以避免挥发损失,这部分误差通常并不显著。第二项来源于β值的估计误差,并且与Ki有关。如果β值的误差是0.001,Ki=3,则该项相对误差贡献为0.002,对应于组分质量分数的相对误差是0.2%,或者组分活度系数的相对误差也是0.2%。
3 连续配制方法与应用
通过置换沸腾器内物料,将一部分含有离子液体的物料置换为体积相当、不含离子液体且挥发性组分比例相同的物料,可以连续测定挥发性组分比例保持不变、离子液体含量不同的一系列数据。图3 给出了水(1) + 乙醇(2) + [bmim]BF4(3)[33]和水(1) +乙腈(2)+[bmim]BF4(3)不同[bmim]BF4质量分数w3下的泡点温度T[图3(a)]和气相组成y2[图3(b)]。实验测定在p=100 kPa 下进行,沸腾器物料定量置换使得水(1)+乙醇/乙腈(2)拟二元体系中水的摩尔分数x΄1保持在0.050基本不变。
上述体系的液相组成由x΄1和w3描述。现在分析液相组成的计算误差。依据式(6),分为2 个部分。
(1)考虑β取值对应的误差。对于含乙醇体系,K1值随着离子液体浓度下降从9减小到3;对于含乙腈体系,K1值则从4 减小到1。如果β值的误差是0.001,对应的x΄1相对误差小于1%。对离子液体,Ki=0,w3的相对误差是0.1%。
(2)考虑总体物料组成的计算误差。计算表明,如果气相滞留体积误差为0.2 cm3,则wb,3和x΄b,1的相对误差均小于0.1%。应该指出,连续置换过程中总体物料组成的计算误差是累积的,而β取值对应的误差不会累积。对应于270 cm3的总物料,如果置换其中的27 cm3,则wb,3和x΄b,1的相对误差将由0.001累积至0.001×(1+27/270)=0.0011。如果置换量为81 cm3,则新的误差是0.0013。据此,上述体系最后实验点的wb,3和x΄b,1的相对误差小于0.4%。
上述有规律的实验安排有利于讨论[bmim]BF4对水+乙醇和水+乙腈汽液平衡行为的影响。图3(c)给出了乙醇或乙腈对水的相对挥发度α21随w3变化的趋势。离子液体的加入能够明显提高相对挥发度,但两个体系破除共沸所需离子液体质量分数有着明显差异。为了探究更深层次的原因,图3(d)、(e)分别给出了水的活度系数γ1,以及乙醇或乙腈的活度系数γ2与w3的关系。基于气相是理想气体这一假设,相对挥发度与活度系数的关系是


图3 水(1)+乙醇(2)+[bmim]BF4(3)和水(1)+乙腈(2)+[bmim]BF4(3)汽液平衡行为的比较(p=100 kPa;x΄1=0.050)Fig.3 Comparison of vapor-liquid equilibrium behavior of water(1)+ethanol(2)+[bmim]BF4(3)and water(1)+acetonitrile(2)+[bmim]BF4(3)(p=100 kPa;x΄1=0.050)
4 结 论
液相配制、气相分析方法应用于测定离子液体体系汽液平衡,能够避免较为繁琐的含离子液体液相的分析,能够不依赖活度系数模型获得挥发性组分的活度系数。通过连续置换配制,可以实测获得挥发性组分的活度系数,揭示活度系数随组成的变化规律,并应用于萃取精馏溶剂性能的评价及筛选。改进的气相回流器和沸腾器结构,有利于气相逐滴稳定回流,有利于釜内快速达到平衡。本文提出的液相组成计算方法和误差估计适用于任意体系的任意组分。
符 号 说 明
Ki——组分i的气相和总体质量分数比值
mb,i,ms,i,mv,i——组分i的总体、配制和气相质量,g
pisat——组分i的饱和蒸气压
wb,i,wl,i,wv,i——组分i的总体、液相和气相质量分数
wi——组分i的质量分数
x'i——不考虑离子液体存在时拟二元体系组分i的摩尔分数
yi——组分i的气相摩尔分数
αij——组分i对组分j的相对挥发度
β——气相和液相质量流量比值
γi——组分i的活度系数
下角标
b,s,v——总体、配制和气相
i,j——组分i,j

