低共熔溶剂在电池和电催化中的应用
陈钰,牟天成
(1 廊坊师范学院化学与材料科学学院,河北廊坊065000; 2 中国人民大学化学系,北京100872)
引 言
随着世界能源格局的改变和人们对环境的要求越来越高,对新能源的需求日益增加。相比于传统能源,新能源更加高效、绿色和经济。锂离子电池、太阳能电池和燃料电池等是重要的新能源[1-3]。电催化反应如析氢反应(hydrogen evolution reaction,HER)、析氧反应(oxygen evolution reaction, OER)、氧气还原反应(oxygen reduction reaction, ORR)也是获取新能源的关键[4-6]。在电池和电催化反应中离不开电解质和电极材料[4],良好的电解质和电极材料是提高电池和电催化反应效率的关键。绿色化学的核心之一即溶剂绿色、合成过程绿色和低成本[7]。因此,电池中的电解质和合成电极材料所需的溶剂除了满足一定的效率外还必须环境友好。所以,实现绿色能源和绿色电催化反应的关键之一在于设计环境友好的电解质和溶剂[8]。
传统有机溶剂毒性大、容易挥发且容易燃烧,不利于实现电池和电催化反应的绿色化。常规的绿色溶剂包括水、超临界二氧化碳(CO2)、离子液体等[7,9]。超临界CO2的电导率极低,水的电化学窗口窄,所以并不适用于作电池和电催化反应的电解质。离子液体是由有机阳离子和有机或无机阴离子组成,在室温附近或低于100℃时呈液态。离子液体的可设计性使得它在许多领域得到应用[10]。另外,离子液体含有大量的离子键使得其电导率比较大,从而适用于电池和电催化反应的电解质[11-12]。但是,离子液体的不稳定性[13-15]、挥发性[13]、吸湿性[16]、生物毒性、合成复杂及成本高等缺点妨碍其在电池和电催化反应中的大规模应用。所以,新型绿色溶剂和绿色电解质的设计与开发显得十分必要。
低共熔溶剂(deep eutectic solvents, DESs)由氢键供体(一般为离子化合物,如氯化胆碱、溴化胆碱、甜菜碱)和氢键受体(分子化合物,如乙二醇、甘油、氨基酸、乙酰胺、尿素)通过较强的氢键相互作用力而形成[17-19],其熔点比其合成原料的熔点都要低,从而能在室温附近呈液体状态。常规的DESs由两个组分组成,特殊情况下可包含三元组分及更多组分。分子和分子通过卤键、pi-pi 相互作用、硫键等其他类型的非共价相互作用也可以形成低共熔物,将其命名为共熔分子液体(eutectic molecular liquids,EMLs)[20]。通过对组分数及相互作用力类型的调控可以实现DESs 和EMLs 的高度可设计性。另外,DESs 具有合成简便、价格低廉、稳定性高、纯度可靠、能导电等优点。从而,DESs 在气体捕集与转化[21-22]、分离萃取[23-24]、生物质利用[25-26]、电沉积[27]、电池、电催化等领域有着十分广泛的应用,DESs 也被认为是离子液体的替代物[28]。
特别地,DESs在电池和电催化反应领域显示出巨大潜力。由于DESs能导电,所以能作为电池的电解质[29]。DESs 的高调控性更加有利于设计DESs 半凝胶或凝胶用于高效固态和半固态电池[30]。DESs对固体物质的高溶解性使得DESs 成为合成电极材料的优良溶剂[31],且所得材料具有某些特殊的结构和性质,从而对电催化反应显示较高的电流效率。DESs还能增加其与界面之间的相互作用力、吸附底物并活化底物、降低电催化能垒、增加电子的传输速率,进而提高电催化的效率和选择性[32]。另外,DESs 对电极材料中的某些成分具有特殊的相互作用力,使得DESs能高效率地提取电极材料中的某些重要物质[33]。
虽然DESs 在其他领域有很多综述发表[26,34-36],但是,DESs在电池和电催化反应领域现在还处于起步阶段,未见有综述系统介绍。为系统介绍DESs在电池和电催化反应领域中的作用,有必要对DESs在各类电池、各类电催化反应及其机理研究加以总结。本综述内容包括(1)DESs作为电池和电催化反应的绿色电解质;(2)DESs 在电池和电催化反应的相关机理、化工过程及热力学;(3)DESs作为电池和电催化反应电极材料的溶剂;(4)DESs 作为回收电极材料的绿色溶剂;(5)展望及相关问题。其目的旨在探究DESs 促进电池效率和电催化反应的内在机制、DESs 作为电解质的相关机理,进而为设计新型的DESs 用于更加高效绿色的电池和电催化提供科学指引。
1 DESs作为电解质
1.1 锂离子电池
锂离子电池是一种需求日益增加的可持续储能设备,其应用范围十分广泛。电解质是锂离子电池的核心之一。由于锂离子电池要求电解质中含有锂离子,所以设计DESs时均把含有锂盐的组分引入到DESs中。一般有两种引入方法:作为添加剂引入[37-39]、作为DESs的一个组分引入[29,40-46]。文献[29,40-46]表明,在大多数情况下都是把锂盐作为DESs的一个组分。另外,安全绿色高效的锂离子电池对其电解质有着很高的要求,如电导率高、电稳定性好、热稳定性好、不易燃、成本低、合成简易。含锂DESs作为锂离子电池的物理化学性质研究十分重要。
Pandey 课题组[37]研究温度和氯化锂(LiCl)浓度对氯化胆碱∶尿素型(ChCl∶urea,1∶2 摩尔比)DESs密度和黏度的影响。温度和LiCl 浓度的范围分别是30~85℃和0~2.1 mol·kg-1。结果表明ChCl∶urea的密度随着温度的升高而线性降低;ChCl∶urea的密度随LiCl 浓度的升高而线性升高。但是,ChCl∶urea的黏度变化与温度、LiCl 浓度的关系却与之不同。具体来说,LiCl+ChCl∶urea 体系的黏度与温度的关系可以用Arrhenius 表达式来描述;ChCl∶urea 的黏度随着LiCl 的增加而呈指数增加(指数增加的幅度在低温下更为明显)[37]。LiCl 添加在DESs 中的物理化学性质变化规律比其添加在离子液体中的相应规律要简单得多[37]。
利用多维探针芘,Pandey 等[38]还发现温度(30~85℃)的升高能降低ChCl∶urea(1∶2)的偶极性。但是,如果在ChCl∶urea 中加入LiCl 成分,温度升高对ChCl∶urea 偶极性降低的程度影响不显著[38]。衰减时间分为两种:短衰减时间和长衰减时间(τ)。温度对短衰减时间影响并不显著,但是对τ的影响却十分显著。具体来说,无论LiCl 的浓度多少,升高温度都会减少τ。特别地,当LiCl 的浓度为0.832 mol·kg-1时,温度对τ的降低效应最为显著;增加或降低LiCl 的浓度都会单调地减少τ[图1(a)]。LiCl 的浓度对τ的影响也十分显著:在所研究的温度范围内升高LiCl 的浓度都会降低τ的数值,当温度为30℃时τ随浓度升高而降低的速率最大[图1(b)]。Pandey 等[38]把原因归属为LiCl中氯离子能促进芘中激发态电子的非辐射跃迁路径。

图1 LiCl+ChCl:urea体系衰减时间τ随温度的变化(a)及ChCl:urea体系衰减时间τ随LiCl浓度的变化(b)[38]Fig.1 Effect of temperature on decay time τ of LiCl+ChCl:urea system(a),and effect of concentration of LiCl on decay time τ of ChCl:urea(b)[38]
由于离子传输性质对锂离子电池电解质的重要性,Mustarelli 等[39]研究六氟磷酸锂(LiPF6)和双三氟甲基磺酰亚胺锂(LiTFSI)两种锂盐对氯化胆碱∶乙二醇(ChCl∶EG,1∶3)、氯化胆碱∶乳酸(ChCl∶LA,1∶2)电导率和黏度的影响。黏度的顺序可列为:ChCl∶EG <ChCl∶LA、LiPF6<LiTFSI、0.5 mol·L-1<1 mol·L-1。Walden 图是研究液体的离子传输性质的重要手段之一,其对液体离子传输特性可分成以下几类:good liquids(十分接近对角线)、poor liquids(对角线下面)、super liquids(对角线上面)[47]。Mustarelli 等[39]发现在对角线下面的ChCl∶LA+锂盐属于poor liquids,而接近对角线或在对角线上面的ChCl∶EG+锂盐属于good liquids 甚至super liquids。最好的液体是0.5 mol·L-1ChCl∶EG LiPF6,在室温下其电导率值高达7.95 mS·cm-1[39],所以被认为是一种有潜力的绿色电解质。

Biswas 等[46]研究乙酰胺和乙酰胺+锂盐型DESs的介电弛豫谱。锂盐类型包括溴化锂(LiBr)、硝酸锂(LiNO3)、高氯酸锂(LiClO4);DESs 中乙酰胺与锂盐的摩尔比为4∶1。结果表明乙酰胺+锂盐型DESs的静电介电系数比纯乙酰胺的静电介电系数至多能低4/5,可能的原因是纯乙酰胺分子之间的相互作用力比较大会固定住其移动。乙酰胺+锂盐型DESs的水动力学有效旋转体积也大大低于纯乙酰胺的水动力学有效旋转体积,Biswas 等[46]把原因归结为乙酰胺分子的旋转跳跃。另外,含锂DESs中阴离子类型对介电弛豫谱中的实部(ε')和虚部(ε″)都有比较明显的影响,上述两者的大小顺序都可列为ClO4>Br >NO3(图2)[46]。对于乙酰胺+锂盐型DESs体系,Shirota 等[45]用飞秒拉曼感生克尔效应光谱发现阳离子比阴离子对DESs的微结构影响更大。
实际需求中,锂离子电池常常暴露在低温环境中。能在低温下运行良好的锂离子电池关键在于设计其他性质良好且熔点很低的电解质。Anouti等[41]发现N-甲基乙酰胺(N-methylacetamide,NMA)与锂盐组成的DESs 即是这种良好的锂离子电池电解质。NMA 型DESs 的黏度比较低,如NMA∶LiTFSI,NMA∶LiNO3在25℃的黏度分别为78.38,107.19 mPa·s。NMA 型DESs 的 电 导 率 较 好,如NMA∶LiTFSI,NMA∶LiNO3,NMA∶LiPF6在25℃的电导率分别为1.35,0.76,1.41 mS·cm-1。温度对NMA型DESs 的电导率影响也十分显著,在20~80℃温度范围内,电导率的顺序为NMA∶LiPF6>NMA∶LiTFSI >NMA∶LiNO3;而且在高温区间内电导率的差异更加明显(图3)。不仅如此,NMA 型DESs的熔点也非常低。由图4可以看出,NMA∶LiTFSI的熔点最低可达-72℃,对应的摩尔比为4∶1。熔点大小的次序为:NMA∶LiTFSI <NMA∶LiNO3<NMA∶LiPF6。综合电导率、黏度、熔点等参数可以认为NMA:LiTFSI 更适合作锂电池电解质。NMA 型DESs 的电化学稳定性也比较强,其电化学窗口在4.7~5 V 的区间范围内。以上述含锂DESs 作锂离子电池的电解 质 可 以 得 到160 mA·h·g-1的 容 量 和99% 的效率[41]。
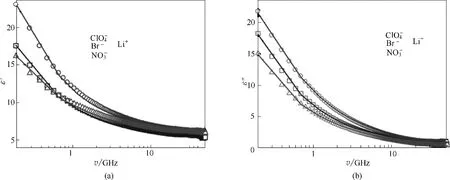
图2 锂盐阴离子对乙酰胺+锂盐型DESs介电弛豫谱中实部(ε')与虚部(ε″)的影响[46]Fig.2 Effect of anion in DESs acetamide:lithium salts on real parts(ε')and imaginary parts(ε″)of measured dielectric relaxation spectra[46]

图3 温度对NMA型DESs电导率的影响[41]Fig.3 Effect of temperature on conductivity of NMA-based DESs[41]
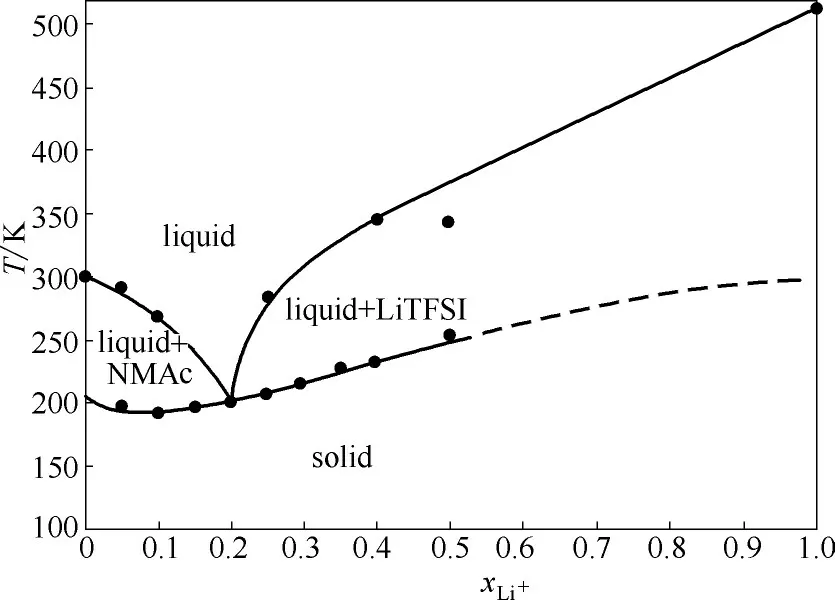
图4 NMA∶LiTFSI型DESs的固液平衡相图[41]Fig.4 Solid-liquid phase diagram of NMA∶LiTFSI[41]
以往报道的基于离子液体(如[Pyrr][NO3])与碳酸丙烯酯混合物的电解质的类别均属于poor liquids,而且随着离子液体浓度的升高电解质体系从poor liquids 向good liquids 靠 近[48]。但 是,Anouti等[42]发现DES NMA∶LiTFSI 属于super liquids 级别,比基于离子液体体系的电解质的级别要高许多。这说明DESs 是一种比离子液体更为优良的锂离子电解质[42]。另外,Anouti 等[42]还研究NMA∶LiTFSI 类DES的挥发性。结果表明NMA∶LiTFSI(4∶1)在40℃时的蒸气压为20 Pa,低于相同条件下原料乙酰胺(50 Pa)和有机溶剂(如水10200 Pa,乙腈73800 Pa)的蒸气压,但是却高于离子液体(如[EMIM][TFSI])的蒸气压。由此可见挥发性顺序大概可列为:常规有机溶剂>DESs >离子液体。
1.2 铝电池
虽然锂离子电池是成功的储能方法,但是依旧有高成本、安全性和能量密度不够高、对空气敏感等问题。铝是地球上元素含量最多的金属,而且具有成本低、传输电子数目多、安全性高、循环性好等优点,所以铝电池很具潜力。Mori[30]报道了基于DESs 的全固态铝空气电池,其中铝作负极,氮化钛作正极,DESs 作全固态电解质。DESs 的组成是氯化铝(AlCl3)、尿素、羧甲基纤维素和甘油(摩尔比为3:2:1:1)。以DESs 为铝空电池的电解质,在正极和负极都检测不到含铝副产物[如Al(OH)3和Al2O3]的生成且具有较高的电池容量(35.0 mA·h·g-1)。在0.1 mA·cm-2的电流密度下,电池的电压在0.2~1.5 V的范围内;第一次循环电池容量是35.8 mA·h·g-1,50次充放电后电池容量几乎不变[30](图5)。

图5 基于DESs型全固态铝空电池的充放电曲线[30]Fig.5 Charge-discharge curve of Al-air battery with DESsbased all solid state electrotype[30]
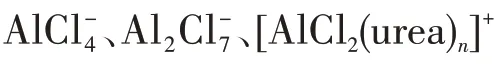
1.3 锌电池
水系锌电池的主要问题在于析氢、锌电极钝化及枝晶生成。研究开发出新型的电解质是一种解决上述问题的方法。目前有两种研究思路:无水DESs 和含水DESs。Kheawhom 等[51]用ChCl∶urea(1∶2)+0.3 mol·L-1ZnCl2作无水电解质则改善了以上的几个缺陷(金属锌为负极、二氧化锰MnO2为正极)。结果发现此锌电池没有检测到枝晶、金属钝化层。这是因为含锌离子能循环地在ChCl∶urea+0.3 mol·L-1ZnCl2型电解质和MnO2电极中可逆地嵌入脱嵌。以ChCl∶urea+0.3 mol·L-1ZnCl2为电解质的锌电池的比容量能高达170 mA·g-1且循环性能较强[51]。Kheawhom 等[51]解释其机理为:放电时金属锌在负极氧化成锌离子;锌离子与DESs电解质中的氯离子结合生成[ZnCl4]2-;[ZnCl4]2-迁移到正极并嵌入到MnO2正极中形成ZnxMnO2。充电时则相反,从正极ZnxMnO2脱嵌的锌离子与电解质形成[ZnCl4]2-迁移到负极上且还原成金属锌。
Cui 等[52]则报道含水DESs 作电解质时的锌电池。他们筛选出urea∶LiTFSI∶Zn(TFSI)2+水(水的摩尔分数为30%)体系作为电解质。DESs的原料均是固体,但由原料组成的二元L-DESs[不含Zn(TFSI)2]和三元LZ-DES[含Zn(TFSI)2]在室温下均呈现液态。组分之间的低共熔现象使得LZ-DES 蒸气压只有水蒸气压的四分之一。随着温度的升高LZ-DES 和LZ-DES+水体系的电导率均降低。增加水的含量能增加LZ-DES 的电导率,但是减少其黏度和熔点。水与urea∶LiTFSI∶Zn(TFSI)2形成很强的氢键网络相互作用力,从而能抑制水在锌电极上的析氢反应;而且由拉曼光谱还发现水浓度较低时LZ-DES 的结构保持得比较完整[52]。所组装的锌电池在0.1 C 300个循环后的可充电效率可达90%,放电电压可达1.92 V,实际能量密度高达52 W·h·kg-1(2 A·h,约9.8倍锌电极量)[52]。
1.4 太阳能电池
染料敏化电池比常规光伏电池的优点在于高效、低成本。但是,染料敏化电池中挥发且有毒的有机电解质大大限制其广泛使用。Tran 等[32]设计了11 种DESs 用于从电解质角度改善染料敏化电池的长期使用效率。结果表明在DESs+乙腈的电解质体系中染料敏化电池能得到比较稳定的效果,原因在于DESs 与二氧化钛表面的强烈相互作用力[32]。但是上述电解质体系仍然涉及到有机溶剂的使用,所以不含有机溶剂电解质体系的使用更具挑战性。Abbotto 等[53]使用氯化胆碱∶甘油(ChCl∶glycerol,1∶2)+水为电解质发现染料敏化电池的能量转化效率与有毒且挥发性大的有机电解质具有相似的效果。Wang 等[54]报道染料敏化电池在碘化胆碱∶甘油(ChI∶glycerol,1∶3)+水体系中也能有较好的电池参数。
1.5 液流电池
含水电解质体系的氧化还原液流电池不仅降低氧化还原离子的稳定性,而且不利于氧化还原离子在电解质的溶解。Yang 等[55]开发非水的DES 电解质ChCl∶urea(1∶2)与相同条件下水系电解质体系相比有以下几个优点:比容量多54.6%、容量保持能力更强、热稳定性更高。原因是ChCl∶urea 不含水且钒离子和铁离子在ChCl∶urea 中的溶解度比在水中的高[55]。但是,DES 电解质的缺点之一在于其较高的黏度和较低的扩散系数。解决的方法之一是升高体系的温度。他们发现升高温度不仅能增加氯化铁FeCl3和氯化钒VCl3在DES中的溶解度,而且能够大大地降低电解质的黏度和电阻[55]。从室温(约22℃)升高到50℃,体系的电阻能降低至1/3,FeCl3+ChCl:urea 和VCl3+ChCl:urea 体系的黏度也能分别降低至约1/2和1/3[55]。
除升高温度,在DESs中添加气体成分也是降低DESs 黏度、增加DESs 电导率的方法之一。液流电池DES(ChCl∶urea,1∶2)电解质中可引入CO2气体添加剂[56]。结果表明在室温条件下通入CO2至饱和后DES 的黏度和电阻分别降低10%和24%;升高温度时由于CO2在DES 溶解度的降低则会使黏度和电阻的降低程度减少[56]。添加CO2能够降低DESs 黏度、增加DESs 电导率的原因在于DESs 与CO2之间的强相互作用力[57]。其他气体,如氨气(NH3)[21]、二氧化硫[58]也能使DESs 的黏度降低、电导率增加。需要注意的问题在于气体的泄漏和气体的电化学还原,比如文献中有许多关于CO2电还原的报道[10,59-62]。同时实现CO2电还原和液流电池的高效利用可能是一个能源高效利用的方略。
铁-铝杂化液流电池由于铁和铝的廉价、含量丰富,从而具有高理论容量和强大应用前景。铁-铝杂化液流电池中铝作负极、铁作正极、AlCl3∶urea作负极电解质、FeCl3·6H2O∶urea∶glycol(FeCl3·6H2O代表六水氯化铁,glycol 代表乙二醇)作正极电解质[63]。不过,单纯DESs 作电解质的黏度较高,电导率较低,所以为改善液流电池的效率仍旧往电解质中掺入有机溶剂,如二氯乙烷、碳酸二甲酯[63]。ChCl∶glycol(1∶2)+1 mol·L-1CuCl2为电解质的全铜杂化液流电池则可达到94%的库仑效率和不低于0.75 V的电池电动势[64]。
1.6 超级电容器
超级电容器即电化学双层电容,是一种高能量密度和能长期使用的储能设备。在高温下也能长期高效使用的超级电容器是当今科学界和工业界的一个挑战,其关键在于设计高温下稳定且高效的电解质。Sawangphruk 等[65]用四丙基溴化氨∶乙二醇(TPAB∶glycol,摩尔比为1∶3、1∶4、1∶5)作为超级电容器的电解质,结果发现此超级电容器能在115℃的温度下长期使用,比文献报道的80℃要高35℃。而且,Sawangphruk 等[65]所设计的超级电容器不含氟元素,比容量随着温度的升高而增加,到115℃时能高达172 F·g-1。聚乙烯醇∶乙酰胺∶高氯酸锂(PVA∶acetamide∶LiClO4)型DESs 凝胶电解质能用于可穿戴超级电容器中,得到约4.2 V 的电压和245 W·h·kg-1的能量密度,而且循环使用6000 次后其稳定性基本不发生改变,电容保持率也能高达91.5%[66]。DESs 凝胶电解质还可以通过DESs(如ChCl∶glycol,1∶2)负载到聚合物上以增加超级电容器的绿色性和效率[67]。
水的电解是超级电容器的副反应。质子性DESs 电解质(LiTFSI∶甲酰胺,1∶4)会使超级电容器在工作时有25%的电荷用于氢气释放,但是气体析出的反应电化学可逆仍可使超级电容器有比较好的能量密度[68]。含钠DESs 电解质(NaNO3∶NMA,1∶9)也能促进超级电容器的效率,开路电压能达到2.0 V 且能在较高的温度80℃下使用[69]。Anouti 等[44]以LiNO3∶NMA (1∶4)和LiTFSI∶NMA (1∶4)作为超级电容器的电解质测试电化学阻抗谱发现一些有趣的结果。当电压差区间ΔE>2 V 时,LiTFSI∶NMA出现两对可逆峰(1)/(1)'和(2)/(2)',意味着锂离子的嵌入脱嵌;但是当ΔE= 1.8 V 时则不出现此锂离子嵌入脱嵌的峰[图6(a)]。在ΔE=2.6 V 时比电容可高达380 F·g-1,此数值与相同条件下水体系电解质和有机电解质的数值比较相似[图6(b)][44]。在循环前LiTFSI∶NMA(6 Ω)的 等 效 系 列 电 阻(ESR,equivalent series resistance)小于LiNO3∶NMA(9 Ω),LiTFSI∶NMA 与LiNO3∶NMA 的等效扩散电阻(EDR,equivalent diffusion resistance)却差不多[图7(a)]。但是,在循环后LiTFSI∶NMA 与LiNO3∶NMA 的ESR 和EDR 都有相应的增大,这意味着阴离子嵌入电极材料的孔道增大相应电阻的数值[44][图7(b)]。LiTFSI:NMA 比LiNO3:NMA 的EDR 要大,原因可能归结为TFSI 阴离子的体积比NO3阴离子的体积大不利于LiTFSI:NMA的扩散[44]。
1.7 CO2电还原
CO2的高效电还原需要合适的电解质。离子液体是最近报道CO2电催化还原的高效电解质[10,62]。与离子液体相比,DESs 有低成本、高降解性、无毒、合成简便等优点,所以DESs 是CO2电催化还原的优良电解质。Dyson 等[70]首次报道DES 作为CO2电还原的电解质,结果表明CO2电还原成CO 的法拉第效率 顺 序 为:[BMIM][Cl]:glycol(1∶2,95.8%)>ChCl∶glycol(1∶2,78.0%)>ChCl:urea(1∶2,59.0%)+15%(体积)水>ChCl∶urea(1∶2,15.8%),[BMIM][Cl]为1-丁基-3-甲基咪唑氯盐。ChCl∶urea的黏度比较大从而法拉第效率只有15.8%,加入水或换成低黏度的ChCl∶glycol 都使得法拉第效率大大提高。但是,水的含量也不能太高,如果水的浓度过高会使得析氢反应大大增加,如1 mol·L-1ChCl∶glycol(在水中)的CO 生成法拉第效率只有23.3%,比在纯ChCl∶glycol中降低了2/3以上[70]。设计在室温条件下黏度低、电导率高、电化学稳定性强、CO2溶解度大且活化CO2程度高的新型DESs 是改善CO2在DESs 电解质中电还原效率和选择性的一种可能方略。

图6 三电极体系5 mV·s-1扫描速率时LiTFSI∶NMA(1∶4)的循环伏安图(a)及ΔE=2.6 V时相应的比电容(b)[44]Fig.6 Cyclic voltammogram of LiTFSI∶NMA(1∶4)at 5 mV·s-1 in three-electrode system(a)and corresponding specific capacity at ΔE=2.6 V[44]
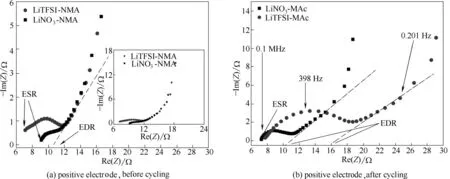
图7 在80℃、5 mV条件下LiNO3∶NMA(1∶4)和LiTFSI∶NMA(1∶4)在正极材料上从100 kHz到10 mHz区间范围内的尼奎斯特电化学阻抗谱[包括等效系列电阻(ESR,equivalent series resistance)和等效扩散电阻(EDR,equivalent diffusion resistance)两个部分][44]Fig.7 Nyquist plots for electrochemical impedance spectroscopy(including ESR,equivalent series resistance and EDR,equivalent diffusion resistance)of LiNO3∶NMA(1∶4)and LiTFSI∶NMA(1∶4)at 80℃and 5 mV in frequency range from 100 kHz to 10 mHz before and after cycling[44]
2 DESs 作为合成电极材料的溶剂/电解质
2.1 锂离子电池
DESs不仅是电池与电催化反应良好的电解质,也是合成电极材料和太阳能电池半导体材料良好的溶剂/电解质。ChCl∶glycol 为溶剂在130℃合成橄榄石形的磷酸锰锂和碳的纳米棒(LiMnPO4/C,约125 nm 长,50 nm 直径)用于锂离子电池,其放电容量128 mA·h·g-1且在1 C 时100 次循环后保持率高达93%[71]。ChCl∶glycol 的作用在于能抑制LiMnPO4新晶面的生成以调控晶体生长的方向和形貌[71]。尼奎斯特电化学阻抗谱测试发现电解质的电阻Re和电荷转移的电阻Rct分别为10.9 Ω 和128 Ω,较低的电阻值说明DESs 合成的LiMnPO4/C 纳米棒促进电解质的迁移和电荷的转移[71]。Gu等[72]以DES为溶剂合成二氧化锡纳米颗粒用于锂离子电池的负极材料,充放电实验表明能量密度高达1045 mA·h·g-1。
2.2 钠电池
钠离子电池与锂离子电池相比优点在于钠元素的含量丰富、便宜及钠离子与锂离子相似的物理化学性质。ChCl∶glycol(1∶2)为溶剂合成的钛酸钠(Na2Ti3O7)片(70℃溶解,500℃焙烧),与传统的合成方法相比较更加温和、便宜与绿色[73]。另外,ChCl∶glycol还能调控钛酸钠的尺寸与形貌。Na2Ti3O7片与片之间会层叠,层与层之间拥有小孔,这些孔为钠离子的嵌入提供空间。合成的Na2Ti3O7能作为钠离子电池的电极,其放电比容能分别达到127 mA·h·g-1(50 个循环,1 C)和72 mA·h·g-1(2000 个循环,5 C)[73]。
2.3 太阳能电池
ChCl:urea(1:2)同时溶解氯化铜(CuCl2)、氯化镓(GaCl3)、氯化铟(InCl3)电沉积出Cu-In-Ga 前体可用于太阳能电池光伏材料铜铟镓硒[Cu(In,Ga)Se2,CIGS][74]。电化学性质测试表明三种离子的扩散系数顺序为:Cu2+>In3+>Ga3+。利用DESs合成Cu-In-Ga 前体的步骤简便、条件温和,与传统的真空喷涂法相比更加节能环保。而且,在电化学沉积过程中DESs 能抑制氢气的析出,提高电化学效率[74]。Malaquias 等[75-76]也一锅法在ChCl∶urea(1∶2)中电沉积出比较理想的Cu-In-Ga 前体用于CIGS。Yang等[77]在DES中电沉积出Cu-Ga前体用于合成CuGaS2的晶形比较完美,而且沉积电势越大越能增加Cu/Ga 的摩 尔比。Dale 等[78]利用DESs 沉积Cu-Ga 前 体也抑制了氢气的析出和提高电沉积的效率,为下一步低成本合成CuGaSe2提供良好的基础。
2.4 液流电池
DESs 也是合成液流电池所需电极材料的电沉积优良电解质。Savinell 等[79]利用FeCl3在ChCl∶glycol(1∶4)中的高溶解性以沉积铁。结果发现当Cl∶Fe ≥4∶1(FeCl2∶ChCl∶glycol,0.5∶1∶4)时 电解质中主要以[FeCl4]-和[FeCl4]2-的形式存在,此时液流电池容量工作14个循环后也基本不发生改变。当Cl∶Fe <4∶1(FeCl2∶ChCl∶glycol,1∶1∶4)时,乙二醇和铁离子能发生强烈的配合相互作用,这种配合作用降低电解质的流动性和电导率也改变铁沉积的机理,此时液流电池不能显示出正常的充放电性能[79]。
2.5 超级电容器
Mu 等[80]用DES 剥离生物蚕丝生成纳米纤维丝薄膜隔离超级电容器能获得高达171 F·g-1(1 A·g-1)的比容和86%的保持率。Some 等[81]用DES 还原氧化石墨烯为硫、氮共掺杂的石墨烯材料。DES 的组分是氯化胆碱∶硫化钠(ChCl∶Na2S),其含有硫元素和氮元素提供掺杂的硫源和氮源。DES的作用是多功能化的,包括溶剂、还原剂、掺杂剂。合成的硫、氮共掺杂的石墨烯材料为超级电容器电极材料时具 有57.3 W·h·kg-1的 能 量 密 度(509 F·g-1,1 A·g-1)[81]。Seo 等[82]也利用DESs 为原料(氯化胆碱:二氧化锡,ChCl∶SnO2,1∶2)一锅法合成三元纳米杂化材料Sn/SnO2@C 用于超级电容器,并取得比较理想的能量密度(109.7 mA·h·g-1,1.42 mA·cm-2)和100%的容量保持率(5000 循环后)。Monte 等[83]则用间二苯酚∶氯化胆碱∶甘油(1∶1∶1)为原料、甲醛和磷酸为催化剂在水溶液中合成含磷碳材料,尽管间二苯酚∶氯化胆碱∶甘油在水中的浓度只有57%,但依旧保持超分子的结构稳定性。能量密度和开路电压分别高达13 W·h·kg-1和1.4 V[83]。
2.6 ORR
ORR 是可持续燃料电池的正极反应,传统的ORR电催化剂含有铂钴等金属[84]不利于工业的广泛应用,所以设计高效的非金属ORR 电催化剂是燃料电池的关键。鞣酸∶尿素(质量比1∶1)为原料、氯化锌为模板和碳化促进剂在一定条件下能高效合成含氮石墨碳材料,此材料显示良好的ORR 效率[85]。ORR 高效率可归结为含氮石墨碳材料的高比表面积、高吡啶氮含量及内在的缺陷。与标准的铂碳材料相比,含氮石墨碳材料的ORR效率比较相近[85]。
2.7 OER、HER、电化学全解水
电化学全解水是获取可持续清洁能源氢气的一种有效方略,其包括两个电极反应:OER、HER。要提高电化学全解水的效率则要提高OER 和HER两个电极反应的效率,特别是OER 反应比较缓慢[86],所以关键在于OER。当然,如果HER 和OER能同时提高对电化学全解水则更佳。Mu 等[87]开发一种基于DESs(六水氯化镍∶丙二酸)的简易、温和、绿色且便宜的合成石墨烯包裹磷化镍(Ni2P@G)的全解水电催化剂。Ni2P@G 的优势在于拥有较低的水全解超电势,获得10 mA·cm-2的电流密度只需要1.51 V 的电压[82]。Bandosz 等[31]电沉积的磷钴电催化剂(ChCl∶glycol 为电解质)对HER 和OER 的过电势只有62 mV 和320 mV(截止电流10 mA·cm-2)。Zhang等[88]在ChCl∶urea中电沉积氧钴和硒钴杂化薄膜电催化剂用于全解水时分别对HER 和OER 拥有85 mV和340 mV的过电势(10 mA·cm-2)。
全解水的其中一个电极反应HER 也可以通过设计合适的电催化剂予以改善。Zhang 等[89]在DES中合成的NiPx薄膜HER 时只有105 mV 的过电势和44.7 mV·dec-1的塔菲尔斜率。Lu 等[90-91]在DESs 中共沉积出Ni金属和Ni-Mo-Cu 三元金属拥有较低的HER 过电势。Mohan 等[92]研究发现在DESs 中电沉积的三元金属Ni-Co-Sn 比二元金属(包括Ni-Sn 和Co-Sn)更适合于HER。
改善OER 的电催化剂更是改善全解水制氢的关键。Fu 等[93]在DESs 介质中合成的氧化铜@碳三氮四(CuO@C3N4)催化剂在33 mA·cm-2的电流密度时只有0.77 V 的OER 过电势。六水氯化钴∶尿素(CoCl2·6H2O∶urea,1∶1)是盐和尿素形成的DES。Li等[94]用CoCl2·6H2O∶urea 为原料一锅法合成无定形的CoOOH 电催化剂用于OER 过程。活化后的电催化剂、活化前的电催化剂、镍泡沫在OER 过程中10 mA·cm-2的条件下过电势分别为291、321、417 mV[图8(a)];塔菲尔斜率分别为65、76、234 mV·dec-1[图8(b)][94]。这意味着活化后的电催化剂电子传输速率最快,最适用于OER。不同扫描速度的循环伏安曲线可计算出活化后的电催化剂双电层电容为8.5 mF·cm-2[图8(c)、(d)],表示此催化剂具有较大的电催化活化位点暴露。
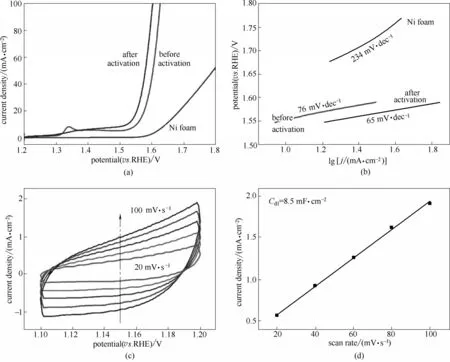
图8 活化前、活化后和镍泡沫的OER过程的极化曲线(a),塔菲尔曲线(b),循环伏安曲线(c)和双电层电容(d)[94]Fig.8 Polarization curve(a),Tafel curve(b),cyclic voltammetry curve(c)and double-layer capacitance(Cdl)(d)of OER with electrocatalyst before activation,after activation and nickel(Ni)foam[94]
Xu 等[95]在DESs 中合成氮和硫共掺杂的铁钴镍三元电催化剂在OER 中可达251 mV 的过电势和58 mV·dec-1的塔菲尔斜率。Seo 等[96]发现温和条件下在绿色DES(氯化胆碱∶丙二酸)介质中可以合成八面体钒酸钴。氯化胆碱∶丙二酸的作用有多个:溶剂、模板;八面体钒酸钴用于OER 只有324 mV 的过电势(10 mA·cm-2)[96]。Mu 等[97]首次使用乙二硫醇∶丁胺型(1∶1)DES和超临界CO2合成硫化钴(CoSx)纳米片。比较有趣的现象是乙二硫醇和丁胺型都不导电,但是两者的共熔物乙二硫醇:丁胺型则具有较高的导电率(12.85 mS·cm-1);钴不溶于乙二硫醇:丁胺但是加入硫后则能完全溶解。在碱性电解质中(1 mol·L-1KOH)CoSx在玻碳电极(GCE)上拥有64.8 mV·dec-1的OER 塔菲尔斜率且显示出302 mV 的过电势,比二氧化铱的过电势(340 mV)要低得多;另外,1000 次循环使用后仍能保持优良的电化学稳定性[图9(a)][97]。电极对OER 有显著的影响:OER 效率在镍泡沫电极上降低,但是在金/镍泡沫电极上则升高[图9(b)]。Arrhenius 曲线表明活化能为54 kJ·mol-1,表明是电压决速步过程[图9(c)]。恒电压测试表明即使超过300 h 电压降也不明显,再次确认电化学催化剂的高稳定性[图9(d)][97]。Mu 等[98]还发现在绿色聚乙二醇型DES(PEG200∶硫脲,2∶1)合成的硫化镍钴(NiCo2S4)过电势和塔菲尔斜率较低,且比氧化物、单金属硫化物或其他比例硫化镍钴数值都要低[图10(a)~(c)]。电化学阻抗谱发现无补偿系列电阻差别不大,但是NiCo2S4的电荷转移电阻最小,表明电子在NiCo2S4的催化剂上的电荷转移最快、NiCo2S4的活性位点和活性面积(8.699 μF·cm-2)最活跃[图10(d)][98]。
2.8 氮气(N2)电还原、乙醇电氧化
电化学固氮的困难之一在于其较高的反应能垒用于断裂氮氮三键,解决方法之一在于合成合适的电催化剂以降低能垒。PEG200 和硫脲的熔点分别为-55℃和176℃,而由上述两者组成DES PEG200∶硫脲(2∶1)的熔点是-89℃。Mu 等[99]用聚乙二醇200∶硫脲(PEG200∶硫脲,2∶1)为溶剂和硫源合成硫化铁(Fe3S4)纳米片,其电催化转化N2为NH3的产率和法拉第效率高达75.4 μg·h-1·mg-1和6.45%。乙醇也是醇型燃料电池的重要原料,所以乙醇电氧化的研究也很有必要。Zhuo 等[100]通过改变DES+水体系中水的浓度合成不同形貌不同尺寸的纳米金颗粒,包括纳米金星、纳米花和纳米牙。结果表明DES 介质中合成的纳米金比商业购买的金电极乙醇氧化电位要低且催化电流要高[100]。

图9 硫化钴负载到玻碳电极GCE(a)和金电极(b)的OER线性扫描伏安曲线及塔菲尔曲线,Arrhenius曲线(c)和电催化剂负载到金电极上的恒电流曲线(d)[97]Fig.9 LSV curve and Tafel curve for CoSx on GCE(a)and gold electrode(b),Arrhenius plot(c)and chrono-potentiometric curve at 30 mA·cm-2 for electrocatalyst on gold electrode(d)[97]
3 DES作为回收电池的萃取剂
废旧电池的回收也是绿色电池的关键环节。文献报道中,锂离子电池中铝箔和正极材料的分离常常需要强腐蚀性的酸碱溶剂,从而会释放有毒有污染的氟化氢等物质。Li 等[101]首次使用ChCl∶glycerol(2.3∶1)能在较为温和(190℃)的条件下快速(15 min)高效地[99.86%(质量)]实现分离。机理研究表明主要是ChCl∶glycerol中的羟基与聚偏二氟乙烯中的氢原子的强相互作用使聚偏二氟乙烯的黏附 效 果 降 低[101]。Ajayan 等[33]发 现ChCl∶glycol 与 炭黑、铝箔、聚偏二氟乙烯在室温到105℃范围内都不发生反应,但是能高效地溶解锂正极材料(如钴酸锂、锂钴镍锰氧化物)。ChCl∶glycol 溶解钴酸锂的最低温度只有80℃,ChCl∶glycol 扮演的角色是溶剂和还原剂,能把钴酸锂还原生成[CoCl4]2-[33]。碱性锌锰废旧电池中有大量的锌元素和锰元素。Romero-Romo 等[102]采用氯化乙酰胆碱:尿素从碱性电池废液中高效地电沉积锰或锌锰合金在GCE 上。Payne等[103]首次使用DESs 从太阳能电池的钙钛矿中高效地电化学沉积出铅,结果发现钙钛矿中99.8%的铅能够用DESs实现回收利用。
4 结论与展望
DESs 是一种绿色、廉价、稳定且易合成的电解质和溶剂。在电池和电催化领域一方面能作为电池的电解质促进电池的效率,另一方面能作为溶剂以合成有特殊功能的电极材料。在电池和电催化反应回收的领域,DESs也扮演着绿色可持续循环使用的萃取剂。所以,DESs是比传统绿色溶剂(水、超临界CO2、离子液体)在电池和电催化领域更有潜力的新型绿色溶剂。
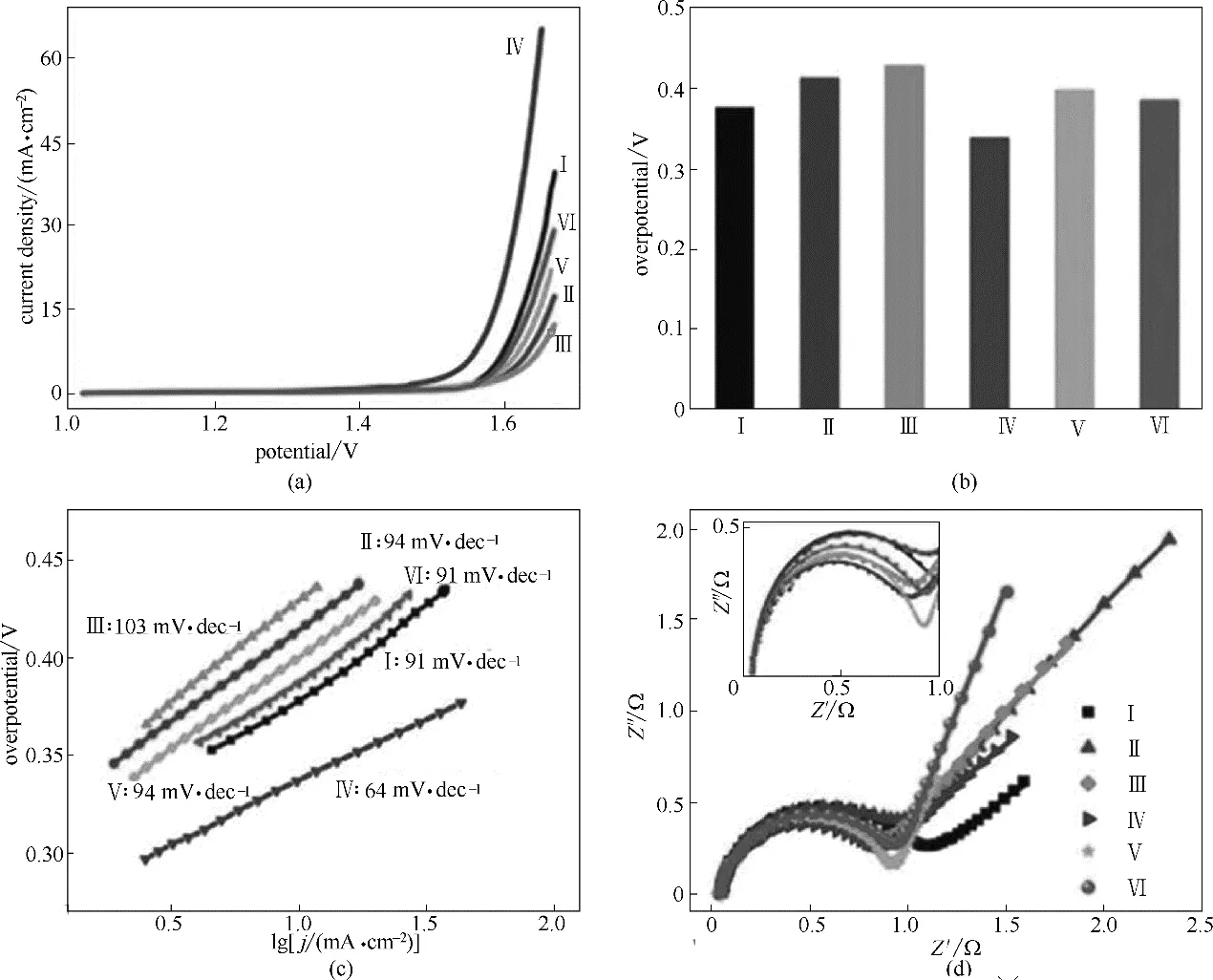
图10 硫化钴镍作OER电催化剂的极化曲线(a),过电势(b),塔菲尔曲线(c)及电化学阻抗(d)[98]Fig.10 Polarization curve(a),overpotential(b),Tafel curve(c)and electrochemical impedance spectroscopy of OER by using NiCo2S4 as electrocatalyst(d) [98]
但是,DESs在使用过程中也会有以下缺陷:(1)在作溶剂合成功能化电极材料时,DESs大多数也是合成的原料,从而不能循环使用。(2)有些DESs具有吸湿性[104],这可能对电池和电催化反应有极大的影响。(3)有些DESs 具有长期不稳定性[105-107]和挥发性[108-109],在使用过程中需要引起注意。
DESs 在电池和电催化反应领域中的应用有以下几点展望:
(1)DESs 的各种稳定性需要特别关注,包括热稳定性、挥发性、电化学稳定性、光化学稳定性及化学稳定性。
(2)DESs 与其他介质相混合时,DESs 微观结构的保持性可能需要予以关注。
(3)DESs回收废旧电池和废旧电极的报道并不多,而且效率也并不高,亟需设计高效的DESs 用以高效回收电池和电催化反应排出的废物。
(4)DESs 为电解质时,DESs 的电导率普遍偏低,而黏度偏高,除改变外界因素外(如温度、添加剂),可以考虑在DESs 引入功能化基团以同时实现电导率高、黏度低、稳定性高等多种目标。

