神经纤维瘤病II型误诊为双侧视网膜母细胞瘤一例
刘羽阳 李琬悦 张家墅 张军*
1解放军医学院(北京100853)
2解放军总医院神经外科(北京100853)
3解放军总医院眼科(北京100853)
1 临床资料
患者,女,15岁。主因“左眼视力下降伴外斜视12年余”于2018年12月入住解放军总医院第一医学中心神经外科。患儿于2005年开始无明显诱因出现左眼视力下降伴外斜视,当时未予相关检查及治疗。上述症状持续缓慢加重,于2008年至某院眼科就诊行相关检查示:“双侧视网膜母细胞瘤、左眼球内占位、右侧视网膜前膜”,并行“双眼底肿物激光封闭术”,术后未行放化疗,治疗后患者左眼视力明显下降,仅存光感。2016年患者突然出现左侧周围性面瘫,左面部电极样疼痛,未予检查及治疗。2018年至某院眼科行检查示:“左眼白内障”,并行“左眼晶状体超声乳化吸除术”。治疗期间患者行眼部MRI检查示:“双侧桥小脑角区占位性病变”,随后收入我院神经外科进行下一步治疗。查体见:左腰背部可见3×3cm褐色肿块(图1),质软、无压痛,界清,患者父自述背部病变于患者3岁即已出现,起初为数个褐色扁平斑点,后逐渐融合扩大直至隆起为褐色肿块。左眼呈外展位、左眼视力仅光感、左侧视野检查不合作、右侧无明显异常、双侧瞳孔等大等圆、直径约3mm、左侧对光反射消失、右侧对光反射无明显异常。左侧闭眼无力、鼻唇沟左侧变浅、示齿时口角向右侧偏斜、左侧周围性面瘫HB(House-Brackmann面神经功能分级)III级。术前头颅及脊柱MRI(图1)所示。纯音测听示双侧无明显异常,听性脑干反应潜伏期示双侧I-V间期延长,主要为I-III间期延长,左侧尤著,言语识别率示双侧无明显异常(图2),双侧纯音听阈AAO-HNS(American Academy of Otolaryngology-Head and Neck Surgery,美国耳鼻喉头颈外科协会)A级。
结合病史及影像学资料,术前诊断为NF2,该病是由22号染色体上NF2基因的遗传性突变或新发突变所引起[1,2],仔细询问家族史,得知患者父亲于2016年因右侧耳鸣伴听力下降,就诊于当地医院行颅脑平扫MRI示:“右侧前庭神经鞘瘤”,随后行前庭神经鞘瘤切除术。为排除患者父亲亦为NF2患者,遂建议行颅脑增强MRI,结果示:“双侧前庭神经鞘瘤,右侧前庭神经鞘瘤术后、颅内多发脑膜瘤”。至此,结合病史及影像学资料,患者父亲诊断明确,亦为NF2患者。此外,二人外周血基因测序显示均携带22号染色体NF2基因致病性突变,突变位点为c.241-9(IVS2)A>G(图3),从基因层面再次验证了NF2的临床诊断。鉴于患者目前左侧面部电击样疼痛症状明显,结合影像学资料考虑左侧继发性三叉神经痛,遂建议行左侧桥小脑角区病变切除术,以达到三叉神经减压目的。与患者家属交代相关风险后,行手术治疗。采用经典左侧枕下乙状窦后入路,全程在神经电生理监测下进行。术中见桥小脑角区黄白色肿瘤,电生理监测面神经于肿瘤腹侧呈膜状铺于肿瘤包膜,与肿瘤组织粘连紧密,分离并切除肿瘤,电生理监测下面神经解剖及保留完好,肿瘤达到全切。此外术中探查可见三叉神经位于肿瘤深面,其表面也有一小的肿瘤,给予分离后切除,至此达到三叉神经全程减压目的。术后患者神经系统查体大致同术前,面神经功能HBIII级,左侧听力AAO-HNS D级,左侧面部电极样疼痛症状完全消失。1周后拆线出院。术后病理检查示:“神经鞘瘤”。
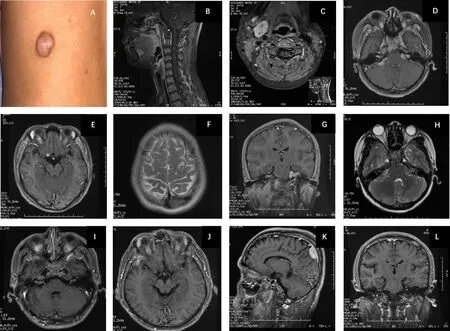
图1 患者(A-H)及其父(I-L)影像学资料A.左腰背部褐色肿块;B.颈段及上胸段髓外硬膜下多发结节;C.右侧颈动脉鞘区丛状神经纤维瘤;D,H.双侧前庭神经鞘瘤;D,E.鞍上池偏右,右侧岩斜区脑膜瘤;F.左额叶缺血灶及左顶骨病变;I.双侧前庭神经鞘瘤;J,K.颅内多发脑膜瘤;L.左侧额顶骨板强化病变Fig.1 Imaging data of patient(A-H)and her father(I-L)A.Brown mass on the left lumbar back;B.Extramedullary subdural multiple nodules in the cervical and upper thoracic segments;C.Right carotid sheath plexiform neurofibroma;D,H.Bilateral vestibular schwannomas;D,E.Right suprasellar cistern and right petroclival region meningiomas;F.Ischemic area of left frontal lobe and left parietal lesions;I.Bilateral vestibular schwannomas;J,K.Multiple intracranial meningiomas;L.Enhanced lesions in left frontal and parietal bone
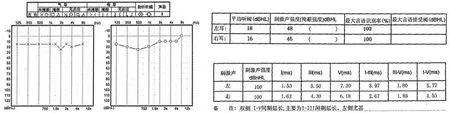
图2 患者听力学评估Fig.2 Audiological evaluation of the patient
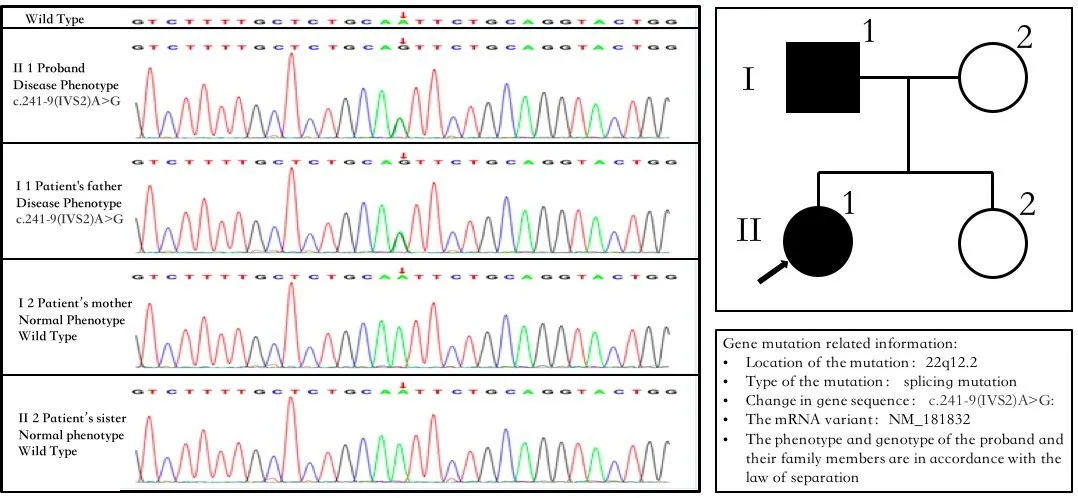
图3 患者及其父携带致病突变;患者家系图;基因突变相关信息Fig.3 The pathogenic mutation carried by the patient and her father;The Family tree of patient;Gene mutation related information
2 讨论
本例患者2岁起病,以眼部异常和皮肤病变为首发症状,由于临床表现不典型,导致误诊为双侧视网膜母细胞瘤。NF2眼部病变种类繁多,缺乏一定的特异性,常导致漏诊误诊。NF2常见的眼部病变有白内障、视网膜前膜,视网膜错构瘤[3,4]。此外,视神经脑膜瘤[5]、动眼神经鞘瘤[6],视神经异常[7]也在一些患者中出现。回顾该患者相关病变有左眼白内障、右眼视网膜前膜、双侧视网膜错构瘤,右侧视神经异常(图4)、神经系统多发病变及皮肤病变(图1),均在一定程度上提示NF2诊断。仅关注眼底病变而未综合考虑其他眼部病变和其他系统病变是本病误诊的主要原因。
视网膜母细胞瘤(Retinoblastoma,RB)是儿童期最常见的眼内原发性恶性肿瘤,占出生后1年内所患恶性肿瘤的10-15%。从遗传学角度,RB分为遗传型和非遗传型,其中遗传型RB通常指双侧患者、多病灶患者,有阳性家族史者以及已知存在种系突变者。遗传型RB外周血检测可在90-95%病例中发现种系突变[8]。该例患者,2岁起病,主要症状为左眼外斜视伴视力下降,首诊时于全麻下行眼底检查可见双眼眼底肿物。回顾患者家族史,其父暂时未发现眼部病变,但仍不能排除患者为遗传型RB的可能,基因检测在该病的诊断中起到关键性的作用。该患者及其父母外周血测序未见RB1基因突变,基本排除遗传性RB诊断。故建议对所有疑诊患者进行基因检测以明确诊断。此外,未经规范化治疗的RB通常在出现临床表现后1年内出现转移扩散[9],出现转移后通常一年内死亡。即使接受了规范化治疗,其生存率仍<10%[10]。大约5%的双侧或遗传型视网膜母细胞瘤患者会出现颅内肿瘤[11,12],其中三侧性RB指患者伴有组织学相似的颅内肿瘤,约75%病例病灶位于松果体,其余位于鞍上或鞍旁[11],通常是致死性的[13]。由此可见,双侧RB伴颅内转移或双侧RB伴颅内肿瘤均呈现病程短、进展迅速,预后不佳等特点,与NF2相对长病程、缓慢进展有一定区别。患者虽为眼部病变伴颅内多发病变,根据病程和病情进展情况,可基本排除RB诊断。
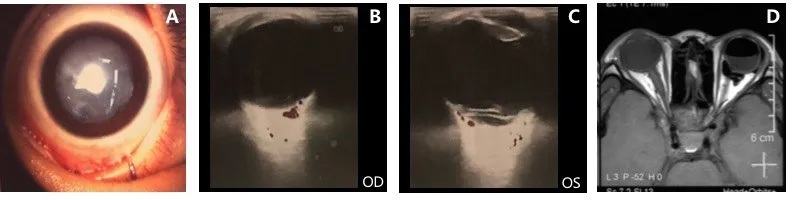
图4 患者眼部病变A.左眼白内障;B.右眼球内异常回声及视网膜前膜;C.左眼球异常回声;D.右侧视神经异常增粗Fig.4 The ocular disorders of patient A.The cataract in left eye;B.Abnormal echo in right eye and epiretinal membrane;C.Abnormal echo in left eye;D.Abnormal enlargement of right optic nerve
NF2双侧前庭神经鞘瘤的主要干预手段包括:保守观察、显微手术治疗、立体定向放射外科治疗及靶向药物治疗。对于该患者治疗策略的选择主要基于以下几个方面:术前患者表现为左侧三叉神经痛,考虑继发于左侧前庭神经鞘瘤,手术切除病灶是继发性三叉神经痛的标准治疗方式,术中证实患者合并术前影像学未发现的三叉神经鞘瘤,术后症状完全缓解。MRI示患者左侧前庭神经鞘瘤最大径2.5cm,肿瘤呈实质性并推挤脑干,与脑干在T2WI序列上缺乏明显界面,考虑肿瘤与脑干粘连紧密,对此类病灶进行放射治疗可能会出现肿瘤内囊性变继而体积增大导致急性压迫症状。据文献报道,放射治疗后的肿瘤体积缩小约见于18%的患者[14],选择该种方式作为初始干预手段缓解三叉神经痛可能性较小。此外,术前影像学考虑右侧颈动脉鞘区病变为丛状神经纤维瘤,该病变可转化为恶性周围神经鞘膜肿瘤[15],且该患者已携带具有重要功能的NF2基因突变,需考虑到放射治疗诱发肿瘤恶变的可能[14]。该患者临床分型属于Wishart型,相较于Gardner型具有发病年龄早、病灶多、病情进展较快等特点[16],基因测序显示该患者突变靠近3’端位于外显子2的剪接点突变,与其他部位的剪接点突变和靠近5’端的突变相比具有更加严重的疾病表现[17],可见保守观察亦不适合作为该患者初始干预手段。现阶段NF2靶向治疗相关研究主要集中于贝伐珠单抗,一项最新的基于17例NF2患者的研究显示,经贝伐珠单抗治疗后,47%患者肿瘤体积缩小,56%患者听力水平较治疗前提高[18],与其他治疗方式相比,靶向治疗有其独特的优势,例如可以免除开颅相关并发症和治疗相关的神经功能损伤,但现有的研究仍存在病例数较少,随访时间较短等问题[19],随着相关研究的深入进展,靶向药物在NF2的治疗中的长期效果将逐渐被揭示,并有望成为未来NF2治疗的主要手段之一。
总而言之,对于该例患者而言,NF2的序贯治疗尤为重要,推荐每半年进行磁共振检查以达到监测目的,若颅内病变快速增长、影像学提示恶变以及出现明显占位效应可行手术治疗,前庭神经鞘瘤手术治疗可考虑同时行听觉脑干植入(Auditory Brainstem Implantation)或耳蜗植入(Cochlear Implantation)以重建部分听力[20],放射及靶向药物治疗可作为重要的补充治疗方式。NF2作为累及多器官多系统的疾病,多学科联合治疗至关重要,加速推进NF2规划化诊疗方案建立,才能使越来越多的患者受益。
3 小结
综上所述,NF2作为累及眼、中枢神经系统,皮肤等多系统多器官疾病[2],早期识别并正确诊断意义重大,关乎到患者干预手段选择及预后。除了常规的问诊和完备的辅助检查外,仔细询问家族史、既往史,规范的神经及全身查体更是必不可少,必要时结合基因测序和家系分析,这些都是准确诊断NF2的基石。此外,对于以眼部及皮肤病变为主要临床表现的儿童患者,要考虑到此病的可能以防漏诊和误诊。随着NF2相关研究的不断推进,相信在不久的将来,NF2的早期诊断准确率和疾病预后都会达到一个全新的水平。

