无水磷酸氢钙固化姜黄素磷脂复合物
张焕焕刘 艺张 兰范君婷鞠建明*
(1.安徽中医药大学,安徽 合肥 230031; 2.南京中医药大学附属中西医结合医院,江苏 南京 210028;3.南京医科大学药学院,江苏 南京 211166)
姜黄素是从姜黄干燥根茎中提取纯化出的一种酚类化合物[1],具有多种药理活性,如抗癌、预防动脉粥样硬化、抗菌等[2-4],被认为是一种安全的植物成分,没有显著毒性和致畸性,亚洲许多国家和地区广泛用作香料、膳食补充剂、药物成分[5-6]。但姜黄素水溶性差,并且代谢迅速和全身消除快速,导致该成分生物利用度较低,从而限制了临床应用[7-8]。
现代研究表明,姜黄素、石杉碱甲、小檗碱等多种难溶性成分的磷脂复合物能有效地提高其溶解度、溶出率、口服生物利用度[9-11]。磷脂是细胞膜的基本成分之一,跨膜能力强,药物与其结合后亲脂性和跨膜吸收能力增加[12],同时它可提高水溶性、脂溶性药物溶解度[13]。但磷脂复合物黏性大,影响药物释放,不利于工业化生产,故必须使用适当的辅料来改善其流动性和可压缩性。
无水磷酸氢钙是白色单斜晶系结晶粉末,具有低吸湿性及良好的流动性、可压缩性,常用于药物制剂的辅料,如直接压片赋形剂、润滑剂,以改善片剂压缩特性和流动性[14],但目前尚无应用其作为赋形剂固化磷脂复合物以改善流动性、溶出度的报道。因此,本实验拟采用无水磷酸氢钙作为载体材料,将姜黄素磷脂复合物固化成粉末,并对其流动性、体外溶出度、生物利用度进行评价,以期确定其可行性。
1 材料
1.1 仪器 DSC449F3 差示扫描量热仪(德国Netzsch 公司);6390LV 扫描电镜(日本电子株式会社);红外光谱仪(美国Ominic 公司);D/max 2500/PC 转靶X 射线衍射仪(日本理学株式会社);Waters 高效液相色谱仪(配置Alliance 2695四元泵及自动进样系统、Waters 2996 PDA 检测器);RCZ8M 溶出仪(天津天大天发科技有限公司);纯化水装置(美国Millipore 公司);AT201电子天平(十万分之 一,瑞 士 Mettler-Toledo公司)。
1.2 试剂与药物 姜黄素(质量分数>97%,大连美仑生物科技有限公司);无水磷酸氢钙(上海昌为医药辅料技术有限公司);卵磷脂(西安泰华医药科技有限公司)。无水乙醇(上海阿拉丁生化科技股份有限公司);乙腈为色谱纯(美国天地公司);其余试剂均为分析纯;水为超纯水。
1.3 动物 SD 雄性大鼠,体质量180~220 g,购自上海斯莱克实验动物有限公司,动物生产许可证号SCXK(苏)2014-0001。
2 方法
2.1 磷脂复合物制备 称取适量姜黄素和磷脂(1∶2)于烧杯中,加入10 mL 无水乙醇,37 ℃下磁力搅拌2 h,完全溶解后转移至圆底烧瓶中,60 ℃下蒸去无水乙醇,刮下半固体,即得,置于干燥器中备用。
2.2 固化粉末制备 采用溶剂蒸发法[15]。称取适量磷脂复合物和无水磷酸氢钙(1∶2)于烧杯中,加入10 mL 无水乙醇,37 ℃下磁力搅拌2 h,转移至圆底烧瓶中,60 ℃下蒸去无水乙醇,刮下固体,即得,置于干燥器中备用。
2.3 物理混合物制备 称取适量姜黄素、磷脂、无水磷酸氢钙(1∶2∶6),置于研钵中混合均匀,过50 目筛,即得,置于干燥器中用。
2.4 样品表征
2.4.1 扫描电子显微镜(SEM)称取适量姜黄素、物理混合物、磷脂复合物、固化粉末,在其表面真空镀金70 s,再通过SEM 观察样品表面和晶体结构。
2.4.2 差示扫描量热法(DSC)以空铝钳锅为参比物,在另一铝锅中放入一定量样品,载气氮气,升温速率20 ℃/min,升温范围0~300 ℃,对姜黄素、物理混合物、磷脂复合物、固化粉末进行DSC 分析。
2.4.3 X 射线衍射(XRD)测试条件为Cu 靶(40 kV,25 mA),步进扫描0.01°/步,扫描范围5°~70°,扫描速度4°/min,对姜黄素、无水磷酸氢钙、物理混合物、磷脂复合物、固化粉末进行XRD 分析。
2.4.4 傅里叶变换红外光谱(FTIR)取适量姜黄素、无水磷酸氢钙、物理混合物、磷脂复合物、固化粉末,在4 000~400 cm-1范围内进行FTIR分析。
2.5 流动性 采用固定漏斗法[16]。将漏斗置于水平表面的固定高度,固化粉末倒入漏斗中,轻微振动,滑下的粉末形成锥体,记录锥体平均直径(D)和粉末堆积高度(h),计算休止角θ,公式为tanθ=2h/D。
2.6 体外溶出度研究 采用2015 年版《中国药典》四部通则中溶出度与释放度测定法中的第一法(篮法)。称取适量姜黄素、物理混合物、磷脂复合物、固化粉末(相当于含姜黄素5 mg)装于空胶囊中,设定转速100 r/min,温 度(37±0.5)℃,溶出介质900 mL 磷酸盐缓冲液(pH=1.2 或6.8)[17-18]。于5、10、20、30、45、60 min各取样5 mL,同时补加同温等量溶出介质,13 000 r/min离心10 min,取上清测定姜黄素含有量,计算其累积溶出率,绘制溶出曲线,平行3 份。
2.7 体内药动学行为研究
2.7.1 血浆样品的制备 24 只大鼠随机分成4组,每组6 只,实验前禁食12 h,自由饮水,按100 mg/kg 剂量分别灌胃给予姜黄素、物理混合物、磷脂复合物、固化粉末(混悬于0.5% CMCNa 溶液中)。于0.17、0.33、0.5、0.75、1、2、4、6、8、10 h 眼眶静脉丛取血各0.5 mL,置于肝素化离心管中,4 ℃下4 000 r/min 冷冻离心10 min,取上清,保存于-80 ℃冰箱中[19]。
2.7.2 血浆样品处理 吸取血浆样品100 μL 于离心管 中,加 入10 μg/L 内标溶液(葛根素)10 μL,涡旋10 s,加500 μL 乙腈,再涡旋3 min,15 000 r/min 离心5 min,取上清液,氮气吹干后加入100 μL 乙腈-水(1∶1)复溶,3 500 r/min离心5 min,取上清待测。HPLC 分析时,取20 μL等分试样注入。
2.7.3 数据分析 根据血药浓度-时间曲线,得到药峰浓度(Cmax)、达峰时间(Tmax);通过DAS 1.1.1 软件,对血药浓度-时间数据进行非房室拟合分析,计算其他药动学参数;采用SPSS 23.0 软件,对主要药动学参数进行独立样本t检验,数据以(±s)表示,以P<0.05 为差异有统计学意义。
3 结果
3.1 SEM 分析 图1 显示,姜黄素、物理混合物中能发现明显晶体,而在磷脂复合物、固化粉末中消失,呈现无定形状态,表明姜黄素可与磷脂完全结合,从而使前者在磷脂复合物中从结晶态转变为非晶态。

图1 样品SEM 图Fig.1 SEM images for samples
3.2 DSC 分析 图2 显示,姜黄素、物理混合物在183.5 ℃附近有晶体吸热峰,而无水磷酸氢钙没有;物理混合物在115 ℃附近出现1 个宽吸热峰,它低于姜黄素晶体峰,可能是由于有一部分受到磷脂、无水磷酸氢钙干扰,导致吸热峰有所减弱;磷脂复合物、固化粉末中上述2 个峰均消失,表明药物以无定形或非晶体状态存在,与“3.2”项下结果一致。
3.3 XRD 分析 图3 显示,姜黄素在5°~35°处具有较强的特征衍射峰,在17.8°处为其晶体特征峰;物理混合物中尽管大多数峰消失,但仍可观察到姜黄素特征峰,表明该成分仅与无水磷酸氢钙和磷脂物理混合,并且仍以结晶形式存在;磷脂复合物、固化粉末中姜黄素特征衍射峰均消失,提示该成分可能以无定形状态存在。
3.4 FTIR 分析 图4 显示,姜黄素在3 434、1 511 cm-1处有强烈的特征吸收峰,前者是该成分苯环骨架峰,而后者为酚羟基伸缩振动;无水磷酸氢钙在1 200 cm-1处显示出特征性P=O 吸收带;物理混合物在1 200 cm-1处存在P=O 吸收带,3 400 cm-1处有酚羟基吸收带;磷脂复合物、固化粉末在3 400 cm-1处酚羟基峰吸收加强,可能是由于辅料和磷脂结构中羰基振动的叠加所致,推测后者中各物质之间没有形成新化学键,可能通过分子间作用力而结合。
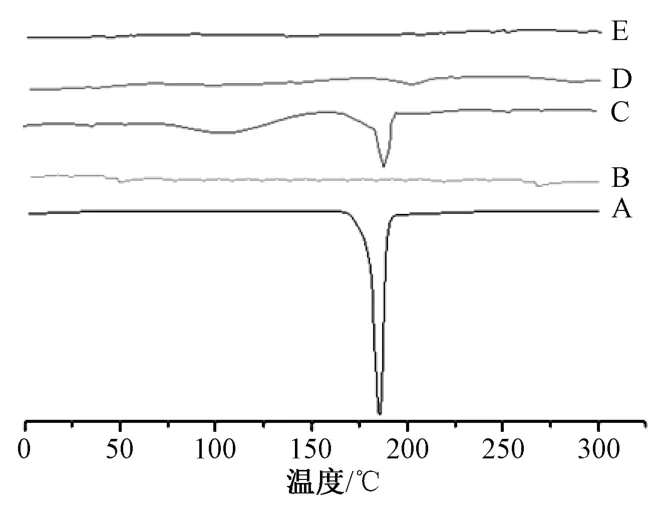
图2 样品DSC 图Fig.2 DSC pattern for samples

图3 样品XRD 图Fig.3 XRD pattern for samples

图4 样品FTIR 图Fig.4 FTIR pattern for samples
3.5 流动性考察 磷脂复合物呈不流动半固体状态,而加入无水磷酸氢钙作为载体后固化粉末休止角为30°,更有利于生产。
3.6 溶出度考察 图5 显示,磷酸盐缓冲液(pH=1.2 或6.8)中固化粉末累积溶出率高于磷脂复合物、物理混合物、姜黄素,这是因为无水磷酸氢钙存在较高的孔隙率,能使药物分散更均匀,溶出速率加快。
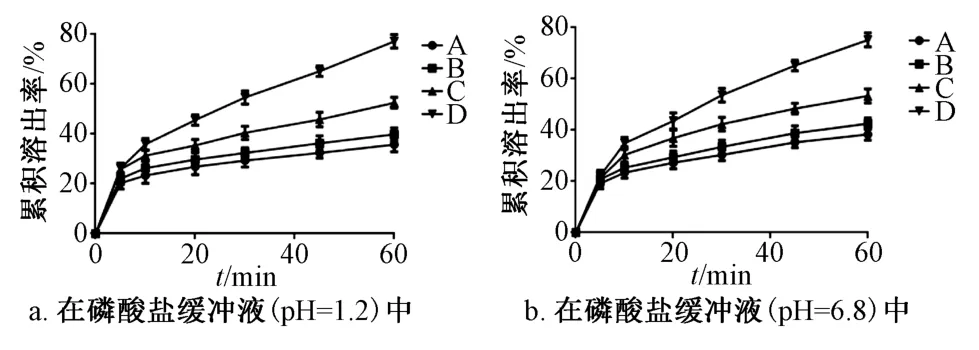
图5 样品累积溶出曲线Fig.5 Accumulative dissolution curves for samples
3.7 生物利用度 图6、表1 显示,固化粉末Cmax、AUC 显著高于磷脂复合物、物理混合物、姜黄素(P<0.05),t1/2显著降低(P<0.05),相对口服生物利用度较磷脂复合物增加了1.53 倍。

图6 样品血药浓度-时间曲线Fig.6 Plasma concentration-time curves for samples
4 讨论
由于姜黄素水溶性差、生物利用度低,本实验通过将其制成磷脂复合物来增强该成分膜渗透性,但由于磷脂复合物黏性大、流动性差,故采用无水磷酸氢钙作为载体固化磷脂复合物形成粉末,从而增加其流动性。结果显示,姜黄素与无水磷酸氢钙具有良好的相容性,前者在固化粉末中以稳定的无定形状态存在,同时磷脂复合物的溶出速率也有所提高。评估了固化粉末的生物利用度,发现它与传统姜黄素磷脂复合物相比有明显的改善作用。因此,无水磷酸氢钙不仅可用于改善磷脂复合物的流动性,有利于以后固体剂量处理,而且还可增加其复合物溶出速率,从而改善口服生物利用度。
表1 样品主要药动学参数(±s,n=6)Tab.1 Main pharmacokinetic parameters for samples(±s,n=6)

表1 样品主要药动学参数(±s,n=6)Tab.1 Main pharmacokinetic parameters for samples(±s,n=6)
注:与磷脂复合物比较,*P<0.05。

