继发性高草酸尿症的诊治进展
于健鹏 谌 卫 综述 郭志勇 审校
继发性高草酸尿症(secondary hyperoxaluria,SH)是由于获得性草酸代谢紊乱导致尿草酸排泄过多、草酸钙晶体沉积的一种多因素代谢性疾病[1],其发病因素包括草酸盐及其前体物质的摄入增加、肠道对草酸盐的吸收增加、肠道菌群失调等。如果不经有效控制,患者可出现复发性肾结石、肾钙质沉着症等疾病,部分患者还会发生急性肾损伤(acute kidney injury,AKI)、慢性肾脏病(chronic kidney disease,CKD)并最终进展为终末期肾病[2-3]。近年来随着研究的不断深入,对该疾病的认知也不断加深。据此本文针对SH的发病机制、临床表现及诊疗方式进行综述。
病因及发病机制
草酸及其前体的摄入增加有研究显示摄入大量富含草酸盐食物(每日约800 mg草酸盐)的患者,其尿草酸排泄量显著高于正常人,而减少草酸盐的摄入能够有效缓解高草酸尿症状,使尿草酸排泄维持在正常水平[4]。三敛(学名Averrhoa bilimbi)是一种草酸含量可达25.1 mg/100g的南印度水果,国外较多研究发现其在用于治疗高血压、糖尿病及血脂异常的过程中能导致患者尿草酸排泄增加并且发生AKI[5]。表1为常见的食物草酸含量[6]。木糖醇作为葡萄糖代用品,在体内会转化为草酸,其过量输注可导致SH的发生、肾草酸钙结晶和AKI,研究发现当输注量超过500g时会导致44%的患者出现严重的肾脏草酸钙晶体沉积[7]。维生素C作为草酸的前体物质,有研究证实每周摄入500 mg持续18个月可显著增加患者的血浆草酸盐水平进而导致SH的发生[8]。此外,由于乙二醇能够在肝脏中经乙醇脱氢酶转化为乙醇酸、乙醛酸并最终形成草酸,因此当患者发生乙二醇中毒时也会导致SH的出现[9]。
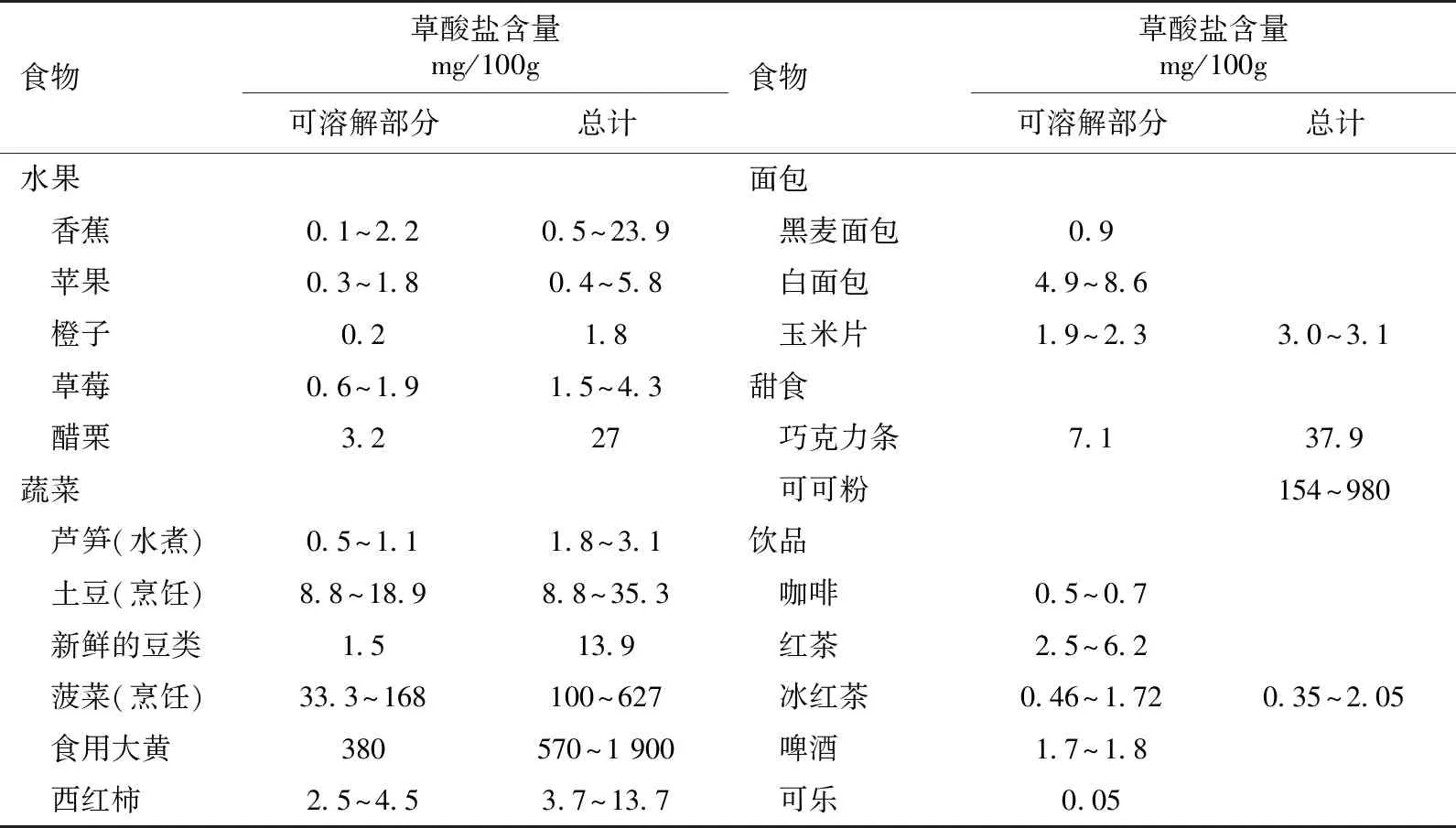
表1 常见食物草酸含量
肠道对草酸盐的吸收增加肠源性高草酸尿症(enteric hyperoxaluria,EH)是由于肠道吸收草酸盐增加而形成的一种继发性高草酸尿症[3],可由炎症性肠病(inflammatory bowel disease,IBD)、胰腺外分泌功能不全、胃旁路手术(Roux-en-Y gastric bypass,RYGB)、空回肠旁路术(jejuno-ileal bypass,JIB)及短肠综合征[1]等疾病引起。其发病机制包括:(1)机体在脂肪吸收不良的状态下,肠腔内增多的游离脂肪酸优先与钙发生竞争性结合,导致肠腔内未与钙结合的可溶性草酸盐增多并通过结肠旁被动运输吸收入血,大量草酸盐进而从尿液中排出形成EH[3]。奥利司他作为胃肠及胰腺脂肪酶抑制剂,有研究显示也会引起脂肪吸收不良进而导致EH的发生[10]。(2)脂肪吸收不良还可以导致维生素B6的缺乏,使得乙醛酸在肝脏中不能有效转化为甘氨酸,乙醛酸进而被氧化为草酸导致内源性草酸盐的合成增加[3]。(3)IBD、肠道内高浓度胆汁酸可引发肠上皮炎症反应,从而增加肠道对草酸盐的通透性使草酸盐的吸收增加[11]。此外,肠道草酸转运蛋白的活性下降也可能导致草酸盐的吸收增加。溶质载体家族蛋白26成员6(solute carrier family 26 member-6,slc26a6)是一种具有氯—草酸盐交换功能的跨膜蛋白,分布在肾小管上皮细胞和肠上皮细胞中[2],动物实验证实其作用是介导草酸盐在肠道和肾小管内的跨细胞分泌,从而减少草酸盐在肠道内的吸收,降低血浆草酸盐水平[12]。而在slc26a6缺陷的小鼠中因草酸盐分泌显著降低导致肠道吸收草酸盐增加,使血浆草酸盐水平升高,过量的草酸盐通过肾小球的滤过作用从尿液中排出,最终可导致SH的出现[13]。
肠道菌群失调肠道菌群失调导致SH发生的机制目前还在积极探索中。动物实验发现,RYGB术后的小鼠由于肠道菌群失调引起食草酸杆菌数量的减少,会使尿草酸排泄量增加4倍,而在定植食草酸杆菌后发现尿草酸排泄量降低了74%[14]。其可能的发病机制如下:(1)食草酸杆菌能够通过编码甲酰辅酶A转移酶和草酰辅酶A脱羧酶降解肠道内的草酸,但在菌群失调状态下这种能力会明显下降[11]。尽管目前还没有定期检测SH患者肠道菌群的相关研究,但有研究发现JIB术后发生SH的患者,粪便中草酸盐降解效率由正常时的0.1~4.8 mmol/(g·h)降至0.01 mmol/(g·h)以下[15]。(2)定植在回肠远端、结肠远端及盲肠的食草酸杆菌能够促进草酸盐向肠道的净分泌,从而减少草酸盐的吸收量,因此菌群失调会导致草酸盐的吸收增加进而出现SH[16]。但这一机制目前仅在动物实验中得到证实,未来还需要在人类中进行大量研究。
临床表现
继发性高草酸尿症的患者由于尿液中的草酸盐与钙结合形成草酸钙结晶,当结晶较小时可出现血尿、蛋白尿[17]。随着结晶不断生长、凝集成更大的结晶颗粒,当黏附或停滞在肾盂处时会发生固定生长,最终形成临床上反复发作的草酸钙结石[18]。若结晶沉积于肾实质中还可导致肾钙质沉着症[19]。如不经有效控制,患者可出现少尿、无尿等AKI表现[20]进而导致CKD,部分患者还可直接以慢性病程起病导致肾功能进一步减退[3]。此外,少数SH患者出现肾功能减退时,由于肾脏排泄草酸的能力下降,还可以导致草酸钙晶体沉积在心脏、骨关节、皮肤等全身各组织器官中并产生相应症状,因此若患者出现不明原因的心肌舒缩障碍、骨痛、网状青斑等肾脏外表现时应考虑有SH的存在[19]。
诊 断
对怀疑SH的患者应特别注意病史采集,如饮食习惯、维生素C及用药史、胃肠道疾病及相关手术史等。此外,对首次发生肾结石的儿童、肾结石反复发作的成年人、任何年龄段首次发生肾钙质沉着症及具有结石家族史的人群也应尽早诊断以免延误治疗[2],同时需鉴别原发性高草酸尿症(primary hyperoxaluria,PH)。检查方法如下:
实验室检查(1)尿草酸排泄量:肾功能正常的SH患者,24h尿草酸排泄量通常为0.7~1.0 mmol/1.73 m2,超过1.0 mmol/1.73 m2时通常出现于PH患者及少数严重EH患者[21]。而肾功能不全的患者由于肾脏排泄草酸的能力受到影响,存在继发性因素时该数值超过0.5 mmol/1.73 m2即可考虑SH[21]。(2)血浆草酸盐水平:该指标的变化长久以来受到国内学者的关注,由于肾小管分泌草酸的储备能力较大,其在肾小球滤过率(GFR)中度降低时仍可保持正常水平[22]。最近有研究发现GFR>45 ml/min的患者,其血浆草酸盐水平波动较大且与GFR的下降无明显相关性[23],而对于GFR<45 ml/min的患者,血浆草酸盐水平通常会维持在30~80 μmol/L(正常值1~5 μmol/L,PH患者>80 μmol/L)[2]。(3)尿液检查:患者可出现高钙尿或低钙尿症[20,24],此外还可发现血尿、蛋白尿及白细胞尿[25],显微镜下大约1/4患者的尿液中存在双折射草酸钙晶体[17]。(4)血生化:部分患者存在低白蛋白血症及低钙血症[20]。
影像学检查双源CT能够有效区分草酸钙结石与其他结石成分,对由SH导致的肾结石诊断效果较好[26]。而对于肾钙质沉着症,当病变发生在肾皮质时CT诊断效果较好,发生在肾髓质时超声诊断效果较好[2,25]。
肾活检活检可发现淡黄色半透明状的草酸钙晶体沉积于皮质区肾小管上皮细胞胞质及管腔中,并在偏振光下呈现出典型的双折射现象[20,25],其他病理发现还包括急性肾小管损伤、肾小管萎缩、肾间质单核细胞浸润等[17]。
其他检查对结石成分进行分析显示为水草酸钙石和草酸钙石的混合体[2],此外通过PCR技术发现粪便中缺乏食草酸杆菌也提示SH的存在[1]。
与PH的鉴别PH是由于乙醛酸代谢障碍引起内源性草酸合成增加的一种罕见常染色体隐性遗传病,其临床表现与SH类似,但肾脏外草酸钙沉积的发生率明显高于SH,可发病于任何年龄且患者一般无继发性病史[2]。通过检测尿草酸及血浆草酸盐水平、尿乙醇酸和甘油酸的明显增加[2]以及分析其结石成分为草酸钙单体[1]可考虑PH的存在。此外,用13C2检测肠道吸收草酸盐的能力大小对鉴别PH也有较大帮助[1]。
治 疗
有效控制病因针对SH的发病因素加以控制十分重要,包括(1)饮食干预:减少含草酸盐和脂肪丰富的食物摄入[1-2],适当补钙以此结合肠道内的草酸盐从而减少其吸收[2]。(2)慎用减肥药、保健品及富含草酸前体的药物[20]。(3)积极治疗IBD等胃肠道疾病、针对胰腺外分泌功能不全者补充胰酶[25]。(4)补充食草酸杆菌:降解肠道内的草酸盐从而减少尿草酸排泄[25]。
保守治疗(1)给予消胆胺:能够与胆汁酸结合从而降低肠道对草酸盐的通透性[25]。(2)给予草酸盐结合剂:有机海洋水状胶质(organic marin hydrocolloid,OMH)是一种不可吸收的肠道草酸盐结合剂,有研究证明其在EH患者中能够与草酸盐发生彻底结合,明显降低尿草酸排泄量并恢复患者的肠功能进而改善预后[27]。(3)摄入大量液体:研究表明摄入大量液体〔2~3 L/(m2·24 h)〕增加尿排泄量可以降低草酸钙晶体的过饱和,预防结石形成以及延缓肾功能恶化[3]。(4)碱化尿液:柠檬酸钾0.1~0.15 g/(kg· d)碱化尿液能够减少草酸钙结晶以预防结石形成[28],对于肾功能不全的患者还可用柠檬酸钠代替,同时应积极纠正代谢性酸中毒[29]。
透析治疗相比于常规透析方法,强化血液透析治疗甚至血液透析与腹膜透析联合治疗能够更有效地清除SH患者体内过量的草酸盐,当GFR处于20~30 ml/(min·1.73 m2)时就应尽早开始治疗,其目标是维持血浆草酸盐水平低于50 μmol/L,但是需注意透析后草酸盐水平可能会发生反弹[2]。
器官移植GFR降至15~30 ml/(min·1.73 m2)时需要做肾移植的相关计划[2],但目前对SH的治疗效果还缺乏足够多的数据来证明。Roodnat等[30]等报道了一项针对10例因SH行肾移植的患者预后的研究,其中5例接受活体肾移植的患者肾功能均得到了迅速恢复,另外5例接受尸体肾移植的患者只有1例迅速恢复,其余4例延迟恢复,其中3例因为并发症对移植肾功能造成影响进而调整治疗计划,1例因草酸盐沉积复发而导致移植失败。而对EH患者行肠肾联合移植可能是未来更有希望的治疗手段。Ceulemans等[31]对2例因短肠综合征导致EH的患者行肠肾联合移植,两者术后肾功能均长期维持在较好水平,尿草酸排泄趋于正常并且摆脱了肠外营养。但这一方法同样也需要在未来大量的研究中评估其治疗效果。
潜在的新治疗手段(1)口服草酸特异性酶ALLN-177:ALLN-177是一种特异性重组草酸脱羧酶,具有降解肠道内草酸盐的作用,近年来相继有研究证明口服ALLN-177能够显著降低SH患者的尿草酸排泄量[32]。(2)NLRP3炎症小体抑制剂:NOD样受体(NOD-like receptor,NLRs)是一组细胞内模式识别受体,它参与识别病原体相关分子模式和宿主来源的危险信号,装配形成炎症小体进而促进白细胞介素1β、白细胞介素18的成熟与分泌[3]。有动物实验表明NLR家族炎症小体3(NOD-like receptor family pyrin domain containing 3,NLRP3)的激活在草酸钙晶体沉积和肾衰竭的发生中起重要作用[33],抑制NLRP3可有效保护高草酸尿症小鼠的肾功能,提示NLRP3可能是SH的潜在治疗靶点[34]。
预 后
绝大多数患者经及时诊断和有效治疗后可使肾功能恢复正常,仅少数需维持性血液透析[20]。而对于预后不良的患者,主要原因包括致病因素未及时有效控制以及存在CKD病史等[20],有研究对其随访后发现超过半数需要依赖透析且死亡率高达33%[17]。
小结:SH是一种获得性草酸代谢紊乱疾病,可在机体摄入过量草酸盐及其前体物质、肠道吸收草酸盐增加以及肠道菌群失调的情况下发生,导致尿草酸增多以及草酸钙结晶,出现血尿、蛋白尿、复发性肾结石及肾钙质沉着症,部分患者进而可发生AKI及CKD。随着肾功能进行性下降,草酸盐排泄减少并在体内聚集沉积会影响其他组织器官。对于可能发病的高危人群应及时诊断从而改善预后,确诊主要通过尿草酸及血浆草酸盐水平、影像学及肾脏活检。目前针对该病的治疗措施主要包括控制病因、保守治疗、透析治疗以及器官移植,此外一些新的治疗手段需要进一步探索其疗效。

