Ag2O/MOF-101复合材料的合成及吸附脱硫性能研究
王 燕,管 旭,石志强,蔡旺锋
(天津大学化工学院,天津300350)
目前,市场上绝大多数的燃油产品都含有微量含硫化合物,含硫化合物的存在不仅腐蚀设备,而且会污染环境,对人体健康产生危害.因此,对燃油制品中含硫化合物的脱除具有重要意义.
目前,在石油炼制工业中应用最为成熟和广泛的脱硫技术是催化加氢脱硫技术[1-3],它需要在高温、高压的条件下完成,并且对噻吩类含硫化合物的脱除效果不佳.吸附脱硫技术由于操作条件温和,不需要消耗 H2,并且可以有效脱除含量较低的噻吩类含硫化合物,已引起研究者们越来越多的关注.Takahashi等[4]通过考察 Cu(I)-Y、Ag(I)-Y、Na-Y、Na-ZSM-5、H型超稳定Y沸石(H-USY)、活性炭、改性的活性氧化铝等吸附剂对苯/噻吩体系的吸附脱硫效果,通过自然键轨道等分子轨道理论进行计算和分析,提出了 π络合吸附脱硫理论.Yu等[5]研究了用不同金属离子改性后的活性炭在二苯并噻吩模型油中的吸附性能,结果表明,在实验测试的不同金属离子中,Ag+改性后的活性炭对二苯并噻吩表现出最强的吸附性能.
当前的吸附脱硫技术研究主要集中在两个方面:一是开发对含硫化合物吸附容量大,同时又较为经济的吸附剂;二是提高吸附剂对含硫化合物的吸附选择性.目前,吸附脱硫中常用的吸附剂主要有活性炭[6]、金属氧化物[7]、硅胶[8]、沸石[9]、金属有机骨架(metalorganic framework,MOF)[10]等.其中,由于 MOF 材料是一种以金属离子为中心节点,刚性有机分子为配体,通过配位键作用组装而成,具有高度有序的周期性网格结构的新型材料,所以它既有传统多孔材料孔隙率大和比表面积大等特点,又有其自身特殊的优势,如孔道形状大小可调、表面易修饰和具有开放的金属活性位点等[11-13].MOF可以通过有机配体与含硫化合物间的相互作用实现对硫化物的吸附,因此,MOF材料不仅被广泛应用于催化、气体储存等领域[14-16],而且在吸附脱硫领域也具有广阔的应用前景[17-19].由于现实油品中往往含有芳烃,而芳烃中的苯环与噻吩类含硫化合物具有相似的π结构,导致二者在吸附过程中存在较强竞争性.所以,制备高选择性的MOF脱硫吸附剂具有非常重要的意义.
本文首先通过热溶剂法在较低温度下合成了以Cu2+为中心离子、2-溴对苯二甲酸为配体的Cu2[o-Br-C6H3(CO2)2]2(H2O)2·(DMF)8(H2O)2(简称为 MOF-101).为了提高其在甲苯/甲噻吩竞争体系中对噻吩的选择吸附性能,在其表面负载Ag2O纳米粒子进行改性,得到了改性的 Ag2O/MOF-101复合材料.通过制得的复合材料在模型油中的吸附实验,得到适宜的吸附条件,并将 Ag2O/MOF-101复合材料应用于模型油中痕量噻吩的脱除.通过 MOF-101和Ag2O/MOF-101复合材料在噻吩/甲苯模型油中的吸附实验,研究了Ag2O纳米粒子的引入对复合材料吸附容量和选择吸附性的影响.结果表明,Ag2O纳米粒子的引入可以有效增强复合材料在低浓度下的脱除噻吩的性能,提高复合材料在甲苯/甲噻吩竞争体系中对噻吩的选择吸附性能.
1 实验材料和方法
1.1 实验原料与试剂
2-溴对苯二甲酸(C8H5O4Br,98%),南京盛必诚华工科技有限公司生产;三水合硝酸铜(Cu(NO3)2·3H2O,99%)、硝酸银(AgNO3,Ar)、N,N-二甲基己酰胺(DMF;C3H7NO,>99.8%)、正辛烷(C8H18,99%)、噻吩(C4H4S,98%)、甲醇(CH3OH,HPLC),天津元立化工有限公司生产.
1.2 吸附剂的制备
1.2.1 MOF-101的合成
MOF-101的合成方法在文献[20]所述的基础上进行了改进.具体如下:称取 0.41g(1.64 mmol)2-溴对苯二甲酸和 0.4g(1.64 mmol)三水合硝酸铜,充分溶解于 40 mL DMF,转移至 50mL聚四氟乙烯内衬的高压反应釜中 70℃反应 24h.反应完成后过滤得到固体产物并用DMF洗涤3~5次,浸泡于DMF中保存.
1.2.2 Ag2O/MOF-101的合成
称取 0.02g、0.04 g、0.10 g硝酸银分别溶解于30 mL DMF,并各加入1.0g MOF-101后在50mL聚四氟乙烯内衬的高压反应釜中70℃反应8h.反应完成后过滤得到固体产物并用 DMF洗涤 3~5次,浸泡于DMF中保存.用0.02g、0.04g、0.10g硝酸银制备得到的复合材料分别用 Ag2O/MOF-101(L)、Ag2O/MOF-101(M)、Ag2O/MOF-101(H)表示.
1.3 表征方法和仪器
粉末XRD在Bruker D/max 2500型X射线衍射仪上测试,扫描速率 10(°)/min,扫描范围 5°~70°,采用 Cu Kα射线(λ=0.15405nm),功率为 2000W(50kV,40 mA).傅里叶红外光谱在 Nicolet FTIR-170SX 型光谱仪上测试,采用 KBr压片,扫描范围400~4000cm-1.SEM 扫描电镜图和 EDS图在日本日立公司制造的S-4800型场发射扫描电子显微镜上测试得到.XRF用 Bruker S4 Pioneer型荧光光谱仪测试,测试电压 40kV.吸附剂的 N2吸附-脱附等温线采用美国Micromeritics公司制造的ASAP-2010型吸附仪测定.
1.4 吸附脱硫性能测试
1.4.1 模型油的配制
为了研究复合材料对噻吩的选择吸附效果,配置了 A、B两种模型油.模型油 A以噻吩为目标吸附物,正辛烷为溶剂,初始硫质量浓度为 1000mg/L.模型油 B以噻吩为目标吸附物,正辛烷为溶剂,甲苯为添加剂,初始硫质量浓度为 1000mg/L,甲苯的质量分数为10%.
1.4.2 吸附脱硫实验
在开始吸附脱硫实验前,首先将吸附剂放入真空干燥箱50℃干燥10h进行活化.称取0.05g活化后的吸附剂和 20g模型油,加入 50mL 带盖广口瓶中,放入摇床 30℃恒温吸附 5h.测定吸附前后模型油中噻吩和甲苯的浓度.模型油中目标吸附物的含量由高效液相色谱法测得,流动相为 90%的甲醇-水混合液,流动相流速为1.0mL/min.
2 结果与讨论
2.1 吸附剂的表征
2.1.1 傅里叶红外光谱
为了测定制备得到MOF-101和Ag2O/MOF-101的组成,以及吸附过程对其组成和结构的影响,对吸附前后的MOF-101和Ag2O/MOF-101进行FT-IR测试,测试结果如图1所示.由图1可知,在MOF-101的红外谱图中,3440cm-1附近的宽峰是由材料表面吸附水的羟基和 H—O—H 振动产生.1681~1550cm-1和 1430~1340cm-1处的特征峰分别对应了羧基官能团的非对称和对称伸缩振动,567cm-1处的特征峰对应了 C—Br的弯曲振动,说明制得的MOF-101材料中含有2-溴对苯二甲酸,这与文献[20]报道的相一致.由图 1还可以看出,吸附前后 MOF-101和Ag2O/MOF-101除表面吸附水的宽峰外,红外图谱大致相同,表明Ag2O颗粒的负载以及在模型油中的吸附过程均没有引入新的官能团,也没有破坏复合材料中 MOF-101本身的组成和官能团结构,吸附过程应为物理吸附过程.
2.1.2 X-射线衍射
为了确定制得的MOF-101和Ag2O/MOF-101的晶体结构,对其进行XRD测试,结果如图2所示.从图 2(a)可以看出,MOF-101和 Ag2O/MOF-101的主要特征峰位置与文献[20]报道的标准模拟曲线一致,进一步论证了本实验制得的MOF-101晶体结构的准确性.由图 2还可以看出,Ag2O/MOF-101复合材料的谱图与 MOF-101相比无明显变化,表明 Ag2O颗粒的负载并未破坏 MOF-101本身的晶体结构,这与FT-IR的测试结果相一致.另由图 2(b)可知,在Ag2O/MOF-101的谱图中,2θ=38.6°处出现了明显的特征峰,该特征峰对应了六方晶型 Ag2O 的(101)晶面,说明Ag2O成功负载到MOF-101表面.
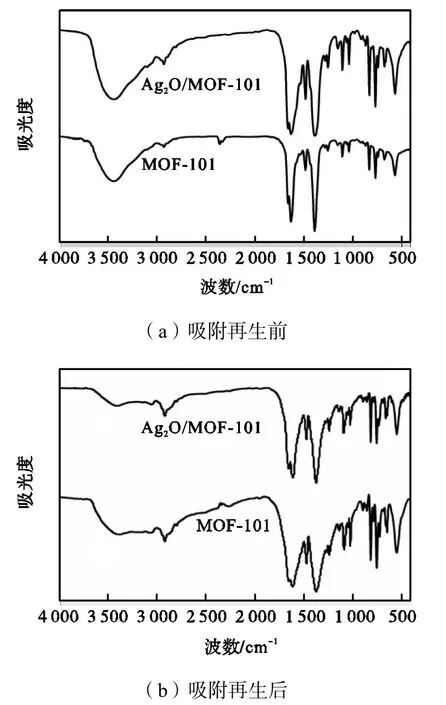
图1 吸附再生前后的 MOF-101和 Ag2O/MOF-101的FT-IR谱图Fig.1 FT-IR spectra of MOF-101 and Ag2O/MOF-101 before and after adsorption and regeneration
2.1.3 X-射线荧光光谱
为了研究在复合材料的制备过程中 Ag+盐浓度对 Ag2O负载量的影响,对实验制得的 MOF-101和多种Ag2O/MOF-101复合材料进行X-射线荧光光谱测试,结果如图 3所示.由图 3可知,复合材料中Ag2O的负载量从高到低依次为Ag2O/MOF-101(H)>Ag2O/MOF-101(M)>Ag2O/MOF-101(L).由此可知,Ag2O/MOF-101复合材料中 Ag2O负载量随制备过程中Ag+盐浓度的提高而增加.
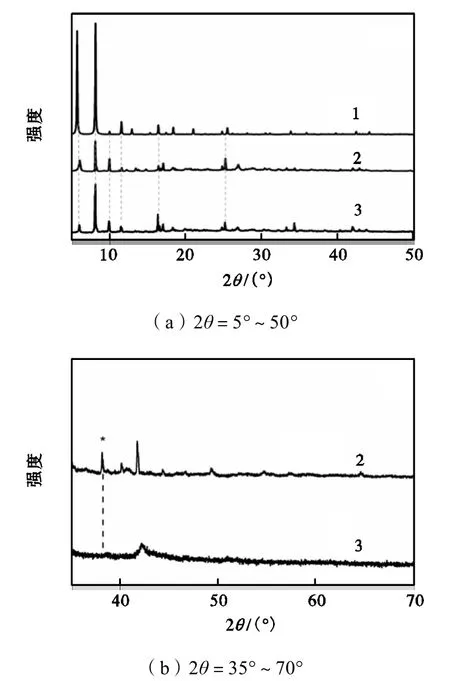
图2 MOF-101和Ag2O/MOF-101在不同2θ时的XRD谱图Fig.2 XRD patterns of MOF-101 and Ag2O/MOF-101 with different 2θvalues

图3 MOF-101和不同Ag2O负载量的Ag2O/MOF-101复合材料的XRF谱图Fig.3 XRF spectra of MOF-101 and Ag2O/MOF-101 adsorbents with different Ag2O loadings
2.1.4 扫描电镜
为了观察真空活化后 MOF-101和 Ag2O/MOF-101的形貌特征,对其进行SEM测试,测试结果如图4所示.从4(a)可以看出,在活化后的MOF-101中,表面较为平整的片状物相互堆叠,形成层状结构,层间留有孔隙,形成狭缝形孔道,增大了 MOF-101的比表面积,为吸附过程提供了更多的有效活性位点.如图 4(b)和(c)所示,球状 Ag2O 纳米颗粒被成功负载在MOF-101层间和表面.另由图4(c)还可以看出,当负载量过大时,Ag2O会在 MOF-101表面形成堆叠和包覆,使 MOF-101的部分孔道结构被覆盖,这可能会影响复合材料对噻吩和甲苯的吸附效果.

图4 MOF-101和Ag2O/MOF-101的SEM图像Fig.4 SEM images of MOF-101 and Ag2O/MOF-101
2.1.5 N2吸附-脱附等温线
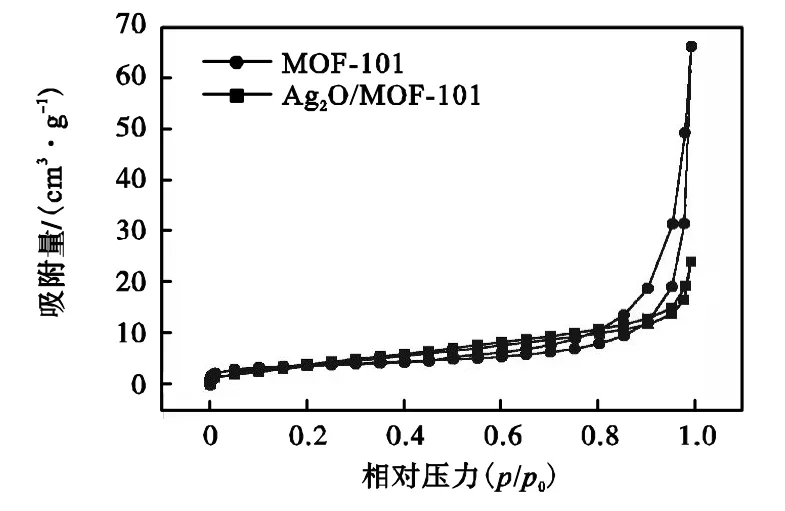
图5 MOF-101和Ag2O/MOF-101的N2吸附-脱附等温线Fig.5 N2adsorption-desorption isotherms of MOF-101and Ag2O/MOF-101
利用N2吸附-脱附法对MOF-101和Ag2O/MOF-101材料进行孔道结构分析,结果如图5所示.MOF-101的BET表面积和DFT孔隙体积分别为16.8 m2/g和 0.154 cm3/g;Ag2O/MOF-101的 BET表面积和DFT孔隙体积分别为 16.6 m2/g和 0.624cm3/g,负载Ag2O后的复合材料孔隙率明显增大.由图 5可知,MOF-101的N2吸附-脱附曲线出现了H3型滞后环,表示材料中含有片状粒子堆积而成的狭缝孔道;Ag2O/MOF-101的N2吸附-脱附曲线出现了H4型滞后环,表示材料中的孔道主要由类似层状结构产生.造成这种差异的原因是,粒状 Ag2O的负载在一定程度上改变了原有的孔道形状,这也与 SEM 的结果基本一致.
2.2 吸附性能测试
2.2.1 时间和Ag2O负载量对吸附脱硫性能的影响
为了研究时间对制得的吸附材料吸附性能的影响,测试了 30℃时,5h内 0.5g吸附剂在 20g 1000 mg(S)/L的模型油A中对噻吩的吸附量随时间的变化曲线,结果如图 6所示.从图 6可以看出,各吸附材料在模型油 A中对噻吩的吸附均在 180 min时基本达到平衡,平衡时 MOF-101、Ag2O/MOF-101(L)、Ag2O/MOF-101(M)、Ag2O/MOF-101(H)的吸附量分别为 27.1、25.8、22.7、19.7mg(S)/g(MOF).由此可知,随着Ag2O负载量的提高,Ag2O/MOF-101复合材料对噻吩的吸附量逐渐下降.这是由于 Ag2O在 MOF-101表面的包覆使得部分孔道被覆盖,使活性吸附位点减少.这在一定程度上说明,为噻吩分子的吸附提供有效活性位点的主要是基底材料 MOF-101,而非负载的 Ag2O颗粒.该结论与 Mckinley等[8]报道的 Ag+不为有机硫化物提供有效吸附位点的结论相一致.基底材料 MOF-101对噻吩分子的吸附过程为物理吸附.根据 Pearson的硬软酸碱理论[21],MOF-101中的金属中心可以与噻吩产生的离域π电子相互作用.同时,MOF-101也可以通过自身骨架产生的电场与被吸附物之间的静电相互作用和色散力,实现对噻吩分子的吸附.

图6 不同吸附剂在模型油 A中对噻吩的吸附量随时间的变化曲线Fig.6 Effect of time on MOF-101 and Ag2O/MOF-101 adsorptive capacities for thiophene in model oil A
由图6中吸附量随时间变化的数据,根据准二阶动力学方程,计算得到吸附剂对模型油中噻吩的吸附动力学常数k2,方程式为

式中:k2为准二阶平衡动力学常数,mg/(mg(S)·min);t为吸附时间,min;qe为平衡时的吸附脱硫量,mg(S)/g;qt为t时刻的吸附脱硫量,mg(S)/g.计算结果如表 1所示.由表 1可知,拟合误差系数R2均在0.990以上,表明该吸附过程符合准二阶动力学模型.复合材料 Ag2O/MOF-101的准二阶平衡动力学常数k2均大于 MOF-101,表明负载 Ag2O后复合材料的吸附速率得到提高.其中 Ag2O/MOF-101(H)的速率常数低于 Ag2O/MOF-101(M),表明 Ag2O负载量过大时,负载的 Ag2O在 MOF-101表面的包覆作用会阻碍噻吩在 MOF-101中的吸附.因此,从计算结果来看,在3个Ag2O/MOF-101样品中,最适宜的Ag2O负载量为Ag2O/MOF-101(M)的2.7%.这与深度脱硫实验和选择吸附实验的结果相一致.

表1 不同材料在模型油A中对噻吩的吸附动力学参数Tab.1 Kinetic parameters of thiophene adsorption by MOF-101 and Ag2O/MOF-101 in model oil A
2.2.2 温度对吸附脱硫性能的影响
为了研究温度对制得的吸附材料吸附性能的影响,测试了 20、30、40、50℃时,0.5 g不同吸附材料在 20g 1000 mg(S)/L的模型油 A中对噻吩的吸附量,吸附时间为3h,实验结果如图7所示.从图7可以看出,20~50℃各吸附材料对噻吩的吸附容量先升后降,最佳吸附温度约为 30℃.造成这一现象可能的原因是,适当地提高温度有利于噻吩分子在MOF-101孔道中的扩散;但同时,随着温度的升高,极性噻吩分子运动活跃,取向力变弱,与 MOF-101骨架间的相互作用力被削弱,使噻吩分子的脱附更易进行.
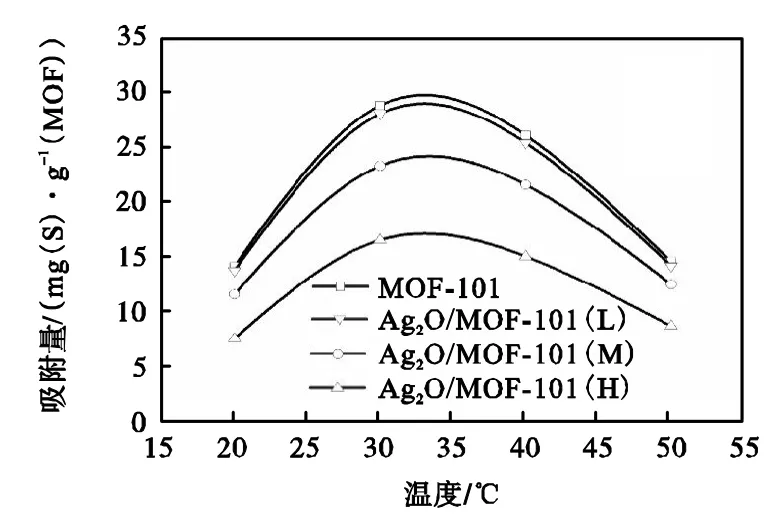
图7 不同吸附剂在模型油 A中对噻吩的吸附量随温度的变化曲线Fig.7 Effect of temperature on MOF-101 and Ag2O/MOF-101 adsorptive capacities for thiophene in model oil A
2.2.3 油剂比对吸附脱硫性能的影响
为了研究吸附过程中,模型油和吸附材料的质量比对复合材料吸附性能的影响,测试了 30℃ 时0.5 g MOF-101和 Ag2O/MOF-101(M)在不同量的1000 mg(S)/L的模型油 A中对噻吩的吸附量,吸附时间为 3 h,结果如图 8所示.从图 8可以看出,MOF-101和 Ag2O/MOF-101(M)对噻吩的吸附量随着油剂比的提高,表现出先增大而后趋于平衡的趋势,而 Ag2O/MOF-101(M)的吸附量先于 MOF-101达到最大值.这是由于在较低油剂比条件下,吸附剂对模型油而言是过量的,复合材料中 MOF-101为噻吩提供充足的吸附位点,此时负载的Ag2O颗粒对部分吸附孔道的包覆没有削弱复合材料的脱硫效果,同时,另一方面,Ag2O与噻吩间的相互作用促进了基底材料MOF-101中吸附位点的充分利用.
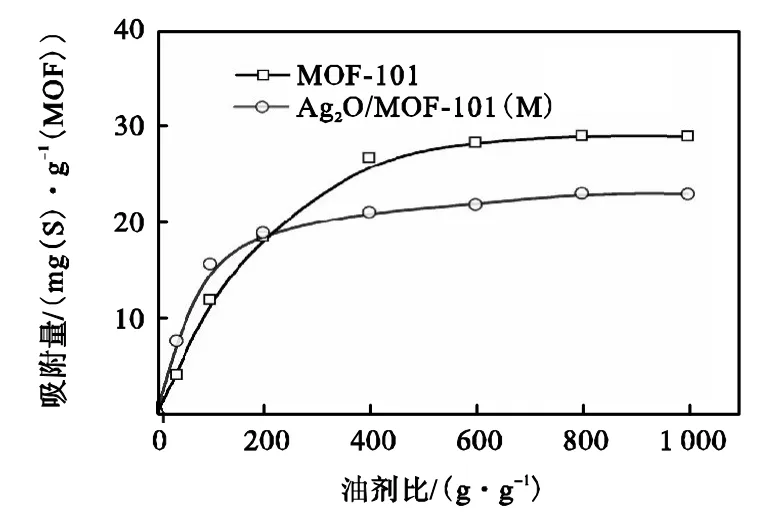
图8 MOF-101和 Ag2O/MOF-101(M)在不同油剂比条件下对噻吩的吸附量Fig.8 Effect of oil/adsorbent mass ratio on MOF-101 and Ag2O/MOF-101(M)adsorptive capacities for thiophene
2.2.4 深度脱硫测试
为了进一步论证 Ag2O颗粒对复合材料脱硫效果的影响,实验测试了 30℃ 时 5.0g吸附剂在 20g 50 mg(S)/L的模型油 A中对噻吩的吸附量,吸附时间为 3h,结果如表 2所示.由表 2可知,相较于MOF-101,负载了 Ag2O颗粒后的复合材料表现出更好的脱硫效果,其中 Ag2O/MOF-101(M)脱硫效果为最优,将模型油的硫质量分数从 50×10-6降低至8.2×10-6.实验中模型油和吸附剂中有效吸附成分MOF-101的质量比如表2所示,吸附剂均为过量,由此可知,在吸附位点充足的条件下,负载的 Ag2O颗粒能有效增强复合材料对模型油中痕量噻吩的脱除效果.Ag2O颗粒与噻吩间的相互作用将进一步在选择吸附实验中讨论.
2.2.5 吸附选择性测试
为了研究复合材料选择吸附含硫化合物的能力,测试了30℃时0.5g制得的吸附材料分别在20g A、B两种模型油中对噻吩的吸附量,结果如图9所示.

表2 不同吸附剂在模型油A中对噻吩的深度脱硫数据Tab.2 Deep adsorption of thiophene by adsorbents in model oil A
从图 9可以看出,对每一种吸附材料来说,在模型油B中对噻吩的吸附量相较于在A中均有不同程度的下降,这表明甲苯与噻吩之间存在吸附竞争.其中,对于 MOF-101,甲苯的竞争吸附使其对噻吩的吸附量降低了60%,而同样条件下Ag2O/MOF-101(M)对噻吩的吸附量只降低了 2.9%,远低于 MOF-101,表明 Ag2O的负载可以显著削弱甲苯的吸附竞争性.从图9中模型油B的吸附数据可知,在存在甲苯的情况下,较于 MOF-101,负载了 Ag2O颗粒的复合材料对噻吩表现出更高的吸附量.这表明Ag2O的负载有效提高了复合材料在甲苯/噻吩的竞争体系中对噻吩的选择吸附能力.
为了进一步研究复合材料对噻吩的选择吸附性能,测试了制得的吸附剂在模型油 B中对噻吩和甲苯的吸附量,分别用Q1和Q2表示,吸附剂对噻吩的选择吸附性用α表示为

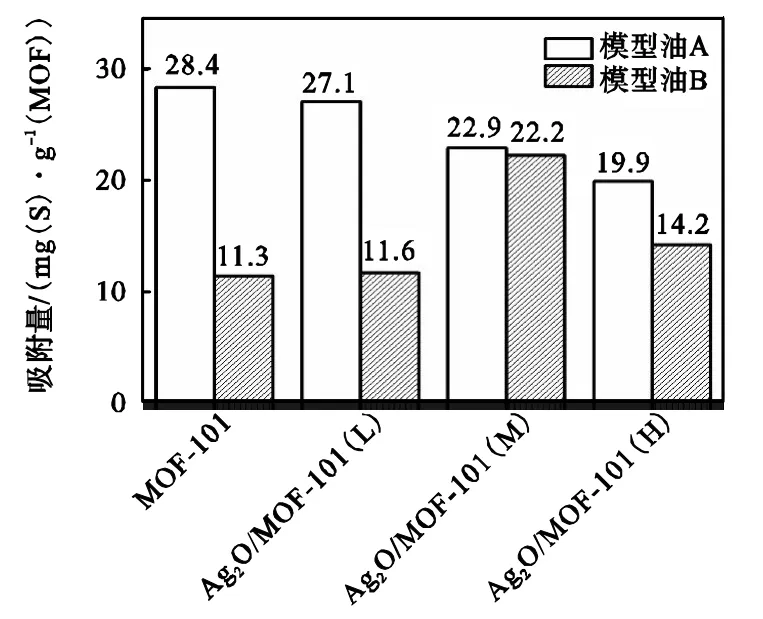
图9 不同吸附剂在A、B两种模型油中对噻吩的吸附Fig.9 Adsorption of thiophene in model oils A and B by different adsorbents
实验结果如表3所示.由表3可知,在含有甲苯/噻吩竞争体系的模型油B中,Ag2O/MOF-101复合材料对噻吩的选择吸附能力显著强于 MOF-101,且随着Ag2O负载量的提高,复合材料吸附剂对甲苯的吸附量逐渐减少,对噻吩的吸附量整体提高,表明在本实验中 Ag+和甲苯、噻吩间的相互作用形式存在差异.甲苯和噻吩具有相似的环状结构,均可产生离域π电子,Ag+可以通过 π络合键与甲苯和噻吩相互作用.同时,噻吩分子也可以通过 S原子带有的孤对电子与 Ag+相互作用[22].甲苯和噻吩的吸附量随 Ag2O负载量变化的差异表明二者和 Ag+间相互作用存在差异,因此π络合键并非Ag+与噻吩分子间的主要作用形式.由此可以推断,Ag+更易通过与 S原子间的相互吸引实现对噻吩分子的优先选择.此外,随着Ag2O负载量的提高,吸附剂对噻吩的吸附量能先升后降,是因为过多的 Ag2O颗粒在 MOF-101表面形成团聚,阻塞孔道,降低了暴露在溶液中的活性吸附位点数量.
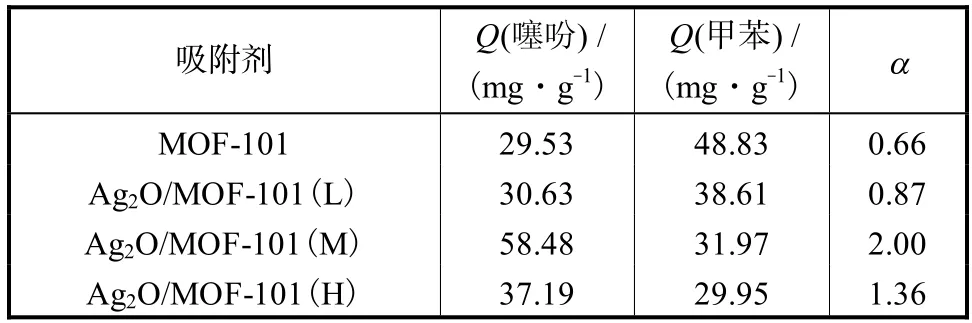
表3 不同吸附剂在模型油 B中对噻吩和甲苯的吸附量及选择吸附性对比Tab.3 Adsorption capacities and selective adsorption for thiophene versus toluene by different adsorbents in model oil B
3 结 语
通过热溶剂法在较低温度下成功合成出 MOF-101,并通过负载Ag2O纳米颗粒对其进行了改性.通过多种表征手段得到 Ag2O/MOF-101复合材料的组成、结构和形貌特点.在 Ag2O/MOF-101复合材料中,基底材料 MOF-101由片状物堆叠形成层状结构,表面具有狭缝形孔道,Ag2O颗粒负载在 MOF-101层状结构的层间和表面.
通过MOF-101和Ag2O/MOF-101复合材料在不同种模型油中的吸附实验,发现在 Ag2O/MOF-101复合材料中,基底材料 MOF-101提供对含硫化合物的有效吸附位点,负载的Ag2O颗粒在吸附位点充足的条件下增强复合材料对噻吩的吸附脱除效果,Ag2O 负载量为 2.7%时,Ag2O/MOF-101(M)将模型油的硫含量从 50×10-6降低至 8.2×10-6.通过 MOF-101和 Ag2O/MOF-101复合材料在噻吩/甲苯的竞争体系模型油中的吸附实验,发现负载的Ag2O颗粒通过 Ag+与噻吩中 S原子之间的相互作用实现复合材料对噻吩的选择吸附性的提高.MOF-101和Ag2O/MOF-101对噻吩的吸附过程符合准二阶动力学模型,拟合系数均在0.990以上.

