羟基磷灰石-果胶复合纳米粒的制备与表征
姚芳莲,罗巧悦,郭 旗,田 亮,李俊杰
(天津大学化工学院,天津 300350)
羟基磷灰石(HAp)是天然骨的主要无机矿物组成部分,无细胞毒性,能支持多种细胞的黏附和生长.相比于微米级 HAp,纳米 HAp的可塑性得到明显提升,降解速率得到明显改善.此外,纳米HAp的比表面积比较高,利于提高细胞附着、生长行为[1-3].然而,纯的 HAp纳米颗粒稳定性差,容易发生团聚,形成较大的颗粒,失去纳米材料的特性,致使其细胞摄取困难,同时这种聚集行为在体内应用时容易引发血管堵塞,使其体内的应用受到很大的限制[4-5].因此,对 HAp纳米颗粒进行修饰,提高 HAp的稳定性,减少团聚现象的发生,是推进其在生物医用方面应用的关键问题之一[6-7].
果胶是一种富含半乳糖醛酸和半乳糖醛酸甲酯单元的天然多糖,是植物的骨骼组织,其结构与哺乳动物细胞外基质中发现的多糖相似.果胶具有良好的生物相容性,而且能够在体内有效降低血糖和胆固醇含量[8],近年来已在生物医药、化妆品等行业得到广泛应用[9].此外,由于其高分子质量和聚阴离子本质属性,果胶可与金属阳离子发生反应,形成物理动态的物理交联结构.例如,Dutta等[10]通过果胶与Ca2+交联形成纳米粒,成功将 Fe3O4和奥沙利铂药物包载到其中,构建了载药纳米粒子,结果发现该载药纳米粒对负载药物具有明显的缓控释放作用.本课题组也成功在壳聚糖/果胶聚电解质配合物中形成 HAp,结果显示该 HAp体系可调控细胞的黏附和生长,相比微米级HAp表面,纳米级HAp表面更能促进间充质干细胞向成骨细胞分化[11],为 HAp基骨组织工程用支架材料的研制提供了一条可行性途径.
本文利用果胶分子链上羧基与金属离子的络合能力,原位制得 HAp与果胶的复合纳米粒子(HAp@pectin),从分子水平上系统研究了HAp@pectin体系中果胶与 HAp特征基团之间的相互作用关系,研究结果可为 HAp纳米复合材料在骨组织修复及药物递送基础研究及临床应用提供实验依据和技术支撑.
1 实 验
1.1 HAp@pectin复合纳米粒的制备
将 0.1 g果胶加入 50 mL去离子水中,加热至55℃,磁力搅拌直至全部溶解.用单通道注射泵以30 mL/h的速率将 CaCl2溶液(0.02mol/L)加入其中.滴加停止后继续搅拌 1h,并以相同的速率将Na2HPO4溶液(6 mL,0.15 mol/L)加入上述果胶钙体系中,继续反应 20h,降至室温.在 9000r/min下离心分离,用去离子水冲洗3次,得到白色固体HAp@pectin.然后将其分散在 30mL去离子水中,最终获得淡蓝色的HAp@pectin浮液.
1.2 HAp@pectin粒径和Zeta电位表征
取 5mL HAp@pectin纳米粒分散液,用激光粒度仪(Malvern Nano Zeta)测量 173°处 HAp@ pectin的粒径大小及分散指数(PDI).同时测定HAp@pectin纳米粒子分散液的Zeta电位.检测温度为25℃,样品测量3次取平均值.
1.3 HAp@pectin复合纳米粒形貌观察
用滴管取少许HAp@pectin纳米粒分散液,滴加到带有支持膜的铜网上,用透射电镜(JEOL型)观察其形貌.
1.4 红外光谱分析
取HAp@pectin复合物及果胶原料,与KBr混合研磨后压片,采用红外光谱仪(Nicolet Magna-560)表征.在 4000~500cm-1范围内进行扫描 32次,记录其傅里叶变换红外光谱(FT-IR).
1.5 X射线衍射分析
将 HAp@pectin纳米复合物用玛瑙钵研磨.在Rigaku D/max2500 v/pc型X射线衍射仪上分析其晶体结构,扫描速率为 10°/min,扫描范围为 20°~70°,Cu Kα辐射,管电流为200mA,管电压为40kV.
1.6 热失重分析
分别称取5mg HAp@pectin及果胶,用综合热分析仪(ZRP-2P)在空气气氛中检测其失重行为,扫描范围为50~800℃,升温速率为10℃/min.
2 结果与讨论
2.1 HAp@pectin复合纳米粒的制备分析
果胶分子链上含有大量的羧基,其可与 Ca2+发生配位络合反应形成果胶钙凝胶(见图1).交联密度是控制该体系凝胶状态的关键因素,可以通过改变体系中 Ca2+的加入量,精确控制果胶钙凝胶的交联密度.先前的研究发现,当 Ca2+与果胶结构单元的物质的量比为1∶50时,恰好达到预凝胶状态[12].
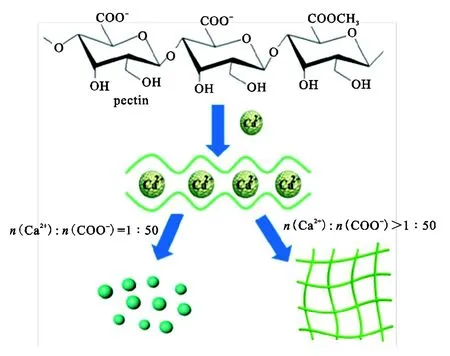
图1 果胶与不同浓度 Ca2+反应时形成凝胶及微凝胶结构示意Fig.1 Formations of hydrogel and microgel via the reactions between pectin and Ca2+ with different concentrations
本实验也发现当果胶分子链上羧基与 Ca2+的物质的量比为50∶1时,果胶钙体系可以形成稳定的微凝胶分散液.若将 PO43-引入果胶钙分散液中,则因为磷酸钙盐沉淀物的生成,原本与钙离子结合的果胶分子中的羧基将逐渐被 PO43-所取代,磷酸钙盐通过聚集、结晶而成核,果胶分子进一步吸附在磷酸钙晶体表面,最终形成具有核壳结构的HAp@pectin复合纳米粒(见图2).
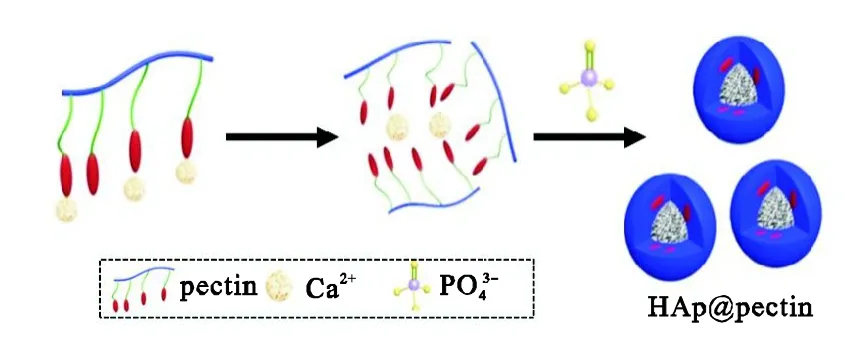
图2 通过预凝胶方法原位形成 HAp@pectin纳米粒的示意Fig.2 Schematic of the formation process of HAp@pectin nanoparticles via the pre-gel method
在上述HAp@pectin复合纳米粒的形成过程中,体系中 Ca2+与 PO43-的加入量不同,所得复合纳米粒中,磷酸钙盐的组成和晶体结构将会有明显的差别.图 3所示为加入不同量的 PO43-时,所形成的HAp@pectin的透射电镜照片.结果发现,当钙磷比(钙与磷物质的量的比)为 1∶9时,PO43-极大过量,所得 HAp@pectin复合粒子全部呈现针状晶体(见图3(a));当钙磷比为 2∶9时,产物则以球形的HAp@pectin纳米粒为主(见图 3(b)),而且在其表面观察到明显的果胶层;而当 PO43-的加入量进一步降低至钙磷比为 4∶9时,复合材料为针状晶体与球形纳米粒共存(见图 3(c)).图 4为不同钙磷比时HAp@pectin形成过程示意.分析 HAp@pectin复合纳米粒的形成过程,其中主要包括的反应过程为:①PO43-在渗透压的驱动下,扩散进入果胶钙微凝胶中;②PO43-与果胶钙凝胶中的钙离子在微凝胶中相遇,生成磷酸钙盐,由于其相对强的相互作用力,Ca2+与果胶分子中羧酸根的结合能力下降,从其表面脱落;③以形成的磷酸钙盐为核,随着 PO43-的加入并逐渐聚集成磷酸钙晶体;④自由的果胶分子重新在溶液体系中排列并通过物理、静电作用附着于磷酸钙晶体表面.表1列出了不同钙磷比对HAp@pectin纳米粒子尺寸和Zeta电位的影响,所有粒子的Zeta电位均为负值,进一步证明上述纳米粒子的形成过程.

图3 不同钙磷比HAp@pectin 纳米粒的形貌Fig.3 TEM images of HAp@pectin nanoparticles with various molar ratios of calcium and phosphorus
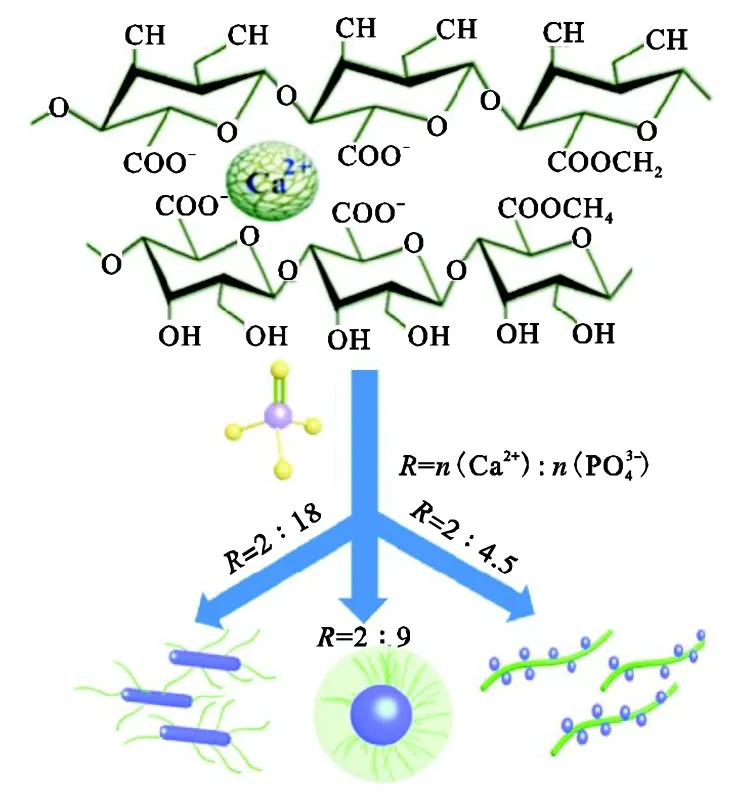
图4 不同钙磷比条件下HAp@pectin形成过程示意Fig 4 Formation process of HAp@pectin with different molar ratios of calcium and phosphorus
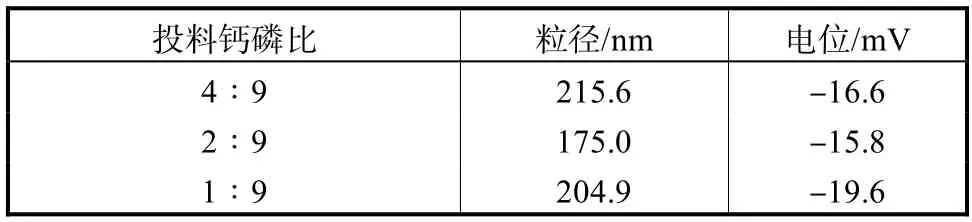
表1 不同钙磷比对 HAp@pectin纳米粒子尺寸和 Zeta电位的影响Tab.1 Effects of various molar ratios of calcium and phosphorus on the particle sizes and Zetapotentials
2.2 HAp@pectin体系中HAp核晶体结构分析
图5给出了HAp和HAp@pectin的X射线衍射图谱,两种物质均在 2θ为 25.8°(002)、31.8°(211)、32.9°(300)、39.8°(310)、49.5°(213)和 53.2°(004)处出现了 HAp晶体的特征衍射峰,这些特征衍射峰与HAp的 ICDD标准卡片一致,说明在水溶液状态和果胶钙凝胶体系中均可以形成 HAp晶体,果胶的引入和体系黏度的增加没有影响 HAp晶体的形成.但是,HAp@pectin的衍射峰强度明显低于 HAp,说明pectin的引入降低了HAp的结晶度.根据谢乐公式,晶体大小与衍射峰的半峰宽相关,半峰宽越大所表示的晶体粒径越小.特别是在果胶存在的条件下,其形成的HAp的各处的半峰宽均比纯HAp大,即粒径减小.主要原因是果胶中 —COOH使 Ca2+在果胶分子上吸附,形成相对较多成核位点,果胶与钙离子的结合能力强,导致游离钙离子浓度下降最大,所以HAp晶体的生长比较慢,形成的粒径较小,衍射峰比较宽[13].
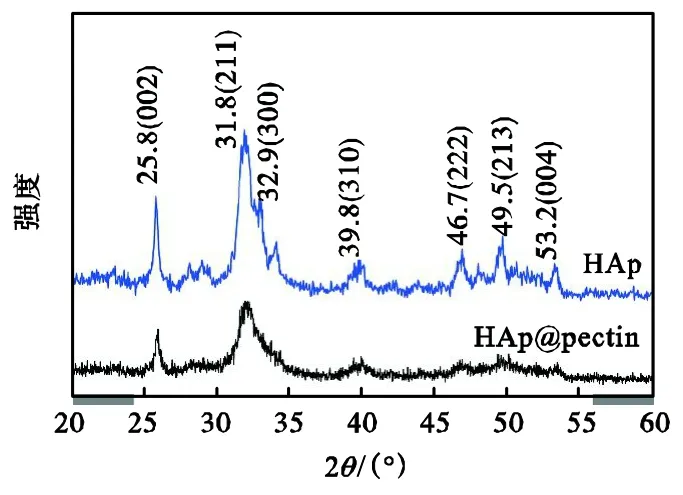
图5 Hap与HAp@pectin的X射线衍射图谱Fig.5 XRD patterns of HAp and HAp@pectin
2.3 HAp@pectin体系中分子间相互作用
采用 FT-IR探索了 HAp@pectin体系中特征官能团间的相互作用关系,如图6所示,3437cm-1处出现的吸收谱带为果胶分子链上糖环中羟基的特征吸收峰,1739cm-1与 1632 cm-1分别为果胶分子结构中—COOH和酯基上—C=O的特征吸收峰.与果胶相比,HAp@pectin在 1025cm-1处出现了 P=O的强吸收峰,607cm-1和576cm-1吸收峰归属于HAp的P—O单键,这些特征吸收峰的出现都证明了HAp在果胶凝胶中形成,与XRD测试结果一致.另外,与果胶的 FT-IR相比,1739cm-1处游离羧酸的吸收峰在HAp@pectin复合中消失,这是由于在HAp@pectin中 COO-与钙离子发生作用形成羧酸盐[14].同时在 1550cm-1及 1400cm-1可以观察到两个羧酸盐中羰基的吸收峰,而 2934cm-1处吸收谱带的吸收强度减弱,表明果胶分子中的羧基与 HAp分子间存在着较强的相互作用,是 HAp在果胶凝胶中形成的主要驱动力,这一过程与天然骨在胶原纤维上矿化的机理相似,也是通过控制体系中果胶的含量调控HAp的形成过程和晶体形貌特征的主要理论依据.

图6 果胶与HAp@pectin的红外谱图Fig.6 FT-IR spectra of pectin and HAp@pectin
2.4 HAp@pectin纳米复合体系的TGA分析
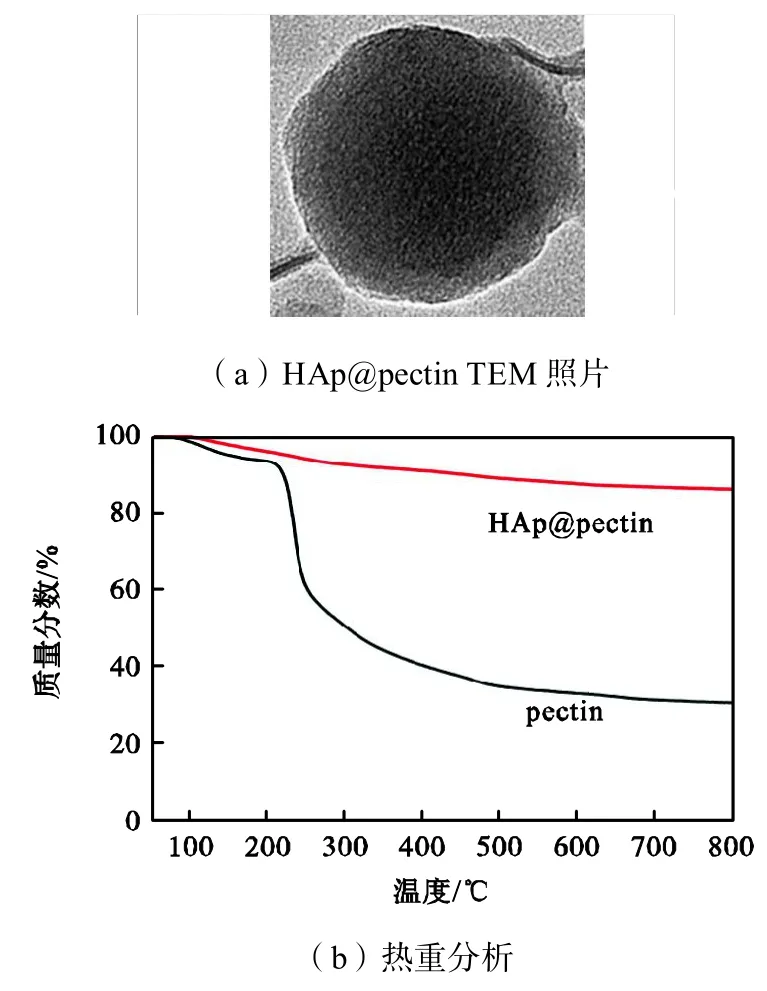
图7 HAp@pectin的透射电镜照片和果胶与HAp@pectin的热重分析曲线Fig.7 TEM image of HAp@pectin and TGA curves of pectin and HAp@pectin
图7(a)为HAp@pectin复合纳米颗粒的TEM照片,可以明显观察到其中的核-壳结构.为了进一步分析 HAp@pectin中 HAp与果胶的相对含量,对其进行了TGA测试(见图7(b)),结果发现随着温度的升高,果胶及 HAp@pectin的质量下降,根据失重情况可以算出 HAp@pectin复合体系中果胶的质量分数为 14.46%.果胶升温过程中的失重主要分为 3个阶段:第 1阶段主要是脱水过程,包括果胶分子之间的酯化反应生成的水及游离水的脱出;第2阶段为羧基分解放出二氧化碳;第3阶段则可能对应分子链上大量—OH的脱落.
3 结 语
利用果胶分子中羧基与 Ca2+的静电作用,成功制备了HAp@pectin复合纳米粒子,明确了复合体系中的分子相互作用规律及果胶组分对HAp形貌的调控作用规律.结果显示在果胶分子链上的羧基与 Ca2+配位反应的驱动下,控制钙磷比为 1∶50时,制得了稳定分散羧酸钙纳米凝胶.进一步将 Na2HPO4溶液加入果胶钙纳米凝胶分散液中,原位合成了HAp@pectin复合纳米粒.通过调节Na2HPO4的加入量,可以控制复合纳米粒的形貌及尺寸,当加入的钙磷比为2∶9时,复合纳米粒呈现球状.借助FT-IR分析证明了 HAp与果胶分子间存在着较强的相互作用.研究结果将为羟基磷灰石与多糖复合材料制备提供一定的理论基础,并拓宽其在组织工程和药物递送中的应用.

