血栓闭塞性脉管炎合并肝素诱导性血小板减少症1 例诊治报告
许岭平 王 璟
血栓闭塞性脉管炎(thrombosis angiitis obliterans,TAO)是一种累及四肢中小动脉的炎性、慢性闭塞性血管疾病;具有节段性、神经病变性、炎性内容物形成、堵塞,和反复发作为特点[1]。使用肝素后或在肝素抗凝治疗过程中,由肝素诱发的血小板减少,若同时伴有血栓形成则称为肝素诱导性血小板减少症(heparin-induced thrombocytopenia,HIT),肝素诱导的血小板减少合并血栓形成。
1 临床资料
患者,男性,13 岁,初中二年级,左下肢间歇性跛行8 月,加重3 天。既往体健,无家族遗传病史,无不良嗜好。查体:心肺腹(—);左下肢股动脉搏动弱,腘动脉及足背动脉均未及、左小腿皮温凉、右下肢正常;辅助检查:下肢动静脉超声显示,左侧髂外动脉、左侧腘动脉、左侧胫后动脉、左侧足背动脉栓塞(完全型),左下肢静脉未见明显血栓。下肢动脉血管成像(CTA)显示,左侧髂外动脉及腘动脉多出栓塞;左侧腓动脉近端由侧枝代偿,显影尚可;左侧胫前动脉、胫后动脉、腓动脉近端、中段及足背动脉、足底动脉显影差。入院诊断左下肢动脉栓塞。
入院后,第一次治疗行左下肢数字减影血管造影(DSA)+支架植入术(PTA)+导管溶栓(CDT)治疗。DSA 显示左髂外至股浅动脉开口处闭塞周围可见大量侧枝形成,股浅动脉全段显影良好;腘动脉于P1 段起始血栓性闭塞周围可见侧枝,以远及膝下三支均未见显影。PTA处理:4.0×150.0 mm Power flex 于髂外动脉闭塞段(10~12 atm)扩张2.0×150.0 mm SAVVY LONG 于股浅远端—腘动脉10 atm 扩张扩张后再次造影显示,髂外动脉闭塞段缩短并可见血栓影,左侧腘动脉以远可见血栓影。CDT 用药每隔12 h 给予80 万单位尿激酶,每隔8 h 给予30 mg 罂粟碱和40 mg 甲强龙。抗凝:采用肝素500 U/h 抗凝,监测活化部分凝血活酶时间(activated partial thromboplastin time,APTT)1.5~2.5 倍延长,纤维蛋白原(FBG)>1.0 g/L。
术后20 h 左下肢疼痛加剧、小腿皮温凉、皮肤紫绀进行性加重,复查DSA 显示,较前无明显改善并再次血栓抽吸、留置导管溶栓。考虑诊断左下肢TAO,寻找致病因子筛查结缔组织全套、血管炎五项、血糖、血沉、甲功、蛋白-C 及蛋白-S 均未见异常。头颈部CTA、全主动脉CTA、内脏动脉CTA 均正常。
确诊TAO 后,第三次拟行下肢动脉DSA+射频消融术(去交感化)。8F 动脉鞘管置换翻山鞘并经鞘送冷盐水消融导管(圣犹达),于胫前、胫后及腓动脉近端大头螺旋状放电(功率5~10 W,走水速度30 ml/min),观察阻抗变化230Ω 下降190Ω;放电时诉疼痛、酸胀、麻木,停止放电疼痛消失。在痛感明显、阻抗下降20Ω 的部位放电3 次,充分消融交感神经节从;放电并回退消融大头于腘动脉内(功率5~10W,走水速度30 ml/min消融),疼痛加重(术中给予地佐辛止痛);术后继续留置导管泵入解痉、扩管,口服“利伐沙班”抗凝;24小时后复查造影、拔管;甲强龙使用3 天后改为强的松60 mg,每月减5 mg,疗程9 个月。
由于5 月28 日晚18:15,血常规检查血小板计数为20×109/L,考虑HIT,心肌酶达3596U/L;晚21:10,患者面色苍白、四肢冰冷、右侧腹股沟区肿胀(血肿),考虑穿刺点出血;血常规检查血红蛋白82 g/L;立即停肝素抗凝、尿激酶溶栓,输血、穿刺点加压、制动。改用“阿加曲斑”抗凝、阿替普酶溶栓,继续监测血小板计数、血红蛋白等指标,表1。复查DSA 显示,股、腘动脉及膝下动脉节段性血栓伴痉挛;再次行血栓抽吸后继续导管溶栓。
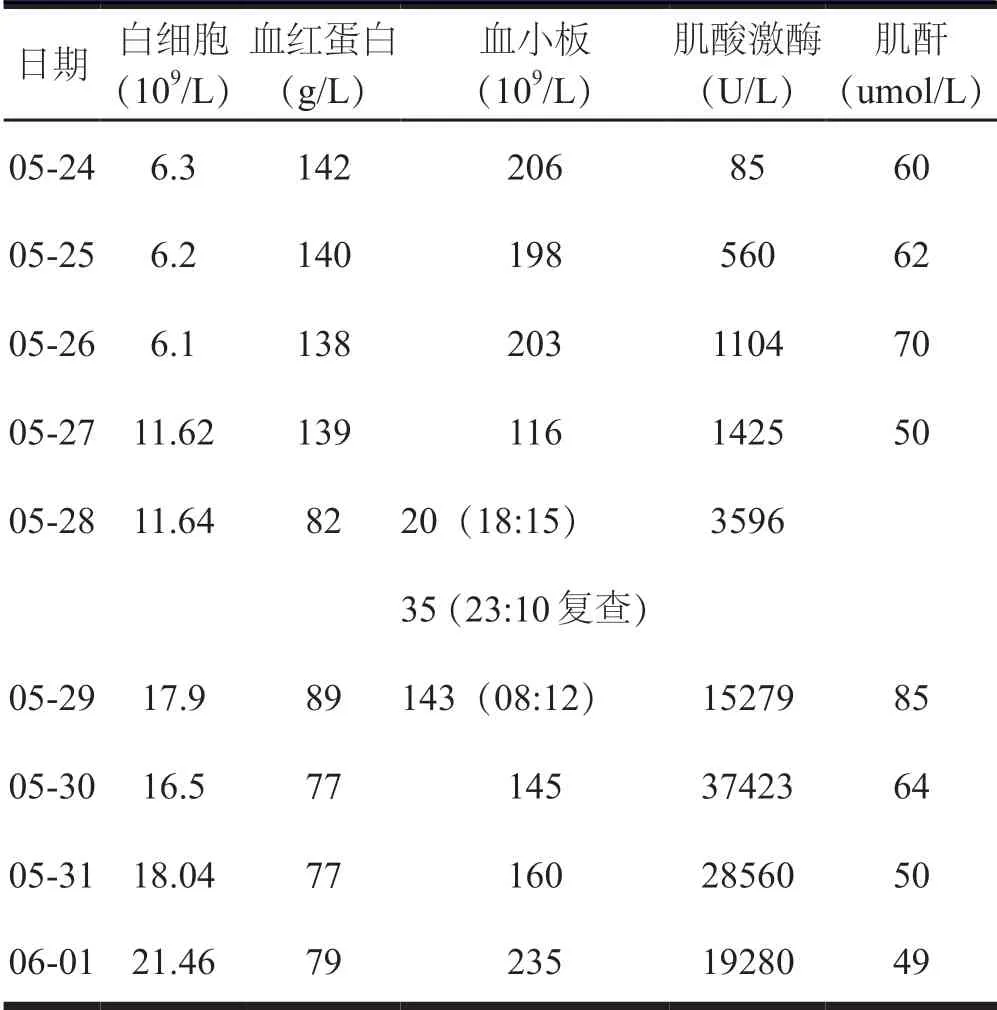
表1 患者入院期间血常规及生化指标变化
下肢组织肿胀、水疱、皮温有所改善、疼痛减轻、肌酶进行性升高,但运动感觉已丧失、神经已坏死,截肢或不可避免,但仍坚持保肢、引导干性坏疽、结痂,病程约2 月。最后造影显示,髂动脉、股动脉通畅,腘动脉、腓动脉通畅,胫前后动脉线样显影、痉挛,最后拔管,返回病房。小腿温度改善,足部冰凉、水泡形成。发生引导干性坏疽,组织坏死、感染、肾功能障碍等一系列问题。家属选择转院后截肢。
2 讨论
青少年男性左下肢间歇性跛行8 月,加重3 天,无吸烟史(不排除被动吸烟),无家族史,下肢间歇性跛行、麻木、怕冷,下肢动脉超声及DSA 均提示腘动脉及远端动脉节段性血栓、痉挛,周围侧枝循环形成;排除动脉硬化闭塞病变、糖尿病、大动脉炎、肢体动脉栓塞、雷诺病、结缔组织病及血管炎,综上所述明确TAO诊断[2]。
2019 年,中国中西医结合学会周围血管疾病专业委员会修订的血栓闭塞性脉管炎的诊断标准[3]:(1)几乎全为男性,发病年龄20~40 岁;(2)有慢性肢体缺血表现,麻木、怕冷、间歇性跛行、淤血、营养障碍改变,常累及下肢,上肢发病者少;(3)40%~60%有游走性血栓性浅静脉炎病史和体征;(4)各种检查证明,肢体动脉闭塞、狭窄的位置多在腘动脉及其远端动脉(常累及肢体的中小动脉);(5)几乎全有吸烟史,或受寒受冻史;(6)排除动脉硬化闭塞症、糖尿病性坏疽、大动脉炎、肢体动脉栓塞、雷诺病、结缔组织性血管病、冷损伤血管病和变应性血管炎疾病;(7)在疾病活动期,病人血液中IgG、IgA、IgM、抗动脉抗体、免疫复合物阳性率增高,T 细胞功能指标降低;(8)动脉造影:①病变多在腘动脉及其远端动脉;②动脉呈节段性闭塞、狭窄,闭塞端之间动脉和近心段动脉多正常;③动脉闭塞的近远端多有“树根”形测值循环动脉;④动脉没有迂曲、僵硬和粥样斑块影像。与闭塞性动脉硬化、肢端动脉痉挛病(雷诺病)、大动脉炎、糖尿病性血管病鉴别诊断。
给予药物治疗,抗血小板聚集、扩血管、肾上腺皮质激素、抗生素、中成药;手术选取截肢(趾)、血管重建、溶栓、球囊扩张(药物球囊)、射频消融等[4-7]。
HIT 的临床表现为血小板减少,血小板减少的发生率高达95%及以上,也是HIT 的首发症状。HIT 以首次使用肝素5~14 天后严重血小板减少为特征,曾用肝素治疗而再次使用24 小时内发生,血小板数量下降超过基数值50%。通常15~150×109/L。血小板下降相对比率较血小板下降的绝对值对诊断HIT 更具有特异性[8-9]。
HIT 可导致血栓栓塞(常见并发症35%~75%);静脉血栓,下肢深静脉血栓也可导致组织缺血、坏死;动脉血栓,可导致肢体或终末气管缺血性坏死、血管闭塞、心肌梗塞、截肢、多脏器衰竭、死亡等;皮损表现为注射部位局部出现的通性红斑或皮肤坏死;非特异性药物反应;发热、寒战、心动过速、呼吸困难等,见表2;HIT 临床评价和实验室结果分布,见表3;治疗时停用肝素,直接凝血酶抑制剂替代治疗(NOAc、阿加曲班、比伐卢定)输注血小板,见表4。
HIT 是肝素应用的严重并发症之一,相对常见疾病较易被忽视,是一种医源性损害,严重者危及肢体及生命。对于高度疑诊(或已确诊)的HIT,应停用一切肝素制剂,包括冲管、封管液、更换抗凝药物、监测血小板计数变化、监测血栓及出血事件,避免预防性输注血小板[10]。患者在应用肝素制剂时是应重点预防,定期复查,以早发现、早诊断、早治疗,从而避免严重不良事件发生。
表2 HIT 临床病理分型及诊断

表3 HIT 临床评价和实验室结果分布
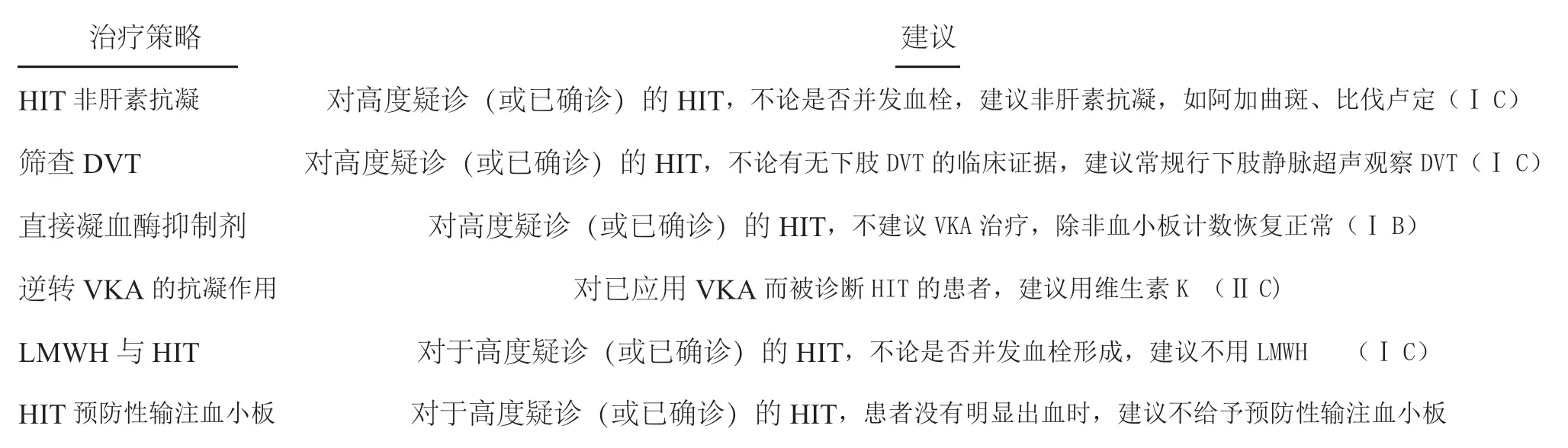
表4 美国胸内科医师学会-9 指南推荐治疗方法

