经导管主动脉瓣置换术中自膨式瓣膜支架释放预测与实际投照角度的差异性分析
郑胜能 李捷 谈文开 李光 范瑞新 罗建方
经导管主动脉瓣置换术(transcatheter aortic valve replacement,TAVR)作为一项成熟的治疗主动脉瓣狭窄(aortic stenosis,AS) 的技术[1],因其非直视特点导致对影像学评估要求较高,取决于瓣膜支架在主动脉瓣根部的三维空间中是否精准定位,因而在术前影像评估时,对于术中在X线透视下的最佳投照角度的预测显得尤为重要。多层计算机断层摄影(multislice computed tomography ,MSCT)不仅在对于TAVR术前评估起到了至关重要的作用,还能预测TAVR术中进行瓣膜支架释放的最佳投照角度[2-5]。为了瓣膜的精准定位,需要借助数字减影血管造影(digital subtraction angiography,DSA)使用垂直于主动脉瓣平面的投影进行术中瓣膜支架释放。最佳投照角度的预测能够为TAVR术中血管造影及工作投照角度提供参考,提高手术成功率的同时减少手术时间,降低手术风险。
自2010年葛均波等[6]成功完成国内首例 TAVR 以来,国内多家心脏中心相继开展了该项技术,并较多应用自膨式瓣膜支架[7-8]。然而,在TAVR操作过程中,使用MSCT预测的投照角度进行自膨式瓣膜支架定位时往往不能得到十分满意的主动脉瓣投影,需要调整投照角度后才能在最佳的投照角度下进行释放,而国内外尚缺乏相关研究。本研究拟探讨TAVR术前应用MSCT预测的投照角度与术中实际投照体位的差异,总结TAVR术中自膨式瓣膜支架释放的最佳投照角度的经验。
1 对象与方法
1.1 研究对象
回顾性收集分析2016年4月至2018年6月因有严重症状的AS在广东省人民医院接受TAVR治疗的患者共38例,均在TAVR手术前于我院行MSCT后经过图像重建分析得到术前预期的一个瓣膜支架释放投照角度,经胸超声心动图(transthoracic echocardiography,TTE)评估主动脉瓣跨瓣压差、瓣口血流速度、左心室射血分数(left ventricular ejection fractions,LVEF)等,经术前评估符合TAVR手术适应证,并经多学科会诊后认为存在外科手术禁忌证或外科手术风险过高,不适合进行传统外科手术者。所有患者在术前均给予书面知情同意。术中瓣膜支架定位时根据瓣膜释放定位需要调整投照角度以达到最佳释放投照角度,在瓣膜支架置入后复查造影及经食管超声心动图 (transesophageal echocardiography,TEE )评估瓣膜位置、功能及瓣周漏情况。
1.2 MSCT图像采集
MSCT图像采集应用主动脉全程和冠状动脉计算机断层扫描血管造影(computed tomography angiography,CTA) ,均无对比剂禁忌证。检查前4 h内禁食、禁水,TAVR术前应用西门子双源SOMATOM Definition MSCT进行扫描,扫描范围上缘起自鼻尖,下缘至小转子。冠状动脉CTA采用前瞻性心电门控旋扫描,曝光时相和采集范围根据心率设置:心率<70次/分,R-R间期70%~80%;心率≥70次/分,R-R间期40%~50%。对比剂注射方案采用对比剂团注跟踪技术,监测层面为降主动脉,采用双筒高压注射器,注射速度4~5 ml/s,经肘前静脉注射非离子型对比剂碘普罗胺(370 mgI/ml)或碘帕醇(370 mgI/ml)70~100 ml后再以同样速度注射30~40 ml 0.9%氯化钠溶液 ,注射剂量依据患者体重进行个体化设定。吸气后屏气完成扫描,扫描参数:管电压80~100 kV,管电流800~1000 mAs,机架转速0.27 s/r,准直宽度128 m m×0.625 m m,主动脉根部扫描层厚度0.75 mm,外周血管1 mm,间隔0.45 mm,矩阵512×512,螺距为0.18 mm。
冠状动脉 CTA 图像重建及分析评价分别由2名有丰富经验影像科医师进行分析。常规重建时相为75% 及45% R-R间期,必要时按照35%~85% R-R间期 (间隔10%) 进行重建。 对心律不齐患者可应用心电图编辑软件进行编辑后重建,选取血管显示最清楚的R-R间期图像作为原始图像,将重建后清晰的图像传至图像处理工作站,应用心血管后处理软件对图像进行曲面多平面重建(curved multiplanar reconstruction,CMPR)和容积重建,利用冠状动脉探针技术逐段分析冠状动脉有无狭窄,并测量狭窄程度。
主动脉全程CTA应用专门为TAVR分析定制的软件3mensio ValvesTM(荷兰3mensio医学影像公司) 评估主动脉瓣瓣环大小、钙化情况、冠状动脉开口高度、二叶式主动脉瓣或三叶式主动脉瓣(按Sievers分型)、是否横位心(心脏长轴与膈面成角大于45°)及股动脉或颈动脉入径等情况,采用CMPR软件进行分析。主动脉瓣环不是一个独立的解剖结构,它是由主动脉瓣叶连接在左心室流出道(left ventricular outflow tract,LVOT)形成的,连接这3个瓣叶最低点的虚拟环称作虚拟基底环。通过升主动脉、主动脉瓣、瓣环和LVOT的中心点产生一条基线,主动脉瓣叶基部附着形成的虚环平面被定义为三个瓣叶的最低点所在且垂直该线的平面。在本研究中,该平面被定义为主动脉瓣的兴趣区。术者在X线透视下置入瓣膜支架的理想投影是所有的主动脉窦在同一平面,右冠瓣在中,左冠瓣和无冠瓣对称地向左和向右,并能清晰显示左、右冠状动脉。在保证虚环平面与投影垂直时,理论上有无限多个并符合线性回归的角度组合能满足这一要求[9],适当手动模拟DSA时C臂旋转角度改变图像投影,向横轴方向左右旋转对应C臂左前斜(left anterior oblique,LAO)或右前斜(right anterior oblique,RAO)、纵轴方向对应头(cranial,CRA)或足(caudal,CAU)的改变,获得预测投照角度(图1)。定义投照角度在横轴方向上LAO为正方向、RAO为负方向,纵轴方向上CRA为正方向、CAU为负方向。

图 1 利用3mensio ValvesTM软件分析患者MSCT图像得到理想的最佳投影 A.TAVR术中理想的主动脉瓣投影;B.选取三个瓣叶最低点(左-红、右-绿、无-红)所确定的虚环平面与通过升主动脉、主动脉瓣、瓣环和LVOT的中心点的基线垂直;C.调整角度使左右冠状动脉开口的到较好的显示;D.调整角度当虚环平面呈一条线时,此时投影是瓣环的切线位置
术中完成入径建立后均以推荐投照角度进行主动脉根部造影,均使用VENUS-A自膨式瓣膜支架(杭州启明医疗器械有限公司),经建立良好的轨道到达预定位置后行主动脉根部造影精确定位。术者在X线透视下调整瓣膜支架使得与轨道同轴,调整角度使支架上不透线的3个标记点处于同一平面并与无冠瓣的最低点持平时,此时的投照角度被认为是合适的瓣膜支架定位及释放角度(图2),得到瓣膜支架实际投照角度。以患者左右为横轴,头尾为纵轴。定义预测投照角度与术中实际投照角度的差异超过10°为差异有统计学意义。定义预测投照角度与术中实际投照角度横轴和纵轴的差异均有统计学意义为完全不相同,横轴或纵轴的差异均无统计学意义为完全相同。

图 2 术中投照角度的调整 A.瓣膜支架经轨道送至主动脉瓣;B.回撤外鞘至3个不透线标记点,调整角度使与虚环平面重合进行瓣膜支架精准定位;C.瓣膜支架的释放
1.3 统计学分析
所有数据采用SPSS 22.0进行统计学分析。正态分布连续变量使用()表示,非正态分布连续变量使用中位数(四分位数间距)表示。分类变量用频率和百分比来描述。通过配对t检验比较推荐投照角度和实际投照角度的差异。以双侧P<0.05为差异有统计学意义。
2 结果
2.1 患者一般临床资料
共38例接受TAVR治疗的患者,其中男性20例(52.6%),年龄(74.43±6.20)岁。其中高血压病21例(55.3%),糖尿病7例(18.4%),经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)史23例(60.5%),卒中史7例(18.4%),肺部疾病13例(34.2%),肾小球滤过率(55.74±17.88)ml/min。
2.2 患者TAVR术前TTE和CTA资料
所有患者均由T T E 提示为重度A S,术前平均跨主动脉瓣压差为(58.08±19.78)mmHg(1 mmHg=0.133 kPa),跨主动脉瓣瓣口血流流速峰值为(4.89±0.76)m/s,术前LVEF 57%(23%,74%)。经主动脉CTA测量的主动脉瓣瓣环周长为(77.76±6.81)mm,主动脉瓣瓣环面积为(463.38±77.36)mm2,瓣环直径为(24.59±2.04)mm,瓣环钙化积分为677.4(41,3565)分,其中包括二叶式主动脉瓣19例和三叶式主动脉瓣19例(表1)。
2.3 TAVR介入资料
所有患者均在全身麻醉下进行手术,其中3例(7.9%)以颈动脉为入径,余下以股动脉作为入径。左心室和主动脉瓣导管监测术前跨主动脉瓣压差为(82.22±28.47)mmHg。38例患者均置入瓣膜支架,其中4例(10.5%)患者瓣膜支架释放后效果不满意,再放入一个瓣膜支架形成瓣中瓣。并于术后即刻TTE检查,轻度瓣周漏14例(36.8%),中度瓣周漏12例(31.6%),重度瓣周漏2例(5.3%),术后即刻跨主动脉瓣压差为(5.41±2.91)mmHg。术中及住院期间无死亡、冠状动脉开口阻塞、瓣膜移位、主动脉夹层并发症发生(表2)。
依据患者预测投照角度与实际投照角度分布在直角坐标系中分别描绘角度散点图,如图3所示。其中预测投照角度基本满足线性回归曲线模型,但实际投照角度存在较大差异,不符合线性回归曲线模型。进一步分析每位患者预测投照角度与实际投照角度的差异,发现38例患者中,两者完全相同14例(36.8%),均为三叶式主动脉瓣且无横位心;完全不相同13例(34.2%),均为二叶式主动脉瓣且横位心。
进一步通过配对样本t检验实际投照角度与预测投照角度,两者横轴上差异无统计学意义[(8.18°±14.68°)比(9.18°±11.25°),P=0.712]。而实际投照体位在纵轴上较预测投照角度向CAU偏移,差异具有统计学意义[(-17.05°±11.56°)比(-6.58°±15.17°),P<0.001]。
3 讨论
本研究通过回顾性分析在本中心接受TAVR治疗的患者在MSCT的指导下自膨式瓣膜支架释放预测与实际释放时投照角度的差异,发现MSCT在正确的预测使用自膨式瓣膜支架的TAVR术中,在DSA指导下瓣膜支架定位时的投照角度与实际投照角度存在明显差异。

表1 38 例患者TAVR 术前CTA 和TTE 评估资料

表2 38 例患者经导管主动脉瓣置换术资料
在TAVR瓣膜支架置入时,在满意的主动脉瓣投影下进行精确定位的重要性毋庸置疑,而C臂的调整使得最终在最佳投照角度下进行是精准定位的保障。国内推广TAVR以来,大部分使用自膨式瓣膜支架,其瓣膜支架主体上较大,由于输送装置材料特性,当释放系统经轨道放入患者主动脉瓣进行定位时,患者在平卧状态下,自膨式瓣膜支架因本身输送系统经过主动脉弓进入LOVT后存在回直力原因,会向CAU方向倾斜,以及支架主体较长,非可调控弯的输送杆顺应性较差,无法克服回直力进行调整导致整个输送系统无法保持在基线位置,这些偏差由于患者个体化的差异而显得更加明显,包括主动脉瓣天生的二叶瓣或者由于病变的瓣叶融合,心脏的横位角度也会为术中输送系统的偏移基线程度带来较大的影响。而在术前预测最佳投照角度时,是以输送轨道处于基线位置的理想情况进行预测的,从而产生差异。为了达到理想投照角度,按照瓣膜支架倾斜方向调整投照角度进行CAU方向的补偿,从而在瓣膜支架偏离基线的情况下,人为进行调整(图4),故而大多数患者实际投照角度较回归曲线模型存在纵轴方向的较大差异[5]。
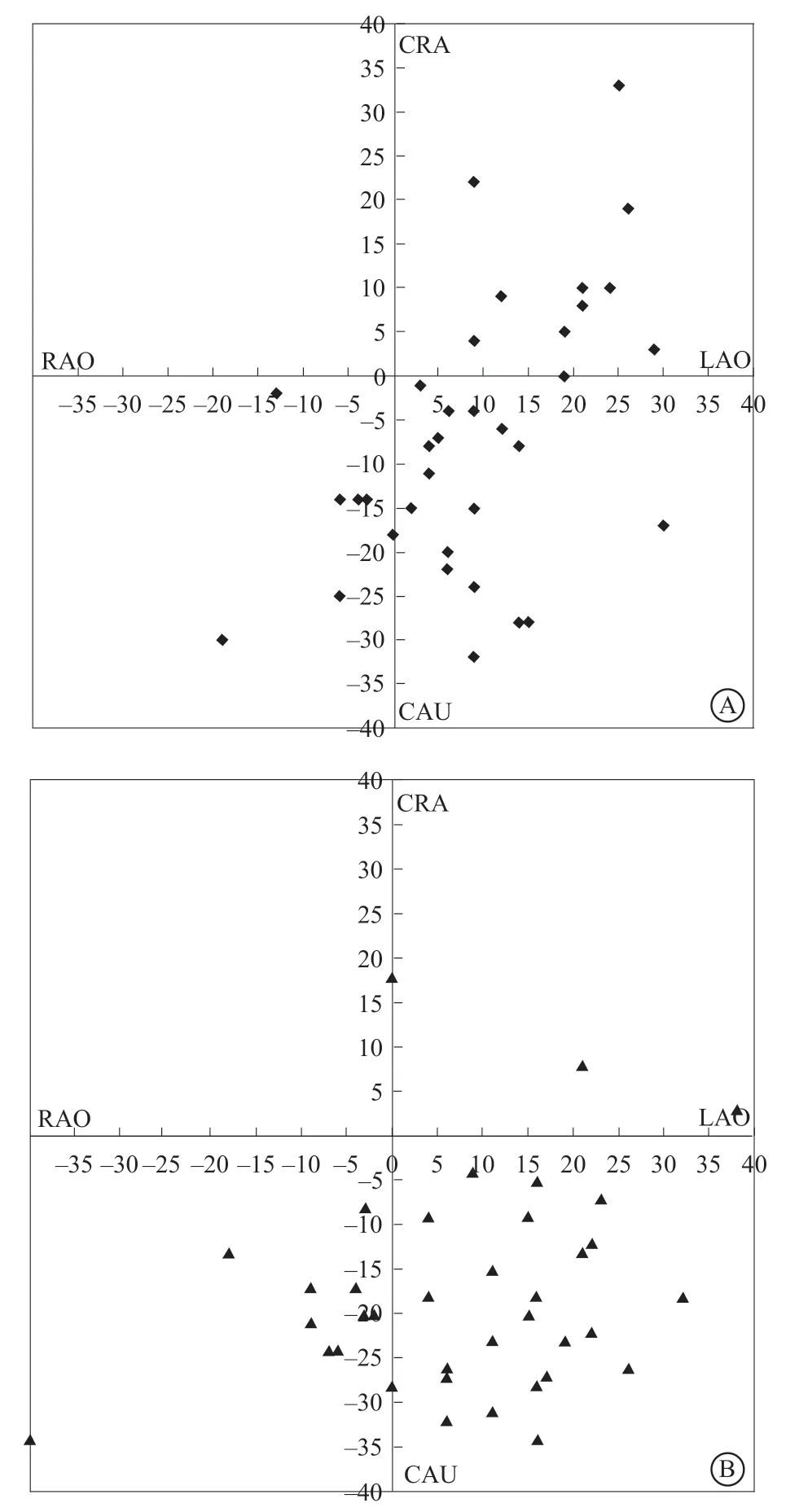
图 3 38例患者投照角度散点图 A.患者术前评估通过软件预测推荐的投照角度;B.患者在TAVR术中瓣膜支架定位释放时的实际投照角度
TAVR在国内广泛开展的同时,利用自膨式瓣膜支架置入AS患者体内达到功能性的主动脉瓣置换,精准的瓣膜支架定位与释放依据满意投照角度下主动脉瓣的投影,不正确的定位可能导致瓣膜栓塞、严重主动脉瓣关闭不全、心脏传导阻滞或左心室功能受损[9]。为了在TAVR中实现精确的装置定位,借助MSCT在术前预测满意主动脉瓣投影的投照角度时,应当考量患者个体化差异及使用瓣膜支架系统自身特点,作为一种非直视、经导管的操作技术,诸多因素的综合考虑,制定相对完善的诊疗方案对于TAVR治疗的成功性有着重要的意义,可以提高TAVR成功率,减少手术时间,降低手术风险。

图 4 输送装置实际位置与基线的偏移 图中白色实线为术前应用MSCT图像以通过升主动脉、主动脉瓣、瓣环和LVOT的中心点产生一条基线,白色虚线为瓣膜支架输送系统送至主动脉窦处实际位置
本研究局限之处在于本中心TAVR开展时间较短,样本量较少,因为患者主动脉瓣解剖结构个体化差异,如主动脉弓角度无法量化探究其对输送系统的影响,以及自动化软件工具或手动评估预测的最佳投照角度也存在潜在的差异。本中心会进一步对行TAVR的患者进行定期随访,并对今后进行TAVR的患者制定相应的研究,对自膨式瓣膜支架在释放中投照角度补偿的定量化进行探究。如果患者需要更大的投照角度时,射线需穿过患者组织层后发生改变,在不影响图像质量的情况下需要改变曝光条件时,基于减少辐射暴露方面也是需要酌情考虑的。
在实现TAVR自膨式瓣膜支架的精准定位时,应当考虑个体化差异(瓣叶分型和是否横位心)和自膨式瓣膜支架输送系统回直力造成与预测基线偏移且顺应性较差难以调整的特点,在瓣膜支架释放的最佳投照角度预测和选择时,需要进行适当的CAU补偿,有助于完善TAVR术前评估准备工作,并提高手术成功率。

