原发性肾上腺平滑肌肉瘤2例并文献复习
周蔚华,梁洁,唐浩
1病例资料
例1,男,55岁。主诉检查发现右侧肾上腺占位3 d。3 d前因饭后上腹不适于外院就诊,B型超声示右侧肾上腺区占位,为进一步诊治,于2013年2月19日转入我院。患者无尿频、尿急,精神良好,体质量无明显变化。入院查体:双肾区无压痛及叩击痛,输尿管经路无压痛。CT平扫示右侧肾上腺区可见一大小3.6 cm×3.3 cm×4.2 cm类圆形占位病灶,密度不均,CT值约33 Hu,邻近下腔静脉及肝实质受压,增强扫描示病灶明显不均匀强化,动脉期、静脉期及延迟期肿瘤内实质病灶CT值分别约58 Hu、66 Hu、71 Hu,其内见片状无强化区,CT考虑占位来源于肾上腺(图1)。遂行后腹腔镜下右侧肾上腺区肿物切除术。病理示:长梭形、类圆形瘤细胞,呈编织状、束样排列(图2见封3),胞浆丰富,嗜伊红,细胞核长梭形或点状,两端钝圆,部分细胞核大深染,可见核分裂象,>10个/10HPF;免疫组化染色显示SMA(+)、Actin(+)(图3见封3)、Vim(+)、Desmin(+)、S-100(-)、CD34(血管内皮+)、CD117(-)、SyN(-)、CgA(-)。病理诊断为右肾上腺低度恶性平滑肌肉瘤。
例2,女,61岁。主诉右侧腰部胀痛1个月,加重2 d。持续性右侧腰部胀痛1个月余,头晕、恶心、胸闷2 d,右上腹偶感不适,无尿频、尿急、尿痛,无排尿困难,门诊B型超声示肝脏右叶与右肾之间实性占位,考虑来源于右侧肾上腺,并下腔静脉癌栓形成,于2007年7月18日入院。近2个月以来,患者食欲下降,体质量减轻约6 kg。入院查体:右肾区有叩击痛,压之酸胀感明显,未触及包块。CT平扫示右侧肾上腺区可见一肿块影,大小8.3 cm×6.7 cm×10.2 cm,密度不均,边界尚清晰, CT值约36 Hu,右侧肾脏及肝右叶明显受压移位,右侧下腔肝段内可见巨大软组织影,增强扫描右肾上腺及下腔静脉内实性病灶中度强化,动脉期、静脉期肿瘤内实质病灶CT值分别约65 Hu、78 Hu,病灶坏死区无强化,诊断为右侧肾上腺皮质癌并下腔静脉巨大癌栓(图4)。遂行右侧肾上腺癌根治术。病理示:梭形或不规则形瘤细胞弥漫分布,呈交错状或漩涡状排列,胞浆丰富红染,核梭形,部分核显著深染并有多形性(图5见封3),可见瘤巨细胞,核分裂象可见,并可见病理性核分裂。免疫组化染色显示SMA(+)、Actin(+),Desmin(弱+)(图6见封3),Vim(+),CD34(+),S-100(-),CD117(-),Myoglobin(-),MyoD1(-)。病理诊断为右肾上腺平滑肌肉瘤。
2 讨 论
原发性肾上腺平滑肌肉瘤(adrenal leiomyosarcoma,ALMS)极为罕见,可能来源于肾上腺中央静脉或其分支的平滑肌[1],多见于中老年患者,双侧肾上腺同时发病者国内外至今仅有极少文献报道[2]。有文献报道ALMS不产生肾上腺激素紊乱,临床上无相应内分泌症状(如高血压、头痛、心悸、高血糖等)出现[3],本组患者也无任何内分泌症状出现,因此,在鉴别ALMS与其他肾上腺占位时,可通过临床是否出现内分泌症状进行排除性诊断。ALMS的临床症状多因压迫邻近软组织而产生,引起上腹不适与腰肋部酸胀、胀痛,压迫或侵犯下腔静脉,可引起下腔静脉综合征,泌尿系方面少有症状出现,无肾上腺内分泌功能异常表现,出现远处转移时,则引起相应部位疼痛与组织器官功能障碍。本组例2因瘤体巨大,且下腔静脉出现巨大瘤栓而出现下腔静脉综合征,表现出头晕、恶心、胸闷症状。

注:A.CT平扫示右侧肾上腺区类圆形实性占位病灶,密度不均,邻近肝脏受压内陷;B、C、D.增强扫描示,动脉期(B)病灶呈明显不均匀强化,静脉期(C)及延迟期(D)肿瘤内实质病灶逐渐强化,瘤内可见片状始终无强化区,于延迟期轮廓更为清晰
图1 例1患者腹部CT扫描表现
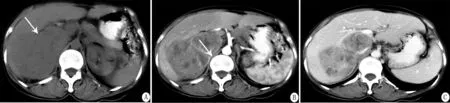
注:A.CT平扫示右侧肾上腺区可见一占位病灶(箭头所示),密度不均,右侧肾脏、肝右叶及下腔静脉明显受压移位;B、C.增强扫描示动脉期(B)实性病灶中度强化明显不均匀,瘤内可见强化的肿瘤供血血管影,静脉期(C)内实质病灶进一步强化
图4 例2患者腹部CT扫描表现
平滑肌肉瘤由弥漫分布的长梭形瘤细胞组成,呈束状纵横交错的编织状、平行状或杂乱排列,胞质丰富,嗜伊红,核呈长圆形或杆状,异型性明显且深染,核分裂象易见。高分化平滑肌肉瘤形态学与平滑肌瘤相似,而低分化平滑肌肉瘤形态学具有多形性,需通过免疫组化与肉瘤样癌和具有异型性的上皮样血管平滑肌脂肪瘤鉴别[4]。免疫组织化学染色显示间叶性及平滑肌源性标记阳性,即Vimentin、Desmin与SMA呈阳性表达。有文献将Desmin、Vimentin及SMA三者共同作为诊断平滑肌肉瘤的特异性标记,且Desmin在良性肌源性肿瘤中强阳性表达,Vimentin 在恶性肌源性肿瘤中强阳性表达[5]。本组2例患者Desmin、Vimentin及SMA均为阳性表达,符合ALMS的免疫组化特点,同时例2的Desmin呈弱阳性表达,提示该患者ALMS生物学行为侵袭性较强,预后不良。
B型超声可以检出肾上腺内直径大于2 cm的肿瘤,能查明病因,明确肿瘤大小、生长方向及与周围组织的关系,且经济、快捷、无辐射,可作为临床筛查首选手段。
腹部CT平扫+增强扫描可清晰显示ALMS各个细节,检查快速、便捷,为重要的影像检查手段。CT平扫,肿瘤一般表现为肾上腺区圆形或类圆形软组织肿块,瘤体较大时其边缘常出现分叶,密度不均匀,钙化罕见;由于其假包膜的形成,边界常较清晰,对周围组织器官多以推压性改变,当对邻近组织器官浸润性生长时,边界模糊,甚至不能区分肿瘤起源部位[6]。增强扫描,由于肿瘤血供丰富,肿瘤实性部分呈中度至明显强化,并有延迟性强化的特性,有文献认为这种特性的病理基础亦为肿瘤富含纤维组织及肿瘤细胞间隙宽大[7]。
本组病例中,1例行动脉期与静脉期扫描,另1例还行延迟扫描,但2例都具有相似的强化特点,即瘤体强化度动脉期<静脉期<延迟期,符合上述文献报道,但此强化特性是否能够认为是ALMS的特点还有待更多病例的总结。病灶坏死液化区始终无强化,而且随着瘤体实质延迟强化,其坏死低密度区轮廓显示更为清晰。ALMS对相邻血管多以推压移位而非包绕生长,腹主动脉旁淋巴结转移与肾静脉、下腔静脉瘤栓形成相对少见[8],本组1例仅见下腔静脉受压移位,另1例侵及下腔静脉,在其管腔内形成巨大瘤栓,临床上出现头晕、胸闷等下腔静脉综合征。
MR对肿瘤组织成分构成、是否出现转移显示更为敏感[9],但检查费用高、耗时长,临床并不将MR作为必要检查方法。ALMS的MR表现具有恶性肿瘤的常见信号改变:在T1WI中呈混杂低信号,瘤内有时可见小片状的高信号出血区,T2WI呈混杂高信号,增强扫描肿瘤丰富血供呈明显不均匀强化,其内可见粗大的供血血管影。
ALMS主要需与肾上腺嗜铬细胞瘤、肾上腺皮质腺癌鉴别:(1)嗜铬细胞瘤为内分泌性肿瘤,其分泌的儿茶酚胺常引起恶性高血压、心力衰竭、剧烈头痛等; CT检查中瘤体常见坏死、出血、囊变,增强扫描动脉期实质部分强化显著,静脉期及延迟扫描强化度减低,有文献报道其三期强化CT值往往超过100 Hu[10];免疫组化中S-100多数呈阳性表达[11]。(2)肾上腺皮质腺癌患者可出现库欣综合征,典型表现为向心性肥胖、满月脸等, CT检查同样存在延迟强化,肿瘤多数无完整包膜,与周围器官分界不清,下腔静脉癌栓、腹膜后淋巴结转移常见[12];免疫组化Syn、NSE、Vimentin阳性。
ALMS治疗以根治性手术切除肿瘤为主,有文献报道当肿瘤与周缘组织器官分界较清、最大径线小于5 cm时,可由腹腔镜行肾上腺单层面肾上腺切除术;当肿瘤对周围大血管、器官侵犯、肿瘤最大径线大于12 cm时,应行开腹肿瘤切除+周围淋巴结清扫术[13]。手术切除效果与肿瘤及其侵犯组织清扫程度,肿瘤分化程度、患者身体状态等密切相关,其中最重要因素是手术后显微镜下的阴性边缘完整度[14]。对于预后不良的ALMS患者,如出现邻近血管、器官侵犯,下腔静脉等出现癌栓,周围多发淋巴结转移等,术后均应辅以放射治疗,降低肿瘤远处转移率。化疗对ALMS疗效甚微,反而会削弱患者自身免疫功能,引起多种并发症。ALMS较易复发与转移,通常经血行转移,肺部为其最常见的靶器官。本研究中例1未作辅助治疗,术后6年出现双肺多发转移瘤;例2因其肿瘤累及范围广,术后进行放疗,但8个月后出现肺部、颈部淋巴结多发转移。由此,手术+放射治疗可延长ALMS患者生存期,同时ALMS生物学行为呈高度恶性,肿瘤复发与转移多见。
综上所述,ALMS中晚期患者多出现腰部胀痛;CT检查可清晰显示肿瘤形态、位置,延迟强化为其特点,但不具有特异性;免疫组化中,Desmin、Vimentin及SMA均为阳性表达;临床治疗方案多采用手术切除病灶,辅以放射治疗,肿瘤总体预后不良。
——一对性格习性迥异的兄弟

