伴神经源性损害的非炎性肌病临床与电生理特点☆
古力切木·艾麦尔 陈静燕 黄姿 何若洁 姚晓黎 廖松洁
针电极肌电图(electromyography,EMG)一直被认为是鉴别神经源性损害和肌源性损害的最方便而有价值的检查手段,它不但可以鉴别损害类型,还可以了解肌肉受累的分布情况;其中运动单位电位(motor unit potential,MUP)为最主要的鉴别点,大多数肌病可以导致运动单位内具有功能的肌纤维数量减少,从而导致MUP 时程缩短及波幅下降,呈现出典型的肌源性损害电位[1]。然而,部分经肌肉活检和(或)基因检测明确诊断为肌肉疾病患者的EMG 检测中,也可合并出现神经源性损害,关于这种引起混淆的情况,有研究指出多数炎性肌病患者EMG 可合并出现神经源性损害[2],在实践中我们发现,有极少数明确诊断为非炎性肌病的患者,EMG 仍出现神经源性损害,有关此类情况的研究甚少,普遍认为是肌病晚期出现失神经和神经再支配的的复杂变化所致[3],我们收集了4例有此特征的患者,详细回顾临床资料及电生理表现,以探究肌肉疾病EMG 出现神经源性损害的原因及肌病诊断与神经电生理检查之间的关系。
1 对象与方法
1.1 研究对象回顾性分析2015 年至2017 年于我院神经内科诊断为肌肉疾病的患者,筛选出EMG 发现合并存在神经源性损害的非炎性肌病患者作为研究对象。纳入标准: ①有肌肉活检和(或)基因检测结果可以明确诊断为肌肉疾病②可查找完整病历资料③可查找完整的肌电图报告;排除标准:有四肢周围麻木、疼痛、麻木伴疼痛、肌痛及其他描述性感觉异常及诊断为I、II 糖尿病、严重肝肾功能不全、心肺功能异常、血液系统疾病、恶性肿瘤、感染、自身免疫性疾病、颈椎病、神经根刺激征及其他一切可疑引起周围神经病变者。
1.2 研究方法
1.2.1 资料收集 收集所有患者的最终诊断和肌电图报告,筛选出其中非炎性肌病且EMG 合并神经源性损害者,详细采集其病史、体格检查及有意义的辅助检查结果,对这些患者的临床表现及肌电图结果进行总结整理、分析。
1.2.2 电生理检查 所收集患者均用 Keypoint 肌电诱发仪(Dantec,Denmark)行神经传导速度(nerve conduct velocity,NCV) 检测和 EMG 检测;针电极型号:37 mm*26G(natus,Germany)。NCV 包括正中神经、尺神经、胫神经和腓总神经的感觉、运动速度和波幅以及运动末端的潜伏期。EMG 检测部位为双上肢三角肌、拇短展肌、小指展肌和双下肢股四头肌、胫前肌等。记录项目主要为肌肉安静状态下的自发电位、 小力收缩时运动单位的时限和波幅及大力收缩时募集电位的变化。
1.2.3 诊断标准 EMG 肌源性损害表现为运动单位动作电位平均时限小于等于本实验室同年龄组正常值20%,可伴有波幅下降、多相电位增多、大力收缩时呈病理干扰相; 神经源性损害为 MUP时限大于等于同年龄组正常值 20%,可伴有波幅增高、多相电位增多、大力收缩时呈单纯相或混合相[3]。肌肉活检肌源性损害表现为:肌纤维大小不一,萎缩纤维与肥大纤维相间存在,可见核内移、颗粒变性、絮状变性、空泡变性和吞噬现象等; 炎性肌病可见炎性细胞浸润、 肌纤维坏死和再生[4]。基因检测提示有明确临床意义的变异。
2 结果
2.1 一般资料收集符合入选标准的患者110 例;其中男71例,女39例,平均年龄(27.0±15.0)岁,平均病程(5.8±6.4)年;其中代谢性肌病45例,先天性肌病49例,炎性肌病 16 例。EMG 出现神经源性损害者10 例,其中非炎性肌病患者4例,分别为1 例代谢性肌病和3例先天性肌病(见表1)。
2.2 临床资料病例1,34 岁男性,主因“肢体无力1 年,加重2 个月”入院;患者于1 年前无诱因出现双下肢无力,下蹲和上下楼梯费力,2个月前开始出现双上肢上举无力,咀嚼费力等症状。体格检查:全身肌肉可见萎缩,以肢体近端肢带肌萎缩明显,肌肉轻度压痛,肌张力降低,四肢近端肌力4级,远端肌力5-级,四肢腱反射减弱。乳酸(运动后)11.9 mmol/L↑;乳酸(休息 15 min) 8.5 mmol/L↑;肌酸激酶CK 396 U/L↑。左下肢肌肉MR:双大腿及小腿各肌肉萎缩,考虑肌营养不良。肌肉活检结果提示 “所见肌细胞可见明显脂质沉积,考虑为脂质沉积性肌病”。
病例2,55 岁男性,因“双下肢无力10 年余”入院;患者于10 余年前无明显诱因出现爬楼梯时双下肢费力,症状进行性加重,逐渐进展为平路行走时常摔倒,自觉双手肌肉萎缩。体格检查:双侧大鱼际肌萎缩,双下肢大腿下1/3 以下肌肉萎缩,双侧弓形足,四肢肌张力正常,双上肢肌力5 级,双下肢近端肌力4 级,远端肌力3 级,双上肢腱反射活跃,双下肢腱反射消失。我院肌肉活检结果提示(右侧腓肠肌)“形态符合中央轴空病形态改变”(见图1)。

表1 入组患者肌病类型,括号内为EMG 出现神经源性损害患者例数
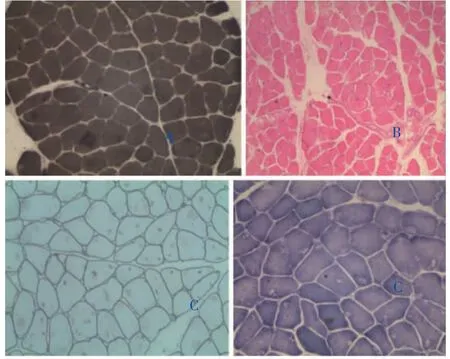
图1 肌纤维大小形态基本一致,仅见散在少数萎缩肌纤维,肌酶染色肌纤维内出现特征性的非着色的空腔结构,形态符合中央轴空病形态改变
病例3,44 岁女性,主因“进行性四肢无力伴肌肉萎缩10 年”入院;患者于10 余年前无诱因出现四肢无力,主要为双上肢抬举费力及上楼梯费力,症状进行性加重并出现双下肢近端肌肉萎缩,双下肢远端不能背屈,走平路需有人扶持。体格检查:旁人扶助下见跨阈步态;可见翼状肩,双上肢近端肌力4 级,远端肌力5 级,双下肢近端肌肉萎缩,双侧髋关节内收及外展肌力2 级,膝关节及踝关节屈伸肌力3 级,双足背屈肌力4 级;吸吮反射阳性,双侧Rossolimo's 征对称性阳性,余病理征阴性。基因检测结果示:“包涵体肌病可能性大”。
病例4,30 岁男性,主因“进行性四肢无力伴肌肉萎缩14 年”入院;患者约14 年前起无诱因出现双下肢无力、肌肉萎缩,走路不稳,久走后易肌肉酸痛,伴麻木,2 年余后出现臀部无力,爬楼梯、下蹲困难,近4 至5 年出现双上肢无力,近端重于远端,伴肌肉萎缩,用力后胸部肌肉跳动。体格检查:四肢肌肉萎缩明显,双上肢近端肌力4 级、远端肌力5-级,双下肢近端肌力3 级、远端肌力1级,四肢腱反射(±),感觉系统未见异常,病理反射未引出。CK:437 U/L↑。家族史:其大弟、母亲、舅舅、表妹及外祖母有类似病史(见图2-A)。基因检测“TIA1 基因 1 个杂合突变,该突变与 Welander 型远端型肌病相关”,其父母及弟弟完善基因检测,结果示其母亲与弟弟相同位点杂合变异(见图2-B)。
2.3 电生理特点EMG 出现神经源性损害的4 例患者均存在不同程度神经传导的改变,其中4 例均有运动传导异常,脂质沉积性肌病及Welander型远端型肌病患者伴感觉传导异常;4 例患者中,Welander 型远端型肌病患者EMG 未见明显肌源性损害,另3 例患者EMG 均为肌源性损害和神经源性损害并存;除脂质沉积性肌病患者外,余患者EMG 静息状态均可见自发电位(见表2)。
3 讨论
肌肉疾病临床上主要以运动症状为主,多数不伴有感觉障碍和自主神经功能障碍,因此大部分肌病患者常规感觉神经传导检查一般正常。由于每个运动单位内兴奋的肌纤维数量减少、 所产生的力量减弱,致MUP 时程缩短及波幅下降,当以一定力量随意收缩时,所兴奋的运动单位增多,以从数量上进行功能性补偿,其增加数量的程度,与无效发放的运动单位成比例,因此典型肌肉疾病EMG 表现为时限缩短、波幅降低并多相电位增多的MUP,其募集时参与运动单位数量和发放频率增多,呈病理干扰相;静息状态时可有纤颤电位及正锐波等自发电位的出现,疾病早期患者自发电位的出现及自发电位数量相对较多[1,3]。

图2 4 号病例家族谱系图(图A 灰色为有类似症状者)、亲属基因检测结果(图B 母亲、弟弟可见杂合变异)及上肢与弟弟对比(图C 左侧为患者、右侧为弟弟)
本研究总纳入患者110 例,均来自本院神经内科住院病例,而非人群调查或多中心研究且不包括门诊病例,可存在一定偏倚。本研究中EMG合并神经源性损害的患者为10 例,其中6 例为炎性肌病,炎性肌病患者可同时伴有肌炎和血管炎性神经病变[5-12],这些神经病变可以是单神经病或是多发性单神经病,后期甚至可出现类似多发性周围神经病的表现,因此炎性肌病患者的EMG 中常可出现神经源性损害[11-12]。本研究中合并神经源性损害的炎性肌病占总炎性肌病37.5%,与既往文献报道的88.7%[2]不符,考虑为纳入偏倚所致。
EMG 出现神经源性损害的非炎性肌病患者为4 例,分别为1 例脂质沉积性肌病、1 例中央轴空病及2 例远端型肌病,既往文献报道脂质沉积性肌病EMG 表现差异较大,部分患者可见MUP时限增宽,表现为神经源性损害,少数患者MUP的时限和波幅可在正常范围;部分患者运动、感觉神经传导测定可见异常,主要表现为动作电位波幅降低,而传导速度相对正常[15-16];中央轴空病电生理检查结果多数病人倾向于肌源性损害,少数病人可出现宽时程 MUP,神经传导检测可有CMAP 波幅减低,传导速度正常或略有减慢[17-18]。既往报道包涵体肌病肌电图无特异性,32%~56%的患者EMG 可以同时出现提示肌源性损害的短时程、低波幅的MUP 和提示神经源性损害的宽时程、高波幅的 MUP[19],且 56%~100%患者 EMG 静息状态可伴有自发电位[20]; Welander 型远端型肌病是迟发的常染色体显性遗传病,主要累上肢并逐渐向下肢远端肌肉进展[21],该病肌电图变化较为复杂,可同时出现短时程、波幅低的多相MUP、病理干扰相、巨大的MUP 及自发电位[22],在少数早期病例中,可出现单纯的肌源性损害[23]。
既往研究指出肌肉疾病肌电图出现神经源性损害大致可分为两类,其一为肌肉病变是出现神经源性损害的直接责任因素,如炎性肌病中肌炎和血管炎性周围神经病变[5-12]、内分泌疾病如甲亢性肌病合并周围神经病[24],感染性疾病,如AIDS出现肌病和神经损害并存[25],其他如包涵体肌炎[26]、危重症性神经肌病[27]、某些遗传代谢性疾病[28]、中毒[29]等;其二为同时存在可导致神经源性损害的基础病,如糖尿病、颈腰椎病、嵌压性单神经病等。此研究中,我们排除了炎性肌病,仍发现了4 例合并神经源性损害的病例; 既往认为肌病肌电图合并神经源性损害是由慢性肌病导致失神经支配所致[30],我们所描述4 例病例,除脂质沉积性肌病者病程仅为1 年,余患者病程均在10 年及以上,符合肌肉疾病经过长时间慢性失神经损害,导致肌电图表现变得复杂,在疾病过程中如果出现轴索末梢损害后神经再支配,可表现为宽大的MUP,或宽大与缩窄的MUP 混合存在;既往研究指出脂质沉积性肌病在早期可出现神经源性损害,认为这与脂质在疾病早期可侵犯周围神经施万细胞相关[31],解释了本研究中病程为1 年的脂质沉积性肌病患者EMG 出现神经源性损害;本研究中Welander 型远端型肌病EMG 仅出现神经源性损害,国内外既往有关该疾病肌电图表现的相关研究甚少,至今所报道多数为神经源性损害与肌源性损害并存,少数可单纯表现为肌源性损害[22-23],无单纯表现为神经源性损害者,本例患者出现此类情况,考虑与所检测肌肉有限有关,需继续随访。

表2 4例EMG合并神经源性损害的非炎性肌病患者肌电图特点
本研究揭示了少数非炎性肌病患者肌电图可出现神经源性损害,该现象给电生理诊断及临床评估带来困难。提示肌病的电生理诊断具有一定复杂性和挑战性,需要谨慎操作与解读,并与临床情况紧密联系。

