纳米过氧化钙对地下水中硝基苯的类-Fenton降解效果
董家麟,付 双,周 昊,李天一,秦传玉*
纳米过氧化钙对地下水中硝基苯的类-Fenton降解效果
董家麟1,2,付 双3,周 昊1,2,李天一1,2,秦传玉1,2*
(1.吉林大学地下水资源与环境教育部重点实验室,吉林 长春 130021;2.吉林大学新能源与环境学院,吉林 长春 130021;3.上海交通大学环境科学与工程学院,上海 200240)
为了探究基于纳米过氧化钙(CaO2)的类芬顿氧化技术(Modified Fenton, MF)修复污染地下水的可行性,本研究先对纳米CaO2制备方法进行改进,制备出有效含量高达88.35%的纳米CaO2粉末;其次,通过分析静态试验中反应体系的pH值、DO以及硝基苯浓度变化,探究纳米CaO2降解硝基苯的过程和影响因素,确定了硝基苯的降解动力学和最佳反应条件;通过掩蔽实验探究不同自由基的作用效力;最后进行一维模拟柱动态模拟,综合分析评估纳米CaO2去除硝基苯的机理和效果.结果表明:CaO2投加量、EDTA-Fe2+浓度与硝基苯初始物质的量浓度满足48:8:1时降解效果最佳,其降解曲线符合一级动力学曲线,且反应过程中起主要降解作用的自由基是•OH,但降解效果会受到HCO3-、SO42-、Ca2+、Mg2+等离子的影响;一维模拟柱的模拟结果表明,在存在适量铁的条件下,纳米CaO2可以作为过氧化氢缓释剂,通过类芬顿催化产生自由基降解污染物,这说明纳米CaO2在场地修复中具有较好的应用前景.
纳米过氧化钙;类芬顿技术;降解效果;影响因素
类-Fenton技术是利用地层中的铁氧化物催化过氧化氢产生羟基自由基(×OH)形成类-Fenton试剂修复难降解有机物污染地下水的技术[1],在场地修复中具有良好的应用前景.但地下环境中H2O2的不稳定性以及反应的快速性成为该技术使用的限制性因素[2].实验表明,在过氧化氢溶液注入井附近,过氧化氢浓度往往较高导致过氧化氢直接大量分解[3];其分解反应是强烈的放热反应,随温度升高,过氧化氢的分解反应逐渐取代类-Fenton反应占据优势;此外过氧化氢分解产生的大量氧气,又会使污染物挥发、扩散而扩大污染面积,不利于污染场地控制与修复的进行.所以,如何规避H2O2溶液的缺陷,证明类-Fenton反应高效进行成为其应用于硝基苯等有机污染物场地修复的关键.
近年来通过对CaO2的进一步研究,发现其可以有效地释放出H2O2[4-7].主要的反应过程如下[8,13]:
CaO2+2H2O→Ca(OH)2↓+H2O2(1)
刘丽娟等[14]发现缓慢溶解可以将土壤中腐殖酸降解70%.郑友平等[15]对PCE、TPH污染的场地进行CaO2可控降解处理,可将其分别降解98%、95.6%.李天一等[16]的研究也表明,CaO2颗粒粒径小、密度小、在介质中迁移过程中受到的阻滞作用较弱,具有良好的迁移性.Janda等[17]使用CaO2作为替代氧源对地下水中有机污染物进行降解,表明污染物去除程度可达80%以上.Pan等[18]也发现在纳米CaO2体系中苯酚可以在30min内迅速降解并完全去除.
而市售的纳米CaO2以及根据国内外现有制备方法制备出的纳米CaO2有效含量普遍较低,因此,本实验创新点及主要研究内容为制备出较高纯度的纳米过氧化钙,并对地下水中以硝基苯为代表的有机污染物进行降解,且降解效果良好.
本实验拟制备有效含量较高的纳米CaO2颗粒,并探究其降解过程发生的主反应,而后探究其对硝基苯 (NB)的降解效果、反应条件及其影响因素,为以后利用CaO2在地下环境中降解难降解有机物的实际应用提供了理论依据.
1 材料与方法
1.1 材料与仪器
试验选取粗砂(0.50~1.00mm)粒径的河沙,其孔隙度约为0.4,渗透系数为5´10-2~1´10-2(cm/s),在水中溶出的Ca2+含量低于0.001mg/g.
试剂:硫酸锰(MnSO4,国药集团化学试剂有限公司,分析纯),十六烷基三甲基溴化铵(HDTMA,国药集团化学试剂有限公司,分析纯),氢氧化钠(NaOH,国药集团化学试剂有限公司,分析纯),30%H2O2水溶液(国药集团化学试剂有限公司,分析纯),聚乙二醇200(H(OCH2CH2)OH,PEG200,国药集团化学试剂有限公司,分析纯),无水氯化钙(CaCl2,国药集团化学试剂有限公司,分析纯),氨水(NH3·H2O,北京化工厂,25%),七水合硫酸亚铁(FeSO4·7H2O,国药集团化学试剂有限公司,分析纯),乙二胺四乙酸二钠(C10H14O8N2Na2,EDTA,国药集团化学试剂有限公司,分析纯),甲醇(CH3OH,北京化工厂,色谱纯). 硝基苯(NB),乙腈(C2H3N),氯化钠(NaCl),十二水磷酸氢二钠(Na2HPO4×12H2O),十二水磷酸二氢钠(NaH2PO4×12H2O),叔丁醇((CH3)3OH,TBA),七水合硫酸亚铁(FeSO4×7H2O),碳酸氢钠(NaHCO3),硫酸钠(Na2SO4),无水氯化钙(CaCl2),氯化镁(MgCl2),三氯甲烷(CHCl3),四水合氯化亚铁(FeCl2×4H2O),六水合氯化铁(FeCl3×6H2O)
主要仪器:磁力搅拌器,振荡器,溶解氧仪,电子天平,pH计(YSI pH100,美国黄泉仪器有限公司),高效液相色谱仪(Agilent1100,美国安捷伦公司).
1.2 纳米CaO2的制备
纳米CaO2可以在碱性的H2O2水溶液中与金属盐发生反应.纳米CaO2可以利用一下反式(1)制取:
CaCl2+ H2O2+2NH3H2O→ CaO2(solid)+2NH4Cl (1)
(1)取一定量去离子水加入到烧杯内,依次加入CaCl2,氨水溶液,十六烷基三甲基溴化铵,放置在磁力搅拌器上进行恒速搅拌.
(2)搅拌完毕后加入一定量H2O2水溶液.反应方程见式(1).
(3)用NaOH调pH值至11左右,使得CaO2沉降,之后进行多次离心,并用无水乙醇进行冲洗,直到泡沫基本清除.
(4)平铺在玻璃皿内,密封,通入氮气进行干燥1~2h,直到粉末完全干燥,进行研磨后收集保存,即为纳米CaO2固体颗粒.
1.3 纳米CaO2降解硝基苯影响因素静态试验

表1 静态降解实验条件一览表
注:表中硝基苯、纳米CaO2和EDTA-Fe2+的比例都为物质的量比.
实验在250mL顶空瓶中进行,加入100mL质量浓度为100mg/L的由缓冲溶液配制的硝基苯溶液,之后加入0.05mol/L的EDTA络合Fe2+溶液,最后投加制备的纳米CaO2颗粒.密封后放置150r/min的震荡培养箱中反应,一定时间间隔取样分析.
通过调节CaO2投加量,EDTA-Fe2+浓度,硝基苯初始浓度,Fe2+与Fe3+投加比例以及添加其他离子等,研究不同实验条件对降解硝基苯的影响;通过参考李天一等[16]研究选取的类-Fenton反应各反应物投加比例,并通过预实验,确定本实验材料投加比例. 依据地下水抽取水样成分检测结果,选取常见的一价、二价的阳离子及阴离子(团)作为添加离子,探究该反应在地下环境中可能的影响因素.
静态降解实验条件如表1.
1.4 纳米CaO2降解硝基苯机理探究
在纳米CaO2,EDTA-Fe2+和硝基苯初始浓度的物质的量比例满足48:8:1的最佳反应条件下,分别加入1.0mL叔丁醇((CH3)3OH,TBA)以及0.5mL三氯甲烷(CHCl3),密封后放置150r/min的震荡培养箱中反应,一定时间间隔取样分析.
1.5 一维柱状动态模拟实验
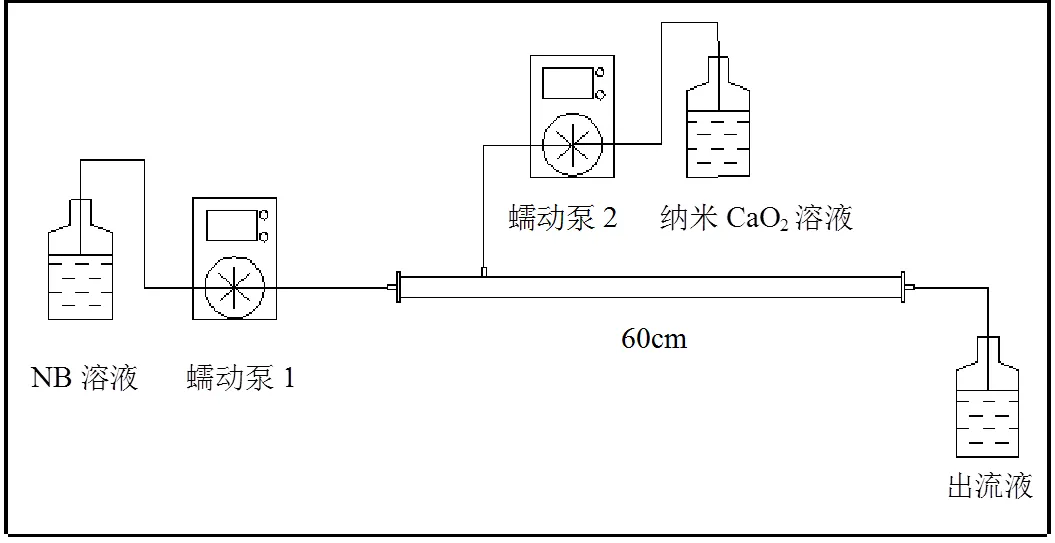
图1 模拟柱试验装置
为了探究纳米CaO2在实际应用中的迁移性以及降解效果,本试验采用将一维实验土柱横放的方式,模拟在水利梯度较小的条件下的地下水流形式,选用内径5cm,长60cm的有机玻璃柱,填充粗河砂介质,利用蠕动泵调节注入流速,以3.5mL/min的进水速率从底部向上饱水,完全饱水后,再以相同方法注入初始溶液,进行饱和.在不同Fe浓度条件下,对比降解效果. 实验一以1.2m/d速率注入4孔隙体积(4PV)的加EDTA-Fe2+的硝基苯.在第13个小时内连续注入1PV的纳米CaO2,其中纳米CaO2投加量、EDTA-Fe2+浓度与硝基苯初始浓度满足48:8:1的最佳物质的量;实验二以1.2m/d的速率注入3PV的加EDTA-Fe2+的硝基苯,在最后1PV注入不加EDTA- Fe2+的硝基苯,同样保持纳米CaO2投加量、EDTA- Fe2+浓度与硝基苯初始浓度满足48:8:1的最佳物质的量,从第1PV开始以一定的时间间隔取样,分析出口处收集液的pH值、DO变化以及硝基苯降解率和TOC.
一维柱状模拟试验装置见图1.
2 结果与讨论
2.1 纳米CaO2的表征以及含量分析
通过投射电镜(TEM)观察可得出:制备出的CaO2颗粒,外围由HDTMA包附形成的圆润球状纳米级颗粒.纳米颗粒大小是50~60nm.由于使用了HDTMA对易团聚的纳米CaO2进行包裹,降低了其静电力,减少了断句的发生.通过滴定实验可得出:制备的纳米CaO2颗粒有效含量达88.35%.
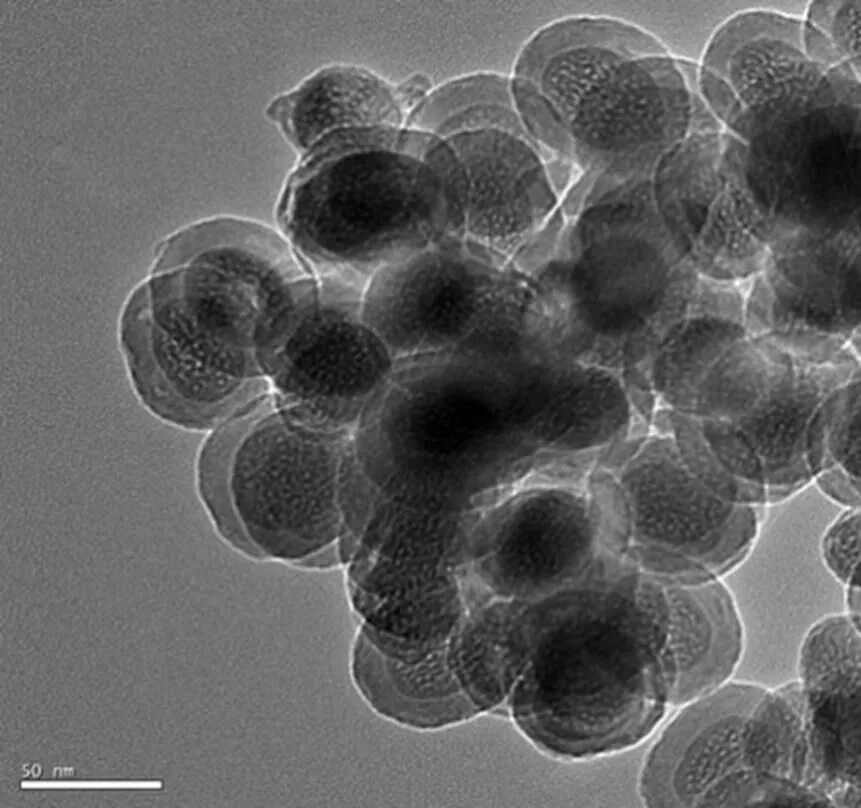
图2 HDTMA包覆的纳米CaO2TEM图
2.2 纳米CaO2降解硝基苯影响因素分析
2.2.1 纳米CaO2投加量对硝基苯降解效果 本试验EDTA-Fe2+与硝基苯的物质的量比为8:1.由图3可知,随着CaO2投加量与Fe2+物质的量比例由12:8升高至96:8时,反应的250min内硝基苯的降解率由43.5%升高至69.8%,即CaO2投加量越多硝基苯的降解效果越显著,且在反应的过程中体系中的pH值、DO值也不断上升.但是投加率的升高与降解率的升高并不一致,随着投加量增加,降解率增加效率降低.这可能是由于副反应CaO2+H2O→Ca(OH)2↓+1/ 2O2↑的发生,不断产生Ca(OH)2和O2[17],从而抑制住反应的发生,导致降解效率增加率下降.
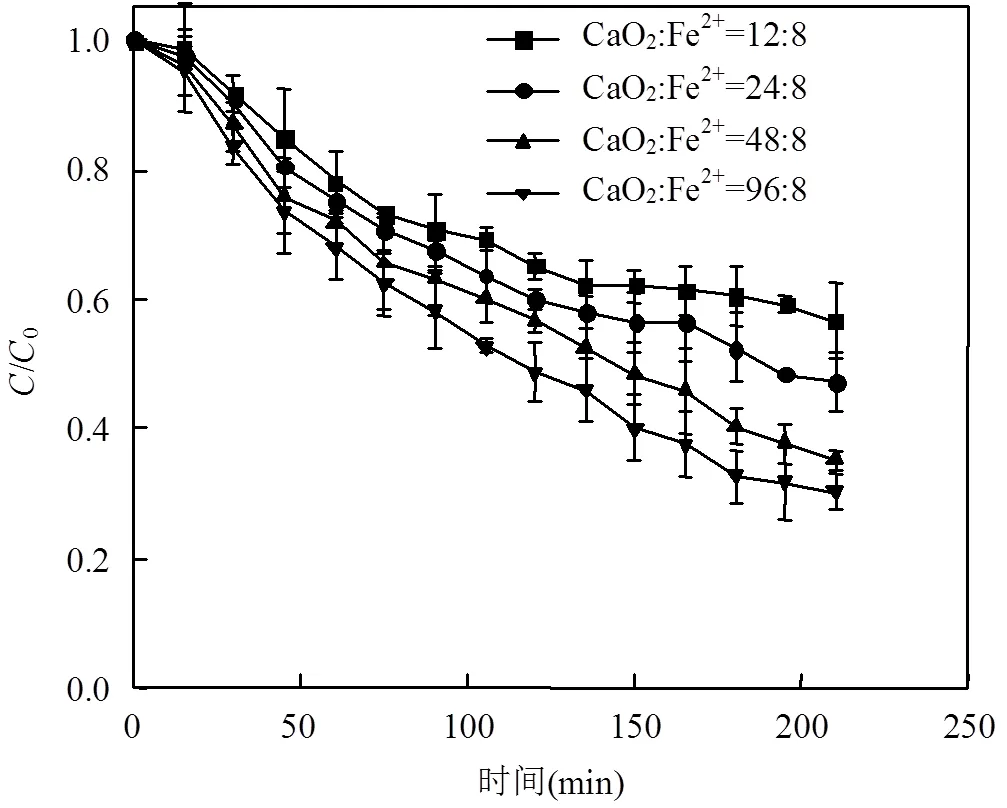
图3 纳米CaO2投加量对硝基苯降解效果的影响
2.2.2 Fe2+投加量对硝基苯降解效果研究 本试验纳米CaO2与硝基苯的物质的量比为48:1.如图4所示,随着反应物Fe2+投加量的增加,体系中硝基苯的降解速率不断提高.当CaO2:Fe2+的比例从48:2提高到48:16,在相同反应时间内,硝基苯降解率从19.4%提高到51.4%,反应符合一级反应动力学.且反应过程中体系中的pH值、DO值与Fe2+投加量成反比[19].这是由于Fe2+的增加会促进芬顿反应的进行,产生大量的∙OH使反应速率在较短的时间内加快,促进反应物的降解,增大降解率.但是,在150min后,CaO2: Fe2+的比例在48:8与48:16的条件下,降解效率相近,降解效率增加率显著下降.同时,过多的EDTA可能会导致纳米CaO2的包覆膜较厚,不利于纳米CaO2的释放,从而影响硝基苯的降解效果.
2.2.3 硝基苯初始浓度对其降解效果研究 本试验纳米CaO2与EDTA-Fe2+的物质的量比为48:8.由图5可以看出,随着硝基苯初始浓度的增加,硝基苯的降解率减小.当浓度由50mg/L升高至200mg/L降解的有效含量由原来的64.5%降低至29.1%,反应符合一级反应动力学.且硝基苯浓度在50mg/L时与100mg/L时最终降解的降解率相近,而降解的有效含量提高了近两倍.这说明硝基苯含量低于100mg/ L时,投入的纳米CaO2的量是足量的,且随着污染物浓度的增加,体系中∙OH的消耗速率增加,促进H2O2生成∙OH[20],促进主反应的发生.但是随着硝基苯的初始含量的加大,投入的纳米CaO2量不足,降解率下降.且反应过程中体系中的pH值变化不大,DO值的变化与硝基苯的初始浓度成反比.

图4 Fe2+投加量对硝基苯降解效果的影响
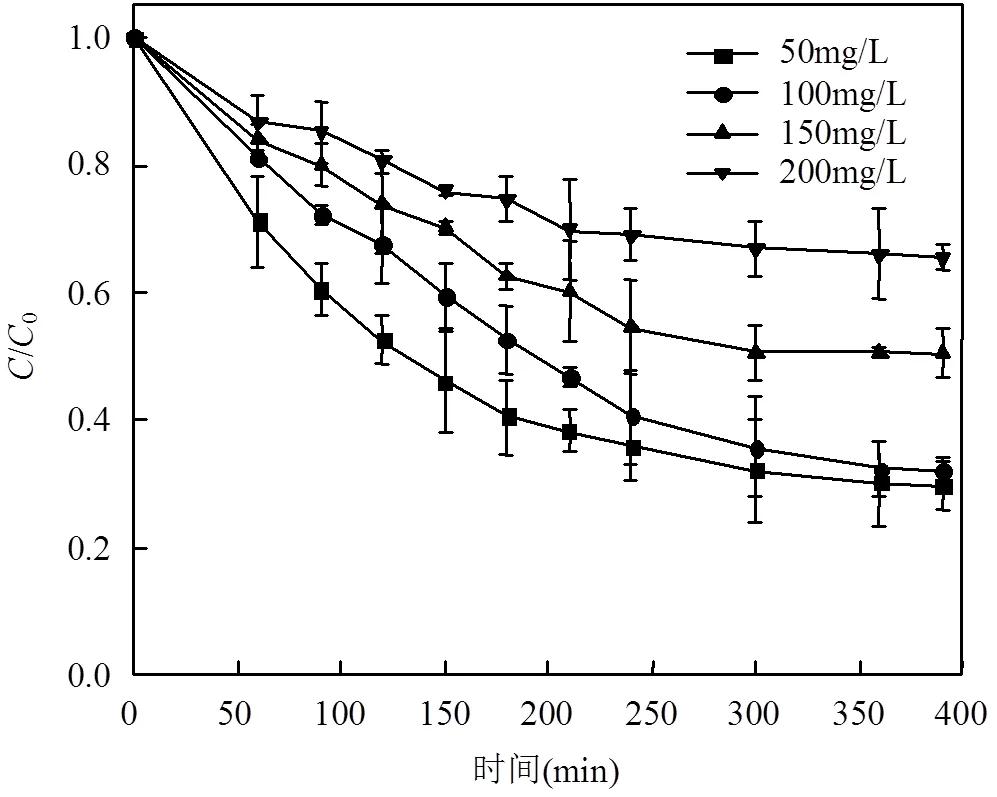
图5 硝基苯初始浓度对其降解效果的影响
2.2.4 投加不同离子对纳米CaO2降解硝基苯影响 本试验纳米CaO2,EDTA-Fe2+和硝基苯初始浓度的物质的量比例满足48:8:1.为了模拟地下水环境,验证地下水中离子对该反应的影响,故添加Na+、Ca2+、Mg2+、Cl-、HCO3-、SO42-等离子研究不同离子对纳米CaO2降解硝基苯影响.由图6可知,添加HCO3-、SO42-、Ca2+、Mg2+都会使硝基苯的降解率下降,即对其有抑制作用,其抑制能力强到弱为Ca2+>SO42->HCO3->Mg2+.且四种离子都会使体系中的pH、DO值升高.根据李明玉等[21]、Lu等[22]和张嫦等[23]的研究,加入阴离子以及阳离子都会对Fenton反应有抑制作用,且加入碳酸盐对Fenton试剂的抑制作用是因为溶液中的CO32-、HCO3-对自由基有清除作用,最终导致硝基苯的降解效果下降.Ca2+的抑制作用是因为Ca2+会与H2O2发生反应,从而降低∙OH的释放.根据文献[20-22],其他离子不会与羟基自由基反应,因此不会影响Fenton试剂的催化性能.使得硝基苯降解率下降的原因可能是SO42-与Mg2+降低了纳米CaO2的缓释H2O2的效率.
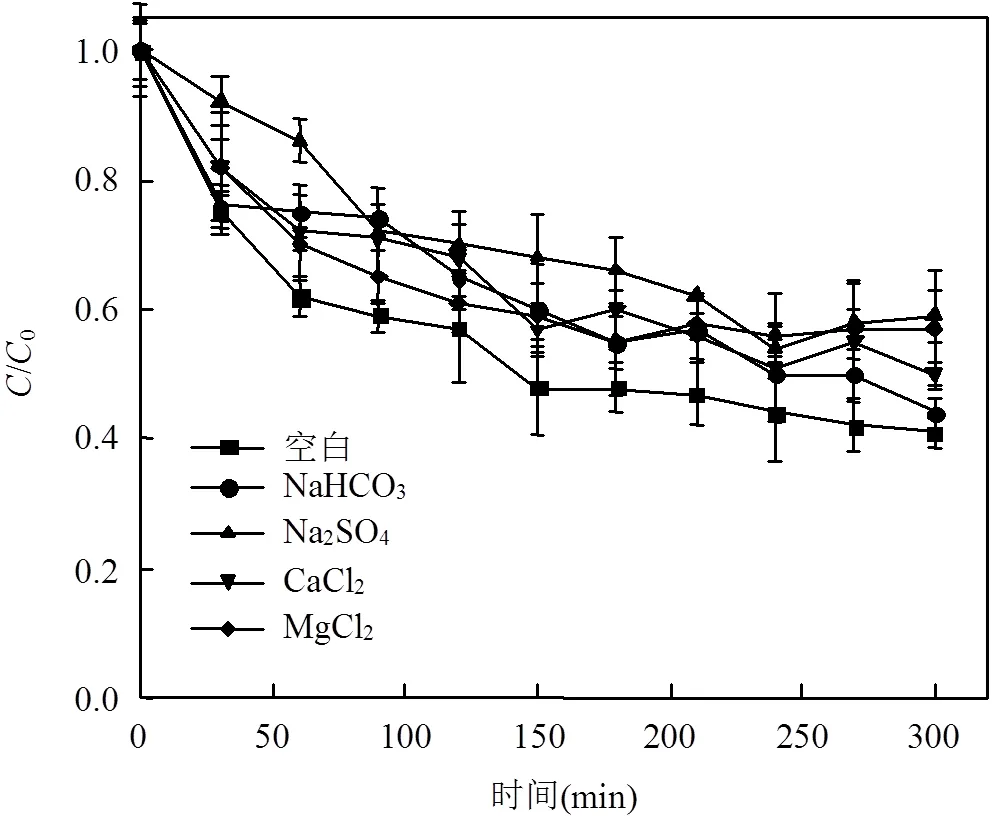
图6 添加不同离子对硝基苯降解效果的影响

图7 不同比例的Fe2+与Fe3+对硝基苯降解效果的影响
2.2.5 不同投加比例的Fe2+与Fe3+对纳米CaO2降解硝基苯影响研究 本试验纳米CaO2,EDTA-Fe2+和硝基苯初始浓度的物质的量比例满足48:8:1.由图7可以看出,当反应体系全部投加Fe2+时降解效果最好,360min时,硝基苯降解率可以达到64.8%,反应符合一级反应动力学;单独投加Fe3+时效果比混合投加Fe2+与Fe3+降解效果要好,且反应过程中体系pH值、DO的变化趋势与反应物Fe2+的投加比例成反比;Fe2+的增加会促进H2O2的分解以及∙OH的生成,使主反应加速,促进降解反应的发生.
2.3 纳米CaO2降解硝基苯机理探究
2.3.1 降解动力学分析 在CaO2投加量、EDTA- Fe2+浓度与硝基苯初始浓度满足48:8:1的最佳物质的量比进行降解动力学曲线拟合,如图8所示.此图线2=0.990>0.98,所以其降解符合一级降解动力学[23-26].
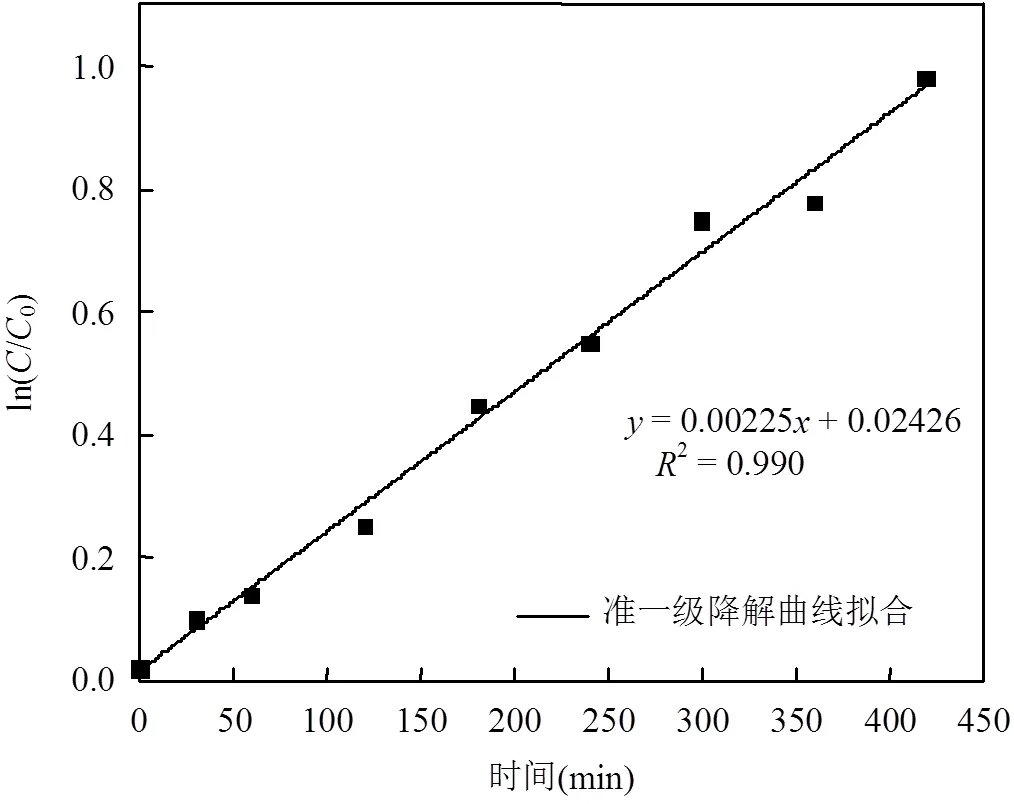
图8 硝基苯静态实验一级动力学反应曲线
2.3.2 纳米CaO2降解硝基苯机理 本试验在CaO2投加量、EDTA-Fe2+浓度与硝基苯初始浓度满足48:8:1的条件下进行.
如图9所示,当不加掩蔽剂时,420min时硝基苯降解率可以达到59.3%;加入CHCl3(掩蔽×O2-)硝基苯降解率为54.8%;加入TBA(掩蔽×OH)硝基苯降解率为21.6%.可以说明在420min的反应时段,反应体系主要是通过×OH氧化分解硝基苯,使得其降解30.7%,而×O2-含量较少,但也能氧化部分硝基苯,约4.5%.同时,反应过程中DO和pH值的变化也符合上述结论.当加入TBA后,反应体系的pH值升高,DO变化更缓,说明体系中发生产生碱性物质以及氧气的降解反应,而加入CHCl3对反应体系的DO和pH影响不明显,说明体系中的反应较缓慢且不明显.
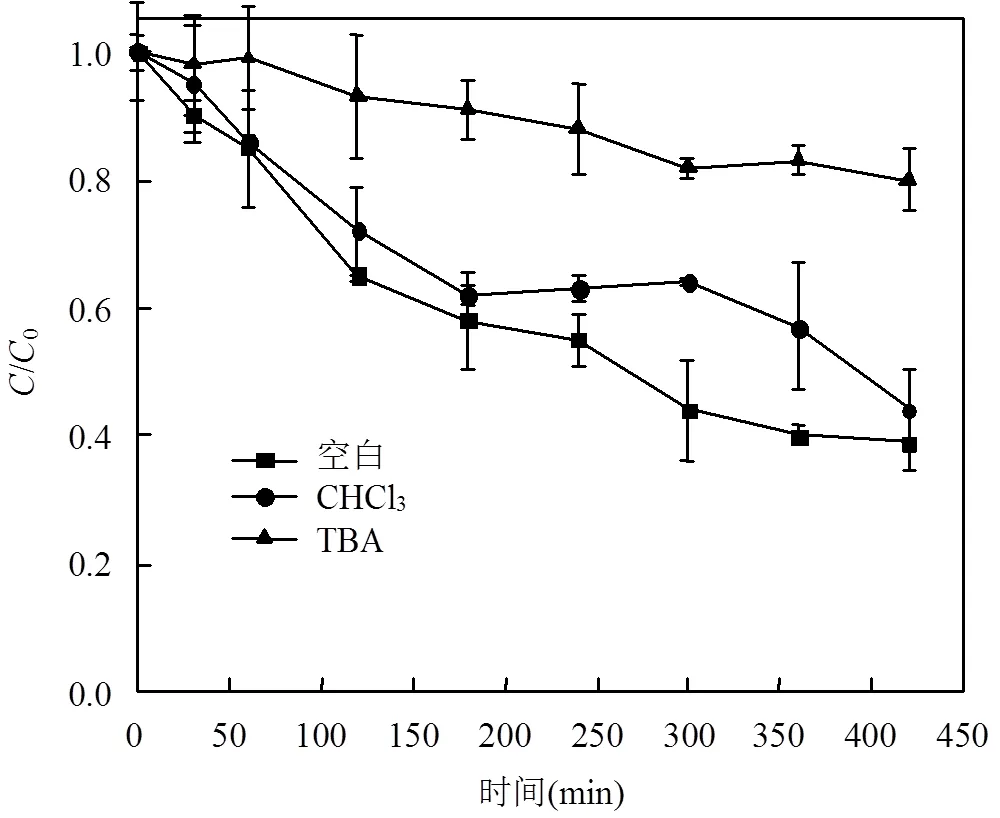
图9 不同掩蔽剂对硝基苯降解效果的影响
2.4 一维柱状动态模拟
图10所表示的为一维柱状模拟中体系中硝基苯的含量变化曲线.随着反应的进行,在不同EDTA- Fe2+注入量条件下,两个反应体系中的硝基苯降解曲线基本一致,在4~5h时动态体系中的硝基苯含量最低,硝基苯约降解77%~86%,且此时pH值、DO都有较明显的上升,说明此时纳米CaO2反应最为明显,其降解速率达到最大.在不同条件下,纳米CaO2的降解效果曲线基本一致,说明在两个反应体系中, EDTA-Fe2+的注入量均可满足实验要求,可以对动态体系中的硝基苯充分降解;12h时可以基本完成, 24h后纳米CaO2反应结束,说明纳米CaO2作为过氧化氢的缓释剂,可以达到缓释×OH进行硝基苯原位修复的效果.
图11表示在一维柱状模拟体系中TOC含量的变化曲线.TOC图像分析,硝基苯本身具有还原性,在刚开始的0~4h, TOC快速下降,说明纳米CaO2氧化反应效率高,大部分有机物直接降解为二氧化碳,在空气中挥发,TOC下降明显;之后,随硝基苯的持续注入,体系中纳米CaO2不足,TOC上升;接着在有足量EDTA-Fe2+的条件下,介质中滞留的少量CaO2在Fe的作用下进行降解,使TOC下降,其中一部分降解为二氧化碳,一部分降解为小分子有机物或者醌类等中间产物,TOC比最初值有所下降;在持续注入硝基苯的后期,体系中纳米CaO2反应完全,TOC逐渐趋于稳定.
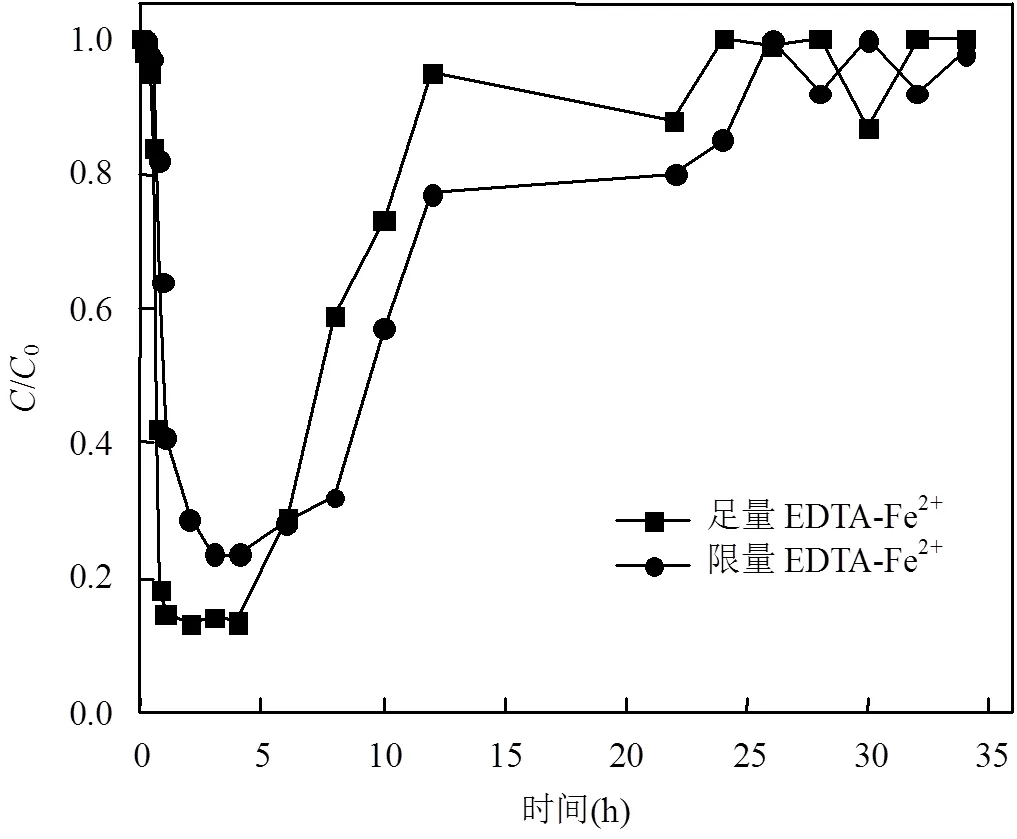
图10 一维柱状模拟硝基苯的降解效果
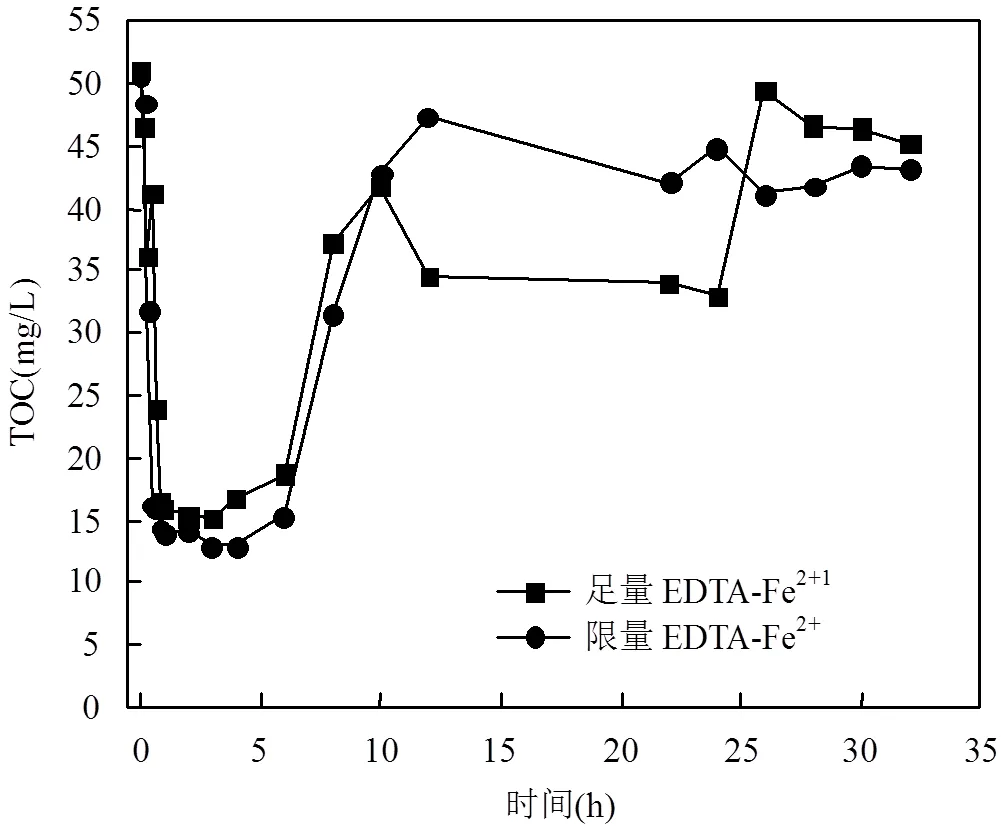
图11 一维柱状模拟体系中TOC变化
3 结论
3.1 在硝基苯浓度为100mg/L的条件下,综合降解率、pH和DO等各项指标,得出CaO2投加量、Fe2+以及硝基苯物质的量比例为48:8:1时,pH波动较小,主反应占优势,硝基苯降解率较高,且在反应体系中主要是通过×OH氧化分解硝基苯.
3.2 在降解最优比条件下,添加HCO3-、SO42-、Ca2+、Mg2+都会使体系pH、DO升高,硝基苯的降解率下降,各离子对该反应抑制能力强到弱为Ca2+> SO42-> HCO3-> Mg2+.
3.3 根据一维柱状动态模拟,在有一定量铁的条件下,纳米CaO2可以作为H2O2的缓释剂,释放×OH,从而达到降解硝基苯的效果,为以后利用纳米CaO2降解粗砂介质地下水环境中有机污染物在实际场地中的应用提供一定的理论基础.
[1] 范春贞,李彩亭,路 培,等.类芬顿试剂液相氧化法脱硝的实验研究.中国环境科学, 2012,32(6):988-993. Fan C Z, Li C T, lu P, et al. Liquid phase oxidation denitrification with fenton reagent Environmental science of China, 2012,32(6):988-993.
[2] Zhang X, Gu X, Lu S, et al. Degradation of trichloroethylene in aqueous solution by calcium peroxide activated with ferrous ion [J]. J. Hazard. Mater. 2015,284:253-260.
[3] 殷雪妍,张 艾,刘亚男.过氧化钙去除水中糖皮质激素的响应面分析[J]. 中国环境科学, 2018,38(2):608-615. Yin X Y, Zhang A, Liu Y N. Response surface analysis of glucocorticoid removal by calcium peroxide in water [J]. Chinese Journal of Environmental Science, 2008,38(2):608-615.
[4] Schmidt J T, Ahmad M, Teel A L, et al. Hydrogen peroxidestabilization in one-dimensional flow columns [J]. Journal of Contaminant Hydrology, 2011,126(1/2):1-7.
[5] 白润英,陈 湛,张伟军,等.过氧化钙预处理对活性污泥脱水性能的影响机制[J]. 环境科学, 2017,38(3):1151-1158. Bai R Y, Chen Z, Zhang W J, Wang D S. Calcium peroxide pretreatment effect on the performance of activated sludge dewatering system [J]. Journal of environmental science, 2017,38(3):1151-1158.
[6] 张金贵.纳米过氧化钙联合污泥裂解液降解土壤中四溴双酚A的研究[D]. 大连:大连理工大学, 2016. Zhang J G. Degradation of tetrabromobisphenol a in soil by nanometer calcium peroxide combined with sludge cracking solution [D]. Dalian: Dalian University of Technology, 2016.
[7] 李 爽,李正阳,马会强.过氧化钙制备方法及在环境修复应用中的研究进展[J]. 当代化工, 2015,44(12):2808-2810. Li S, li Z Y, Ma H Q. Preparation of calcium peroxide and its application in environmental restoration [J]. Contemporary chemical industry, 2015,44(12):2808-2810.
[8] Wang H F, Zhao Y S, Li T Y, et al. Properties of calcium peroxide for release of hydrogen peroxide and oxygen: a kinetics study [J]. Chemical Engineering Journal., 2016,29(4):765-770.
[9] 鲁秀国.过氧化钙的制备及其在环境保护方面的应用研究进展[C]//中国环境科学学会.2014中国环境科学学会学术年会(第十二章).中国环境科学学会, 2014:5. Lu X G. The preparation of calcium peroxide, and its application research progress in the field of environmental protection [C]//China environmental science society. 2014 academic annual meeting of China Environmental Science Society (chapter 12). China Environmental Science Society, 2014:5.
[10] 孙远军.4种稳定剂对河流底泥黑臭现象的改善效果及对重金属毒性的影响[C]//中国环境科学学会.2013中国环境科学学会学术年会论文集(第五卷).中国环境科学学会, 2013:6. Sun Y J. 4kinds of stabilizer on the improvement of the phenomenon of river sediment black smelly effect and toxicity ofheavy metals by [C]//China environmental science society. 2013 academic essays of China environmental science society (v.). China Environmental Science Society, 2013:6.
[11] Xu J, Pancras T, Grotenhuis T. Chemical oxidation of cable insulating oil contaminated soil [J]. Chemosphere, 2011,84:272-277.
[12] 吴长安.过氧化钙对土壤中砷生物有效性的影响[J]. 广东化工, 2012,39(8):29-30,19. Wu C A. Effects of calcium peroxide on the bioavailability of arsenic in soil [J]. Guangdong chemical industry, 2012,39(8):29-30,19.
[13] 周彦波,王英秀,周振华,等.过氧化钙缓释氧剂的制备及其释氧特性研究[J]. 中国给水排水, 2012,28(7):64-67.Zhou Y B, Wang X Y, Zhou Z H, et al. Preparation of calcium peroxide sustained-release oxygen agent and its oxygen release characteristics [J]. China Water Supply and Drainage, 2012,28(7):64-67.
[14] 刘丽娟,廖运文,高 辉.过氧化钙降解污水中腐植酸的初探[J]. 绵阳师范学院学报, 2018,37(5):118-122,127. Liu L J, Liao Y W, Gao H. Preliminary study on humic acid in wastewater degraded by calcium peroxide [J]. Journal of Mianyang Normal University, 2008,37(5):118-122,127.
[15] 郑友平,林亲铁,姜洁如,等.过氧化钙修复有机污染土壤的研究进展[J]. 土壤通报, 2017,48(5):1275-1280. Zheng Y P, Lin Q T, Jiang J R, et al. Research progress on the repair of organic contaminated soil by calcium peroxide [J]. Chinese Soil Science Bulletin, 2017,48(5):1275-1280.
[16] 李天一,张成武,郭 超,等.纳米CaO2在含水层的迁移特性及对氯酚降解效果[J]. 中国环境科学, 2017,37(8):3028-3035 Li T I, Zhang C W, Guo C, et al. The migration characteristics of nano-CaO2in the aquifer and its degradation effect on chlorophenol [J]. Chinese Journal of Environmental Science, 2017,37(8):3028-3035
[17] Janda A,Marcinkowski T. Fenton process modification pssibilities for oxidation effectiveness of hard degradable organic pollutants. [J]. Orhrona Srodowiska, 2019,41:47-53.
[18] Pan Y, Su H R, Zhu Y T, et al. CaO2based Fenton-like reaction at neutral pH: Accelerated reduction of ferric species and production of superoxide radicals [J].Water Research, 2018,145:731-740.
[19] 饶品华.过氧化钙和零价铁对EDTA溶液中铜的去除研[C]//武汉大学.Proceedings of Conference on Environmental Pollution and Public Health.武汉大学, 2010:3. Rao P H. Calcium peroxide and zero-valent iron copper removal in the process of EDTA solution [C]//Wu Han university. Proceedings of Conference on Environmental Pollution and Public Health: Wuhan University, 2010:3
[20] Qian Y J, Zhang J, Zhang Y L, et al. Degradation of 2,4 dichlorophenol by nanoscale calcium peroxide:Implication for groundwater remediation [J]. Separation and Purification Technology, 2016,166:222-229.
[21] 李明玉,田依林,唐启红.无机离子对Fenton降解水中苯胺的影响[J]. 化学通报, 2003,6:54-57. Li M Y, Tian Y L, Tang Q H. Effect of inorganic ions on degradation of aniline in Fenton water [J]. Chemical bulletin, 2003.6:54-57
[22] Lu Ming-Chun, Zhang Hui, Huang Yin-Yeb, et al. Influence of inorganic irons on the mineralization of 2,4Dintrophenol by the fenton reaction.Fresenius environmental bulletin, 2005,2:101-104
[23] 张 嫦,吴莉莉,周小菊,等.过氧化钙的制备及其在废水处理中的应用[J]. 化工环保, 2004,(1):62-65. Liu S, Wu L L, Zhou X J, et al. preparation of calcium peroxide and its application in wastewater treatment [J]. Environmental Protection of Chemical Industry, 2004,(1):62-65.
[24] Mon-Lin Chou, Jiin-Shuh Jean, Chwen-Ming Yang, et al. Inhibition of ethylenediaminetetraacetic acid ferric sodium salt (EDTA-Fe) and calcium peroxide (CaO2) on arsenic uptake by vegetables in arsenic-rich agricultural soil [J]. Journal of Geochemical Exploration, 2016,163:19-27.
[25] Abraham Northup, Daniel Cassidy. Calcium peroxide (CaO2) for use in modified Fenton chemistry [J]. Journal of Hazardous Materials, 2007,152(3):1164-70.
[26] Qian Yajie, Zhou Xuefei, Zhang Yalei, et al. Performance and properties of nanoscale calcium peroxide for toluene removal [J]. Chemosphere, 2013,91(5):717-723.
Effect of nano calcium peroxide on the fenton-like degradation of nitrobenzene in groundwater.
DONG Jia-Lin1,2, FU Shuang3, ZHOU Hao1,2, LI Tian-Yi1,2, QIN Chuan-Yu1,2*
(1.Key Laboratory of Groundwater Resources and Environment, Ministry of Education, Jilin University, Changchun 130021, China;2.College of Environment and Resources, Jilin University, Changchun 130021, China;3.College of Environmental Science and Engineering, Shanghai Jiaotong University, Shanghai 200240, China)., 2019,39(11):4730~4736
To investigate the feasibility of using the modified fenton (MF) with nanometer calcium peroxide (nano-CaO2) for the remediation of contaminated groundwater, this study firstly improved the method for preparation of the nano-CaO2, and achieved the effective content of 88.35%. Then, through the evaluation of changes in pH, DO and nitrobenzene concentrations in a static test, the nano-CaO2based nitrobenzene degradation process and the influencing factors were investigated, and the kinetics and the best reaction conditions of the nitrobenzene degradation were also clarified. In addition, the validity of different free radicals was studied by the masking experiments. Finally, by performing the dynamic simulation in a one-dimensional simulation column, the mechanism and efficacy of the nano-CaO2based nitrobenzene removal were also accessed. The results showed that the degradation efficacy was best, when the concentration ratio of CaO2, EDTA-Fe2+and the nitrobenzene was 48:8:1, and the degradation curve fitted to the first-order kinetic curve. It was also demonstrated that the main degradation radical in the reaction process was×OH, and the degradation efficiency was affected by HCO3-, SO42-, Ca2+and Mg2+plasma. According to the simulation test in the one-dimensional simulation column, it was revealed that with existing proper amount of iron, nano-CaO2could be a sustained release agent of hydrogen peroxide, and correspondingly, free radical induced degradation would be enabled through Fenton-like catalytic reaction, which indicated nano-CaO2would have a good application prospect in site remediation.
nanometer calcium peroxide;Fenton-like technology;degradation effect;influencing factors
X523
A
1000-6923(2019)11-4730-07
董家麟(1995-),女,广西南宁人,吉林大学本科生,主要从事水土污染控制与治理方面的研究.发表论文1篇.
2019-03-07
国家自然科学基金资助项目(41572213,41530636)
* 责任作者, 副教授, qincyu@jlu.edu.cn

