多因素对ANAMMOX菌利用零价铁还原硝酸盐过程影响
宋 歌,张文静,2,3,毕 贞,2,3*,黄 勇,2,3,董石语,3
多因素对ANAMMOX菌利用零价铁还原硝酸盐过程影响
宋 歌1,张文静1,2,3,毕 贞1,2,3*,黄 勇1,2,3,董石语1,3
(1.苏州科技大学环境科学与工程学院,江苏 苏州 215009;2.城市生活污水资源化利用技术国家地方联合工程实验室,江苏 苏州 215009;3.苏州科技大学环境生物技术研究所,江苏 苏州 215009)
以厌氧氨氧化(ANAMMOX)菌利用零价铁还原硝酸盐体系为研究对象,采用单因素调控法结合中心复合法(CCD)系统研究铁形态、进水pH值、温度、Fe/N等对该体系中硝酸盐去除率的影响.结果表明,在相同的反应条件下,投加纳米铁时ANAMMOX体系中硝酸盐的去除效果最优;反应温度和Fe/N对体系中硝酸盐去除率影响十分显著,而进水pH值影响较弱.利用CCD法得出模型预测的最佳反应条件为:进水pH值为4.00,反应温度为35.00℃,Fe/N为38.23,预测的硝酸盐去除率为94.70%,实际实验得出的硝酸盐去除率为88.99%.
厌氧氨氧化(ANAMMOX);硝酸盐;零价铁;中心复合(CCD)法
厌氧氨氧化(ANAMMOX)作为一种污水处理领域新兴起的脱氮工艺,因其低耗高效的脱氮方式成为人们研究的热点[1],该过程由厌氧氨氧化细菌 (AnAOB)以NO2-为电子受体将NH4+氧化为氮气[2].从污水处理角度来看,ANAMMOX技术是已知最经济、节能、环保、高效的生物脱氮技术[3].目前以ANAMMOX技术为核心的新型脱氮工艺,如全程自养脱氮、部分亚硝酸化-厌氧氨氧化等主要是用来处理高氨氮废水[4-5].但是,该工艺会产生10.00%左右的硝酸盐副产物,因此无法达到总氮的完全去除,导致出水水质难以达标该过程[6].为了解决这个问题,ANAMMOX工艺通常会与异养反硝化工艺联合以去除ANAMMOX过程产生的硝酸盐.然而,在ANAMMOX联合异养反硝化工艺中,外源性有机物的投加会导致反硝化细菌的大量滋生,增加污泥产量,提高运行成本[7-8].因此若要解决联合异养反硝化带来的一系列问题,就必须找到一种有效的方法利用ANAMMOX菌自身解决其残留的硝酸盐问题.
零价铁化学性质活泼、来源丰富、价格低廉;具有强还原能力,已被应用于地下水中硝酸盐原位与异位修复.2013年,Oshiki等[9]发现ANAMMOX菌可以利用Fe2+为电子供体,将硝酸盐还原成亚硝酸盐和氨,再由ANAMMOX反应生成氮气.周健等[10]报道投加ANAMMOX污泥可以强化Fe0还原硝酸盐.上述理论研究成果为解决ANAMMOX工艺硝酸盐残留问题提供了一种新思路.然而,在Fe0化学还原硝酸盐体系中,硝酸盐还原速率受Fe0形态、pH值、温度、Fe/N等影响.因此若要将此机理应用于实际工艺中,就必须找到合适的反应条件优化硝酸盐去除效果.基于此本实验采用单因素调控结合CCD法探究Fe0形态、进水pH值、温度和Fe/N对ANAMMOX菌利用Fe0去除硝酸盐体系的影响,旨在优化ANAMMOX菌利用Fe0去除硝酸盐工艺条件,对ANAMMOX工艺自身产生的硝酸盐进行原位处理提供一种新的思路.
1 材料与方法
1.1 实验材料与水质
实验污泥来自于实验室长期运行的有效体积为60.00L的ANAMMOX反应器,污泥颗粒平均粒径1.60mm、呈砖红色,污泥性状较好,总氮去除速率在9.00kg/(m3·d)左右.实验选用不同形态和粒径的Fe0,包括:铁粉(粒径150.00μm)、铁屑(粒径5.00mm)和纳米铁(粒径50.00nm),铁含量³98.00%.为去除Fe0表面覆盖的氧化物,使用前需活化,即先用0.50mol/L HCl淘洗,再用脱氧一级水反复冲洗数次、直至浸出液的 pH值为中性.为避免被空气氧化,活化后的Fe0须立即使用.反应条件(pH值、温度、Fe/N)根据各批式实验需要调节.
实验采用人工配制的含硝酸盐废水,主要成分包括硝酸钠和ANAMMOX菌生长所必须的营养盐,如表1组成.
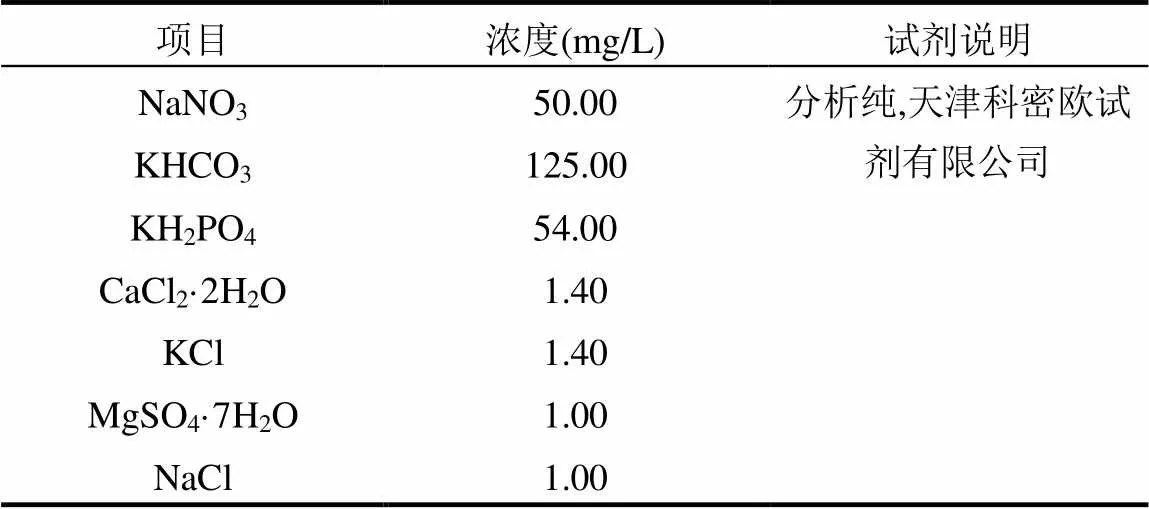
表1 废水组成
1.2 实验装置和操作过程
实验所使用的装置均为容量120.00mL的厌氧血清瓶,依据实验设计(详见1.4),向每个瓶中加入一定量的ANAMMOX微生物(MLVSS为150.00mg/L)、Fe0和配制的硝酸盐废水定容至100.00mL,并分别调节pH值.为了保持厌氧条件,每个血清瓶使用 99.50%的氮气曝气10.00min以排除溶解氧,并立刻用橡胶塞加铝盖密封.将血清瓶固定于恒温水浴振荡器内、遮光处理,保持转速为150.00r/min.在反应过程中用注射器连续取样2.00mL(0,12,24,36h)测定以下指标.
1.3 测定指标和方法
运行过程中反应器进出水pH值、NH4+-N、NO2--N、NO3--N、Fe2+、总Fe按照文献[11]进行测定,如表2所示.

表2 测定项目与方法
1.4 中心复合法(CCD)分析方法
采用CCD法对硝酸盐去除率受进水pH值、温度、Fe/N多个变量影响的问题进行建模分析.每个影响因素取3个水平,以-1、0、1编码.应用Design- Expert 8.0.6中CCD法设计实验表,其中分别设定进水pH值为4.00, 6.00, 8.00,温度为15.00,35.00, 55.00 ℃, Fe/N为2.00, 26.00, 50.00.根据Design- Expert 8.0.6中CCD法设计实验生成的实验组共有17个,其中前12组是3个因子的交叉影响实验,后5组是3个因子在0自由度的重复实验.对实验结果进行二次回归拟合,生成含有变量因子交互项和平方项的二次方程:
Y=0+∑bXi+∑bXij+∑bX2(1)
式中:Y是预测的目标值(即硝酸盐去除率);X和X是变量;0是常数项;b是线性系数;b是交互作用系数;b是二次项系数.通过对模型的方差、值、值以及回归系数分析,判断该模型的拟合程度以及对目标值的响应程度.各项系数值反映出对应的变量因子及其交互作用对目标值的影响程度,由此可以探讨进水pH值、温度、Fe/N对硝酸盐去除率影响的显著程度,以及三因素交互作用对硝酸盐去除率的影响[12-14].
2 结果与分析
2.1 不同形态的零价铁对体系内硝酸盐去除效果影响
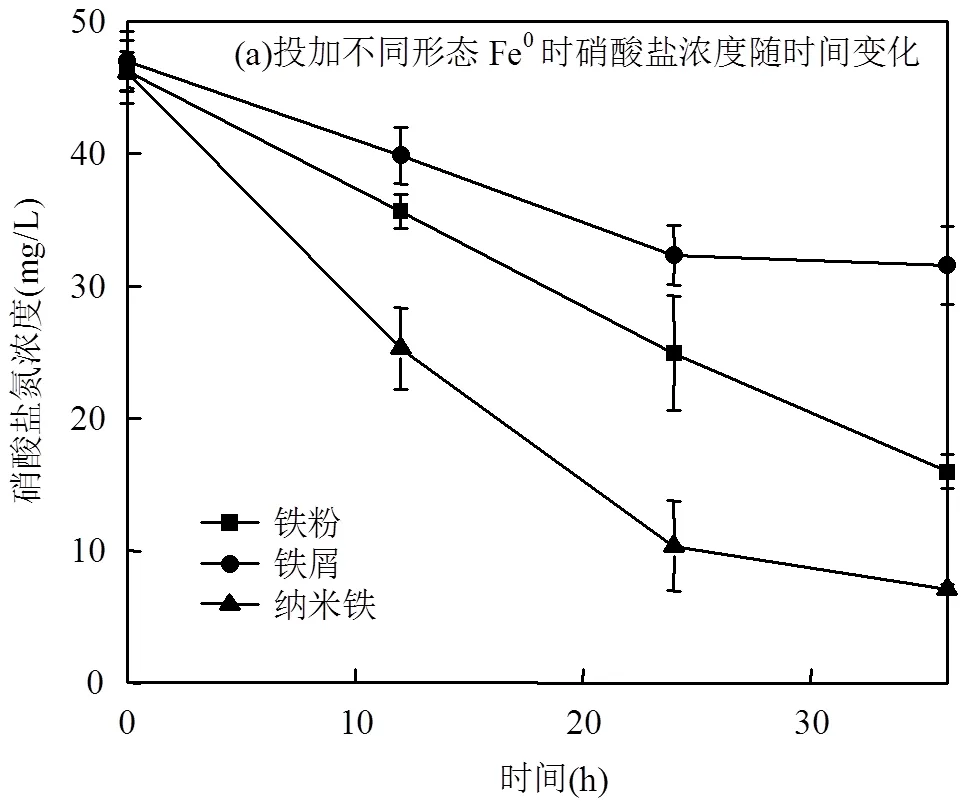
本实验采用单因素调控法研究在进水pH值为6.00,温度为35.00℃,Fe/N为50.00的情况下不同形态的Fe0(铁粉、铁屑、纳米铁)对ANAMMOX菌还原硝酸盐体系的影响.反应过程中液相硝酸盐浓度变化如图1(a)所示.在相同的反应条件下,不同形态的Fe0对硝酸盐的去除速率和效果有很大差异.反应12h后,各组内硝酸盐浓度都呈现下降趋势,纳米铁组、铁粉组和铁屑组剩余硝酸盐浓度分别为(25.29 ± 3.08)mg/L、(35.66 ± 1.26)mg/L、(39.89 ± 2.14)mg/L.此后各组液相硝酸盐浓度随反应时间延长不断下降,第36h,纳米铁组剩余的硝酸盐浓度仅为(7.09± 0.38)mg/L,而其余两组剩余的硝酸盐浓度明显高于纳米组,其中铁屑组硝酸盐浓度最高(31.58± 2.96)mg/L.同时,根据液相中氨氮、亚硝酸盐氮浓度变化可知,反应36h后,3组实验液相中都出现了明显的氮损失(图1(b)),计算可得3组硝酸盐去除率分别是84.97%、65.58%、33.38%,相应的总氮去除率分别为81.48%、61.36%、32.99%.显然,纳米铁组硝酸盐去除率和总氮去除率均明显优于其他两组.基于此结果,后续应用CCD法研究均使用纳米铁作为电子供体.
2.2 温度、pH值和Fe/N对体系内硝酸盐去除效果影响与最优解
应用CCD法探究进水pH值、温度、Fe/N对ANAMMOX菌还原硝酸盐体系的影响以及各因子交互作用对硝酸盐还原的影响.由软件生成的实验设计表以及实验结果见表3.根据实验结果,对硝酸盐去除率与各变量因子进行二次拟合,得到下列方程:
=83.20-6.251+19.502+26.003+1.5012+
3.0013+7.0023-0.6012-17.1022-22.6032(2)
式中:表示硝酸盐去除率%,1、2、3分别代表进水pH值、反应温度()以及Fe/N.由表3可以看出,在设定实验范围内,反应条件的变化对硝酸盐去除率有显著影响.不同实验条件组合下,模拟得到的硝酸盐去除率最高可达93.75%,最低仅为7.59%.表4是方差分析表,详细提供了值、值以及回归系数.模型的值是回归均方和与残差均方和的比值,模型的越大表明该模型越接近实际,模型越显著;拟合模型的值£0.0500,说明回归方程的关系是显著的;若£0.0100,说明回归方程的关系是极显著的.本实验模型的值为30.69,值<0.0001,表明该模型对实验值能高度拟合,且出现误差的几率仅有0.01%.
另外,该模型的相关系数2为0.98,也表明该模型的拟合程度很好,实验误差小;模型的校正系数Adj2为0.94,说明该模型能解释94.35%的响应值变化.由表4可知,由于反应温度与投加Fe/N的值均小于0.0001,所以这2个因素是影响硝酸盐去除率最关键的因素.相比之下,进水pH值这一因素的值为0.0345,说明在实际过程中,反应进水pH值在4.00~8.00范围对体系内的硝酸盐去除效果影响较弱,这一结果与模拟出的二次方程的各因素前的系数相吻合.二次项中,12的回归系数不显著(>0.0500),而22和32的回归系数达到极其显著水平(<0.0100),说明进水pH值的二次效应对体系内的硝酸盐去除率无显著影响,温度和Fe/N的二次效应对体系内的硝酸盐去除率有极其显著影响.模型方程的信噪比“Adeq.precision”值为17.57,大于4.00,表明该模型可以很好的模拟硝酸盐去除率.
利用CCD法可以进一步分析进水pH值、温度、Fe/N 3个因素交互作用下对硝酸盐去除率的影响.如图2所示,每个等高线图代表2个独立影响因素之间的相互作用,此时第3个影响因素保持在最佳水平.图2(a)是当Fe/N为26.00、受进水pH值与温度交互影响下的硝酸盐去除率等高线图.当温度由15.00℃升高到55.00℃时,硝酸盐去除率明显提高,且pH值越低时硝酸盐去除率的增幅越明显;同时,当进水pH值由4.00~8.00之间变化时,硝酸盐去除率随pH值的升高会略有下降.与进水pH值相比,温度对硝酸盐去除率的影响更为显著.当温度大于35.00℃,进水pH值在4.00~8.00范围内,硝酸盐去除率均能达到80.00%以上.
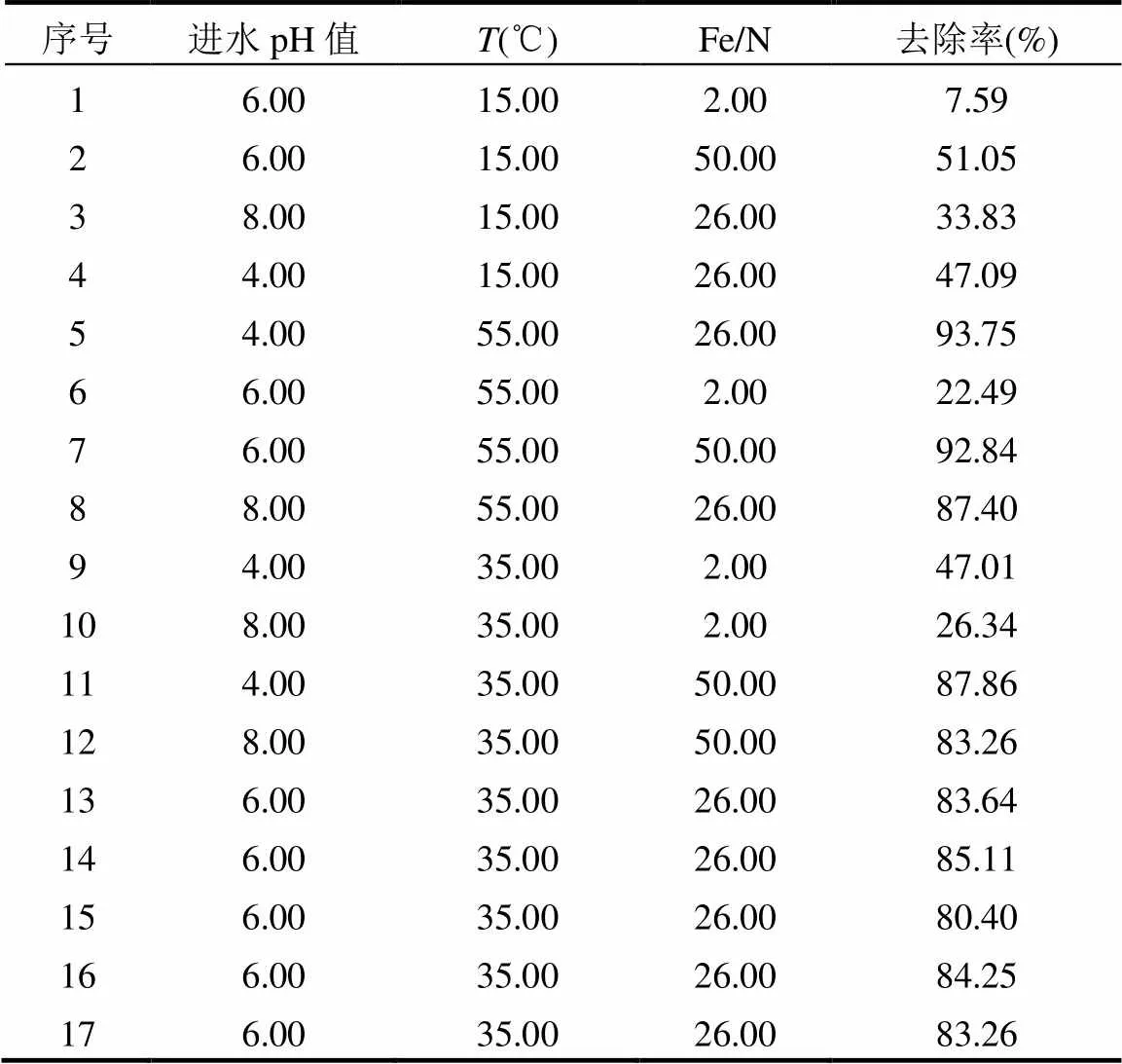
表3 实验设计矩阵和结果
图2(b)是当反应温度为35.00℃、受进水pH值与Fe/N交互影响下的硝酸盐去除率等高线图.当Fe/N由2.00逐渐提高至26.00时,硝酸盐去除率相应由40.00%提高至89.00%,继续增大Fe/N至50.00,硝酸盐去除率并未明显提高,这表明当投加的Fe0已足量时,继续增大Fe/N反而会造成铁的过剩.相比之下,进水pH值对硝酸盐去除率的影响十分有限,随着pH值的升高,硝酸盐去除率只是略有下降.模拟结果显示,只要Fe/N大于26.00,进水pH值在4.00~7.00范围内,硝酸盐去除率均能达到88.00%以上.
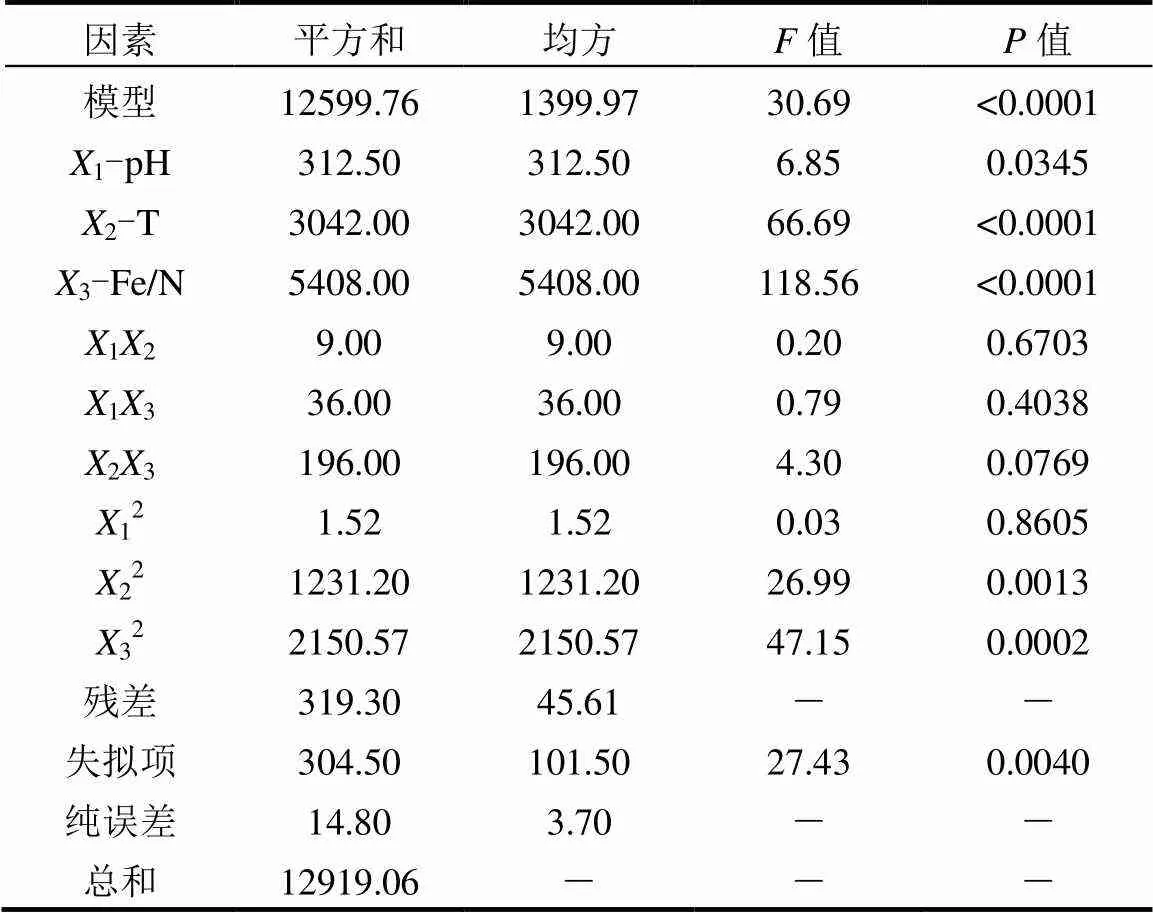
表4 方差分析表
注:相关系数(2)=0.98;校正系数(Adj2)=0.94;信噪比(Adeq precision) = 17.57.
图2(c)是当反应进水pH值为6、受温度与Fe/N交互影响下的硝酸盐去除率等高线图.与图2(a)和(b)不同的是,图中各条等高线的曲度明显增大,且温度和Fe/N同时对硝酸盐去除率产生了显著的影响.当温度由15.00℃升高至55.00℃时,硝酸盐去除率随Fe/N的增大而明显提高,且温度越高,这种趋势越明显.同时,Fe/N在2.00~50.00之间变化时,硝酸盐去除率随温度上升而提高,且Fe/N越高,这种趋势越明显.由此可见,当温度大于35.00℃、Fe/N大于26.00,硝酸盐去除率均能达到90.00%以上;在此基础上提高温度或Fe/N,对于进一步提高硝酸盐去除率并无明显作用.
根据软件模拟出的模型方程,自动生成各因素对硝酸盐去除率的最优解以及预测的响应值.模型生成的最优反应条件为:进水pH值为4.74、温度为45.27℃、Fe/N为38.72,此时模拟出的硝酸盐去除率能够达到100.00%.然而,实际实验中当反应温度为45.00℃时,ANAMMOX菌活性大大降低,体系内硝酸盐与Fe0之间的化学反应占主导,还原产物主要为氨氮和少量亚硝酸盐氮,此时体系的总氮去除率仅为14.49%.因此,综合考虑硝酸盐去除率与总氮去除率,将温度设定为35℃,在此条件下模型预测的最优反应条件应为:进水pH值=4.00、温度=35.00℃、Fe/N=38.23,此时硝酸盐去除率达到最优值94.70%.通过实验验证,在此条件下实际测得的硝酸盐去除率为88.99%,略低于模型预测值.

3 讨论
在本实验中,通过单因素实验考察了不同形态Fe0作用下ANAMMOX菌还原硝酸盐的速率,再通过CCD法探讨进水pH值、温度、Fe/N及其交互作用对这一过程的影响. ANAMMOX 菌可以有效利用不同形态的Fe0还原硝酸盐,其还原速率和效率与Fe0的形态有关;同时,温度、进水pH值和Fe/N 3个因素在不同程度上影响硝酸盐的去除率.
3.1 Fe0形态对硝酸盐去除率的影响
纳米铁对体系内硝酸盐的去除效果明显优于铁粉组和铁屑组.首先,Fe0的粒径越小,其比表面积越大,因此纳米铁可以很容易地通过孔隙扩散到细胞的各个区域;其次,由于比表面积大,纳米铁表面与液相接触的活性质点多,相较于铁粉和铁屑具有更高的反应活性,越有利于反应的进行[15];此外,纳米铁具有较高的表面位点内在活性和较高的活性表面位点密度[16].因此,纳米铁可获得更优的硝酸盐去除效果.在本实验中,经过36h反应,加入纳米铁的实验组硝酸盐去除效果最佳.但是延长反应时间,铁粉组可以获得与纳米铁组几乎相等的硝酸盐去除率.因此,在实际应用过程中,考虑到成本问题,选择铁粉是更经济的方案.
3.2 进水pH值、温度、Fe/N对硝酸盐去除率的影响
进水pH值、温度、Fe/N是影响硝酸盐还原效果的重要因素.本实验中,在初始硝酸盐浓度相同的情况下,当温度和进水pH值皆在最优的条件下, Fe/N成为影响硝酸盐去除率的重要因素之一.随着纳米铁投加量的增加,即Fe/N增大,硝酸盐的去除率明显提高.当Fe/N大于34.00,体系内的硝酸盐去除率均能达到90.00%以上,总氮去除率达到84.00%.在此基础上再增加Fe/N,对硝酸盐的去除效率并没有显著改善.Fe/N对ANAMMOX菌还原硝酸盐过程的影响,体现在化学反应和生物反应两方面.化学反应方面,当硝酸盐浓度一定时,Fe/N成为影响硝酸盐还原的限制因素,增加Fe/N可以提高Fe0化学还原硝酸盐的反应速率.生物反应方面,铁元素对包括ANAMMOX菌在内的多种微生物均能起到加快反应速率、提高代谢活性的作用[20].Fe0通过水解作用不断释放出铁离子,可以提高ANAMMOX微生物代谢活性,强化硝酸盐的生物还原过程.因此,当温度和pH值在合适的范围内,只要保证体系内的Fe0过量,硝酸盐的去除效果就能达到90.00%以上.在其他研究零价铁还原硝酸盐的文献中,由于反应条件不同,得出的最佳Fe/N也不同[17-19].
温度是决定硝酸盐去除率的另一个重要因素,其影响体现在Fe0化学还原硝酸盐和ANAMMOX微生物代谢两方面.一方面,Fe0还原硝酸盐的化学反应受温度影响,提高温度可以激发反应活化能,有利于反应的进行,最终的脱氮效果越好[21-22].另一方面,ANAMMOX菌为嗜中温菌,其对温度较为敏感,适宜的生长温度在30.00~37.00℃之间,低温会阻碍ANAMMOX菌细胞间的物质传递,导致细胞活性降低直至死亡;高温则易使ANAMMOX菌细胞内的温度敏感组分变性,导致菌体失活[23].本实验表明,在pH值和Fe/N在合适的范围内,温度越高, ANAMMOX菌体系内硝酸盐去除率越高,当温度大于35.00℃时,硝酸盐去除率均能达到80.00%以上,总氮去除率达到70.00%,在此基础上继续升高温度对硝酸盐去除率并无显著影响.但若温度过高、超过ANAMMOX菌适宜温度范围后,硝酸盐的转化是以Fe0的化学还原为主,液相中氨氮、亚硝酸盐氮会有明显积累,导致总氮去除率降低.
Fe0化学还原硝酸盐反应是酸驱动过程,pH值越低则体系中的H+质量浓度越大,越有利于铁表面的腐蚀,可有效提高硝酸盐的还原速率[24-25].Zhang等[24]发现,pH值越低,零价铁去除垃圾渗滤液中的硝酸盐效率越高.当pH值为2时,反应24h后,几乎所有的硝酸盐都被去除,且硝酸盐去除率随pH值的升高而降低.而当pH值大于5时,体系内被还原掉的硝酸盐几乎可以忽略不计.而在本实验,当进水pH值从4变化到8时,硝酸盐去除率并没有显著下降,这是由于在本反应体系中,除化学反应外还有ANAMMOX菌的生物反应.ANAMMOX反应消耗H+产生碱度,从而能够中和体系内偏酸性环境,而且ANAMMOX菌能够利用零价铁溶出的Fe2+将硝酸盐生物还原.因此,进水pH值对硝酸盐去除影响不显著,当温度和Fe/N在合适的范围内,保持进水pH值在4.00~ 8.00之间,此体系内的硝酸盐能得到有效去除.
综上所述,ANAMMOX菌利用Fe0去除硝酸盐的过程受温度和Fe/N的影响显著,而受进水pH值影响较弱.当温度为35.00℃,Fe/N大于34.00,进水pH值在4.00~8.00之间变化时,ANAMMOX菌能够利用Fe0有效去除水体中88.99%的硝酸盐.上述结果为ANAMMOX工艺自身产生的硝酸盐进行原位处理提供了一种新的解决方案,在后续的研究中可以将Fe0投加到ANAMMOX反应器内,以考察其自身将反应生成的硝酸盐去除的能力.
4 结论
4.1 在适宜的反应条件下,ANAMMOX菌可以利用Fe0去除水体中的硝酸盐.
4.2 在ANAMMOX利用Fe0还原硝酸盐体系中投加等量不同形态Fe0时硝酸盐的去除效率由高到低分别为:纳米铁>铁粉>铁屑.
4.3 根据CCD法拟合出的模型方程值为30.69,值<0.0001,2为0.98,表明该模型拟合程度很好.
4.4 Fe/N和温度这2个因素的值均小于0.0001,表明Fe/N和温度对ANAMMOX菌去除硝酸盐过程的影响显著.相比之下,进水pH值这一因素的P值为0.0345,其对硝酸盐去除效果影响较弱.当温度为35.00℃,Fe/N为38.23,进水pH值为4.00时,硝酸盐去除率最高,可达88.99%.
[1] Oshiki M, Satoh H, Okabe S, et al. Ecology and physiology of anaerobic ammonium oxidizing bacteria [J]. Environmental Microbiology, 2016,18(9):2784-2796.
[2] Feng Y, Zhao Y P, Guo Y Z, et al. Microbial transcript and metabolome analysis uncover discrepant metabolic pathways in autotrophic and mixotrophic anammox consortia [J]. Water Research, 2018,128:402-411.
[3] 周 正,王 凡,林 兴,等.中试一体式部分亚硝化-厌氧氨氧化反应器的启动与区域特性[J]. 环境科学, 2018,39(3):1301-1308. Zhou Z, Wang F, Lin X, et al. Start-up and regional characteristics of a pilot-scale integrated PN-ANAMMOX reactor [J]. Environmental Science, 2018,39(3):1301-1308.
[4] Lackner S, Gilbert E M, Vlaeminck S E, et al. Full-scale partial nitritation/anammox experiences-An application survey [J]. Water Research, 2014,55(10):292-303.
[5] Soliman M, Eldyasti A. Ammonia-oxidizing bacteria (AOB): opportunities and applications-a review [J]. Reviews in Environmental Science and Bio/Technology, 2018,17(2):285-321.
[6] Cao Y, Hong K B, van Loosdrecht M C, et al. Mainstream partial nitritation and anammox in a 200,000m3/day activated sludge process in Singapore: scale-down by using laboratory fed-batch reactor [J]. Water Science and Technology, 2016,74(1):48-56.
[7] Cao Y, Hong K B, Zhou Y, et al. Mainstream partial nitritation/ anammox nitrogen removal process in the largest water reclamation plant in Singapore [J]. Journal of Beijing University of Technology, 2015,41(10):1441-1454.
[8] 付昆明,付 巢,李 慧,等.主流厌氧氨氧化工艺的运行优化及微生物的群落变迁[J]. 环境科学, 2018,39(12):5596-5604. Fu K M, Fu C, Li H, et al. Optimization of the mainstream anaerobic ammonia oxidation process and its changes of the microbial community [J]. Environmental Science, 2018,39(12):5596-5604.
[9] Oshiki M, Ishii S, Yoshida K, et al. Nitrate-dependent ferrous iron oxidation by anaerobic ammonia oxidation (ANAMMOX) bacteria [J]. Applied and Environmental Microbiology, 2013,79(13):4087-4093.
[10] 周 健,黄 勇,袁 怡,等. ANAMMOX菌利用零价铁转化氨和硝酸盐实验[J]. 环境科学, 2015,36(12):4546-4552. Zhou J, Huang Y, Yuan Y, et al. Simultaneous biotransformation of ammonium and nitrate via zero-valent iron on anaerobic conditions [J]. Environmental Science, 2015,36(12):4546-4552.
[11] 国家环境保护总局.水和废水监测分析方法 [M]. 4版.北京:中国环境科学出版社, 2002.
[12] Su J F, Shao S C, Huang T L, et al. Anaerobic nitrate-dependent iron(II) oxidation by a novel autotrophic bacterium, Pseudomonas sp. SZF15 [J]. Journal of Environmental Chemical Engineering, 2015,3: 2187-2193.
[13] Zhang Q, Ji F F, Xu X Y, et al. Optimization of nitrate removal from wastewater with a low C/N ratio using solid-phase denitrification [J]. Environmental Science and Pollution Research, 2016,23:698-708.
[14] Wang H B, Hu C, Shen Y, et al. Response of microorganisms in biofilm to sulfadiazine and ciprofloxacin in drinking water distribution systems [J]. Chemosphere, 2019,218:197-204.
[15] Wang S S, Zhou Y X, Gao B, et al. The sorptive and reductive capacities of biochar supported nanoscaled zero-valent iron(nZVI) in relation to its crystallite size [J]. Chemosphere, 2017,186:495-500.
[16] Xu J, Cao Z, Wang Y, et al. Distributing sulfidized nanoscale zero-valent iron onto phosphorus-functionalized biochar for enhanced removal of antibiotic florfenicol [J]. Chemical Engineering Journal, 2019,359:713-722.
[17] Zhang Y P, Douglas G B, Pu L, et al. Zero-valent iron-facilitated reduction of nitrate: Chemical kinetics and reaction pathways [J]. Science of the Total Environment, 2017,598:1140-1150.
[18] Sun Y K, Li J X, Huang T L, et al.The influences of iron characteristics, operating conditions and solution chemistry on contaminants removal by zero-valent iron: A review [J]. Water Research, 2016,100:277-295.
[19] Han L C, Yang L, Wang H B, et al. Sustaining reactivity of Fe0for nitrate reduction via electron transfer between dissolved Fe2+and surface iron oxides [J]. Journal of Hazaradous Materials, 2016,308: 208-215.
[20] Liu H B, Chen Z H, Guan Y N, et al. Role and application of iron in water treatment for nitrogen removal: A review [J]. Chemosphere, 2018,204:51-62.
[21] 李海玲,李 东,张 杰,等.调控温度和沉降时间实现ANAMMOX颗粒快速启动及其稳定运行[J]. 环境科学, 2019,2:1-11.Li H L, Li D, Zhang J, et al. Adjusting temperature and settling time to achieve ANAMMOX particles rapid start-up and stable operation [J]. Environmental Science, 2019,2:1-11.
[22] 周 同,于德爽,李 津,等.温度对海洋厌氧氨氧化菌脱氮效能的影响[J]. 环境科学, 2017,38(5):2044-2051. Zhou T, Yu D S, Li J, et al. Effect of temperature on nitrogen removal performance of marine anaerobic ammonium axidizing bacteria [J]. Environmental Science, 2017,38(5):2044-2051.
[23] 陈方敏,金 润,袁 砚,等.温度和pH值对铁盐型氨氧化过程氮素转化的影响[J]. 环境科学, 2018,39(9):4289-4293.Chen F M, Jin R, Yuan Y, et al. Effect of temperature and pH on nitrogen conversion in Feammox process [J]. Environmental Science, 2018,39(9):4289-4293.
[24] Zhang Y P, Douglas G B, Pu L, et al. Zero-valent iron-facilitated reduction of nitrate: Chemical kinetics and reaction pathways [J]. Science of the Total Environment, 2017,598:1140-1150.
[25] Sun Y K, Li J X, Huang T L, et al. The influences of iron characteristics, operating conditions and solution chemistry on contaminants removal by zero-valent iron: A review [J]. Water Research, 2016,100:277-295.
Effects of multiple factors on the process of ANAMMOX bacteria strengthening nitrate reduction by zero-valent iron.
SONG Ge1, ZHANG Wen-jing1,2,3, BI Zhen1,2,3*, HUANG Yong1,2,3,DONG Shi-yu1,3
(1.School of Environment Science and Engineering, Suzhou University of Science and Technology, Suzhou 215009, China;2.National and Local Joint Engineering Laboratory of Municipal Sewage Resource Utilization Technology, Suzhou 215009, China;3.Institute of Environmental Biotechnology, Suzhou University of Science and Technology, Suzhou 215009, China)., 2019,39(11):4666~4672
Effects of iron form, pH, temperature and Fe/N on the process of ANAMMOX bacteria strengthening nitrate reduction by zero-valent iron (Fe0) were studied by single factor control experiment combined with Central Composite Design (CCD) methodology. The results demonstrated that the test with nano- Fe0addition showed the highest nitrate removal efficiency compared with the iron powder and iron filings addition. According to the CCD analysis, the temperature and Fe/N had significant effects on the nitrate removal efficiency, while the effect of pH was weak. The optimum reaction conditions predicted based on CCD analysis were initial pH of 4.00, temperature of 35.00℃, and Fe/N of 38.23. The predictive nitrate removal efficiency was 94.70%, which was closed to the actual experimental value of 88.99%.
ANAMMOX;nitrate;zero-valent iron (Fe0);Central Composite design (CCD) methodology
X703.1
A
1000-6923(2019)11-4666-07
宋 歌(1998-),女,新疆克拉玛依人,苏州科技大学环境工程专业本科生,主要研究方向水污染控制.
2019-04-08
国家自然科学基金资助项目(21607110);城市生活污水资源化利用技术国家地方联合工程实验室(苏州科技大学)开放课题(2018KF02);苏州科技大学大学生科研立项基金资助项目(无项目编号)
* 责任作者, 讲师, bzhen.xi@163.com

