溶剂热法制备MOF-5和Zn-BTC及其催化合成查尔酮*
徐 舸,刘英琦,常人丽,谭继鹏
(沈阳工业大学 理学院,沈阳 110870)
查尔酮及其衍生物具有较高的生物活性和药用价值[1-2],且为重要的有机合成中间体[3].传统方法合成查尔酮时,采用强碱为催化剂,存在催化剂具有腐蚀性、产率低以及选择性差等问题.一般采用改性酸、碱催化剂[4-5]、超声或微波合成方法来解决上述问题.金属有机骨架化合物(MOFs)因具有可调的孔道结构,且活性位点多、比表面积大等优点[6-10],已广泛应用于多个领域,例如催化领域、药物传输领域、气体分离与存储领域[11-13]等.在催化领域MOFs可以非均相催化多种有机合成反应,如偶联反应[14]、还原反应、苯羟基化反应[15]、氧化脱氢反应[16]、Knoevenagel缩合反应等.
常用MOFs催化剂制备方法包括溶剂(水)热法、室温搅拌法等.金属有机化合物、氧化镁、碱性活性炭、碱性沸石和树脂等其他非均相催化剂[17]在催化前通常需要进行前处理高温煅烧,且反应温度较高,反应时间较长,制备过程还需添加其他助剂.马鑫[18]研究了利用IRMOF-3在110 ℃下催化合成查尔酮的方法,IRMOF-3催化剂制备较为复杂,得到初产物后需要利用二氯甲烷在常温下进行洗涤-过滤,需要每天更换二氯甲烷一次,三天后才可制得产物IRMOF-3.
本文采用溶剂热法制备MOF-5和Zn-BTC催化剂,相比IRMOF-3其制备周期明显缩短,样品后处理、清洗纯化操作仅需12 h.通过在不同制备参数下进行对比实验,确定金属盐和有机配体的比例是催化剂制备的关键影响因素,本文成功制备了MOF-5和Zn-BTC催化剂.MOF-5和Zn-BTC均为酸碱双活性催化剂,本文研究了MOF-5和Zn-BTC对查尔酮合成的催化活性,结果表明具有酸碱双活性中心的催化剂比具有单一活性中心的强碱催化剂催化效率更高.
1 实 验
1.1 催化剂的制备
将六水硝酸锌、对苯二甲酸或均苯三甲酸按一定摩尔比加入20 mL DMF溶剂中,通过磁力搅拌使其充分溶解,之后将混合溶液放入含有聚四氟乙烯衬里的不锈钢反应釜中.分别在140 ℃加热24 h,在150 ℃加热48 h,然后自然冷却,利用DMF溶液冲洗、抽滤三次并真空干燥12 h,分别制得产物MOF-5与Zn-BTC.
1.2 查尔酮的合成
在三口烧瓶中加入1 mL浓度为0.2 mol/L的NaOH水溶液(或7.5 mmol的MOFs产物)作为催化剂,再加入25 mmol苯乙酮和100 mL纯度为99%的乙醇水溶液,加热搅拌使得苯乙酮和催化剂均匀分散于乙醇水溶液中,利用恒压漏斗在15 min内滴加25 mmol苯甲醛.滴加完毕后,加热搅拌6 h.抽滤除去不溶物得到粗产物母液,并将其放置于冰箱中冷却12 h,待产物结晶析出后抽滤得到粗产物,然后利用无水乙醇进行溶解-重结晶处理,反复处理三次后得到产物查尔酮.
1.3 催化剂的表征与分析
采用MiniFlex 600型台式X射线衍射仪、Hitachi S-3400N场发射扫描电子显微镜和TA Q50型热重分析仪对催化剂的晶体结构、表面形貌和热稳定性进行测试;利用JW-BK122W型比表面与孔径分析仪测出催化剂比表面积与孔径大小;利用Quantachrome ChemBET Pulsar TPR/TPD程序升温化学吸附分析仪表征催化剂的酸碱活性;采用Waters型高效液相色谱进行查尔酮定量分析.
2 结果与分析
2.1 不同物料比对催化剂制备的影响
表1、2为Zn盐和有机配体的摩尔比对MOF-5、Zn-BTC的产率和比表面积的影响.由表1、2可见,催化剂的产率和比表面积受其影响较大.较高的物料比,会导致金属中心离子不够,因而催化剂产率较低;较低的物料比导致有机配体剩余,孔道堵塞,从而降低催化剂比表面积.因此,制备两种催化剂时,Zn盐与配体的较佳摩尔比为1∶1~3∶1.

表1 Zn盐与有机配体的摩尔比对MOF-5合成的影响Tab.1 Effect of molar ratio of Zn salt to organic ligand on synthesis of MOF-5
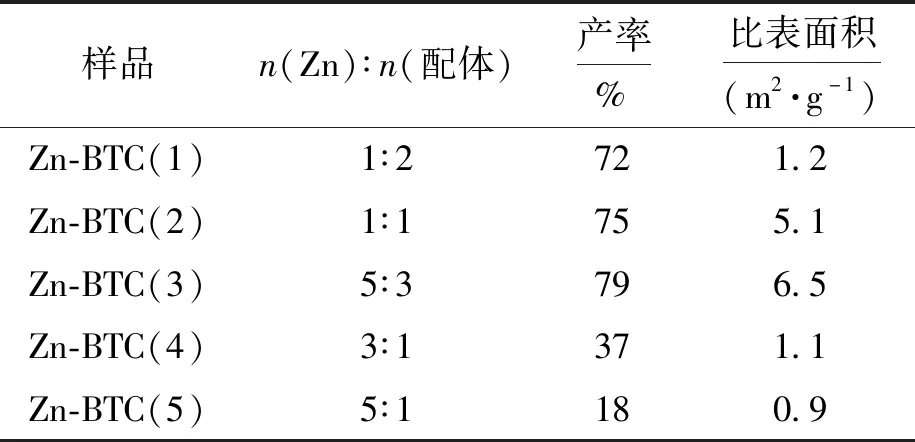
表2 Zn盐与有机配体的摩尔比对Zn-BTC合成的影响Tab.2 Effect of molar ratio of Zn salt to organic ligand on synthesis of Zn-BTC
2.2 催化剂的XRD分析
图1为MOF-5的模拟图谱和MOF-5(3)的XRD图谱.由图1可见,MOF-5(3)样品具有4个主要特征峰[19],对应的衍射角分别为6.8°、9.7°、13.7°和15.4°,这与MOF-5的标准卡片完全吻合,未发生分裂且峰强度较高,表明MOF-5(3)样品框架完整,结晶度较好.

图1 MOF-5的模拟图谱和MOF-5(3)的XRD图谱Fig.1 Simulated spectrum of MOF-5 and XRD spectrum of MOF-5(3)
图2为Zn-BTC的模拟图谱和Zn-BTC(3)的XRD图谱.由图2可见,Zn-BTC(3)样品的吸收峰与由PDXL2软件模拟得到的Zn-BTC的吸收峰基本吻合,且特征峰的峰高、峰宽对应较好,表明合成的产物确为Zn-BTC.
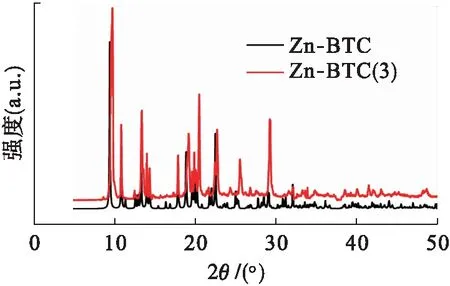
图2 Zn-BTC的模拟图谱和Zn-BTC(3)的XRD图谱Fig.2 Simulated spectrum of Zn-BTC and XRD spectrum of Zn-BTC(3)
2.3 催化剂的SEM分析
图3、4分别为MOF-5(3)与Zn-BTC(3)样品的SEM图像.由图3、4可见,MOF-5(3)样品的外观近似为立方体,而Zn-BTC(3)的外观为长方体;MOF-5(3)和Zn-BTC(3)的样品表面具有鳞片状凸起;MOF-5(3)样品的尺寸约为30 μm×30 μm×30 μm,而Zn-BTC(3)样品的尺寸约为150 μm×50 μm×40 μm.
2.4 催化剂的TGA分析
图5为MOF-5(3)和Zn-BTC(3)的热重分析图谱.Zn-BTC(3)的起始质量为11 mg,MOF-5(3)的起始质量为6 mg.由图5可见,MOF-5(3)在200 ℃附近质量开始减少,MOF-5(3)首先脱去的物质为DMF溶剂分子,上述温度可作为产物的氮吸附实验预处理温度,便于首先除去DMF溶剂分子,打开产物孔道;当温度高于400 ℃之后,MOF-5(3)的质量迅速下降直到分解完全.Zn-BTC(3)在温度低于200 ℃时其质量就开始持续减少,Zn-BTC(3)开始脱去水分子、DMF溶剂分子等物质;同样当温度高于400 ℃后,Zn-BTC(3)的质量迅速下降直到分解完全.比较两种催化剂可知,MOF-5(3)在温度低于150 ℃时的热稳定性更好.

图3 MOF-5(3)的SEM图像Fig.3 SEM images of MOF-5(3)

图4 Zn-BTC(3)的SEM图像Fig.4 SEM images of Zn-BTC(3)

图5 MOF-5(3)和Zn-BTC(3)的TGA图谱Fig.5 TGA spectra of MOF-5(3)and Zn-BTC(3)
2.5 催化剂的程序升温化学吸附-脱附实验
图6为MOF-5(3)和Zn-BTC(3)的NH3-TPD图谱.由图6可见,MOF-5(3)在200 ℃附近出现峰值,主峰范围较广,在80~350 ℃内均具有较强的吸收效果.Zn-BTC(3)在375 ℃附近出现的强吸收峰是由部分残留的溶剂大分子和未成键的—COOH脱附形成的.对比两种催化剂的峰面积大小可知,MOF-5(3)的吸收峰面积更大,表明其酸性更强.

图6 MOF-5(3)与Zn-BTC(3)的NH3-TPD图谱Fig.6 NH3-TPD spectra of MOF-5(3)and Zn-BTC(3)
图7为MOF-5(3)和Zn-BTC(3)的CO2-TPD图谱.由图7可见,Zn-BTC(3)为双重吸收峰并在410、450 ℃附近出现峰值,而MOF-5(3)则为多重吸收峰并在510 ℃附近出现峰值.两个产物的吸收峰强度均很高,表明MOF-5(3)和Zn-BTC(3)具有较强的碱度.Zn-BTC(3)的CO2-TPD和NH3-TPD图谱均存在吸收现象,表明其为酸碱双活性中心催化剂,根据峰面积大小可知该催化剂碱性更强.MOF-5(3)的CO2-TPD和NH3-TPD图谱均存在吸收现象,因而MOF-5(3)也是一种酸碱双活性中心催化剂,对比峰面积大小发现该催化剂酸性更强.
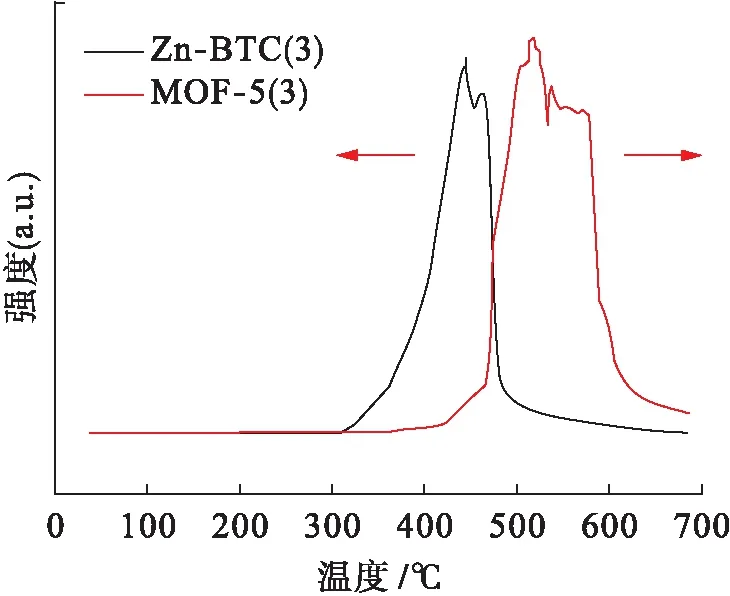
图7 MOF-5(3)与Zn-BTC(3)的CO2-TPD图谱Fig.7 CO2-TPD spectra of MOF-5(3)and Zn-BTC(3)
2.6 催化剂的N2等温吸附-脱附实验
表3为MOF-5(3)和Zn-BTC(3)的比表面积与孔径分析结果.由表3可见,MOF-5(3)的比表面积为771.5 m2/g,平均吸附孔径为1.86 nm,所制备的MOF-5(3)为具有较高比表面积且微孔与介孔共存的多孔材料,具有优良的催化应用价值.Zn-BTC(3)的比表面积为6.5 m2/g,该数值相比文献[20]低很多,结合XRD图谱分析可知该产物含有杂质分子,因而阻塞了框架结构孔道.此外,由TGA分析可知,Zn-BTC(3)的热稳定性不好,在100 ℃开始就有溶剂分子不断发生分解,此外,由于热处理温度较高,随着溶剂的不断分解,Zn-BTC(3)发生孔道崩塌,因而直接降低了其比表面积.
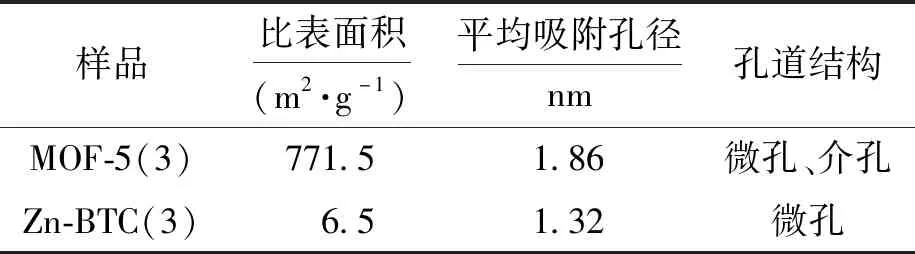
表3 MOF-5(3)与Zn-BTC(3)的比表面积与孔径Tab.3 Specific surface area and pore size of MOF-5(3)and Zn-BTC(3)
2.7 查尔酮的分析与表征
表4为采用三种不同催化剂所合成产物查尔酮的液相色谱分析结果.由表4可见,三种催化剂催化合成的查尔酮出峰时间基本相同,表明产物结构相同.液相色谱的峰面积代表产物纯度,则产物纯度排列顺序为:Zn-BTC(3)>NaOH>MOF-5(3).三种产物的纯度都很高,但Zn-BTC(3)作催化剂时所得产物的纯度最高.查尔酮的产率由高到低为:MOF-5(3)>Zn-BTC(3)>NaOH,两种MOFs作催化剂时所得查尔酮产率均高于NaOH为催化剂的情况,且MOF-5(3)和Zn-BTC(3)的催化活性约为NaOH催化剂的两倍.
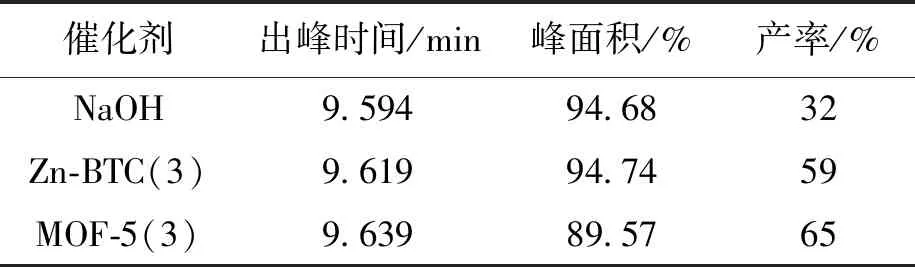
表4 不同催化剂所合成查尔酮的液相色谱分析结果Tab.4 Analysis results of liquid chromatography of chalcone synthesized with different catalysts
2.8 催化查尔酮的机理分析
当NaOH为催化剂时,可以首先脱去苯乙酮的α-碳原子上的氢原子,促使其形成碳负离子杂化物,该结构可在共振平衡后生成烯醇盐.随后烯醇盐与苯甲醛的羰基碳缩合生成β-羟基酮,脱水后即可生成查尔酮.
具有酸碱双活性中心的MOFs催化羟醛缩合反应机理为:首先在碱性中心作用下,苯乙酮的α-碳原子失去氢原子形成碳负离子杂化物及其共振结构烯醇盐;之后在酸性活性中心作用下,苯甲醛的羰基氧原子发生质子化,增强了羰基的诱导作用并促进其与苯乙酮的烯醇盐缩合生成产物查尔酮.因此,对于具有双活性中心的MOFs催化剂而言,碱性中心与酸性中心协同作用可以完成查尔酮的合成,显著提高了反应效率的同时减少了副产物.
3 结 论
采用溶剂热法制备了MOF-5、Zn-BTC催化剂,对比分析了NaOH、MOF-5和Zn-BTC对查尔酮合成的催化性能,主要结论如下:
1)锌盐与有机配体的摩尔比是制备MOFs催化剂的关键因素,制备MOF-5的较佳摩尔比为3∶1,制备Zn-BTC的较佳摩尔比为5∶3.
2)MOF-5和Zn-BTC均具有酸碱双活性中心,且MOF-5的比表面积更高,当温度低于150 ℃时,其热稳定性更好.
3)与NaOH催化剂相比,MOF-5、Zn-BTC催化剂提高了所合成查尔酮的纯度和产率,且由碱性活性中心更强的Zn-BTC催化剂所得到的查尔酮纯度更高,表明查尔酮的合成中形成碳负离子是抑制副反应的关键步骤.

