膦配体在Suzuki偶联反应中的应用
孙静 杨燕
1.西安建筑科技大学理学院 710055
2.西安瑞联近代电子材料有限责任公司 710077
膦配体在Suzuki偶联反应中的应用
孙静1杨燕2
1.西安建筑科技大学理学院 710055
2.西安瑞联近代电子材料有限责任公司 710077
Suzuki反应具有反应条件温和、环境友好等诸多优势,使用膦配体的钯催化剂使Suzuki反应结果优异。文章介绍了不同类型的膦配体在Suzuki偶联反应中的应用。
Suzuki;催化;催化剂;膦配体;应用
Suzuki偶联反应是用以形成碳-碳键的重要工具。和其它过渡金属催化下的芳烃偶联反应相比,Suzuki反应具有明显的优势:温和的反应条件;对多种官能团的可容忍性;化学选择性及立体选择性很高;在水中即可进行该反应,环境友好;有机硼试剂较有机锌试剂、格氏试剂、锡试剂相对温和,对空气稳定,且已商业化,此外含硼副产物无毒(对环境危害较小),易于除去[1]。因此,Suzuki偶联反应被广泛用于化学和制药业,而且其应用逐年增加。
钯催化的Suzuki反应取得了令人瞩目的成果,如经典钯催化剂Pd(PPh3)4,通常使用膦配体来稳定活性的钯中间体,尤其是当空间体积庞大的单膦、二膦、二茂铁衍生物膦用作配体时钯催化剂的Suzuki反应结果更加优异。本文主要针对近年来膦配体在钯催化Suzuki偶联反应中的应用进展做一综述。
1 、芳基膦配体
早期多数催化剂应用三苯基膦作为配体,直到90年代中期,虽然三(甲基苯)膦配体作为配体能得到较好的结果,但Suzuki偶联反应较多的应用Pd(PPh3)4催化剂。
90年代后期,Buchwald报道了一类很重要的以联苯为骨架的单膦配体结构,此类配体具有耐氧化性,在空气中可稳定存在,有广泛的商业化应用。如下图1所示[2,3,4,5]。这类配体结合一个钯,形成有效的催化剂催化Suzuki偶联反应。
芳基膦配体已被证明可广泛的应用于钯催化的偶联反应。以此配体为催化剂的Suzuki偶联反应的底物为:溴代芳烃,三氟甲磺酸芳香酯,钝化氯代芳烃,芳烃甲苯磺酸盐,各种各样的杂环体系和具有位阻的化合物。
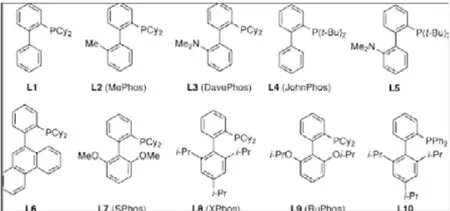
图1 二芳基膦配体
2010年Gholinejad[6]报道了2-氨基苯二苯基膦(L-11)作为Suzuki-Miyaura反应多相钯催化剂配体,水为溶剂,没有加入任何有机溶剂的反应。通过2-氨基苯二苯基膦作为配体,Pd(OAc)2为主催化剂,结构不同的卤代芳烃(I, Br, Cl)与苯硼酸在水中反应可取得较高收率。优点:其配体简单易得,可回收再利用七次,无明显丧失其催化活性。
2011年Bourissou[7]报道了邻-(二均三甲苯硼基)二苯基膦衍生物(L-13、L-14)具有较强的催化性能,Pd/L-13 > Pd/ L-14≈Pd/L-10。但是Pd/L-13体系较难催化具有立体位阻效应的底物,它在催化4-溴苯甲醚和2-甲基苯硼酸偶联反应时收率为75%,但是催化具有立体位阻效应的2,4,6-三(异丙基)溴苯和2-甲基苯硼酸时收率不足20%。
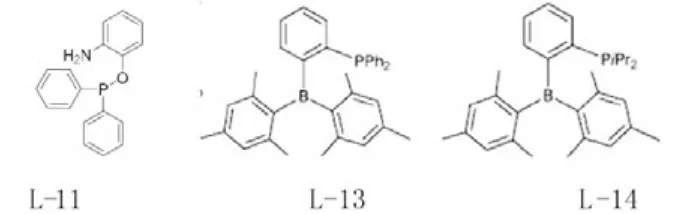
2 、庞大的膦配体
2.1 单齿膦配体
2000年,Beller等[8]报道了大位阻的单齿膦配体二金刚烷基-正丁基膦配体L-15催化氯代芳烃的Suzuki偶联反应。后来,Beller应用二金刚烷基膦盐做配体参与偶联反应。
2.2 二齿膦配体
二苯基膦丙酸钠是一个含有P、O双齿配位原子的阴离子型水溶性膦配体,它可以和镍、钯等过渡金属元素形成配合物[9]。
1999年,Guram等报道了以苯基为骨架的P,O双齿配体1和2,配体2的催化活性较小。Pd(dba)3/L-16对带有吸电子基或给电子基,以及空间位阻较大的氯苯衍生物均有较好的催化活性(收率:83%~97%)。
2001年,Andersoon也报道了二齿膦配体L-18可以作为稳定的钯催化剂应用于Suzuki偶联反应[10],同时在溴苯和碘苯的Suzuki反应中无Pd黑生成。二齿配体L-19也能应用于溴苯和苯硼酸的Suzuki偶联反应。
2005年Liang报道了二齿配体NP-Pd(Ⅱ)配合物:{[NP]PdCl}2、[NP]PdCl(PCy3),它们能够高效的催化Suzuki偶联反应(其中[NP]-为N-(2-(二苯基膦)苯)-2,6-二异丙基苯胺)。NP-Pd(II)配合物在高温下对空气和水稳定,能广泛的催化卤代芳烃,包括带有立体位阻效应、富电子的非活性底物及杂环底物。其中,[NP]PdCl(PCy3)的活性高于{[NP] PdCl}2,而且在反应过程中无Pd黑形成。应用[NP]PdCl(PCy3)催化活性氯代物的收率大于95%。
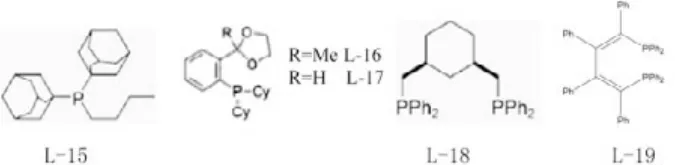
2.3 四齿膦配体
Santelli报道了四齿膦配体L-20,对于催化空间位阻大的溴代杂环芳烃、溴代芳烃和带有吸电子基团的氯代芳烃的Suzuki偶联反应效果很好。这类配体不能提供高的σ-碱度(能活化氯代芳烃),说明σ-碱度不是催化剂活性的先决条件。由于配体L-20的四个二苯基膦基处于戊环的同一面,因此增大了与钯的配位能力,同时增强了配合的稳定性。
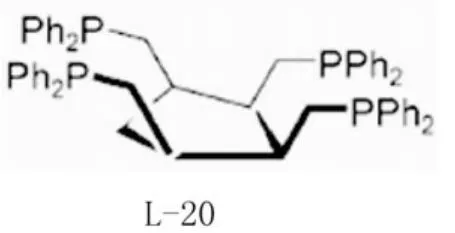
2.4 二茂铁衍生物膦配体
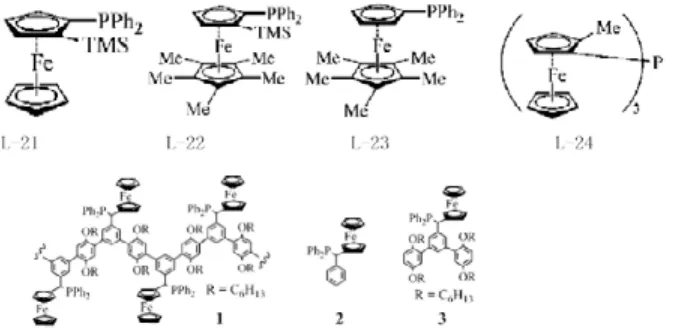
近年来,二茂铁类配体的合成和应用受到极大的关注,其配体与钯催化剂催化卤代芳烃,主要配体如下所示。
对配体L-21进行衍生,在其底部引入5个甲基,增大其空间位阻,经优化后的配体L-22催化活性显著提高,催化活性低的或空间位阻大的氯代芳烃的Suzuki偶联反应时产量很高(82%~95%),通过去掉三甲基硅基形成配体L-23,催化活性降低,说明TMS对配体的催化活性贡献很大。
新型配体C3-对称性二茂铁膦配体L-24和Pd2(dba)3作为Suzuki催化剂催化带有吸电子基的氯代芳烃,表现出较高的催化活性。但反应5小时后,产生Pd黑,即催化剂分解。
大分子的二茂铁膦配体1在空气中稳定,可溶于常用溶剂如二氯甲烷、THF、甲苯。其在室温下催化带有吸电子基的氯代芳烃的Suzuki偶联反应取得较好的效果。
二茂铁基比苯基大,而且具有较多的电子,但同三烷基膦相比为缺电子,即限制其应用。
3 、结语
配体以膦配体最为常用,包括各种简单的膦配体如R3P(R=Ph,i-Pr,t-Bu)、dppm、dppe 、dppp、dppf、1,2-(Ph2P)2C6H4、Buchwald配体等。
虽然Suzuki偶联反应取得了长足的进步,大量新型的配体不断涌现,但目前应用较广、较成熟的仍然是膦配体,例如富电子的三烷基膦配体和钯催化剂可催化钝化的氯代芳烃的Suzuki反应。
[1] FranciscoAIr, ina P B,MiguelY.Non-conventionalmethodolog for transitionmectaatl alyzedc arbon-carbocon uplinAg: critic la overviewP. art 2: The Suzuki reaction[. J].Tetrahedr on, 2008, 64: 3047-3101.
[2] A. Aranyos, D. W. Old, A. KiyomorJi,. P. Wolfe, J. P. Sadighi, S. L. BuchwaldJ., Am. Chem. Soc. 1999, 121, 4369.
[3] D. W. Old, J. P. Wolfe, S. L. BuchwaldJ., Am. Chem. Soc. 1998, 120, 9722.
[4] J. P. Wolfe, R. A. Singer, B.H. Yang, S. L. Buchwald, J. Am. Chem. Soc. 1999, 121, 9550.
[5] J. P. Wolfe, S. L. BuchwaldA, ngew. Chem.I nt. Ed. 1999, 38, 2413.
[6]Journaol f OrganometCahlliec mistr2y 010, 695(18):2093-2097.
[7]Chemical Communications (Cambridge, United Kingdom) (2 47(28),8163-8165.
[8] A. Zapf, A. Ehrentraut, M. Beller, Angew. Chem. Int. Ed. 2000, 39, 4153.
[9]Gloker P W,Keim W,MasoRn F,et.Ger Often 2 053 758[P],1971.
[10]S.Sjovall, M. H. JohanssonC,. AnderssoEn, ur. J. Inorg. Chem. 2001, 2907.
[11]Chem. Commun.2001,2408.
10.3969/j.issn.1001-8972.2012.11.023

