964例丹红注射液不良反应报告关联规则分析
李 艳,刘 欢,边 原,李 刚*
0 引言
丹红注射液是将中药丹参和红花按科学配方提取的复方制剂,与注射用水配伍而成[1],具有活血化瘀、通脉舒络等药理作用。现代药理学证实,丹红注射液中的活性成分具有抗血栓[2]、保肝[3-4]等作用。随着丹红注射液在临床上的广泛应用,对于其不良反应的监控尤为重要。本文通过对四川省药品不良反应监测中心药品不良反应自发呈报系统(Spontaneous reporting system,SRS)中2010年1月1日至2017年12月30日接收到的996份丹红注射液不良反应报告进行统计分析,总结丹红注射液在四川人群中不良反应的发生特点。
1 材料与方法
1.1 数据来源 选取四川省药品不良反应监测中心药品不良反应SRS 2010年1月至2017年12月的丹红注射液ADR报告,共996份。
1.2 数据处理
1.2.1 信息标准化 对丹红注射液ADR报告类型、患者一般情况(年龄、性别、体重、民族、药品食物过敏史、原患疾病、既往药品不良反应史)、用药信息(药品通用名、用药剂量、用药频次、给药途径、用药时间、用药原因、合并用药)、ADR情况(ADR名称、ADR发生时间、严重程度、具体表现、ADR处理及结局转归等条目)进行标准化,以国家食品药品监督管理局发布的《药品不良反应/事件报告表》作为标准统一数据库结构。
1.2.2 ADR名称标准化 依照WHO公布的不良反应术语集(WHOART)[5-12]标准进行名称分类统计。对于ADR名称的规范化,具体到“不良反应过程描述”中摘取信息。
1.3 关联规则分析[13]探索发现数据源对象的内在结构,同时归纳总结数据的隐含规律,但不直接用于分类预测。其中,置信度、支持度、提升度(效益)是评价关联规则的重要指标。
规则置信度(Confidence)是指包含项目X的事务中同时包含项目Y的概率,以测量关联规则的准确度,反映X出现的条件下Y出现的可能性。
规则支持度(Support):表示了项目X和项目Y同时出现的概率,反映的是关联规则的普遍性。
另外,支持度还有前项支持度(也称为条件支持度)和后项支持度。
规则提升度(Lift):也称作效益,是指置信度与后项支持度的比,反映了项目X的出现对项目Y出现的影响程度。一般大于1才有意义。规则提升度越大越好。
部署能力=前项支持度-规则支持度,反映了样本中满足前项X但不满足后项Y的情况。
理想的关联规则应该是具有较高的置信度和较高的支持度,如果支持度较高但置信度较低,则规则可信程度差,如果置信度较高但支持度较低,则规则应用机会少,提示该规则没有太大的应用价值,故关联规则分析前需给定一个最小置信度和最小支持度的标准,大于最小置信度和支持度阈值的规则为有效规则。本研究选取置信度50%及以上,支持度2%及以上进行分析。
2 结果
在996份丹红注射液不良反应报告中,剔除32份评估为“可能无关”、“待评价”以及“无法评价”的病例,共获得964份有效报告。
2.1 一般情况分析
2.1.1 ADR逐年上报具体数量 从2011年起,丹红注射液每年ADR报告数量呈上升趋势。其中,2010年22份,2011年7份,2012年40份,2013年79份,2014年141份,2015年190份,2016年240份,2017年245份。
2.1.2 年龄、性别与民族分布 男461例,女503例。非汉族人群44例,汉族人群920例。年龄最小为8岁,最大为97岁。未成年者13例,60岁及以上老年患者超过一半。见表1。

表1 发生ADR患者年龄分布[14]
2.1.3 ADR累及器官-系统 发生ADR的患者中,超过50%的病例伴有皮肤及其附件损伤,其次为心血管系统一般损伤。见表2。
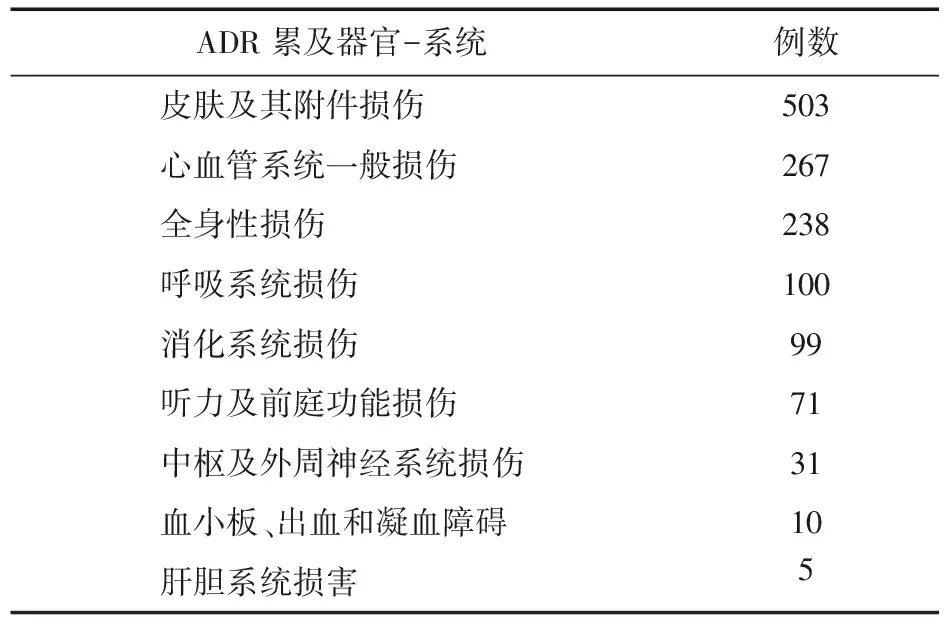
表2 ADR累及器官-系统及其主要临床表现
2.1.4 发生ADR后的处理措施 见表3。一旦发生ADR,均应立即停药,其次为静推地塞米松抗过敏处理。经处理后,ADR转归良好,症状均缓解。
2.2 关联分析结果
2.2.1 ADR具体表现之间的关联分析 严重ADR表现之间的关联分析结果:964份有效报告中共有53例严重ADR,对严重ADR报告中的具体表现进行关联分析,按照置信度百分比大小顺序选择前5项,以“皮肤及其附件损害+心血管系统一般损害+初次用药时发生ADR”的组合支持度最高,提示在发生严重ADR的患者表现中,此类表现组合最常见,有较好的准确度和普遍性,同时在发生严重ADR的患者中,同时有“皮肤及其附件损害”和“心血管系统一般损害”的患者全部为初次用药时发生。见表4。

表3 发生ADR后的处理措施
一般ADR报告病例中的具体表现:964份有效报告中,共有911份一般ADR报告,按照置信度百分比大小排列并剔除掉增益无效的组合后前5项组合见表5。其中,最常见的“心血管系统一般损害+皮肤及其附件损害”组合的患者有77.273%的可能“初次用药时发生ADR”。
2.2.2 患者基本情况与用药后ADR发生时间之间的关联分析 517例ADR发生在该次住院首次输注丹红注射液时。此类报告中,关联分析发现,“年龄(20~39)+骨关节疾病+原患疾病数量=1+合并用药个数=0”组合的患者中,85%为“初次用药时即发生ADR”,具体见表6,而剩余447例ADR报告发生在输注丹红注射液超过1次之后,“皮肤疾病+汉族”的组合中80%在用药超过1次时发生ADR。见表7。
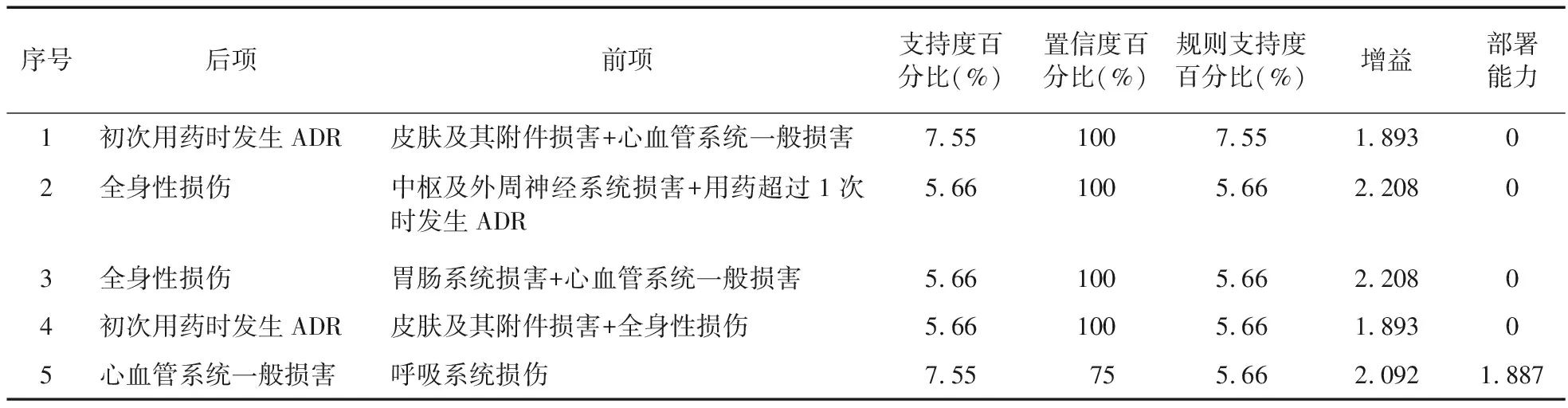
表4 严重ADR表现之间的关联分析结果

表5 一般ADR表现之间的关联分析结果

表6 患者基本情况与初次用药时发生ADR之间的关联分析
2.2.3 ADR表现与患者基本情况之间的关联分析 在最小支持度和置信度的条件下,有效的关联规则仅对涉及“皮肤及其附件损害”、“全身性损伤”以及“心血管系统一般损害”的3种ADR表现进行了探索,根据置信度大小顺序各选取前5项规则。
其中“非汉族+性别男”的组合超过90%发生了皮肤及其附件损害,“年龄(20~39)+骨关节疾病”的组合,有85.714%的可能发生“皮肤及其附件损害”。将“全身性损伤”设为后项时,条件“脑部及血管疾病+原患疾病数量=2+年龄(60~79)+合并用药个数=0”的组合导致“全身性损伤”发生的可能性可达58.333%。在“心血管系统一般损害”中,“呼吸系统疾病+原患疾病数量=2.0+性别男+汉族”有54.545%的可能发生该类不良反应。见表8。
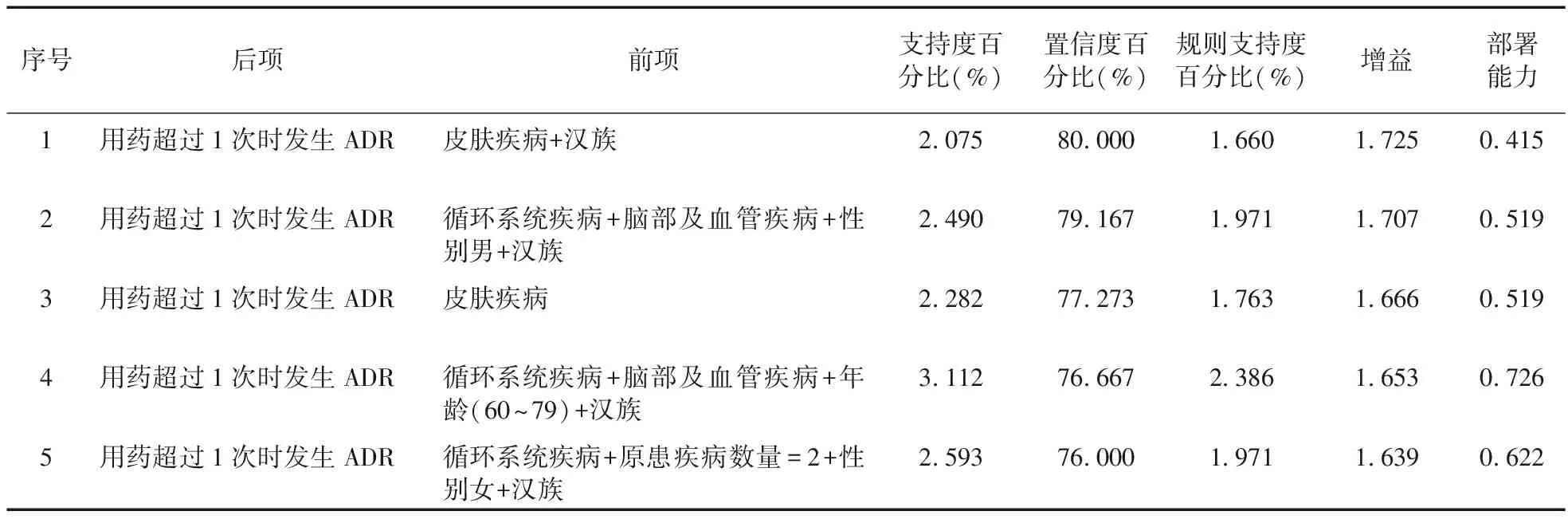
表7 患者基本情况与用药超过1次时发生ADR之间的关联分析
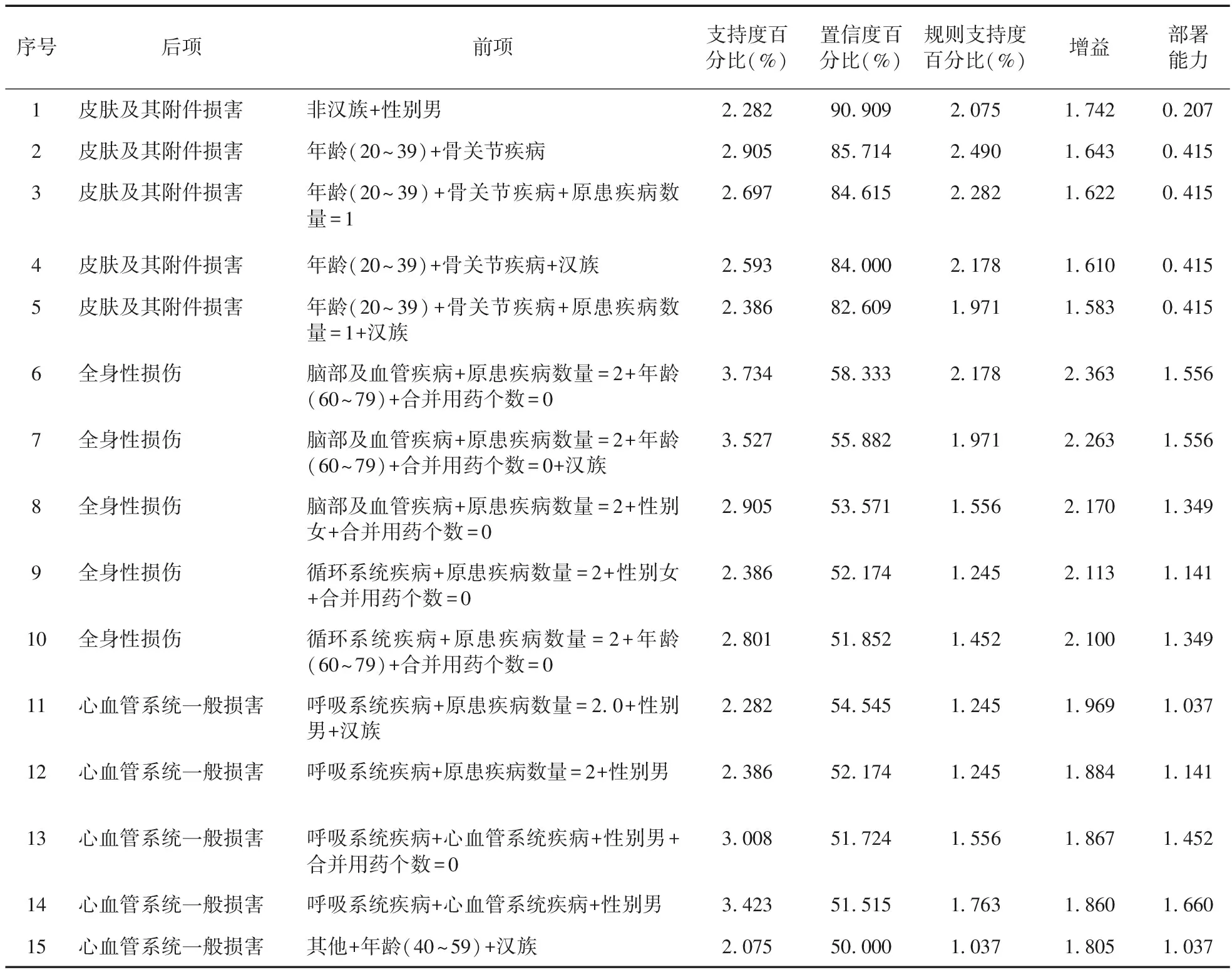
表8 ADR表现与患者基本情况之间的关联分析
3 讨论
丹红注射液作为临床常用的复方中成药注射液,其人体内的药代动力学和药效学尚不明确,既往对于其不良反应的研究方法多集中于频数排列和构成比。本研究使用SPSS Modeler软件,对使用丹红注射液发生ADR的报告进行关联分析,与既往文献相比[15-17],一些结论是相似的,如:丹红注射液最常见ADR为皮肤系统及附件损害,男女性别无差异,ADR转归良好,在停药或者给予对症处理后均能好转。除此之外,发现了很多新的有效且有意义的规则,如:年龄在20~39岁并患有骨关节疾病的患者极有可能在初次输注丹红注射液时发生ADR,并且多为皮肤及其附件的损害;患有皮肤病的男性患者有可能在输注超过1次后才发生ADR,非汉族的男性患者输注丹红注射液后若发生ADR,伴随皮肤及其附件损害的可能性较大。这些有效规则对于临床治疗中丹红注射液给药前的患者安全性评估提供了一定的证据支持。
在传统的商业决策关联分析中,要求有较高的置信度和较高的支持度,但是把关联分析应用到医学领域时会稍有不同,如:规则“年龄(20~39岁)+皮肤及其附件损害”支持度百分比为6.33%,置信度百分比高达77.05%,说明年龄(20~39)的ADR患者中77.05%发生了皮肤及其附件损害,尽管此项关联条件支持度不高,但结合临床实际,由于患者人口学特点中,年龄(20~39岁)的占比较少,导致条件支持度较低,所以该项规则可以较准确地体现该类人群输注丹红注射液后发生ADR的特点。这也体现了挖掘出的有效关联规则需要结合临床实际情况进一步分析,为临床工作提供准确的参考。
由于本次研究基于ADR报告,没有详细的合并用药信息,无法得出相关的临床规则。有报道,丹红注射液发挥作用的7种主要药效物质除丹参素外,原儿茶醛、p-香豆酸、丹酚酸D、迷迭香酸、紫草酸和丹酚酸B 的人血浆蛋白结合率均>60%,属中强型结合[18]。在临床上联合用药时可能会发生血浆蛋白竞争性结合,特别是联用治疗窗较窄的药物如地高辛等时,应注意药物毒性作用的发生。丹红注射液的ADR报告中,有患者既往明确丹红注射液输注过敏史,但该次住院时仍有使用,最终导致再次出现ADR,给患者带来了不必要的损伤,也造成医疗资源的浪费,提示临床安全用药意识仍需加强。

