黄连解毒丸质量标准的再评价
张文文,王 姚,曾 嵘,张文静,罗 虹,张 倩,刘 涛,∗
(1.成都大学四川抗菌素工业研究所,四川 成都 610052;2.成都大学药学与生物工程学院,四川 成都 610106;3.成都九芝堂金鼎药业有限公司,四川 成都 610051)
黄连解毒丸由大黄(酒炒)、黄连(酒浸)、黄芩(酒蒸)、黄柏(酒炒)、滑石、栀子(炒)、川木通7 味药材组成,为黄褐色水丸,是成都九芝堂金鼎药业有限公司的独家品种,具有泻火、解毒、通便等功效,用于三焦积热、口舌生疮、目赤头痛、便秘溲赤、心胸烦热、热痢泄泻、咽痛衄血、疮疖痔血,其质量标准收载于《国家中成药标准汇编(中成药地方标准上升国家标准部分 内科 脾胃分册)》,但仅采用薄层扫描法对黄连、黄柏含有量进行测定[1],方法重复性、准确度较低,受操作人员影响较大,难以进行有效控制。
准确度是指采用该方法测定的结果与真实值或参考值接近的程度,一般用回收率表示[2]。在对同时测定黄芩苷、盐酸小檗碱含有量的方法学进行考察时发现,加样回收率远低于限度要求,无法准确测定;对黄连解毒丸中主要成分的理化性质进行分析发现,黄连与包括黄芩、大黄在内的许多中药共煎煮时均有沉淀物产生[3],而且可溶于吡啶、稀酸、稀碱,微溶于冷甲醇、乙醇,不溶于水、氯仿、石油醚,在热甲醇中能不断溶解,冷却后又生成沉淀[4]。但目前含黄芩、黄连、黄柏的中成药几乎都建立了黄芩苷和(或)盐酸小檗碱含有量测定项,故方法学考察中应进行准确度研究,即加样回收率试验。
课题组前期发现,由于黄芩苷与盐酸小檗碱生成沉淀,故两者加样回收率均不符合要求。基于此,本实验以黄连解毒丸为代表,对黄芩苷、盐酸小檗碱含有量测定方法的准确度进行研究,考虑到该制剂由7 味药材组成,再以栀子苷为指标。同时,根据中药多组分、多靶点整体综合作用的特点[5-7],从全成分角度出发建立黄连解毒丸HPLC指纹图谱,它是一种综合的、可量化的鉴别模式,具有快速准确的特点[8],可有效检测和控制中药产品的真实性、质量一致性、稳定性[9-10],可为制定该制剂全面整体的质量控制方法提供实验依据。
1 材料
Waters 2695 型高效液相色谱仪,配置Waters 2996 型PAD 检测器(美国Waters 公司);FA2004型电子分析天平(上海良平仪器仪表有限公司);P230Ⅱ型高效液相色谱仪(大连依利特分析仪器有限公司);SQP 型电子分析天平[赛多利斯科学仪器(北京)有限公司];KQ-100E 型超声波清洗器(昆山市超声仪器有限公司);
栀子苷(批号16052902)、黄芩苷(批号150718)、盐酸小檗碱(批号16072302)、黄芩素(批号150307)、汉黄芩素(批号140217)、盐酸巴马汀(批号16060803)、盐酸药根碱(批号16070305)对照品均购于四川省维克奇生物科技有限公司。大黄(酒炒)(批号170108)、黄连(酒浸)(批号161124)、黄芩(酒蒸)(批号170302)、黄柏(酒炒)(批号161224)、栀子(炒)(批号161002)、川木通(批号161223)、滑石(批号170119)均经成都大学刘涛研究员鉴定为正品。黄连解毒丸(批号20170425、20170426、20180122、20180301、20180302、20180307、20180308、20180320、20180321、20180412,编号S1~S10)由成都九芝堂金鼎药业有限公司提供。甲醇、乙腈为色谱纯;其他试剂均为分析纯;水为纯净水。
2 方法与结果
2.1 黄芩苷、盐酸小檗碱含有量测定
2.1.1 色谱条件 Hypersil ODS-2 色谱柱(250 mm×4.6 mm,5 μm);流动相乙腈(A)-0.2% 磷酸(B),梯度洗脱(0~32 min,8% →24% A;32~46 min,24% A;46~55 min,24% →34% A;55~63 min,34% →54% A;63~80 min,54% →68%A);体积流量1 mL/min;柱温30 ℃;检测波长238 nm;进样量10 μL。
2.1.2 对照品溶液制备 (1)精密称取黄芩苷、盐酸小檗碱对照品适量,甲醇制成每1 mL 分别含两者347.2、569.6 μg 的溶液,即得。(2)精密称取黄芩苷、盐酸小檗碱对照品适量,甲醇制成每1 mL分别含两者1 209.6、579 μg 的溶液,即得。(3)精密称取黄芩苷、盐酸小檗碱对照品适量,二甲基亚砜制成每1 mL 分别含两者378、651 μg的溶液,即得。
2.1.3 供试品溶液制备 取丸剂适量,研细,精密称取约0.25 g,置于具塞锥形瓶中,精密加入甲醇25 mL,称定质量,超声(100 W、40 kHz)30 min,取出,冷却至室温,甲醇补足减失的质量,摇匀,滤过,取续滤液,过0.45 μm 微孔滤膜,即得。
2.1.4 阴性样品溶液制备 按处方比例分别除去黄芩及黄连、黄柏,作为阴性样品,按“2.1.3”项下方法制备,即得。
2.1.5 专属性试验 吸取“2.1.2”~“2.1.4”项下溶液,在“2.1.1”项色谱条件下进样测定,结果见图1。由图可知,阴性样品无干扰,方法专属性强。
2.1.6 线性关系考察 精密吸取“2.1.2”项下对照品溶液(1)1、2、3、4、5、6 mL,置于10 mL量瓶中,甲醇定容,摇匀,在“2.1.1”项色谱条件下进样测定。以进样量为横坐标(X),峰面积为纵坐标(Y)进行回归,得方程分别为黄芩苷Y=1.00×106X-9.84×104(R2=0.999 5)、盐酸小檗碱Y=8.34×105X-7.66×104(R2=0.999 5),分别在0.347 2~2.083 2、0.569 6~3.417 6 μg 范围内线性关系良好。
2.1.7 精密度试验 精密吸取“2.1.3”项下供试品溶液,在“2.1.1”项色谱条件下进样测定6次,测得黄芩苷、盐酸小檗碱峰面积RSD 分别为1.33%、0.73%,表明仪器精密度良好。
2.1.8 重复性试验 取样品(编号S2)适量,按“2.1.3”项下方法制备供试品溶液,平行6 份,在“2.1.1”项色谱条件下进样测定,测得黄芩苷、盐酸小檗碱含有量RSD 分别为2.18%、2.56%,表明该方法重复性良好。
2.1.9 稳定性试验 取样品(编号S2)适量,按“2.1.3”项下方法制备供试品溶液,于0、2、4、6、8、10、12、24 h 在“2.1.1”项色谱条件下进样测定,测得黄芩苷、盐酸小檗碱峰面积RSD 分别为1.49%、1.17%,表明溶液在24 h 内稳定性良好。
2.1.10 加样回收率试验 取样品(编号S2)适量,研细,精密称取约0.125 g,平行6 份,精密加入黄芩苷、盐酸小檗碱对照品适量,按“2.1.3”项下方法制备供试品溶液,在“2.1.1”项色谱条件下进样测定,计算回收率,结果见表1。
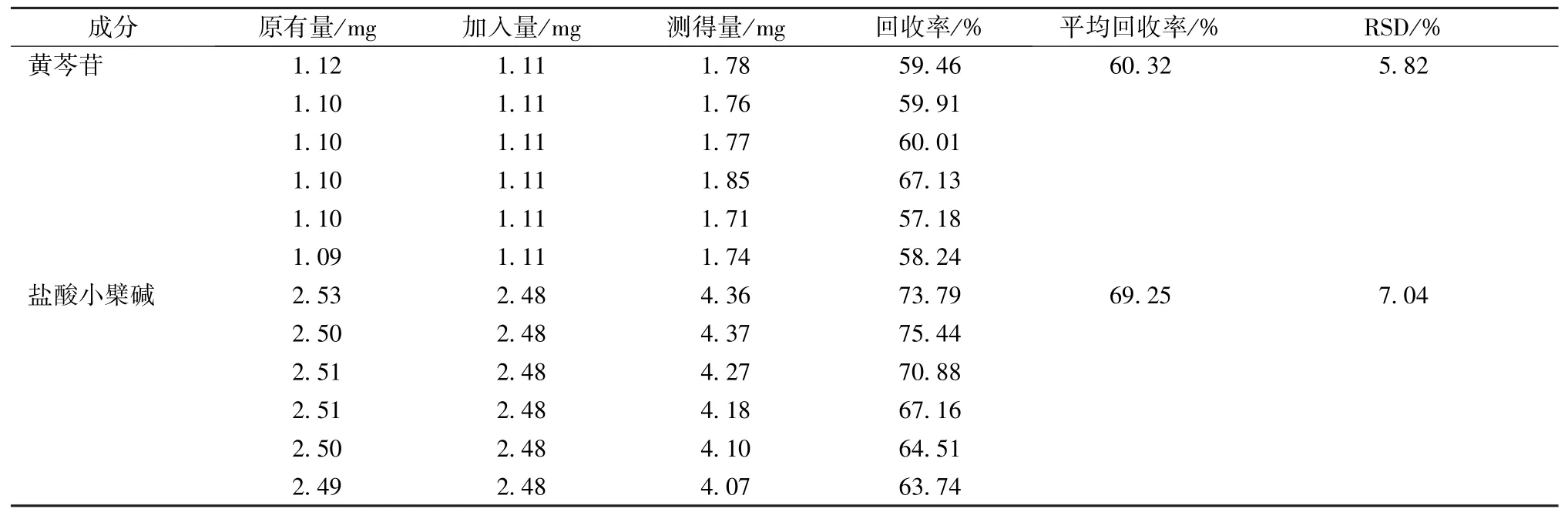
表1 黄芩苷、盐酸小檗碱加样回收率试验结果(n=6)Tab.1 Results of recovery tests for baicalin and berberine hydrochloride(n=6)
2.1.11 样品含有量测定 取“2.1.2”项下黄芩苷对照品溶液(2)0.4 mL、盐酸小檗碱对照品溶液(2)1.3 mL,置于5 mL 量瓶中,甲醇定容至刻度,摇匀,0.45 μm 微孔滤膜过滤;取“2.1.2”项下黄芩苷对照品溶液(3)1.4 mL、盐酸小檗碱对照品溶液(3)1.2 mL,置于5 mL 量瓶中,二甲基亚砜定容至刻度,摇匀,0.45 μm 微孔滤膜过滤,平行3 份,在“2.1.1”项下色谱条件下进样测定,结果见表2,可知在以甲醇、二甲基亚砜为溶剂配制的对照品溶液中,各成分含有量均低于理论值。

表2 黄芩苷、盐酸小檗碱含有量测定结果(n=3)Tab.2 Results of content determination of baicalin and berberine hydrochloride(n=3)
2.2 栀子苷含有量测定
2.2.1 色谱条件 Hypersil ODS-2 色谱柱(250 mm×4.6 mm,5 μm);流动相乙腈(A)-0.2%磷酸(B),梯度洗脱(0~32 min,10% →24%A;32~42 min,24% A;42~80 min,24% →50%A;80~90 min,50% →52% A);体积流量1 mL/min;柱温30 ℃;检测波长238 nm;进样量10 μL。
2.2.2 对照品溶液制备 精密称取栀子苷对照品适量,甲醇制成每1 mL 含662.0 μg 该成分的贮备液,精密称取适量,甲醇制成每1 mL 含70.96 μg该成分的溶液,即得。
2.2.3 供试品溶液制备 取丸剂适量,研细,精密称取约0.25 g,置于具塞锥形瓶中,精密加入25 mL 甲醇,称定质量,超声30 min,取出,冷却至室温,甲醇补足减失的质量,摇匀,滤过,取续滤液,过0.45 μm 微孔滤膜,即得。
2.2.4 阴性样品溶液制备 按处方比例除去栀子,作为阴性样品,按“2.2.3”项下方法制备,即得。
2.2.5 专属性试验 吸取“2.2.2”~“2.2.4”项下溶液,在“2.2.1”项色谱条件下进样测定,结果见图2。由图可知,该方法专属性强,阴性无干扰。
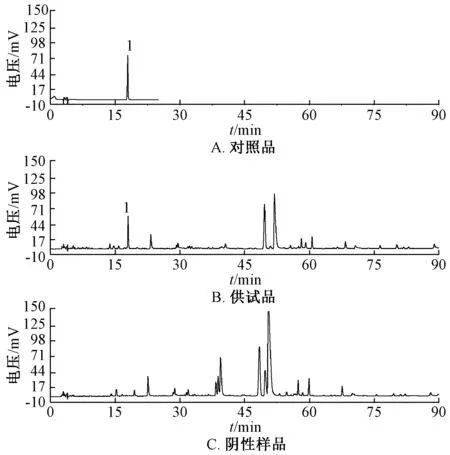
图2 栀子苷HPLC 色谱图Fig.2 HPLC chromatograms of geniposide
2.2.6 线性关系考察 精密吸取“2.2.2”项下贮备液0.2、0.4、0.6、0.8、1.0、1.2 mL 于10 mL量瓶中,甲醇定容,摇匀,在“2.2.1”项色谱条件下进样测定。以进样量为横坐标(X),峰面积为纵坐标(Y)进行回归,得方程为Y=1 002.1X-13.361(R2=0.999 5),在0.132 4~0.794 4 μg 范围内线性关系良好。
2.2.7 精密度试验 精密吸取“2.2.3”项下供试品溶液,在“2.2.1”项色谱条件下进样测定6次,测得栀子苷峰面积RSD 为1.89%,表明仪器精密度良好。
2.2.8 重复性试验 取样品(编号S2)适量,按“2.2.3”项下方法制备供试品溶液,平行6 份,在“2.2.1”项色谱条件下进样测定,测得栀子苷含有量RSD 为2.75%,表明该方法重复性良好。
2.2.9 稳定性试验 取样品(编号S2)适量,按“2.2.3”项下方法制备供试品溶液,在“2.2.1”项色谱条件下于0、2、4、6、8、10、12、24 h 进样测定,测得栀子苷峰面积RSD 为1.47%,表明溶液在24 h 内稳定性良好。
2.2.10 加样回收率试验 取样品(编号S2)适量,研细,精密称取约0.125 g,平行6 份,精密加入栀子苷对照品适量,按“2.2.3”项下方法制备供试品溶液,在“2.2.1”项色谱条件下进样测定,计算回收率,结果见表3。
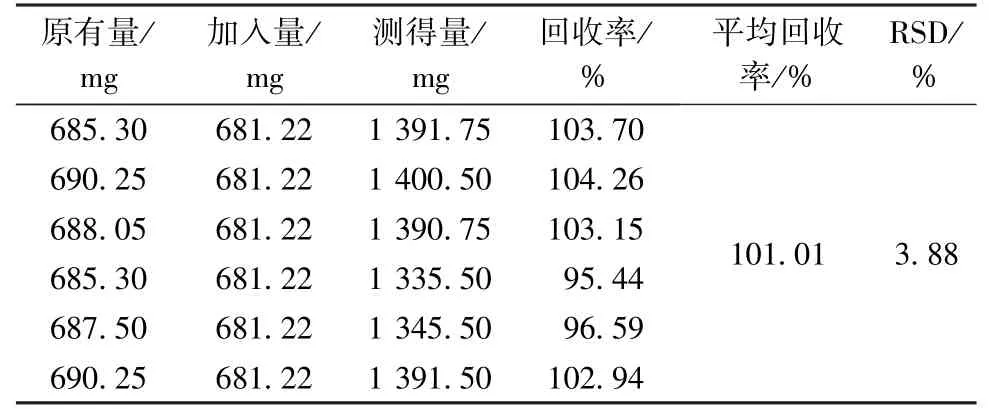
表3 栀子苷加样回收率试验结果(n=6)Tab.3 Results of recovery tests for geniposide(n=6)
2.2.11 样品含有量测定 取10 批丸剂,每批2份,按“2.2.3”项下方法制备供试品溶液,在“2.2.1”项色谱条件下进样测定,计算含有量,结果见表4。以平均值的80%为最低限度,栀子苷含有量应不低于4.62 mg/g。
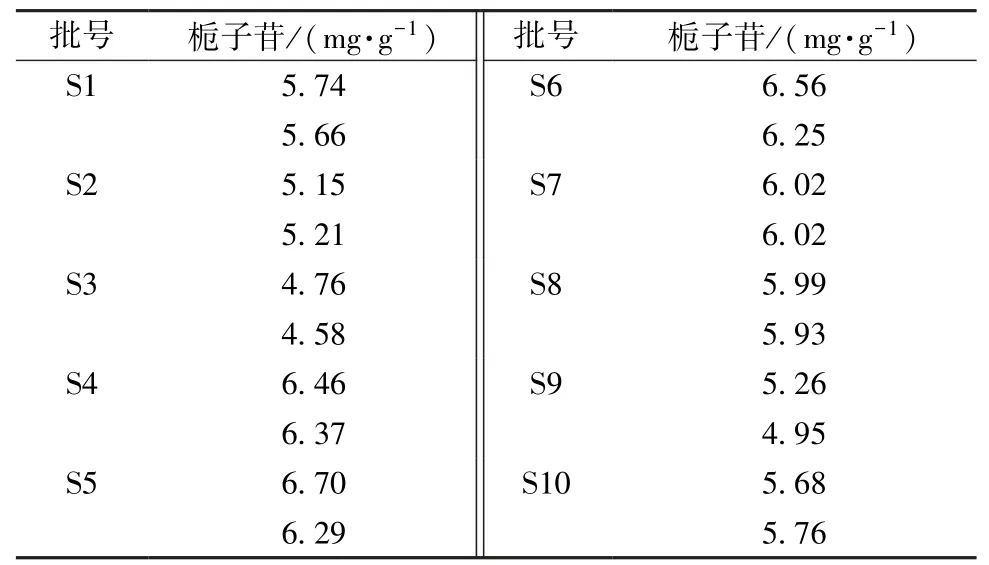
表4 栀子苷含有量测定结果(n=2)Tab.4 Results of content determination of geniposide(n=2)
2.3 指纹图谱建立
2.3.1 精密度试验 取样品(编号S2)1 份,按“2.2.3”项下方法制备供试品溶液,在“2.2.1”项色谱条件下进样测定6 次,以栀子苷为参照峰,测得13 个色谱峰相对保留时间RSD 均小于0.63%,相对峰面积RSD 均小于2.95%,表明仪器精密度良好。
2.3.2 重复性试验 取样品(编号S2)6 份,按“2.2.3”项下方法制备供试品溶液,在“2.2.1”项色谱条件下进样测定,以栀子苷为参照峰,测得13 个色谱峰相对保留时间RSD 均小于0.80%,相对峰面积RSD 均小于2.65%,表明该方法重复性良好。
2.3.3 稳定性试验 取样品(编号S2)1 份,按“2.2.3”项下方法制备供试品溶液,于0、2、4、6、8、12 h 在“2.2.1”项色谱条件下进样测定,以栀子苷为参照峰,测得13 个色谱峰相对保留时间RSD 均小于0.27%,相对峰面积RSD 均小于2.15%,表明溶液在12 h 内稳定性良好。
2.3.4 共有峰分析 按“2.2.3”项下方法制备供试品溶液,在“2.2.1”项色谱条件下进样测定,得到指纹图谱(图3),确定18 个共有峰,其峰面积占总数的90% 以上。以4 号峰(栀子苷)为参照峰(S),计算各色谱峰相关保留时间、相对保留峰面积,结果见表5~6,可知前者RSD 小于0.65%,后者为7.79%~26.98%,表明各批样品中成分种类较稳定,但其含有量有较大差异。
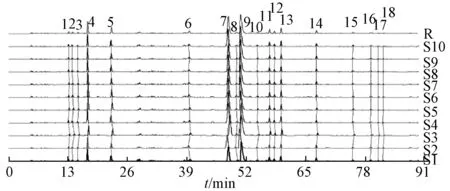
图3 10 批样品HPLC 指纹图谱Fig.3 HPLC fingerprints of ten batches of samples

表5 共有峰相对保留时间Tab.5 Relative retention time of common peaks
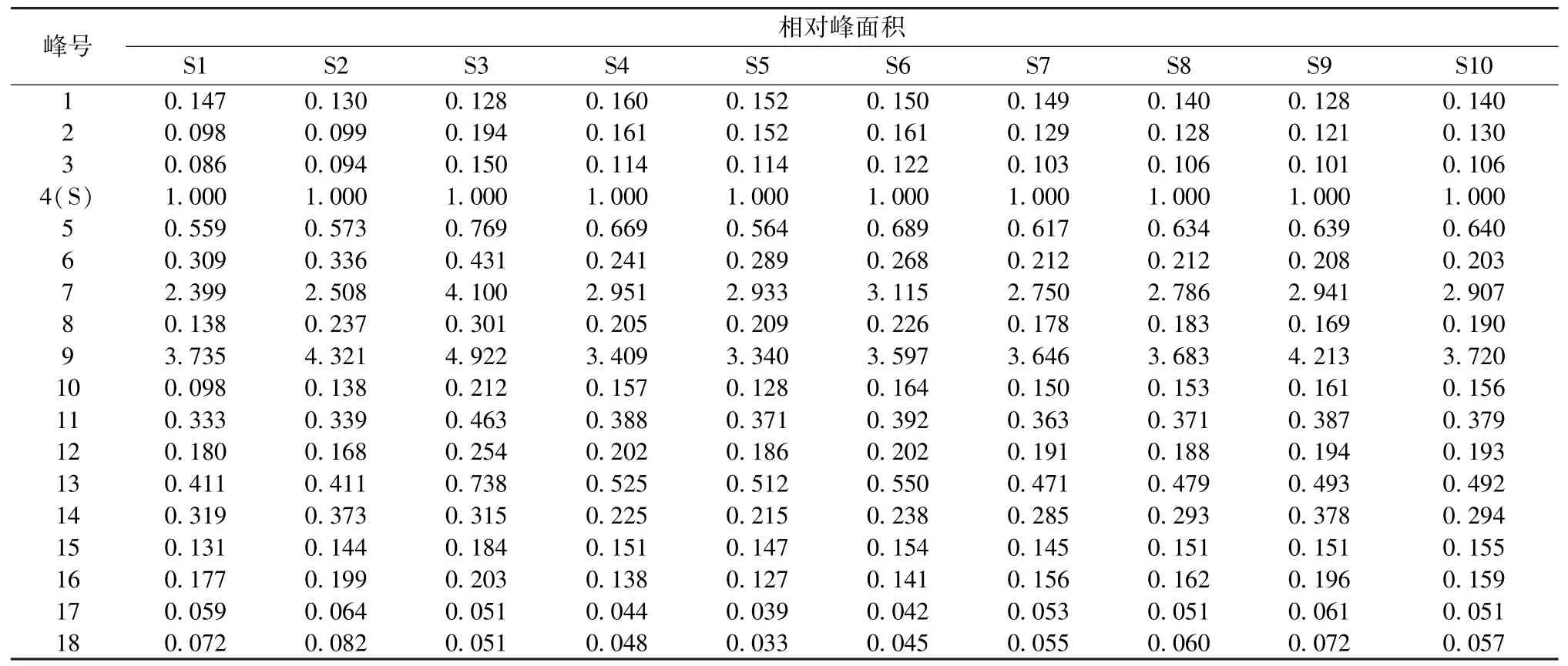
表6 共有峰相对峰面积Tab.6 Relative peak areas of common peaks
按“2.2.3”项下方法制备供试品溶液及除滑石以外其余6 味药材溶液,在“2.2.1”项色谱条件下进样测定,共确认7 个色谱峰所含成分,分别为4 号峰(栀子苷)、6 号峰(盐酸药根碱)、7 号峰(黄芩苷)、8 号峰(盐酸巴马汀)、9 号峰(盐酸小檗碱)、14 号峰(黄芩素)、16 号峰(汉黄芩素),以及15 个特征峰来源,其中3 个不能得到归属,其余峰来自栀子(1、4 号峰)、大黄(12、15号峰)、黄柏(2、3、5 号峰)、黄连(6、8 号峰)、黄芩(7、11、13、14、16 号峰),而9 号峰归属于黄柏、黄连。见图4。

图4 共有峰指认Fig.4 Identification of common peaks
2.3.5 相似度评价 将10 批样品指纹图谱导入国家药典委员会颁布的“中药色谱指纹图谱相似度评价系统”(2004A 版)进行色谱峰匹配,测得相似度分别为0.995、0.990、0.996、0.998、0.997、0.998、1.000、1.000、0.998、1.000,拟规定其应大于0.900。
3 讨论
文献报道,黄连与包括黄芩、大黄在内的许多中药共煎煮时均有沉淀物产生,而且黄连与黄芩复方煎出液中黄连生物碱、黄芩黄酮含有量下降[11-13],沉淀物主要由黄连碱、小檗碱、表小檗碱、巴马汀、药根碱、黄芩苷、汉黄芩苷等组成。前期以甲醇为溶剂制备供试品溶液,发现黄芩苷平均加样回收率为60.38%,RSD 为5.79%,而盐酸小檗碱分别为69.25%、7.04%,远低于限度,同时RSD 较大,不符合相关技术要求,其原因是由于对照品溶液与黄芩苷、盐酸小檗碱发生反应,生成沉淀后被滤去,无法正确评价含黄芩与黄连、黄柏中成药含有量测定的准确度。因此,课题组前期分别以甲醇、二甲基亚砜为溶剂配制黄芩苷、盐酸小檗碱对照品溶液,研究两者发生沉淀反应的规律,发现其含有量均低于加入量。由此可知,测定含黄芩-黄连、黄柏配伍的中成药中黄芩苷、盐酸小檗碱含有量时,无法保证其准确度。
10 批黄连解毒丸中栀子苷平均含有量为5.77 mg/g,按照平均值的80%为最低限度,拟规定其不低于4.62 mg/g;HPLC 指纹图谱中标定了18 个共有峰,并将其中15 个归属到各药材,明确了7 个所含的化学成分,相似度0.995~1.000,拟规定其应大于0.900。根据各共有峰的tR(RSD<0.65%)和相对峰面积(RSD 7.79%~26.98%)可知,10 批样品中成分种类较稳定,但含有量有明显差异,可能是由于所用药材质量不一,也可能是因为黄芩-黄连、黄柏共煎产生的沉淀大部分不能溶于甲醇。今后,课题组将建立一种准确的方法来测定黄连解毒丸中黄芩苷、盐酸小檗碱含有量,并将其应用于三黄片、黄连上清片、黄连上清丸、黄连羊肝丸等制剂[14]的质量控制中。

