经皮肾镜碎石术治疗经腰开放取石术后复发性肾结石的疗效与安全性探讨
季健 普超 储永波 孙晓磊 代兴锐云南省第三人民医院泌尿外科6500昆明云南省老年病医院内三科
PCNL因其结石清除率高、创伤小,目前已成为治疗肾结石的首选方法之一[1]。但在PCNL常规开展以前,上尿路结石主要通过经腰切口的开放手术来治疗。而泌尿系结石作为一种全球性的疾病,治疗后易复发,10年复发率可高达50%[2]。在临床工作中,早期患者曾经因上尿路结石行经腰切口的开放手术,术后结石复发并不罕见。对此类患者的治疗,目前我们还是以PCNL为主。但现阶段国内外对经腰开放取石术后复发性肾结石通过PCNL治疗的研究较少,因此有必要对此类患者的特点、治疗效果和可能存在的风险进行总结。
本研究采用回顾性病例对照研究,通过比较经腰开放取石术后复发性肾结石患者和首次PCNL患者术前临床检验和影像学特点,以及手术安全性及手术效果等指标,为临床决策提供参考。
1 资料与方法
1.1 临床资料
选取云南省第三人民医院2016年6月-2018年5月收治的52例患者,根据既往是否行经腰开放取石术,将52例患者分为开放取石术后PCNL组(A组12例)和首次PCNL组(B组40例)。A组均因泌尿系结石行经腰腹膜后路径切开取石术,其中既往行肾盂切开取石术患者6例,输尿管切开取石患者4例,肾实质切开取石术2例;均因开放取石术后6~10年结石复发就诊。病例纳入标准:①直径2~4 cm的肾盂或肾盏结石;②肾积水深度为0~4 cm;③无明确的手术禁忌证。排除标准:①先天性肾脏畸形;②严重的心肺功能不全,不能耐受俯卧位及全麻手术的患者;③严重凝血功能异常的患者;④肾实质或肾盂内严重感染证据者;⑤输尿管结石。患者术前均完善血、尿、粪便常规、肝肾功能、中段尿培养等检查。行泌尿系超声、KUB或IVU、泌尿系CT检查等明确结石体积、位置及肾积水程度。所有患者术前均预防性应用抗生素治疗3 d,完善常规术前准备。如有泌尿系感染致发热等全身症状者,则以敏感抗生素积极抗感染及相关对症支持治疗控制发热等全身症状1周以上,待血白细胞,血清降钙素原(procalcitonin,PCT)及血培养正常后方可手术。两组患者组间年龄、性别及结石罹患侧、结石负荷等数据差异无统计学意义(P>0.05),详见表l。所有患者均为一期手术,手术由同一医师完成,患者对于手术均知情同意,上报并得到医院伦理委员批准。

表1 两组患者基本资料比较
1.2 手术方法
患者全麻,首先取截石位。膀胱镜直视下于患侧输尿管逆行置入F5输尿管导管,留置F20三腔导尿管。改体位为俯卧位,调整腰桥。超声引导下经腋后线与肩胛下线之间第12肋下或10、11肋间选择穿刺点,穿刺成功后,留置超滑导丝。使用筋膜扩张器从F4依次扩张至F22后,成功建立皮肾通道,置入F18李逊肾镜。两组患者均使用低压重力滴注法进行冲洗,具体操作为3 000 mL生理盐水持续滴注,平均流量约200 mL/min,盐水袋底部高于肾平面40~60 cm[3]。使用气压弹道超声联合碎石系统击碎结石并吸出碎石或钬激光将结石击碎后直接钳夹取出。认真检查视野内结石清除情况及损伤情况,在输尿管内留置F4.8双J管1根后退镜。留置F22肾造瘘管。术后1个月于膀胱镜下拔除双J管。
1.3 观察指标
记录两组患者入院尿液常规白细胞数、术前血红蛋白值。由CT检查计算肾积水程度、肾皮质厚度、结石占据的肾盏个数。肾皮质厚度具体方式为测量肾皮质最大径、最小径取两者平均值。术后2~3 h测定血红蛋白值、血白细胞值、术后16~18 h测定血PCT值,如有异常升高给予连续PCT检测直至正常,并记录最高PCT值。术后统计最高体温值、碎石取石时间、相关并发症发生率。术后2~3 d行胸片及KUB检查,结石长径>4 mm定义为残留结石并统计残石数。
1.4 统计学方法
采用SPSS 17.0统计软件处理数据,计量资料数据采用±s表示,正态分布且满足方差齐性的计量资料比较采用方差分析。计数资料无序分类变量采用χ2检验。不能满足正态分布或方差齐性的计量资料以及计数资料有序分类变量采用中位数(四分位间距)[M(IQR)]表示,采用Mann-WhitneyU检验。以P<0.05为差异有统计学意义。
2 结果
52例患者均全部一次性成功建立通道,未发生大出血、周围器官损伤等相关并发症,无脓毒血症、感染性休克及死亡病例。开放术后PCNL组有3例患者PCT异常升高,4例患者术后出现发热,6例患者出现白细胞异常升高。首次PCNL组1例PCT异常升高,2例患者术后出现发热现象,3例患者出现白细胞异常升高。
2.1 术前资料比较
A组入院时尿液常规白细胞数、术前肾积水程度、结石占据的肾盏个数明显大于B组(P<0.05);A组肾皮质厚度小于B组(P<0.05),结果详见表2。

表2 两组术前资料比较
2.2 术中及术后资料比较
B组术后发热人数、血白细胞值、PCT值低于A组(P<0.05),A组碎石取石时间大于B组,差异有统计学意义(P<0.05)。两组之间血红蛋白下降值差异无统计学意义(P>0.05)。A组术后残石数量大于B组(P<0.05),结果详见表3。
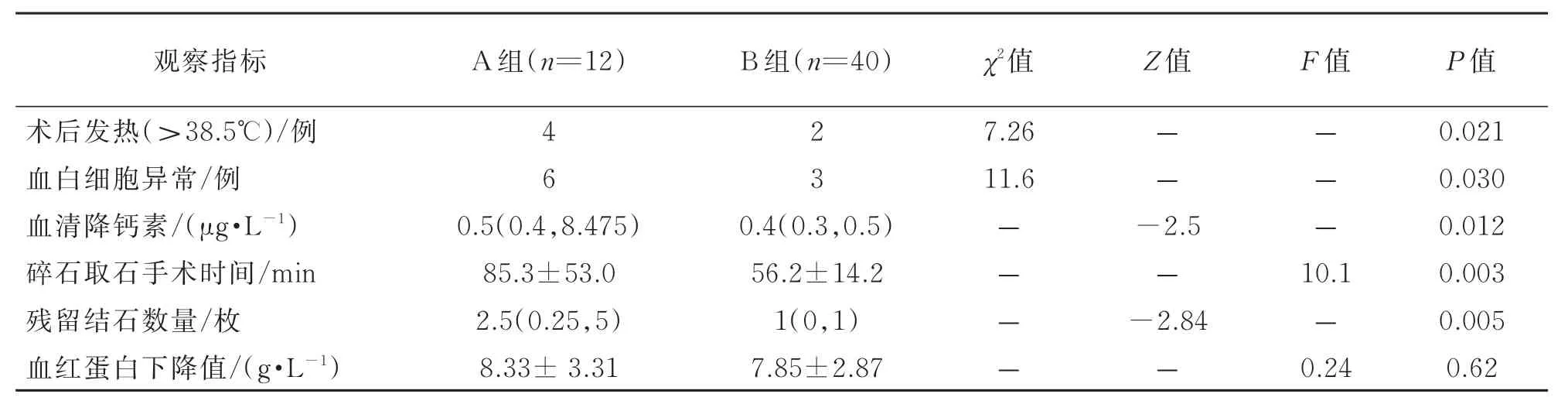
表3 两组术中及术后资料比较
3 讨论
对于经腰切口开放取石术后结石复发的患者,如果具备经皮肾镜手术指征,目前主要以PCNL作为主要的处理手段。但此类患者的临床特征具有一定的特殊性,B超主要表现为肾脏形态相对不规则、肾脏轮廓及实质回声欠均匀以及结石分布较为分散。此外,患者还常伴有不规则的肾积水,且通常合并有较为严重的泌尿系统感染。为此,我们通过回顾性病例对照研究来探讨经腰开放取石术后复发性肾结石PCNL与首次PCNL在术前尿液白细胞数、肾脏积水、肾皮质厚度和结石特点以及手术安全性和手术效果方面的异同。
PCNL会出现发热、感染、出血和结石残留等并发症,其中术中和术后出血是最主要的并发症之一[4-6]。有学者发现有开放取石手术史的患者肾脏以及肾周组织脆性增大,再次PCNL时易撕裂肾组织,损伤肾内血管[7]。另外,由于肾脏组织脆性大,损伤后的收缩能力也差,造成术中和术后出血增多。本组12例患者均成功建立通道,碎石取石操作的视野较为清晰,无一例发生术中及术后大出血的情况。推测其可能的原因是开放取石术后患者肾积水较重,肾皮质较薄,建立穿刺通道相对容易,导致出血的风险较小。因此,虽然开放术后PCNL组患者可能存在着肾脏组织脆性增大,开放术后肾及肾周组织瘢痕形成等不利因素,增加出血的风险,但在手术技术成熟的情况下,如果不进行大角度碎石,其大量出血的可能性并不明显增加。本研究中两组患者术后血红蛋白下降值没有明显的差异,除了以上原因之外,也可能是由于PCNL大出血并发症发生率较低,由于样本量较少,在统计学上尚不足以检测出二者之间的差异性,所以需要进一步研究来明确开放术后PCNL患者的出血风险。最后,本研究发现A组肾积水程度较B组严重,其肾脏解剖形态不规则,肾皮质较薄,其产生原因可能与开放手术的组织损伤愈合过程中产生的粘连有关。虽然A组有更明显的肾积水,客观上B超定位和手术穿刺的难度会有所降低,但A组患者结石占据的肾盏个数明显多于B组,结石位置的不确定性和非连续性,以及肾脏集合系统的不规则形态却增加了手术难度。最终导致碎石取石手术时间较长和残石数较高。
经皮肾镜手术安全性研究多集中于出血和感染等方面,重症感染是PCNL比较严重的并发症之一,根据文献报道PCNL后发热率为25.8%~37.0%,其引发的严重的脓毒血症可能导致患者感染性休克甚至死亡[8-10]。本研究通过比较术前相关指标,发现A组入院尿液常规白细胞数明显高于B组,分析其主要的原因可能与反复的结石复发、梗阻以及首次开放手术治疗体内植入物有一定的关系。目前多数学者认为,尿路感染是PCNL术后具有潜在危险性的并发症之一[11]。本研究同样发现,A组术后无论在发热还是在感染指标方面均明显高于B组。因此,对于开放术后PCNL患者,其术中和术后感染风险可能会明显的增加,除需要给予足够的重视之外,术前有必要通过有效的治疗来干预和控制泌尿系感染来减低PCNL重症感染等严重并发症发生。PCT是降钙素的前体物质,其已被证明可作为PCNL后尿脓毒血症早期诊断较理想的标志物。此外,PCT对尿脓毒症的早期诊断具有良好敏感性和特异性,可作为尿脓毒症患者的常规检测指标[12-13]。本研究发现A组PCT值明显高于B组。虽然A组所有患者循环系统稳定,未发生严重的脓毒血症,无感染性休克及死亡病例,但其感染和潜在发生脓毒血症的风险需要引起足够的警觉。有研究表明,由灌注引起的术中肾集合系统压力失衡,是导致细菌毒素和致热原入血而出现术后发热或脓毒血症的重要原因[14-15],本研究两组手术患者均使用低压重力滴注法冲洗而没有使用常见的灌注泵灌注法冲洗。灌注泵灌注法比低压重力滴注法可能产生的更高的肾盂压,因此,在采用灌注泵灌注法处理开放取石术后肾结石患者时其感染的风险可能增加,需要引起手术医师的重视。
综上所述,经腰开放术后肾结石复发患者无论在术前评估、准备以及术中操作等多方面均较首次经皮肾镜难度有一定程度的增加。经腰开放术后肾结石复发患者术后感染风险较大,术后结石清除率低,但出血风险还需要进一步观察。因此,此类患者需要更为完善围手术期的处理、评估和解释工作。
——肾结石

