冻干法制备Fe掺杂C3N4光催化降解有机污染物
刘洪燕, 陈少伟, 封可心
(廊坊师范学院 化学与材料科学学院, 河北 廊坊 065000)
随着我国经济的高速发展,工业化不断进行,污染问题也随之而来.水作为人类的生命之源,“水污染”问题成了环境问题中的主要问题.我国水体污染不仅在江河湖流,也存在于乡村城镇生活用水,这对人类的身体健康有着很大的威胁[1].不管是地表水还是地下水,水质问题存在的很大危机,治理水资源污染变得刻不容缓[2].由于我国是染料大国,染料产量居世界首位,同时,染料行业也属高能耗、高污染产业.在水体污染中,染料废水已经成为我国水环境污染重要原因之一.目前,主要的污水处理方法有物理法、化学法和生物法.物理法常见吸附法,吸附剂用活性炭和矿物吸附;在生物法中,虽然经济成本较低,但是处理和反应时间较长,适应能力也较差,有些水处理生物可能会使水的毒性加大;化学法中,有电化学法和高级氧化法,电化学方法以往存在能耗大、成本高的缺点,而最近发展起来的光催化氧化技术是新兴起的一种水污染治理方法,由于能将较稳定且难分解的有机分子转化为无害无毒的物质,反应产物大多数为二氧化碳、水和无机离子,并且不用加入氧化剂,因此该方法成为处理污水的研究热点.光催化氧化技术是在光化学氧化的基础上发展起来的,相对于光化学法,有更强的氧化能力,可使有机污染物更彻底地降解[3].
1972年,Fujishima等[4]发现TiO2电极可以光解水而产生H2和O2,引领人类打开通过半导体光催化材料获得清洁能源和治理环境污染的探索之门.TiO2作为一种半导体材料,其化学性质稳定、无毒,能够将水光解为氢能和将污染物光解为无害的小分子.由于TiO2的禁带宽度较大,吸收光谱主要在紫外区,不能有效利用太阳光,并且光生电荷易于复合,在很大程度上阻碍了TiO2在工业中的应用,虽然采用了离子掺杂、半导体复合等手段来改善光谱吸收,提高光催化效果,得到一定改善,但并没有达到理想效果,开发和寻找新的光催化剂材料势在必行[5].
具有片状结构的C3N4也是一种光催化剂,其还原势能高,而且稳定廉价,在pH为0~14时都比较稳定,同时具备聚合物半导体的化学组成和能带结构易调控等一些特点,满足了人们对于大量使用光催化剂方面的需求.C3N4作为典型的半导体聚合物,在可见光催化条件下产生光生电子空穴、生成超氧自由基和羟基自由基等活性物种,能够迅速有效地降解有机污染物且无二次污染.但是C3N4仍然需要提高其光催化效率,由于其比表面积小、传质作用差、光生载流子复合严重等缺点,于是,对C3N4的改性引起了人们极大地关注[6-12].研究者们已经提出了多种改性方法来解决这个问题,如金属掺杂、非金属掺杂、强酸质子化、多孔结构化和形成异质结等方法,在这些方法中,掺杂法是最为有效和方便的方法之一[13].掺杂法中,在C3N4掺杂了钾离子后,其样品表面的小孔增加,催化剂比表面积增大,能带宽度减小,同时降低了光生电子空穴对的复合率,所以样品光催化性能得到显著的提升[9].碱金属负载在C3N4中有利于电子的跃迁,且对于C3N4的表面电子有较好的活化作用[14].SrTiO3/g-C3N4/Bi2O3复合物也能显著提高光催化剂的活性[15].
本文以尿素和硝酸铁为原料,采用冻干法制备Fe掺杂的氮化碳复合催化剂.以罗丹明B为目标污染物,考察制备的复合材料在可见光下的光催化活性,研究Fe掺杂对氮化碳催化性能的影响.
1 实验部分
1.1 光催化剂的制备
1.1.1 C3N4光催化剂的制备
使用电子天平称取8 g尿素置于250 mL烧杯中,然后加入85 mL无水乙醇搅拌溶解,溶解后转移入250 mL圆底烧瓶,在80 ℃中回流1 h,回流结束后减压蒸馏,圆底烧瓶中剩余的结晶物冷却干燥后,分别盛于编号为1、2、3的刚玉坩埚中,随后置于马弗炉中煅烧,马弗炉初始温度为50 ℃,升温速度15 ℃/min,目标温度500 ℃,保温120 min,待马弗炉降温至常温时,取出催化剂, 装在10 mL的塑料试管内,编号.
1.1.2 Fe-C3N4光催化剂的制备
称取一定量的硝酸铁,8 g尿素,一同置于250 mL烧杯中,然后加入85 mL无水乙醇搅拌溶解,溶解后转移入250 mL圆底烧瓶,在80 ℃中回流1 h,回流结束后减压蒸馏,圆底烧瓶中剩余的结晶物冷却干燥后,分别盛于编号为1、2、3的刚玉坩埚中,随后置于马弗炉中煅烧,马弗炉初始温度为50 ℃,升温速度15 ℃/min,目标温度500 ℃,保温120 min,待马弗炉降温至常温时,取出催化剂, 装在10 mL的塑料试管内,编号.
1.1.3 lyo-Fe-C3N4光催化剂的制备
称取一定量的硝酸铁,8 g尿素,一同置于250 mL烧杯中,然后加入35 mL水搅拌溶解,溶解后转移入250 mL圆底烧瓶,在80 ℃中回流1 h,回流结束后放入冻干机中,经过72 h得到冻干粉,分别盛于编号为1、2、3的刚玉坩埚中,随后置于马弗炉中煅烧,马弗炉初始温度为50 ℃,升温速度15 ℃/min,目标温度500 ℃,保温120 min,待马弗炉降温至常温时,取出催化剂, 装在10 mL的塑料试管内,编号.
1.2 光催化剂的表征
催化剂晶体结构采用日本理学2500 型X 射线衍射仪(XRD)进行测定,Cu Kα 辐射(λ=0.154 06 nm),掠角为1°,扫描范围10°~90°,工作电压40 kV,电流200 mA.紫外-可见漫反射光谱(UV-Vis DRS)采用岛津UV2550 型积分球紫外-可见分光光度计进行测定.
1.3 光降解实验
称取C3N4、Fe-C3N4和lyo-Fe-C3N4各20 mg分别置于90 mL超纯水中,并使用吸量管移取10 mL质量浓度为200 mg/L的罗丹明B溶液加入其中,利用超声波超声30 min达到吸附平衡后,搅拌,置于氙灯下进行降解,观察罗丹明B的褪色程度,每隔15~30 min取样一次至降解完全,得到不同降解时间的罗丹明B溶液样品,用高速离心机离心样品,取上层清液.用紫外可见分光光度计(UV2550 ,日本岛津)对溶液样品进行200~800 nm波长扫描得到吸光度变化曲线.
2 结果与讨论
2.1 XRD分析
从图1可以看出:样品在27.5°有很明显的特征峰,通过对比标准卡片 (PDF87-1526),此处的强衍射峰对应 C3N4的(002)晶面,27.5°处的衍射峰可以归因于堆叠的共轭芳香环,类似石墨的层状结构,表明石墨相的C3N4已经形成,Fe引入后没有改变C3N4的峰位,说明Fe掺杂进去后并没有改变C3N4的结构;另外也没有出现新的特征峰,没有Fe及其他氧化物形态的衍射峰出现,表明Fe是掺杂到C3N4晶格内的,而不是负载到催化剂表面.
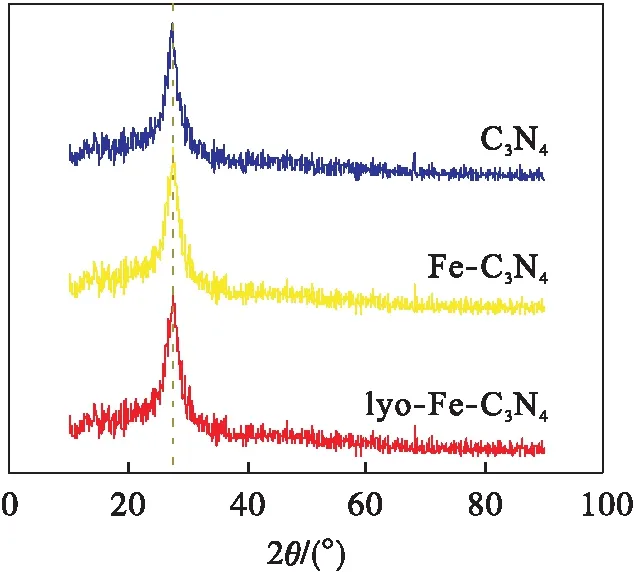
图1 催化剂的 XRD图谱Fig.1 XRD patterns of the catalysis
2.2 催化剂的吸收光谱
图2为催化剂的 UV-Vis 漫反射吸收光谱.光激发C3N4后产生的光电子从 N 2p轨道形成的价带(VB)能级转移到C 2p轨道形成的导带(CB)能级,从而展现出典型的半导体吸收[16].Fe掺杂后催化剂在可见光区的吸收略有提高,也表现出一定的吸收边界位移.
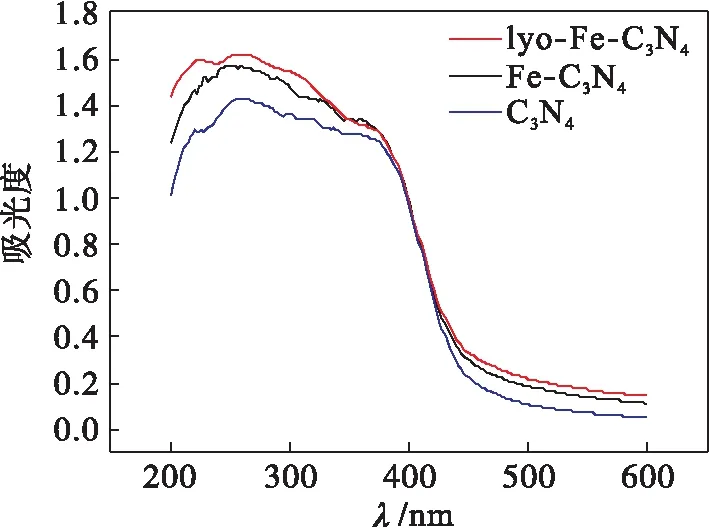
图2 光催化剂的UV-Vis漫反射吸收光谱Fig.2 UV-Vis diffuse reflection spectra of photocatalysts
2.3 光催化剂降解性能
C3N4、Fe-C3N4和lyo-Fe-C3N4在可见光下对罗丹明B的降解反应结果如图3所示.C3N4在150 min内对罗丹明B的降解率为87 %,Fe-C3N4在150 min内对罗丹明B的降解率几乎为100 %, lyo-Fe-C3N4在 105 min 内对罗丹明B几乎完全降解.由图4可以看出lyo-Fe-C3N4的降解速率明显优于C3N4和Fe-C3N4.
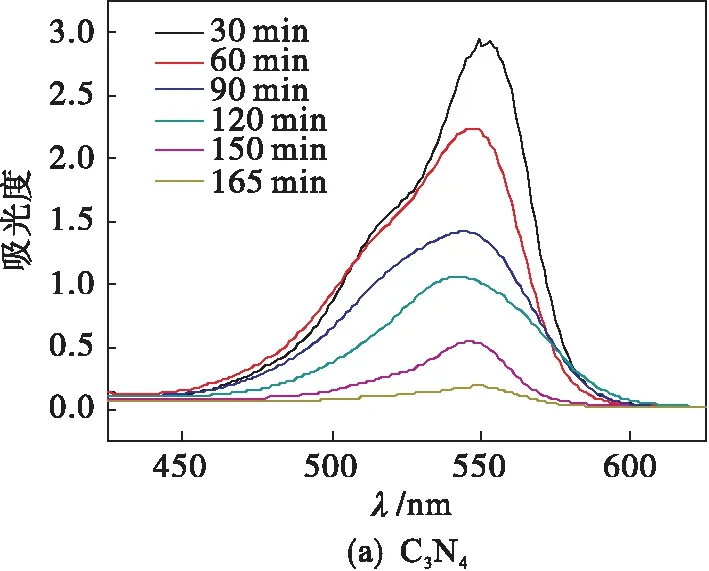
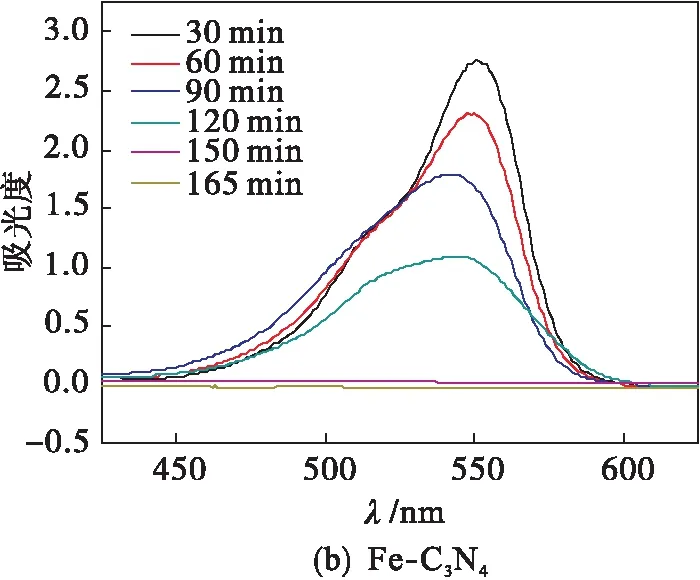
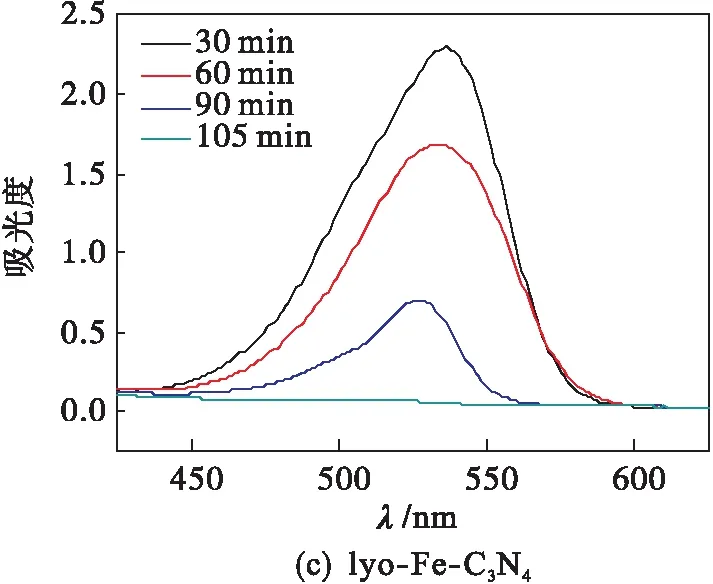
图3 不同催化剂降解罗丹明B随时间变化吸收光谱Fig.3 Absorption spectra of rhodamine B degraded by different catalysts over time
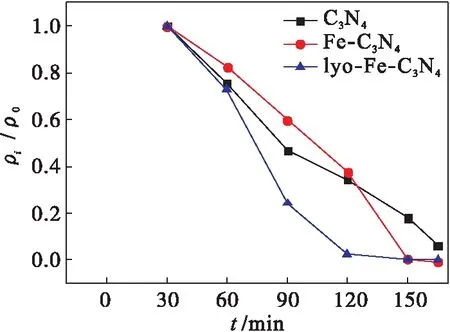
图4 不同催化剂对罗丹明B的降解速度Fig.4 Degradation rate of rhodamine B by different catalysts
图5是lyo-x%Fe-C3N4在可见光下的催化性能.从图5可以看出:通过冻干法制备的前驱体得到的光催化剂降解效果普遍较好,在105 min内基本降解完全,其中Fe的掺杂量(质量分数,下同)为0.4 %时效果最好,在90 min内降解率达到99.5 %.
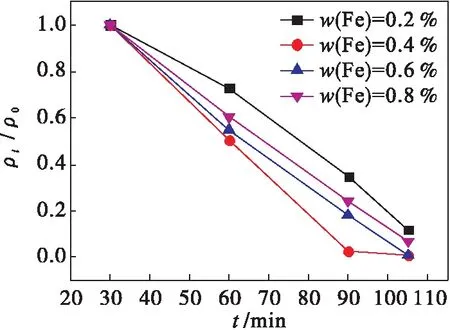
图5 lyo-x %Fe-C3N4在可见光下的催化性能Fig.5 Photocatalytic performances of lyo-x % Fe- C3N4 under visible light
为进一步探究lyo-Fe-C3N4光催化剂催化效果的优异性,对其进行BET表征,结果如图6所示.
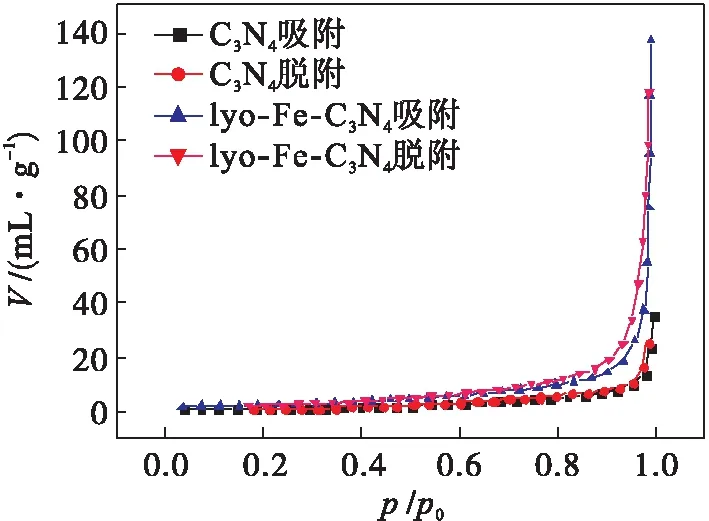
图6 C3N4 与lyo-Fe-C3N4吸附-脱附等温线Fig.6 Isothermal adsorption/desorption curves of C3N4 and lyo-Fe-C3N4
通过对比等温线发现,随着相对压力的升高,吸附量也越来越多,说明有孔充填.而以冻干方式掺杂Fe的lyo-Fe-C3N4吸附和脱附等温线要比C3N4的吸附和脱附量高很多,表明经过冻干法掺杂Fe使C3N4孔径和孔容增大.另外,通过BET分析,经过冻干方式掺杂Fe的lyo-Fe-C3N4比表面积也增加为C3N4的2.275倍.详细数据如表1所示.
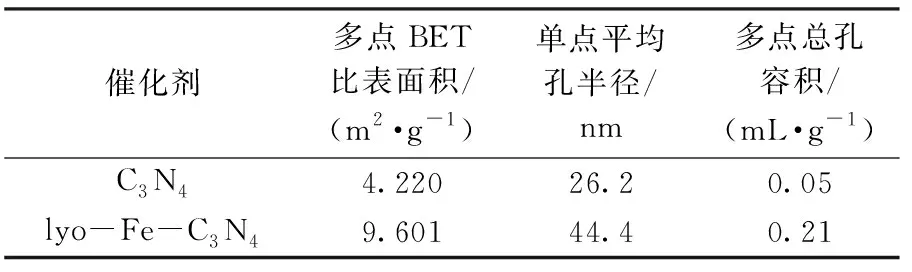
表1 BET数据摘要
2.4 光催化机理分析
为了进一步研究催化剂在可见光下催化降解罗丹明B的反应机理,通过向光催化体系中分别添加羟基自由捕获剂异丙醇(IPA)、空穴捕获剂乙二胺四乙酸二钠(EDTA-2Na)和超氧自由基捕获剂对苯醌(BQ)来验证可能存在的自由基种类,结果如图7所示.
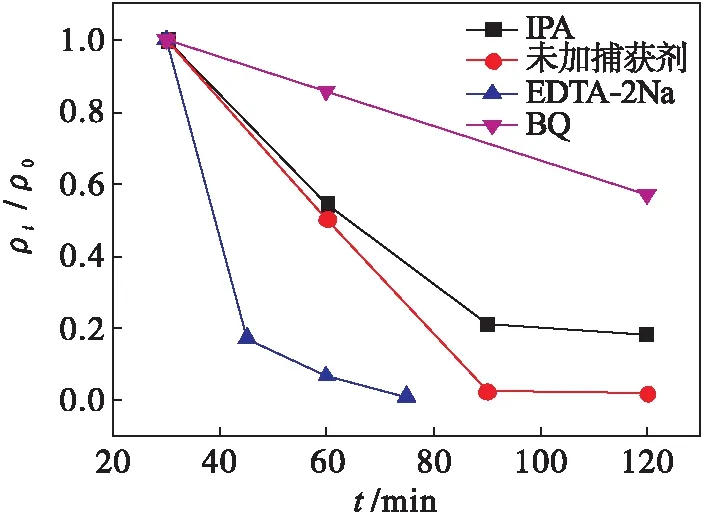
图7 不同捕获剂下lyo-Fe-C3N4光催化降解效果Fig.7 Photocatalytic activity of lyo-Fe-C3N4with different scavengers
从图7可以看出:加了异丙醇之后,降解速度变化不大,说明活性物种不是羟基自由基起主要作用;加入对苯醌后降解速度明显变慢,说明超氧自由基对降解速率起到关键作用,而加入乙二胺四乙酸二钠后,降解速率明显变快,这一现象可能是由于加入乙二胺四乙酸二钠(EDTA-2Na)捕获h+,抑制了e-/h+对复合, 提高了量子效率,产生了更多的超氧自由基活性物种,因而光催化性能显著增强.
由此可以得出:lyo-Fe-C3N4起催化作用活性物种主要是超氧自由基,lyo-Fe-C3N4具有较大的比表面积和丰富的孔隙结构,活性位点较多催化效果较好.
3 结 论
通过冻干法成功地把铁掺杂到C3N4中,制备出了lyo-Fe-C3N4光催化剂,其表现出良好的光催化活性,在同等条件下,90 min内降解率达到99.5 %,而C3N4在90 min内降解率达到55 %.XRD、UV-Vis表征结果表明Fe的引入没有改变C3N4的石墨相结构,吸收光谱没有明显变化;BET测试发现,经过冻干方式掺杂Fe的lyo-Fe-C3N4孔洞较多、孔径较大,比表面积也增加为C3N4的2.275倍.这种以冻干方式掺杂Fe得到的光催化剂孔洞多,比表面积大,因此反应活性位点较多,是提高光催化效率的主要因素.通过光催化机理研究表明,该催化体系中的主要活性物种是超氧自由基.

