喹诺酮在抗真菌领域的研究进展
韩冰,冯连顺 编写 刘明亮,郭慧元 审校
(1 西南民族大学药学院,成都 610041;2 中国医学科学院北京协和医学院医药生物技术研究所,北京 100050)
1 前言
真菌是第二大类真核微生物,约有150~510万种,具有形态、生态、代谢和物种多样性。其代谢产物结构丰富,在农业、工业和医药等领域有着广泛的应用。大约50种真菌对人类致病,每年3亿人罹患侵袭性真菌感染(IFIs),135万患者因此丧命。其中,白色念珠菌、新型隐球菌和烟曲霉是导致IFIs的主要致病菌。目前,临床上使用的抗真菌药物屈指可数,且药效、抗菌谱和安全性不尽如人意。更为严峻的是,真菌已对临床上使用的抗真菌药物产生了耐药性。目前,多个抗真菌候选物处于临床研究阶段,但仍不能满足患者的需求。因此,研发新型抗真菌药物迫在眉睫。
喹诺酮类化合物具有抗菌、抗肿瘤、抗结核、抗疟疾和抗真菌等多种生物活性,是临床上常见药物。研究表明,喹诺酮不仅具有潜在的抗真菌活性,而且某些产品如曲伐沙星与抗真菌药物如氟康唑和两性霉素B联合给药时对真菌感染具有协同作用。因此,有必要对喹诺酮类化合物的抗真菌活性进行研究。
喹诺酮可修饰的位点较多,药物化学家对其N-1、C-5、C-6、C-7和C-8位进行了系统而广泛的修饰。近年来,药物化学家筛选了众多喹诺酮衍生物的抗真菌活性,发现某些化合物对药敏型和耐药型真菌具有良好的活性。本文综述了该领域的最新研究进展,并归纳这类化合物的构-效关系(SAR)以指导药物化学家更合理的设计此类化合物。
2 2-喹诺酮衍生物
2-喹诺酮衍生物GSK945237(见图1)和AZD9742目前正处于治疗细菌感染的临床评价阶段,有望于不久的将来为人类健康服务,故2-喹诺酮类化合物引起了药物化学家的极大兴趣。
2-喹诺酮-噻唑烷酮杂合体1(见图2)对所测的黑曲霉、白色念珠菌、烟曲霉和棒曲霉菌具有弱到中等强度的活性,最小抑制浓度(MIC)为6.25~100 μg/mL,弱于对照药酮康唑(MIC: ≤3 μg/mL)。其中,杂合体1b对黑曲霉(MIC: 6.25 μg/mL)、棒曲霉菌(MIC:12.5 μg/mL)和白色念珠菌(MIC: 12.5 μg/mL)的活性最高,而杂合体1e和1o (MIC: 12.5 μg/mL)对烟曲霉的活性最高。SAR显示,苯环上的取代基与活性息息相关,且卤素氟、氯和溴对活性有利,而氨基、羟基和羧基对活性不利;以吗啉基、哌嗪基或哌啶基取代二甲胺基时并不能显著的提高抗真菌活性。
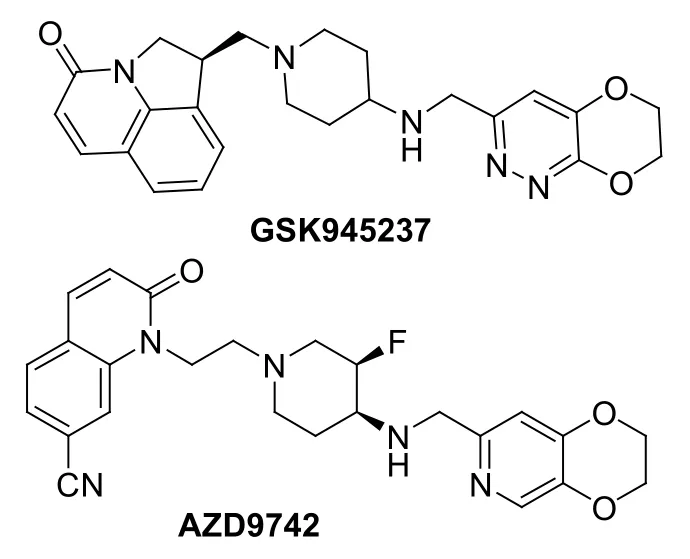
图1 2-喹诺酮衍生物GSK945237和AZD9742的化学结构
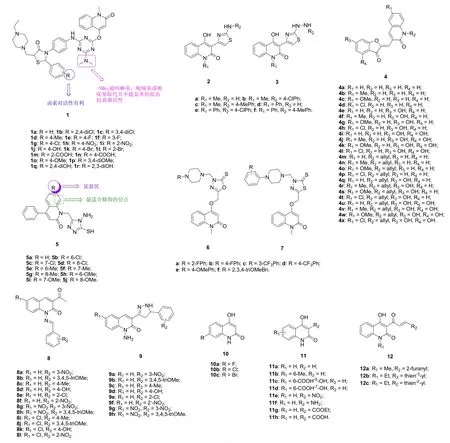
图2 2-喹诺酮衍生物1~12的化学结构
2-喹诺酮-噻唑杂合体2和3对黑曲霉和白色念珠菌的MIC为25~100 μg/mL,活性弱于氟康唑(MIC:12.5 μg/mL)。SAR表明,向噻唑(R2)引入取代苯基时并不能提高抗真菌活性,但氯苯基优于甲苯基。用苯基取代2-喹诺酮母核N-1位的甲基时可在一定程度上提高抗真菌活性,且肼衍生物3的活性优于相应的胺基衍生物2。杂合体2a,b和3d,e对黑曲霉和白色念珠菌的MIC为25 μg/mL,略弱于氟康唑。
绝大多数2-喹诺酮衍生物4 (MIC: 100~500 μg/mL)对棒曲霉菌和白色念珠菌的活性与制霉菌素(MIC: 100 μg/mL)和灰黄霉素(MIC: 500和100 μg/mL)相当或更优。SAR显示,向R1位引入吸电子基可提高抗真菌活性。化合物4d和4t (MIC: 100 μg/mL)抗白色念珠菌活性与制霉菌素相当,而化合物4d、4p和4x (MIC: 100 μg/mL)抗棒曲霉菌活性与灰黄霉素相当。其中,化合物4d对所测真菌的活性不次于制霉菌素和灰黄霉素,值得进一步研究。
2-喹诺酮-三氮唑杂合体5 (MIC: 1~>256 μg/mL)对黑曲霉、烟曲霉和白色念珠菌具有潜在的活性。SAR显示,吸电子基氯优于供电子基甲基和甲氧基,且贡献顺序为氯>甲氧基>氢>甲基;2-喹诺酮的C-8位是最适合引入取代基的位点。其中,杂合体5d (MIC: 1~32 μg/mL)的活性与氟康唑(MIC: 1~16 μg/mL)相当,值得进一步研究。
2-喹诺酮-1,3,4-噁二唑杂合体6和2-喹诺酮-1,3,4-噻二唑杂合体7对黑曲霉和白色念珠菌的MIC为12.5~200 μg/mL,且杂合体6的活性优于相应的7。SAR显示,供电子的甲氧基对活性有利,而吸电子的氟和三氟甲基对活性不利。含有苄基的杂合体6f(MIC: 25和25 μg/mL)和7f(MIC:25和50 μg/mL)活性最高,但低于氟康唑(MIC:6.25和12.5 μg/mL)。
2-喹诺酮衍生物8 (2 mg/mL时的抑菌圈为5~16 mm)和9 (2 mg/mL时的抑菌圈为6~15 mm)的抗黑曲霉和白色念珠菌活性弱于氟康唑(0.5 mg/mL时的抑菌圈为23和26 mm),但某些化合物的抗炎活性优于双氯芬酸钠。4-羟基-1H-2-喹诺酮10在浓度为50、100和150 μg/mL时对黑曲霉未显示出任何活性,进一步研究发现向C-3、C-5、C-6和C-7 位引入羟基、硝基、氨基、羧基和羧酸乙酯(11)并不能提高对白色念珠菌、热带假丝酵母、克鲁斯假丝酵母、光滑假丝酵母、白吉利毛孢子菌、烟曲霉、伞状毛霉菌和须癣毛癣菌活性。向2-喹诺酮的C-3位引入查耳酮所得的杂合体12a-c(100 mg/mL时的抑菌圈为7~14 mm)对白色念珠菌、黄曲霉和黑曲霉的具有微弱的活性,弱于克霉唑(1 mg/mL时的抑菌圈为16~18 mm)。
3 4-喹诺酮衍生物
3.1 氟喹诺酮衍生物
以氟喹诺酮为代表的4-喹诺酮在临床上广泛用于各种细菌感染的治疗,是仅次于头孢菌素的第二大类抗感染化疗药物。除抗菌活性外,氟喹诺酮还具有诸如抗真菌等多种生物活性。氟喹诺酮的结构特征有C-3位的羧基、C-4位的羰基、C-6位的氟和C-7位的碱性氮杂环。
Al-Hiari等评价了7个氟喹诺酮衍生物的抗菌和抗真菌活性,发现化合物13a(见图3)和13b (MIC:1.56和0.78 μg/mL)对白色念珠菌的活性优于对照药环丙沙星(MIC: 3.13 μg/mL)。氟喹诺酮酯14和15对枯草杆菌和金黄色葡萄球菌的活性较弱,对烟曲霉和白色念珠菌几乎无活性,提示C-3位的羧基对活性有显著影响。对氟喹诺酮-噻二唑杂合体16而言,无论是酯16a还是羧酸16b,c均对酿酒酵母、热带假丝酵母和黑曲霉无活性,用取代苯基代替N-1位的烷基也不能改善活性。

图3 氟喹诺酮衍生物13~29的化学结构
氟喹诺酮-噻唑烷酮杂合体17~19对黑曲霉、棒曲霉菌和白色念珠菌仅显示出较弱的活性,MIC为100~>1000 μg/mL。所有杂合体的抗真菌活性均在同一水平,提示向氟喹诺酮的C-7位引入碱性氮杂环并不能提高抗真菌活性。代表物17c (MIC: 100 μg/mL)抗白色念珠菌活性与制霉菌素(MIC: 100 μg/mL)相当,是灰黄霉素(MIC: 500 μg/mL)的5倍,但对黑曲霉和棒曲霉菌的活性弱于2个对照药。
氟喹诺酮-1,2,3-三氮唑杂合体20对白色念珠菌、褶皱假丝酵母、酿酒酵母、黄曲霉和黑曲霉显示出弱到中等强度的活性,弱于对照药两性霉素B。除杂合体21b外的克林沙星-1,2,4-三氮唑杂合体21具有优秀的广谱抗菌和抗真菌活性, MIC为0.25~2 μg/mL,活性与对照药氯霉素、克林沙星和氟康唑相当或更优。SAR表明,向苯环引入第二个卤素对抗真菌活性有利。代表物22e,g不仅对药敏型和耐药型革兰阳性菌和阴性菌的活性极高(MIC: 0.25~1 μg/mL),对白色念珠菌和假丝酵母也具有良好的活性(MIC: 0.5 μg/mL)。二者的抗菌和抗真菌活性不亚于克林沙星和氟康唑,可作为先导物进一步优化。
8-甲氧基环丙沙星衍生物22在浓度为150 μg/mL时对白色念珠菌的抑菌圈为6~9 mm,普遍弱于母药8-甲氧基环丙沙星(150 μg/mL时的抑菌圈为9 mm)。SAR显示,向R位引入氨基比醚对活性更有利,但环胺和链状胺对活性贡献相当。
诺氟沙星-/环丙沙星-萘啶酸杂合体23a(MIC: 250和500 μg/mL)和23c(MIC: 125和250 μg/mL)对白色念珠菌和酿酒酵母的活性较弱,远逊于氟康唑(MIC:<8.0 μg/mL)。SAR显示,氟喹诺酮和萘啶酸之间的连接子对活性有显著影响,且以1,2,4-三氮唑-5(4H)-硫酮为连接子的杂合体23b,d对白色念珠菌和酿酒酵母未显示出任何活性。司帕沙星杂合体24a-c不仅对多种革兰阳性菌和阴性菌的活性与司帕沙星相当,对茄皮腐镰孢、红色毛癣菌、寄生曲霉和白色念珠菌等大多数所测真菌的活性优于司帕沙星、加替沙星和吉米沙星。诺氟沙星-/环丙沙星-苯并咪唑杂合体25即使在浓度为50 μg/mL时对黑曲霉、黑根霉和白色念珠菌也未显示出任何活性,无进一步研究价值。
包括氟喹诺酮在内的4-喹诺酮衍生物26~28对白色念珠菌、黄曲霉和假丝酵母具有优秀的活性,其中化合物26a-h(MIC: 0.5~16 μg/mL)对黄曲霉的活性优于氟康唑(MIC: 256 μg/mL)。值得一提的是,化合物26e-g (MIC: 0.5 μg/mL)对黄曲霉的活性是氟康唑512倍。不仅如此,化合物26a-h对白色念珠菌和假丝酵母的活性也优于氟康唑。进一步研究发现,用1,2,4-三氮唑代替环氧丙烷所得的杂合体27和28不能显著提高抗真菌活性。
氟喹诺酮衍生物29对黑曲霉、烟曲霉、黄曲霉和白色念珠菌具有良好的活性,MIC为6.25~25 μg/mL,其中的某些化合物活性与咪康唑(MIC:6.25~12.5 μg/mL)相当,提示C-3位的羧基可能不是高抗真菌活性所必需,这与抗菌活性大相径庭。
3.2 氟喹诺酮金属螯合物
研究表明,氟喹诺酮与金属螯合是此类药物发挥抗菌活性的关键步骤。因此,向氟喹诺酮引入金属离子可能会提高其生物活性。加替沙星-Mg2+,Fe2+, Mn2+, Cu2+, Zn2+, Ca2+, Cr3+, Co2+, Cd2+和Ni2+螯合物30(见图4)尽管对酿酒酵母无活性,但大多数螯合物对红色毛癣菌、白色念珠菌和茄皮腐镰孢的活性与加替沙星、司帕沙星和吉米沙星相当或更优。其中,加替沙星-Fe2+和-Cd2+螯合物对所测对红色毛癣菌、白色念珠菌和茄皮腐镰孢的活性高于加替沙星、司帕沙星和吉米沙星,而加替沙星-/司帕沙星-Y3+, Zr4+和U6+螯合物对所测真菌基本上无活性。
司帕沙星-Fe2+螯合物31a (5 μg/mL时的抑菌圈为8, 11和14 mm)和司帕沙星-Cd2+螯合物31b (10μg/mL时的抑菌圈为12, 12和10 mm)对寄生曲霉和酿酒酵母等具有潜在的活性,而司帕沙星、加替沙星、吉米沙星和莫西沙星则未显示出任何活性。
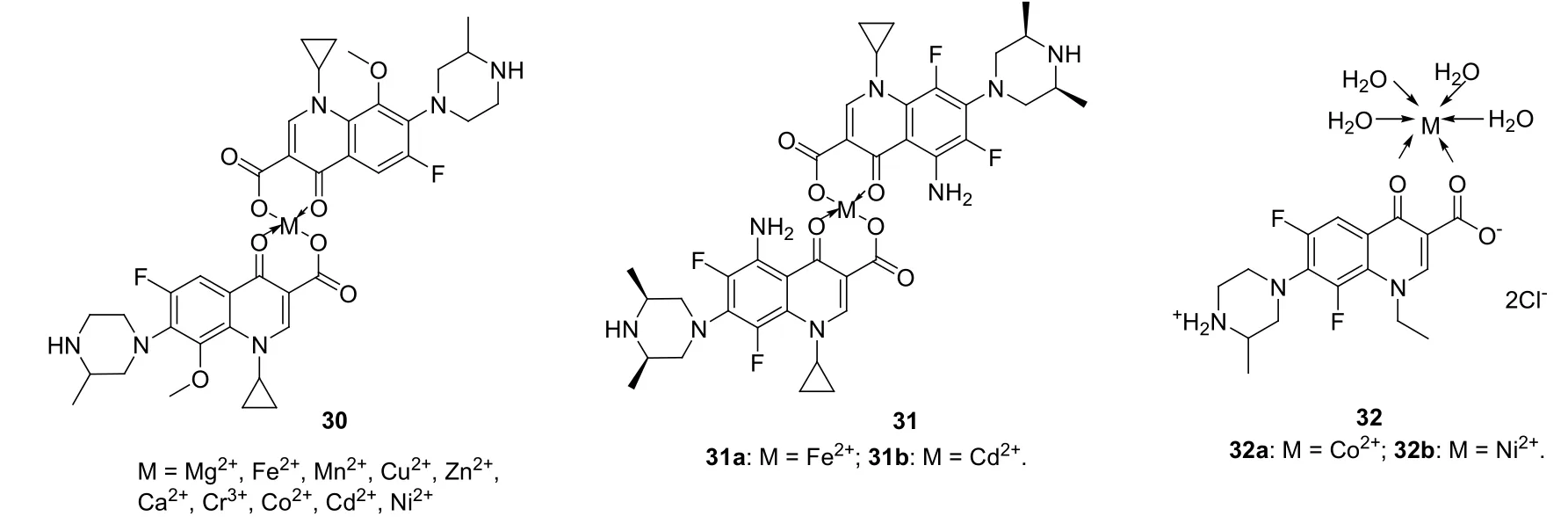
图4 氟喹诺酮金属螯合物30~32的化学结构
洛美沙星-Cr3+, Mn2+, Fe3+, Co2+, Ni2+, Cu2+, Zn2+,Th4+和UO26+螯合物32对白色念珠菌也具有潜在的活性,抑菌圈为11~21 mm/mg,且绝大多数金属螯合物的活性优于母药洛美沙星(抑菌圈: 11 mm/mg)。其中,代表物32a,b (抑菌圈: 20和21 mm/mg)抗白色念珠菌活性高于两性霉素B (抑菌圈: 19 mm/mg),但所有螯合物对黄曲霉均未显示出任何活性。
左氧氟沙星-/莫西沙星-Cu2+/Ni2+/Co2+螯合物(100μg/mL时的抑菌圈为6.4~29.2 mm)的抗稻黑孢菌、黄曲霉和白色念珠菌活性优于母药左氧氟沙星和莫西沙星(100μg/mL时的抑菌圈为4.5~6.8和10.2~12.2 mm),且左氧氟沙星金属螯合物的活性优于相应的莫西沙星金属螯合物。诺氟沙星-Ag+/Cu2+/Au3+螯合物的抗Penicillium verrcosum活性高于母药,但三者对黄曲霉和茄皮腐镰孢无活性。
3.3 其它4-喹诺酮衍生物

图5 4-喹诺酮衍生物33~36的化学结构
大多数4-喹诺酮衍生物33(见图5)对白色念珠菌和热带念珠菌具有潜在的活性, MIC为1.56~62.5 μg/mL。SAR显示,向苯环上引入卤素氟和氯可改善抗真菌活性,但甲氧基对活性无显著影响。代表物33h(MIC: 3.12 μg/mL)对热带念珠菌的活性与氟康唑(MIC: 3.9 μg/mL)相当,而化合物33i(MIC: 1.56 μg/mL)对白色念珠菌的活性优于氟康唑(MIC: 1.9 μg/mL)。
除化合物34f外的4-喹诺酮衍生物34对烟曲霉和白色念珠菌具有潜在的活性,MIC为3.9~62.5 μg/mL。SAR显示,氯在喹诺酮的C-7位比C-6位位置异构体对活性更有利。在苯环上(R2位)含有两个取代基的衍生物活性普遍高于单取代基衍生物,代表物34b对烟曲霉和白色念珠菌的MIC为3.9 μg/mL,略弱于两性霉素B(MIC: 1.95和0.98 μg/mL)。
4-喹诺酮-腙杂合体35和4-喹诺酮-氮杂环丁烷杂合体36对白色念珠菌、黄曲霉和棒曲霉菌具有潜在的活性,但普遍弱于制霉菌素(MIC: 100 μg/mL)。其中,化合物35b和36h (MIC: 100 μg/mL)对白色念珠菌生物活性与制霉菌素(MIC: 100 μg/mL)相当,而是灰黄霉素(MIC: 500 μg/mL)的5倍,可作为先导物进一步优化。
某些含有4-喹诺酮结构片段的天然产物及其衍生物也具有一定的抗真菌活性,但普遍远逊于对照药。尽管如此,此类研究丰富了喹诺酮抗真菌的SAR,为进一步合理设计打下基础。
4 结束语
约50种真菌对人类致病,每年3亿人罹患侵袭性真菌感染,其中的135万患者因此丧命。目前,临床上使用的抗真菌药物屈指可数,且真菌对这些药物的耐药性日益严峻。因此,有必要开发新型抗真菌药物。
喹诺酮具有广谱抗菌活性,广泛应用于临床。某些喹诺酮如曲伐沙星与抗真菌药物如氟康唑和两性霉素B联合给药时对真菌感染具有协同作用。因此,有必要对喹诺酮类化合物的抗真菌活性进行研究。近年来,药物化学家筛选了多个系列喹诺酮衍生物的抗真菌活性,发现某些化合物对真菌具有良好的活性。本文综述了该领域的最新研究进展,并归纳这类化合物的构-效关系以指导药物化学家更合理的设计此类化合物。

