二氟甲基化反应研究进展
李中原,曾慧意,黄金文,吴晶晶,吴范宏
(上海应用技术大学 药物创新研究所,上海 201418)
有机氟化合物在新药研发、农业、材料科学等领域方面一直发挥着不可或缺的作用。目前,市场上含氟农用化学品占比35%,含氟药物约为20%~30%。药物分子中引入的氟原子或含氟官能团有助于调节分子的膜渗透性、代谢稳定性及改善生物利用度,具有强吸电子性和亲脂性,还能成为药物分子中的氢键供体,影响药物分子在人体内的生理作用。氟原子的引入不仅是单氟、二氟、三氟原子的引入,更包括了含氟甲基、含氟片段(砌块)的引入;值得注意的是,二氟甲基(CF2H)在药物设计中不仅可以作为替代酰胺、醇、硫醇和异羟肟酸的亲脂的电子等排体,还可作为氢键供体,二氟甲基化反应也受到越来越多研究者的关注。然而引入二氟甲基的方法还相对较少,也缺少稳定、易得的二氟甲基化试剂,因此,二氟甲基化试剂的开发以及将二氟甲基高效引入分子中的方法是目前有机氟化学及药物合成领域的研究热点。
吕剑课题组[1]此前就不同化合物的二氟甲基化反应类型进行综述,本文将以近年来二氟甲基化反应中所涉及的二氟甲基化试剂进行归纳总结,并对吕剑课题组综述未涉及内容进行补充。
通常来看,目前各种进行二氟甲基化反应的试剂按照其反应机理可分为亲核二氟甲基化试剂、亲电二氟甲基化试剂以及二氟甲基自由基供体等。按照二氟甲基化试剂的不同结构,本文将分以下几个部分进行讨论。第一部分为含氟甲烷类(XCF2H,X=F、Br、Cl、I),简明介绍了该类试剂在设计和合成中的应用;第二部分为TMS类,由于该类试剂应用较为广泛,该部分较为详细介绍了TMS类试剂对不同杂化碳原子、巯基、杂环、醛、酮、羧酸等结构的二氟甲基化反应;第三部分为含氟羧酸及羧酸衍生物类,较为详细介绍了芳基、O、N原子的二氟甲基化反应;第四部分为含氟磷酸酯类,简要介绍了N、O原子的二氟甲基化反应;第五部分为含氟砜类,介绍了烯烃、杂芳环、O原子的二氟甲基化及扩环反应;第六部分为二氟甲基金属试剂,主要介绍了酰氯、烯丙位、芳杂环的二氟甲基化反应;第七部分为其他类型试剂,介绍了相应的反应实例。具体的试剂分类及反应类型如表1所示。

表1 试剂分类及反应一览表Tab.1 Reagent classification and reaction list
1 含氟甲烷类试剂XCF2H(X=F,Br,Cl,I)
1.1 CHF3对α-氨基酸的二氟甲基化反应
CHF3是特氟龙制造中产生的副产品,具有温室效应,将其作为一种二氟甲基试剂开发,是三氟甲烷废气资源转化利用的方向之一。CHF3具有很小的电流合成值,也是最有潜力的二氟甲基化反应试剂之一。由于CHF3的低反应性,到目前为止报道的应用非常少。2017年,Schmitt等[2]报道了使用CHF3作为二氟甲基化试剂对sp3碳的二氟甲基化反应(见图1)。

图1 二氟甲基氨基酸的合成设计[2]Fig.1 Synthesis of difluoromethyl amino acids[2]
反应工艺使用CHF3在气液连续流动的操作中对底物进行二氟甲基化反应。重要的是,该图适用于受保护的α-氨基酸直接Cα-二氟甲基化反应。此氨基酸化合物是磷酸吡哆醛依赖性脱羧酶的高选择性抑制剂。原料α-氨基酸甲酯易于获得,在简单水解和沉淀后以优异的纯度和产率获得最终产物。
1.2 BrCF2H对芳烃的二氟甲基化反应
除了CHF3之外,还可使用其他卤代二氟甲烷作为氟化试剂进行二氟甲基化反应。2017年,张新刚课题组[3]报道了金属镍催化的芳烃与BrCF2H二氟甲基化反应(见图2),收率92%,是芳基硼酸与BrCF2H的镍催化交叉偶联的一个重要例子。尽管BrCF2H在碱性条件下易产生二氟卡宾,但目前的镍催化方法可避免二氟卡宾的发生,并使反应通过二氟甲基自由基机制进行,从而补充了BrCF2H在有机合成中的应用案例。除使用BrCF2H之外,2018年张新刚课题组[4]还通过镍催化,使用ClCF2H与芳基氯化物的交叉偶联也可获得芳烃二氟甲基化反应的产物(见图3)。该反应在温和的反应条件下进行,效率高,并且反应易于操作,没有芳基金属中间体的形成步骤,同时还有较为广泛的底物范围,包括各种杂芳族化合物和上市药物。

图2 Ni催化芳基硼酸与BrCF2H的二氟甲基化反应[3]Fig.2 Ni-catalyzed difluoromethylation of arylboronic acids with BrCF2H[3]

图3 镍催化还原交叉偶联ClCF2H与芳基氯化物的反应[4]Fig.3 Reaction of the nickel-catalyzed reductive cross-coupling of ClCF2H with aryl chlorides[4]
1.2.1 ClCF2H的杂环N-二氟甲基化反应
除了在碳原子上引入二氟甲基,ClCF2H可在杂环氮原子上引入二氟甲基。2018年,Petko等[5]报道了母体唑类的N-二氟甲基化方法,即1,2,3-三唑,1,2,4-三唑和四唑的二氟甲基化反应(见图4),其中就包括使用氯二氟甲烷对吡咯和1,2,3-三唑的二氟甲基化反应。
1.2.2 ICF2H对芳烃的二氟甲基化反应
相比前文所述含氟甲烷试剂,二氟碘甲烷(ICF2H)具有毒性小、蒸汽压低、活性高的特点,且对臭氧层无害,可作为氟溴甲烷的替代品并应用于医药合成及新材料等领域的研发。
2019年,Hori等[6]在水/甲苯体系中使用了 Pd(PPh3)2/DPEphos 作为催化剂催化芳基硼酸与二氟碘甲烷进行交叉偶联二氟甲基化反应,获得中等至高收率的二氟甲基化产物(见图5)。

图4 母体唑类的二氟甲基化反应[5]Fig.4 Difluoromethylation of parent azoles[5]

图5 钯催化芳基硼酸的 Suzuki-Miyaura 交叉偶联二氟甲基化反应[6]Fig.5 Pd-catalyzed Suzuki-Miyaura cross-coupling difluoromethylation of aryl boronic acids[6]
这是一种Suzuki-Miyaura型交叉偶联二氟甲基化反应,Pd(PPh3)4作为预处理催化剂,DPEphos作为双齿配体,用于加速配体交换和还原消除。
2 TMS类试剂
在有机物的二氟甲基化反应中,二氟甲基硅试剂的应用备受关注,特别是具有TMS离去基团的Ruppert-Prakash试剂(TMSCF3)、TMSCF2H、TMSCF2Br、TMSCF2Cl等,因其具有稳定、易操作、易活化和反应条件温和的特点,应用较为广泛。
2.1 Ruppert-Prakash试剂(TMSCF3)的二氟甲基化反应
Ruppert-Prakash试剂(TMSCF3)是传统的三氟甲基化试剂,在有机物的三氟甲基化实验中广泛应用,但在相应的Lewis碱存在下,Ruppert-Prakash试剂可用于二氟甲基化反应,制备相应的α-二氟甲基化产物。最近就有越来越多的研究将其用于二氟甲基化反应。
2.1.1 TMSCF3对sp3碳进行二氟甲基化反应
2015年,Aikawa等[7]利用Ruppert-Prakash试剂(TMSCF3)对各种腈化合物的sp3碳进行二氟甲基化反应(见图6),获得相应的α-硅二氟甲基化腈产物。使用n-BuLi、TMSCF3和腈衍生物作为反应物,反应仅在几分钟内完成,获得相应的二氟甲基化产物。

图6 用Ruppert-Prakash试剂进行α-二氟甲基化反应[7]Fig.6 α-siladifluoromethylation with Ruppert-Prakash reagent[7]
n-BuLi和TMSCF3共同形成一种理想的氟甲基化试剂,其特点是反应迅速,操作简单,无需过渡金属和其他添加剂。
2.1.2 TMSCF3对sp2碳进行二氟甲基化反应
2015年,胡金波课题组[8]报道TMSCF3试剂与碘化钠一起合用(或TMSCF2Br与催化量四丁基溴化铵组合)可原位产生二氟卡宾,与重氮化合物直接亲核加成,然后消除N2,可以获得相应的偕二氟乙烯产物,并伴有少量四氟环丙烷产物生成(见图7)。与Cu催化的TMSCF3与重氮化合物反应制备偕二氟烯烃方法相比,该方案具有更好的底物适用性。
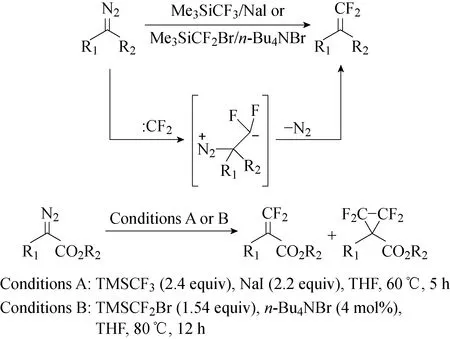
图7 α-重氮乙酸盐的偕-二氟烯化反应[8]Fig.7 Gem-difluoroolefination of α-diazoacetates[8]
2.1.3 TMSCF3进行S-二氟甲基化反应
Prakash等[9]报道了在LiH或Li2CO3作用下,Rupert-Prakash试剂可与硫酚和硫醇进行直接S-二氟甲基化反应,再用无机氟离子处理脱除TMS,制得相应的二氟甲基硫醚。该反应时间较短,条件温和,并且在 —OH,—NH2和 —CO2H官能团存在下可选择性进行S-二氟甲基化反应(见图8)。

图8 芳基的直接S-二氟甲基化[9]Fig.8 Direct S-difluoromethylation of aryl and aliphatic thiols[9]
当LiH对底物有害时,可改用Li2CO3这类温和碱预形成硫醇锂来进行反应。鉴于硫醇盐具有独特的酸性和亲核性,选择性S-二氟甲基化反应便可耐受具有各种官能团的硫醇。2018年,该课题组[10]继续报道了在三苯基膦,碘化锂和四氟硼酸锂存在下,Ruppert-Prakash试剂可与芳香醛发生选择性反应制备偕二氟化鏻盐再经过简单碱性水解可产生二氟甲基化产物(见图9)。该反应体系使用高度离子化的LiBF4盐有助于形成TMS基团保护的鏻盐产物,极性非质子溶剂DMPU用于调节TMSCF3和碘化物的反应性,并且需要相对较低的反应温度。

图9 醛和酮的亲核二氟甲基化方法和芳香醛的最佳条件和底物反应[10]Fig.9 Approaches for nucleophilic difluoromethylation of aldehydes and ketones and optimized conditions and substrate reaction of aromatic aldehydes[10]
2.2 TMSCF2H参与的二氟甲基化反应
Ruppert-Prakash试剂在工业上的应用成本过高,研究发现与Ruppert-Prakash试剂相似的TMSCF2H同样具有良好的二氟甲基化反应性。
2.2.1 TMSCF2H对末端炔烃进行二氟甲基化反应
对末端炔烃进行二氟甲基化反应是制备炔烃二氟化物的重要途径。2015年,卿凤翎课题组[11]使用9,10-菲醌作为氧化剂,铜作为催化剂,使用TMSCF2H对末端炔烃进行氧化二氟甲基化反应(见图10)。反应产物产率可达72%,同时有较好的底物扩展性。虽然之前Burton和Hartgraves报道了1-碘炔与热不稳定试剂CuCF2H的交叉偶联反应制备二甲基氟化炔,但缺点是需要预官能化的末端炔烃;另外,Kitazume和Hu也报道通过产生乙炔化锂中间体与二氟卡宾前体的二氟甲基化反应,然而,仍存在一些敏感官能团与这些系统中使用的炔基-Li和/或二氟卡宾不相容的问题。此方案避免了使用预官能化的炔烃或产生炔基-Li中间体,而使反应更高效和经济。

图10 铜介导的末端炔烃的氧化二氟甲基化反应[11]Fig.10 Copper-mediated oxidative difluoromethylation of terminal alkynes[11]
2.2.2 TMSCF2H对菲啶进行二氟甲基化反应[12]
目前,很少有报道制备二氟甲基化菲啶的方法,二氟甲基化菲啶的合成方法多是基于 CF2H 自由基源光氧化还原催化二氟甲基化/环化反应。2017年,卿凤翎课题组[12]使用TMSCF2H在银催化剂下由高价碘试剂氧化C-H发生二氟甲基化反应制备二氟甲基化菲啶(见图11),完成了菲啶的C-H官能化二氟甲基化反应,得到相应的6-(二氟甲基)菲啶,产率中等至良好(见图12)。该课题组初步机理研究表明,该二氟甲基化反应通过银介导的亲核加成和氧化芳构化进行。这项工作是通过菲啶的C-H官能化合成氟化菲啶的首例报道。

图11 二氟甲基化菲啶的合成方法[12]Fig.11 Synthetic methods of difluoromethylated phenanthridines[12]

图12 银介导的菲啶二氟甲基化反应[12]Fig.12 Reaction of silver-mediated difluoromethylation of phenanthridines[12]
2.2.3 TMSCF2H对醛、酮进行二氟甲基化反应
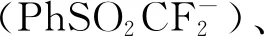
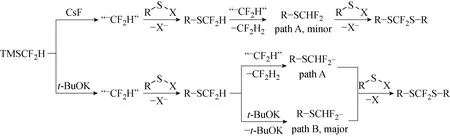
图14 由RSX(X = SR,Cl,SO2Ph)和TMSCF2H制备二氟甲基硫醚和二氟双(芳硫基)甲烷可能的机理[14]Fig.14 A proposed mechanism for the production of difluoromethylthioethers and difluorobis(arylthio)methanes from RSX (X=SR,Cl,SO2Ph)and TMSCF2H[14]
TMSCF3可以将酮直接一锅转化为三氟甲醇,与TMSCF3一样,TMSCF2H以高产率对醛和不可烯醇化的酮进行二氟甲基化反应,但是对可烯醇化的酮的亲核加成通常伴随副反应,导致低产率和污染的产物。尽管TMSCF2H和PhMe2-SiCF2H以良好的收率将醛转化为二氟甲基醇(在100 ℃下在DMF中存在KF),但它们与酮的反应以低产率进行(20%~25%)。近年来,其他作者使用TMSCF2H在环境温度或低温下以DMF或THF为溶剂使用不同碱获得了类似的结果。显然,需要一种更为有效的通用方法来使TMSCF2H对可烯醇化酮进行二氟甲基化反应。2016年,Michurin等[13]公开了一种可将烯醇化酮直接二氟甲基化的方法,二氟甲基化试剂TMSCF2H能够在HMPA的存在下,由醛和酮在温和的条件下制备二氟甲基醇(见图13)。报道指出,DMPU可用作HMPA的无毒替代物,但在这种情况下产率略低。该方法适用于环状、非环状酮及芳基酮并且耐受各种官能团,实现了更有效、更温和的醛、酮(包括可烯醇化的酮)二氟甲基化方法。
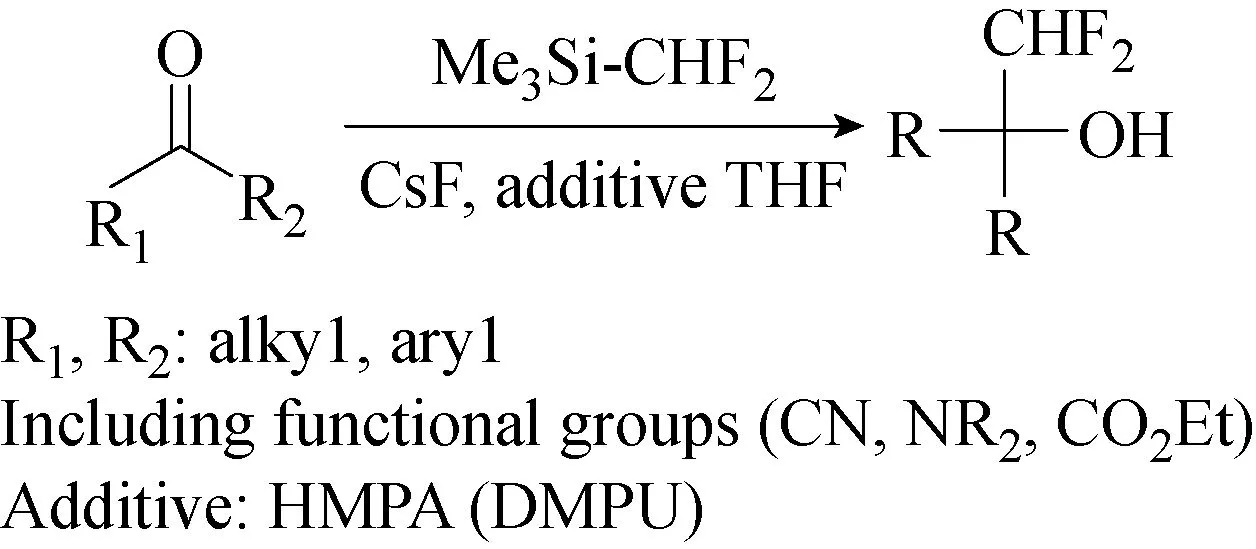
图13 醛和酮与二氟甲基化试剂Me3SiCF2H在HMPA存在下合成二氟甲基醇[13]Fig.13 Synthesis of difluoromethyl alcohol from aldehydes and ketones with difluoromethylation reagent Me3SiCF2H in the presence of HMPA[13]
2.2.4 TMSCF2H进行S-二氟甲基化反应
二氟甲基硫醚(-SCF2H)的传统合成方法涉及硫醇盐对原位产生的二氟甲基卡宾中间体的亲核进攻。这包括一些二氟甲基卡宾试剂的使用,如HCF2Cl、FSO2CF2CO2M、BrCF2P(O)(OEt)2、XCF2CO2Na,TMSCF2Y等。使用TMSCF2H进行铜介导的有机硫氰酸酯的亲核二氟甲基化反应,以及类似的二氟甲基化与Al-硫氰酸根合琥珀酰亚胺(NTS)在AlCl3催化下芳烃的C-H硫氰化反应和N-二氟甲基硫代邻苯二甲酰亚胺用于温和条件下对各种亲核底物的直接二氟甲基硫醇化反应都具有一些缺点,例如环境友好性低或价格昂贵等,这也抑制了这些方法在大规模生产中的使用。为了解决环境友好、经济高效的问题,2016年,Ha等[14]在无过渡金属的条件下由RSX(X=SR,Cl,SO2Ph)和TMSCF2H直接制备二氟甲基硫醚(见图14)。在CsF存在下RSX和TMSCF2H反应获得二氟甲基硫醚,而在t-BuOK存在下用TMSCF2H处理RSX以良好的收率得到二氟双(芳硫基)甲烷。RSX、TMSCF2H和碱的物质的量的比例显著影响反应历程。这与早起文献报道的在相似反应条件下使用TMSCF3的观察不同。该反应与各种官能团相容,例如卤素,硝基,氰基,酰胺,甲氧基和杂芳基。这一研究不仅为制备二氟甲基硫醇醚和二氟甲基(芳基硫代)烷提供了有效的途径,而且对 TMSCF2H 的反应活性也有了深入的了解,对进一步开发亲核的直接二氟甲基化反应有一定的参考价值。
2.2.5 TMSCF2H对芳基进行二氟甲基化反应
芳基卤化物与二氟甲基亲核试剂的反应成为目前芳基进行二氟甲基化反应的一种有效方法。2019年,Ferguson等[15]实现了钯催化的芳基Cl/Br化物与TMSCF2H的交叉偶联反应。使用BrettPhos或Pd(PttBu3)2为配体均可以良好的收率获得各种二氟甲基化的芳烃(见图15)。

图15 钯催化芳基氯化物和溴化物的二氟甲基化反应[15]Fig.15 Palladium-catalyzed difluoromethylation of ARYL chlorides and bromides[15]
该方法使用富电子单膦配体(BrettPhos和PtBu3)与TMSCF2H组合作为二氟甲基源,该研究表明,使用富电子和空间大的单齿配体如PtBu3和/或二烷基二芳基膦可以促进芳基Cl/Br化物底物的活化和进一步的二氟甲基化反应,并与带有给电子和吸电子取代基的芳基Cl/Br化物底物及几种杂环相容。这一结果将有促进TMSCF2H试剂用于其他反应的研究和开发。
2.3 TMSCF2Br参与的二氟甲基化反应
TMSCF2Br作为二氟卡宾试剂在苯酚、硫醇、烯烃等化合物的二氟甲基化研究中应用较多,TMSCF2Br作为独特且实用的二氟卡宾源,在弱碱性或酸性条件下合成伯、仲和甚至叔烷基二氟甲基醚。实际中常用溴代二氟甲基三甲基硅烷(TMSCF2Br),三苯基膦的组合在温和条件下用作二氟化磷内鎓盐Ph3P=CF2的来源,反应大多经过磷盐化合物产生二氟卡宾中间体的过程,但对于以该类化合物为前体得到碳自由基用于二氟甲基化的研究报道相对较少。
2.3.1 TMSCF2Br对酮和硝基烯烃进行二氟甲基化反应
磷酸甜菜碱可以用作二氟甲基碳阴离子的等价物,脱羧产生不稳定的磷内鎓盐,进而形成鏻盐,然而,由于内鎓盐的不稳定性及其适度的反应性,亲电子试剂的范围仅限于醛和其他特定的底物,如高亲电子偶氮甲基和带有两个吸电子基团的迈克尔受体。2016年,Trifonov等[16]报道了一种不同的生成内鎓盐的方法,同时形成能够活化亲电底物的路易斯酸性硅物质。该反应实现了在碱性条件下难以发生的亲核氟代烷基化酮和硝基烯烃的亲核二氟甲基化反应(见图16和图17)。该系统中路易斯酸性甲硅烷基物质激活底物以进行亲核攻击可能是加快反应速率的原因。
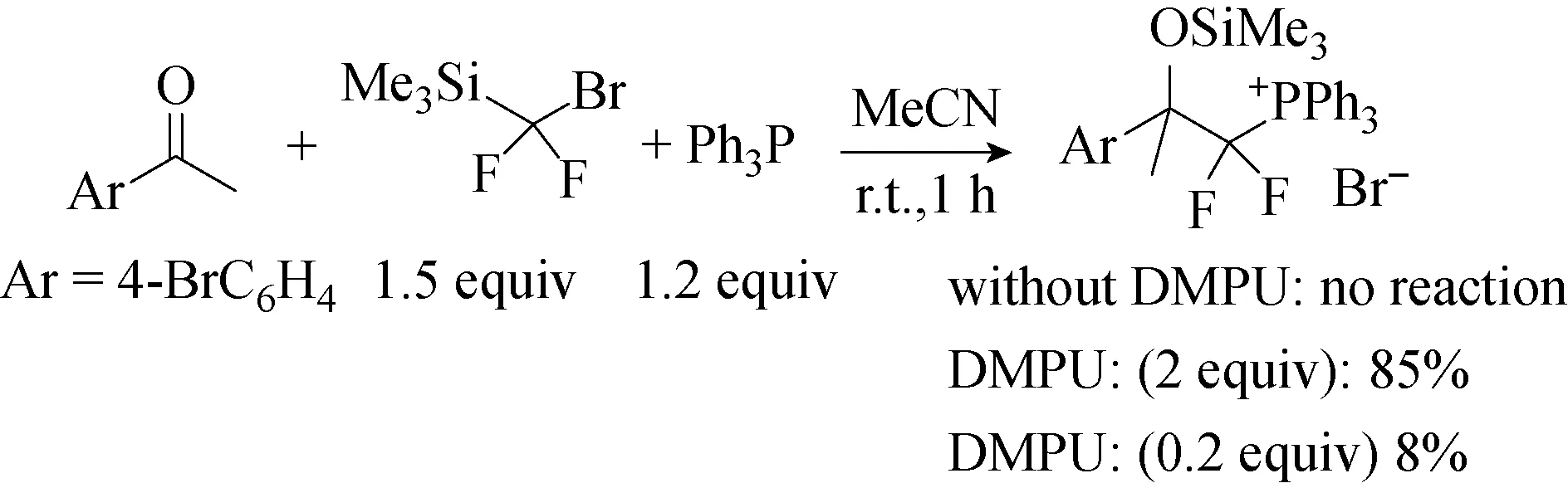
图16 4-溴苯乙酮的二氟甲基化反应[16]Fig.16 Difluoromethylation of 4-bromoacetophenone[16]
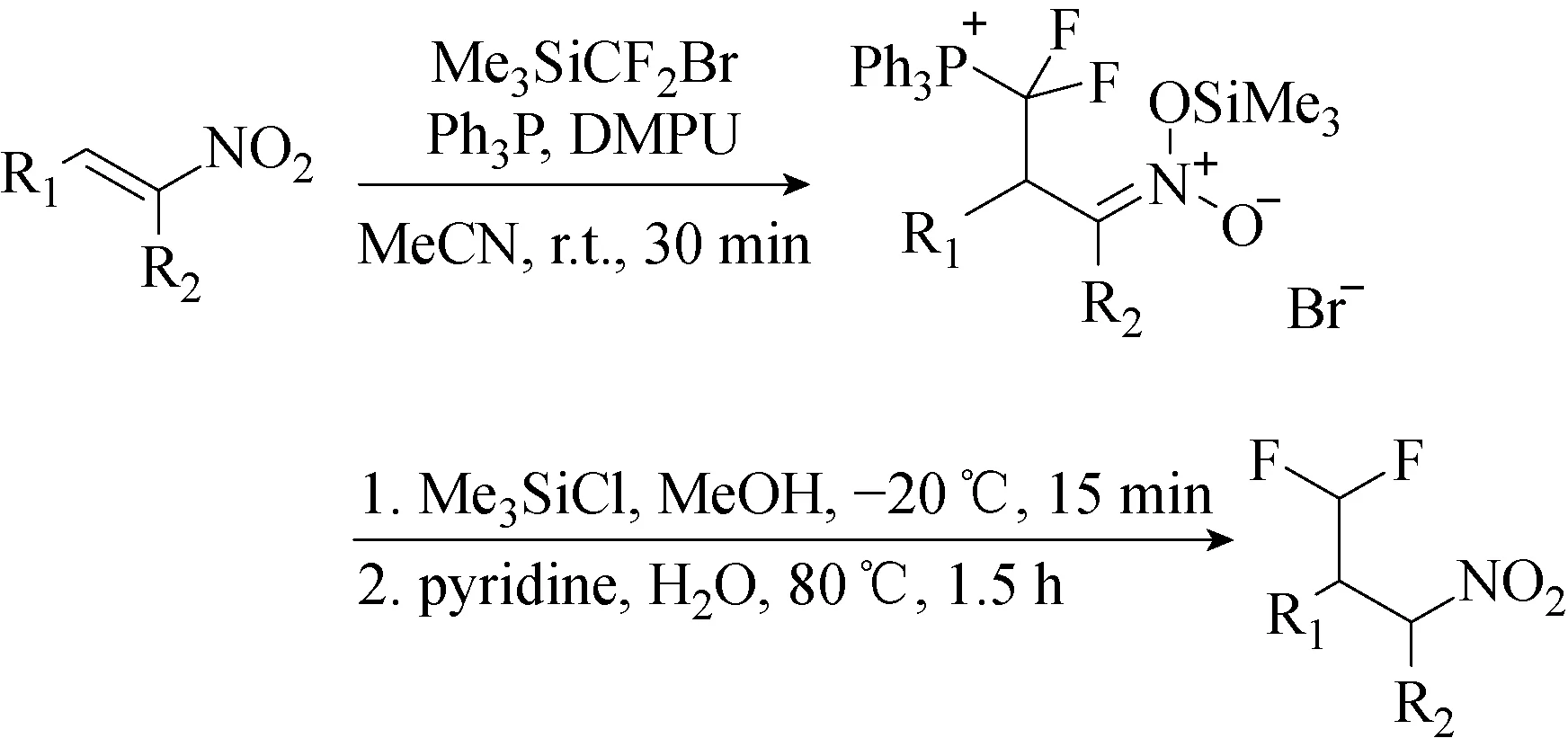
图17 硝基烯烃的二氟甲基化反应[16]Fig.17 Difluoromethylation of nitroolefins[16]
2.3.2 TMSCF2Br制备S-二氟甲基二硫代氨基甲酸酯
二硫代氨基甲酸盐是一类具有各种生物活性的药效团化合物,相关文献报道中已制备出几种类型的含氟二硫代氨基甲酸酯。但是相关文献中仅描述了对硫原子进行CF2H基团取代获得二硫代氨基甲酸酯的一个例子。为了开发二硫代氨基甲酸根阴离子与二氟卡宾合成这类化合物的有效方法,2015年,Smirnov等[17]报道了一种制备S-二氟甲基二硫代氨基甲酸酯的方法(见图18),反应采用TMSCF2Br作为二氟卡宾的有效来源,用甲醇中的二硫化碳处理仲胺,然后用二溴代氨基甲酸乙二醇酯生成的二氟卡宾对中间体二硫代氨基甲酸根阴离子进行S-二氟甲基化反应。
2.3.3 TMSCF2Br对羧酸进行二氟甲基化反应
醛类和酮类化合物是较好的亲电性化合物,可与叶立德反应制备二氟甲基取代醇。然而,二氟甲基化醇的制备方法目前仍很少见,2017年,Alexey等[18]利用羧酸获得的酰氯与Ph3P和TMSCH2Br原位产生的二氟化叶立德Ph3P=CF2相互作用进行一步二氟甲基化反应(见图19)。根据具体的反应条件,芳香族羧酸可以在一步反应中选择性地转化为双-二氟甲基化醇或二氟化酮。对于庞大的α-支链化羧酸,仅产生酮。根据反应条件,芳香族羧酸可以转化为双(二氟甲基)-取代的醇或二氟化酮。生产酸的反应在单加成步骤停止,酮为单一产物。

图18 S-二氟甲基二硫代氨基甲酸酯的合成及底物拓展[17]Fig.18 Synthesis of S-difluoromethyldithiocarbamate and substrate development[17]
2.3.4 TMSCF2Br进行S-二氟甲基化反应
迄今为止只有少量使用[Ph3P-CF2H]+Br-作为自由基前体的报道。在过去的十年中,各研究者已经报道了芳基硫醇的光引发的SRN1型反应。目前已知芳香硫醇盐阴离子是一种非常有效的SRN1亲核试剂,主要以卤代苯衍生物为偶联剂,不仅可以通过卡宾进行,也可以通过自由基中间体进行。为了对[Ph3P-CF2H]+Br-加以应用,2017年,Niklas等[19]在温和反应条件下,使用TMSCH2Br与Ph3=P在无需过渡金属的情况下对各种硫醇进行二氟甲基化反应(见图20)。循环伏安法测量表明,二氟甲基化通过SRN1型机制发生。底物范围广,可耐受各种官能团(OH、NH2、酰胺、酯)。
机理研究表明,这一过程本质上是自由基反应。显然,在官能团耐受性方面,自由基过程在卡宾路线方面具有优势。
图20表明,鏻盐可以参与SRN1型反应,并且考虑到不同的SRN1反应型,其在未来可作为自由基反应的前体。
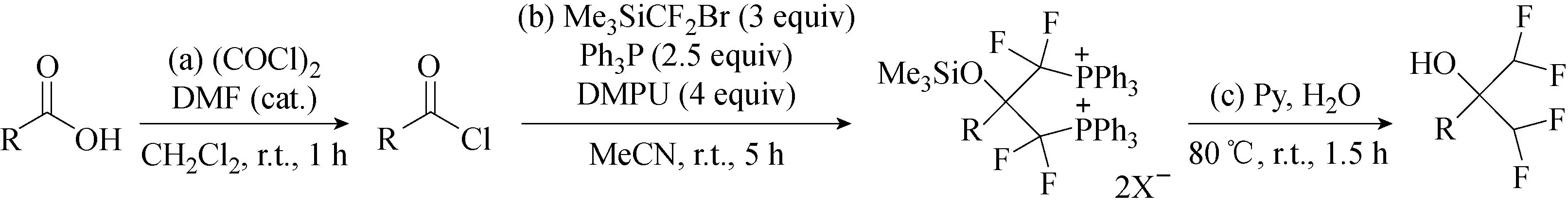
图19 二氟甲基化醇的合成[18]Fig.19 Synthesis of difluoromethylated alcohol[18]

图20 硫醇与(二氟甲基)三苯基鏻的自由基二氟甲基化反应[19]Fig.20 Radical difluoromethylation of thiols with (difluoromethyl)triphenylphosphonium bromide[19]
2.3.5 TMSCF2Br引起的二氟甲基化及扩环反应
自由基二氟甲基化反应的发展一直是氟化学深入研究的主题,已有有许多报道研究了从各种前体形成二氟甲基自由基,如双(二氟甲烷亚磺酸锌)、二氟甲基亚磺酸钠、二氟甲磺酰氯、二氟甲基鏻盐、二氟甲基砜或二氟甲基亚砜亚胺。相对于传统的化学合成途径,可见光介导的光催化氧化物催化的方法被证明是相当具有重要特征的有力合成工具,具备反应经济性,环境友好和操作简单性。2018年,Kim等[20]在对二氟甲基化反应的催化条件研究中,使用fac-Ir(ppy)3和由TMSCH2Br与Ph3=P产生的二氟甲基溴化鏻在光照条件下,可对1-(1-芳基乙烯基)环丁醇衍生物进行二氟甲基化,同时引发1,2-碳迁移的环扩展,得到二氟甲基取代的环戊酮衍生物(见图21)。
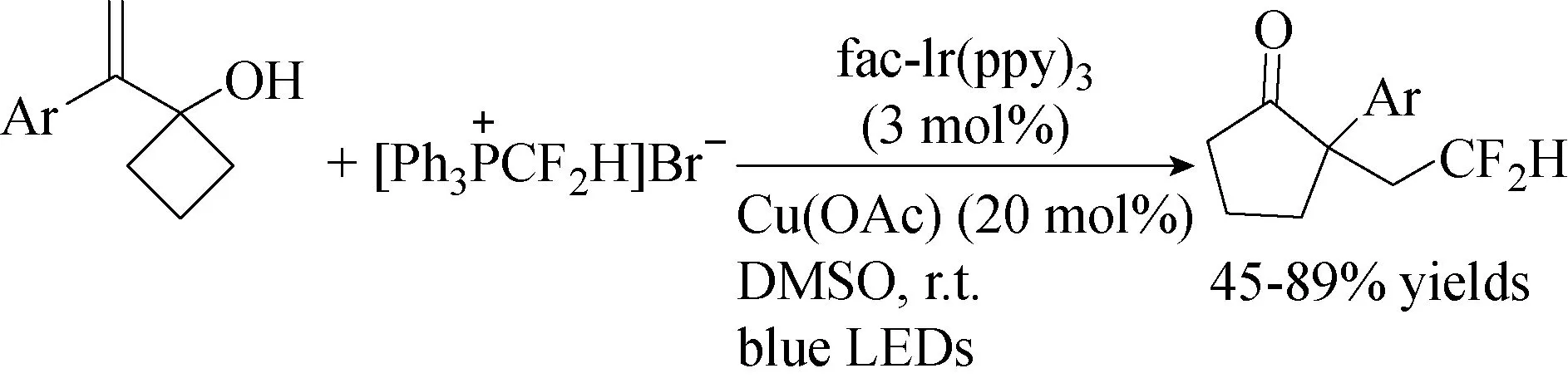
图21 1-(1-芳基乙烯基)环丁醇的二氟甲基化和环扩展反应[20]Fig.21 Difluoromethylation and ring expansion of 1-(1-arylvinyl)cyclobutanols[20]
3 含氟羧酸及羧酸衍生物类试剂
3.1 ClCF2COONa
3.1.1 ClCF2COONa进行酚O-二氟甲基化反应
ClCF2COONa作为二氟卡宾的前体可实现对部分烯烃、卤代苯类化合物的二氟甲基化或三氟甲基化。查尔酮是从植物中获得的各种生物活性化合物的重要核心结构这些分子具有众多不同的生物活性,如抗癌,抗氧化,抗炎和抗菌活性。因此,设计新的具有芳基二氟甲基醚结构的二氟甲基化2-羟基查尔酮将在药物中具有潜在的应用价值。2015年,Wang等[21]使用2-氯-2,2-二氟乙酸钠作为二氟甲基化剂对2-羟基查尔酮进行二氟甲基化,在温和的条件下,获得了多种芳基二氟甲基醚,产率为36%-80%(见图22)。所得产物2-二氟-甲氧基查尔酮,可用作迈克尔反应供体。

图22 羟基查尔酮的二氟甲基化反应[21]Fig.22 Difluoromethylation reaction of hydroxychalcone[21]
芳腈是一类重要的有机合成中间体,可转化为各类化合物,鉴于芳腈的众多用途,也有很多研究报道了制备芳腈的方法,但传统方法有原料毒性大、高温及成本较高等问题,限制了其在大规模制备中的应用。而在微波辅助下可快速、高效制备芳腈类化合物。2016年,王韬等[22]以ClCF2COONa为二氟甲基化试剂,碳酸钾为碱,实现了微波促进水杨醛肟一锅脱水成腈及二氟甲基化反应(见图23)。在300 W微波环境下,以水杨醛肟类化合物为原料,氯二氟乙酸钠为二氟甲基化试剂,碳酸钾为碱,N,N-二甲基甲酰胺为溶剂,经一锅脱水成腈及二氟甲基化反应制备了一系列2-二氟甲氧基苯腈类化合物。该反应无需额外添加催化剂即可向化合物中同时引入二氟甲基和氰基,具有反应迅速、条件温和、操作简便和实用性强的优点。
3.1.2 ClCF2COONa进行N-二氟甲基化反应[23]
苯并恶唑-2-硫酮作为核心结构存在于各种生物活性分子和药物中,并发挥着关键作用。通常,苯并恶唑-2-硫酮是由2-氨基苯酚与二硫化碳、乙基黄原酸钾、苯基氯硫代碳酸酯、或四甲基秋兰二硫化物反应合成的。但是这些方法通常具有原料毒性大,成本较高和操作繁琐的问题,由于苯并恶唑-2-硫酮在各领域均有重要的用途,因而开发一种高效经济的合成苯并恶唑-2-硫酮含氟衍生物的方法仍然是重要的。2018年,Li等[23]报道了在NaO、t-Bu存在下,2-氨基苯酚、氯二氟乙酸钠和硫的反应可得到3-二氟甲基苯并恶唑-2-硫酮的单一产物,收率良好(高达98%)。该反应的机理可能是硫代羰基氟化物首先环化2-氨基苯酚,然后用二氟卡宾进行N-二氟甲基化(见图24)。该反应整个过程可能是通过硫代羰基氟化物环化2-氨基苯酚和二氟化碳进行氟甲基化而进行的。过程简单、操作单一和原料经济,这一方法对于制备不同的3-二氟甲基苯并恶唑-2-硫酮衍生物具有一定的实用价值。

图23 二氟甲氧基苯腈类化合物的合成路线[22]Fig.23 Synthesis route of difluoromethoxybenzonitrile[22]
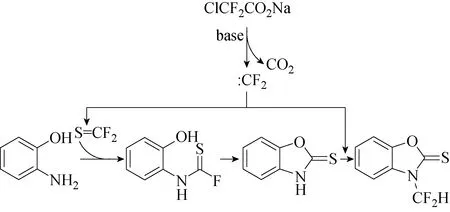
图24 一锅法合成3-二氟甲基苯并恶唑-2-硫酮[23]Fig.24 One-pot synthesis of 3-difluoromethyl benzoxazole-2-thione[23]
3.2 BrCF2COOH进行酚O-二氟甲基化反应
2017年,Yang等[24]报道在光敏剂2-苯基吡啶铱络合物[fac-Ir(ppy)3]的催化和可见光照射下,溴二氟乙酸经碳酸铯处理可产生二氟卡宾与苯酚和苯硫酚进行二氟甲基化反应(见图25),以良好的产率获得相应的O和S-二氟甲基化醚,该反应具有较好的官能团耐受性。
3.3 BrCF2CO2Et试剂
在过去几年中,已经许多有效的二氟甲基化反应被发现。值得注意的是,CF2CO2Et 基团在二氟化基团中是有独特功能的,因为该结构可以转化为许多含CF2的官能团。

图25 可见光还原氧化催化酚类的二氟甲基化反应[24]Fig.25 Visible light reduction oxidation catalyzed difluoromethylation of phenols[24]
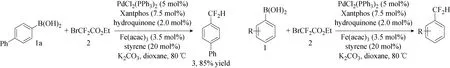
图28 Pd催化的芳基硼酸与溴代二氟乙酸盐的二氟甲基化反应[26]Fig.28 Pd-catalyzed difluoromethylation of arylboronic acids with bromodifluoroacetate[26]
3.3.1 BrCF2CO2Et对咪唑杂环的二氟甲基化反应[24]
咪唑并[1,2-a ]吡啶类化合物因其多种生物学特性而受到广泛关注,被认为是一种特殊的药物化学骨架,而且这种稠合双环5-6杂环化合物在材料科学领域也具有重要意义。存在于咪唑并[1,2-a]吡啶不同位置的取代基和官能团的性质决定了它们的药理活性。2016年,Mishra等[25]利用BrCF2CO2Et,在铜催化剂作用下对咪唑并[1,2-a]吡啶进行区域选择性的乙氧基羰基-二氟甲基化反应(见图26)。获得了一系列具有乙氧基羰基二氟甲基化咪唑并[1,2-a]吡啶衍生物。这种方法也适用于咪唑并[2,1-b]噻唑和苯并[d]咪唑并[2,1-b]噻唑(见图27)。在此之前,还没有关于咪唑并[1,2-a ]吡啶衍生物的乙氧基羰基二氟甲基化的文献研究。因此这种C-H官能化方法对于有机合成,药物化学和材料科学较为重要,它是咪唑杂环的乙氧基羰基二氟甲基化的有效且经济的途径。
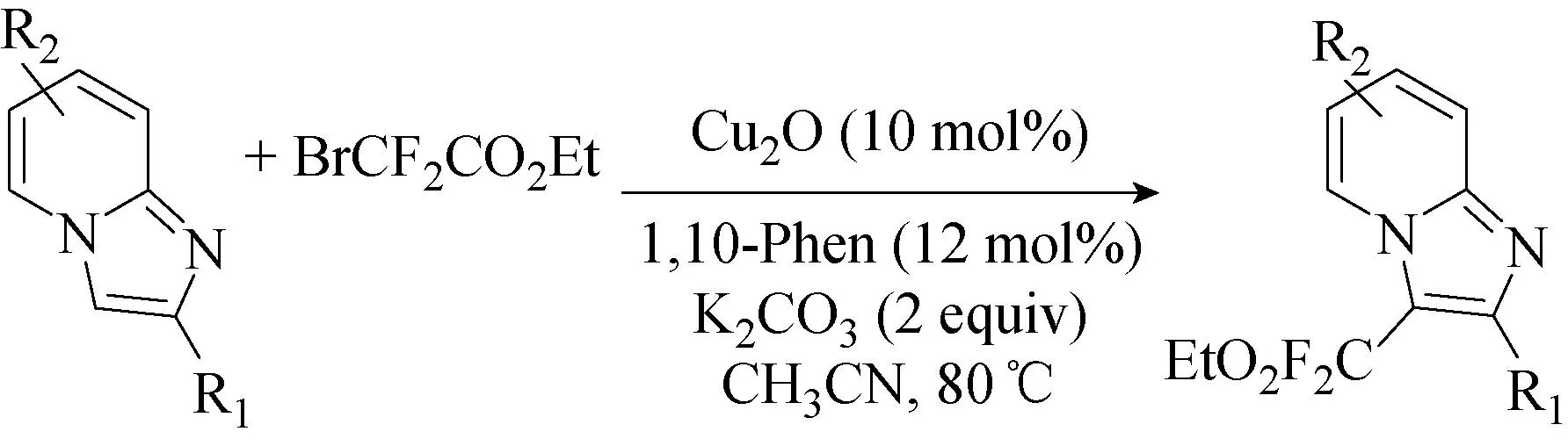
图26 咪唑并吡啶的C-H乙氧基羰基二氟甲基化反应[25]Fig.26 C-H ethoxycarbonyldifluoromethylation of imidazopyridines[25]
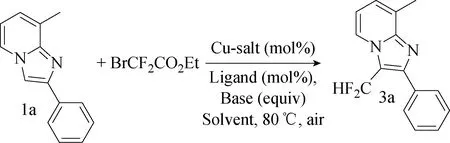
图27 咪唑并[1,2-a]吡啶的二氟甲基化反应[26]Fig.27 Difluoromethylation of imidazo[1,2-a]pyridine[26]
3.3.2 BrCF2CO2Et对芳基的二氟甲基化反应
2015年,张新刚课题组[26]报道了Pd-催化剂用于芳基硼酸与BrCF2CO2Et的二氟甲基化反应(见图28)。在温和的反应条件下,反应在氢醌和Fe(acac)3共同作用下进行。初步的机理研究表明,反应经历了二氟卡宾途径,与大多数传统方法相比,具有一定的特殊性。该反应具有高效率和优异的官能团相容性的优点,甚至对溴和羟基也是如此,也为药物发现和开发提供了新的方案。该方案是Pd催化芳基硼酸与BrCF2CO2Et进行二氟甲基化反应的第一个实例。
3.3.3 BrCF2CO2Et 进行O-二氟甲基化反应
由于其简单的反应过程,O-亲核底物与二氟卡宾的O-二氟甲基化反应被证明是制备二氟甲基醚最有效的策略之一。目前,大量的研究主要集中在用二氟卡宾进行醇和酚的O-二氟甲基化反应,分别得到二氟甲基烷基醚和芳基醚。S-(溴二氟甲基)二芳基锍盐[ArS+(CF2Br)Ar′X-]可作为二氟卡宾试剂实现O-二甲基甲基化反应,而ClCF2CO2Et对1,3-二酮的O-二氟甲基化也非常有效。尽管这些方法非常有效,但它们需要碱性反应条件。在某些情况下,甚至需要低反应温度或更强的碱性条件。2016年,Liu等[27]由BrCF2CO2Et和Ph3=P产生PH3P+CF2CO2-生成二氟卡宾,与1,3-二酮在无碱条件下发生O-二氟甲基化反应,得到二氟甲基烯醇醚(见图29)。这一方法温和有效,简单地加热1,3-二酮混合物与二氟卡宾试剂便可以获得所需的产物而避免了低温反应的能源消耗及碱的使用。

图29 (Ph3P+CF2CO2-)与1,3-二酮的O-二氟甲基化反应[27]Fig.29 O-difluoromethylation of(Ph3P+CF2CO2-)with 1,3-diketone[27]
3.3.4 BrCF2CO2Et 进行N-二氟甲基化反应
通常,亲核底物的二氟甲基化反应可由HCF2Cl、HCF3、CHF2I、PhSO2CF2X、ArCOCF2Cl、ClCF2CO2Na、FSO2CF2CO2H、BrCF2P(O)(OEt)2、TMSCF2Br、HCF2OTf、PhS(O)(NTs)CF2H、FSO2CF2CO2TMS等试剂完成。然而,臭氧、吸湿性酸盐等成本昂贵且难以获得的试剂的使用,和苛刻的反应条件限制了它们的应用。因此,非常需要在操作上简单的二氟甲基化与环境友好的试剂。2018年,Polley等[28]使用廉价易得且环境友好的BrCF2CO2Et试剂,在LiOH和CsCO3的作用下,对具有甲苯磺酰基保护基的苯胺和缺电子酚进行了二氟甲基化反应(见图30)。有趣的是,将氢氧化锂替换为4-N,N-二甲基氨基吡啶(DMAP)时,甲苯磺酰基保护的苯胺仍为原料会得到相应的N-乙基化产物(见图31)。高度亲核的苯硫酚在酯水解之前通过对溴原子的快速SN2进攻获得相应的S-乙氧基二氟甲基化产物,在DMAP存在下,可抑制酯的水解,从而使乙基部分亲核进攻获得N-乙基化产物。

图30 N-二氟甲基化反应[28]Fig.30 Reaction of N-difluoromethylation[28]
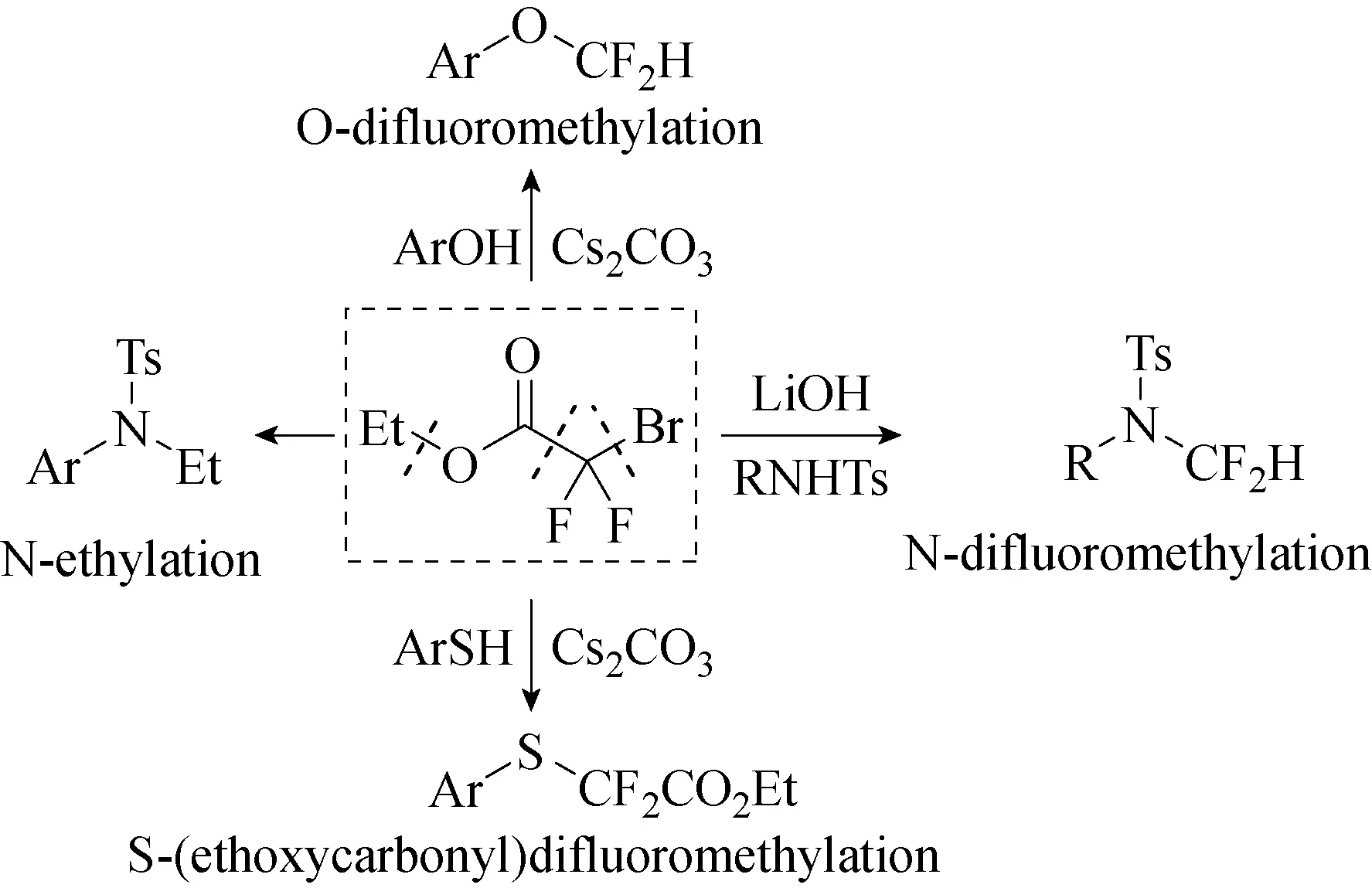
图31 溴二氟乙酸乙酯的化学反应性差异[28]Fig.31 Divergent chemical reactivity of ethylbromodifluoroacetate[28]
相反,N-乙基化由N,N-二甲基氨基吡啶促进,通过SN2进攻溴原子,产生活化的加合物,然后亲核加成到邻近羧基的乙基碳上。对于高亲核性硫醇,BrCF2CO2Et的亲核取代发生在酯水解之前。因此,对BrCF2CO2Et进行机理调控可获得不同的反应产物。2019年,Deng等[29]报道了亚硫酸盐促进的唑类N-二氟甲基化和硫化反应获得N-二氟甲基硫脲,突破了使用昂贵且不易获得的试剂三甲基甲硅烷基氟磺酰基二氟乙酸盐(TFDA)并且反应底物范围小的限制,在该反应中,廉价的BrCF2CO2Et和无毒硫元素分别用作二氟甲基化和硫化试剂(见图32)。各种唑类,包括苯并咪唑类、咪唑类和三唑类,反应表现良好,可获得中等至良好收率的各种唑类硫脲。该研究发现,HOCH2SO2Na 作为一种有效的脱卤剂,可以促进偶氮唑类化合物 N-二氟甲基化反应中二氟卡宾的形成。HOCH2SO2Na还可以作为活化硫化元素硫的单一电子转移还原剂。该方法合成了酮康唑硫脲、益康唑硫脲和氟康唑硫脲。

图32 唑类的二氟甲基化反应[29]Fig.32 Difluoromethylation of azoles[29]
4 含氟磷酸酯试剂
4.1 BrCF2PO(OEt)2进行N-二氟甲基化反应
BrCF2PO(OEt)2在用作二氟甲基化反应试剂的时候,尽管是通过自由基机制生成二氟卡宾中间体步骤,但它较多应用于N原子上的二氟甲基化反应。由于季铵盐带电部分决定了这些化合物的独特性质,与阳离子中心相连的二氟甲基对带电部分的影响引起人们的关注。对于一些重要的铵化合物,如药物、手性相转移催化剂、单体、聚合物等,通常含有其他反应性/敏感性官能团,这些官能团在反应过程中可能不稳定,为了确保这些不稳定结构不受影响,2016年,Zafrani等[30]使用BrCF2PO(OEt)2和氟化物对官能化叔胺进行二氟甲基化反应。膦酸盐与氟化物离子作用,产生二氟卡宾中间体,在质子源和叔胺存在下,产生相应的α-二氟甲基铵化合物(见图33),产率较高。尽管该二氟甲基化反应的机理涉及二氟卡宾中间体,但它几乎仅在氮原子上发生,甚至在含有羟基,炔基或链烯基的分子中也是如此。使用膦酸盐、CsF对叔胺进行二氟甲基化的方法对于合成各种二氟甲基化季铵化合物非常实用。尽管二氟卡宾中间体性质活泼(见图34),但在温和条件下使用氟化物作为触发剂能够耐受官能团,例如羟基、烯基、炔基、酯等。季铵盐与含氟基团的结合可能会引起物质理化性质的有趣变化,并且有望应用于表面活性剂、离子液体、相转移催化剂、药物和聚合物等研究领域。
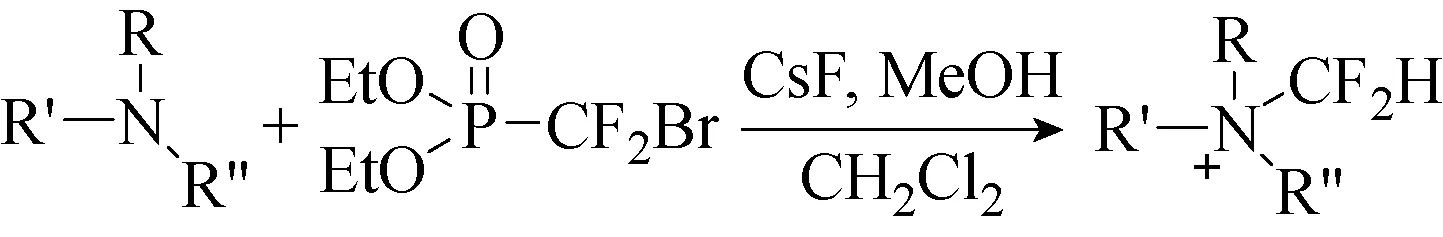
图33 合成二氟甲基烷基铵盐的方法[30]Fig.33 Methods for the synthesis of difluoromethylalkylammonium salts[30]

图34 叔胺和膦酸盐在乙醇存在下的反应机理Fig.34 Reaction mechanism of tertiary amines and phosphonates in the presence of ethanol
2018年,Ting等[31]开发了一种简单有效的咪唑和吡唑的N-二氟甲基化方法。该反应利用BrCF2PO(OEt)2作为二氟卡宾供体,对咪唑和吡唑进行N-二氟甲基化反应(见图35)。
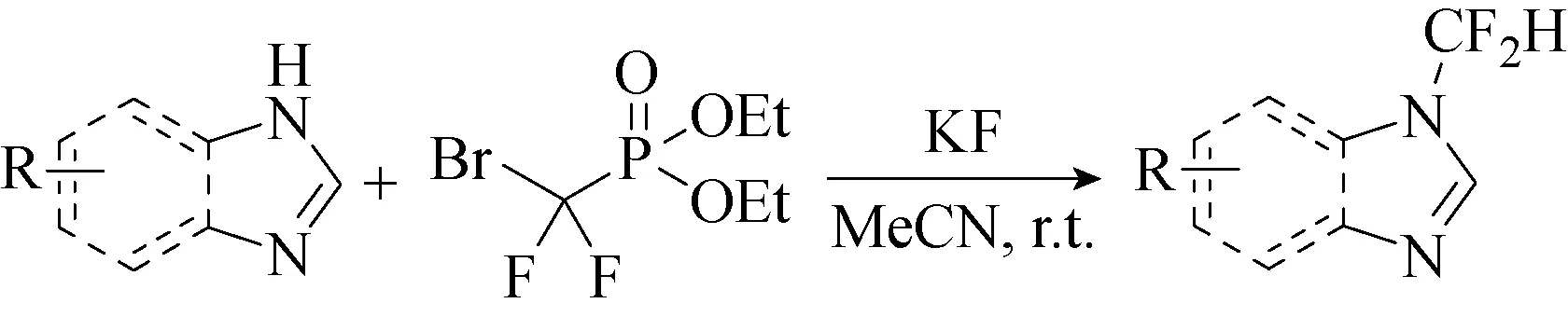
图35 苯并咪唑和咪唑的N-二氟甲基化[31]Fig.35 N-Difluoromethylation of benzoimidazoles and imidazoles[31]
4.2 BrCF2PO(OEt)2进行酚的O-二氟甲基化反应
虽然用于酚的二氟甲基化的一些试剂可以在非碱性条件下进行反应,但是用这些试剂合成芳基二氟甲基醚会导致低产率,或底物范围很小。因此,开发一种适合于天然的含羟基分子的后期修饰的温和二氟甲基化方法仍然是十分重要的。2018年,Huang等[32]使用BrCF2PO(OEt)2对异黄酮、类黄酮和香豆素的酚羟基进行二氟甲基化反应(见图36)。由于条件中所用碱相对较弱,因此具有高选择性。相比于之前报道的O-二氟甲基化反应,此法避免使用对臭氧层有害且有毒的氯二氟甲烷,同时具有温和的反应条件,合成简单性和高选择性的优点。与其它二氟甲基化试剂与酚的反应不同,该反应条件温和、底物适用性好,收率高,具有高选择性,适合于天然的含羟基分子的后期二氟甲基化修饰。

图36 芒柄花素及其衍生物的二氟甲基化反应[32]Fig.36 Difluoromethylation of formononetin and its anaglogues[32]
5 含氟砜类二氟甲基化试剂
除前文提到的几种二氟甲基化试剂外,含氟砜类二氟甲基化试剂也是二氟甲基化试剂中的一大类别,其具体种类较多,应用广泛,反应机理也多种多样,在最近的二氟甲基化反应研究中成为热点之一。
5.1 HCF2SO2Cl试剂
5.1.1 HCF2SO2Cl对菲啶的二氟甲基化反应
菲啶作为核心骨架在天然产物和生物分子中广泛存在。制备在6位带有取代基菲啶的方法通常涉及各种基团(包括三氟甲基)与2-异氰基-1,1′-联苯的反应。2015年,Zhang等[33]报道了一种异氰酸酯的直接二氟甲基化方法。在光氧还原催化下,CF2HSO2Cl可以是非常好的二氟甲基自由基前体,产生的自由基对富电子和电子双键都显示出良好的反应性。因此,该课题组将HCF2SO2Cl于光氧化还原催化下与2-异氰基-1,1′-联苯反应,然后中间基团环化,随后氧化和去质子化形成6-(二氟甲基)-菲啶(图37)。相应的磺酰氯是二芳基甲基和1,1-二氧乙基自由基的优良前体,而溴代苯甲酰基苯是α,α-二酰基苄基自由基的前体。

图37 异氰酸酯的二氟甲基化反应[33]Fig.37 Reaction of difluoromethylation of isocyanides[33]
5.1.2 HCF2SO2Cl 进行直接二氟甲基化/环化反应
目前,制备二氟甲基化杂环的实例比较少见。2016年,Hua等[34]开发了一种可见光介导的N-苄基丙烯酰胺与HCF2SO2Cl作为CF2H自由基前体进行二氟甲基化反应。结合串联环化/脱芳构化方法(见图38),在温和条件下获得各种二氟甲基化的2-氮杂螺[4.5]癸-6,9-二烯-3,8-二酮。

图38 光氧化还原催化的二氟甲基化/螺环化反应[34]Fig.38 Reaction of photoredox-catalyzeddifluoromethylation/spirocyclization[34]
可见光在炔烃的二氟甲基化反应中同样发挥着氧化还原催化的作用,而以简便有效的方法合成异喹啉二酮在有机合成和药物化学中一直是关注重点。
2017年,Zou等[35]使用二氟甲基砜完成了可见光诱导的N-甲基丙烯酰基苯甲酰胺的直接二氟甲基化反应(见图39)。该方法能以中等至良好的产率合成各种含CF2H的异喹啉-1,3(2H,4H)-二酮。该反应具有温和的反应条件,操作简便性和底物范围广泛等优点,以较好的产率获得一系列含有CF2H或CF3的异喹啉1,3(2H,4H)-二酮,具有优异的官能团耐受性[38]。
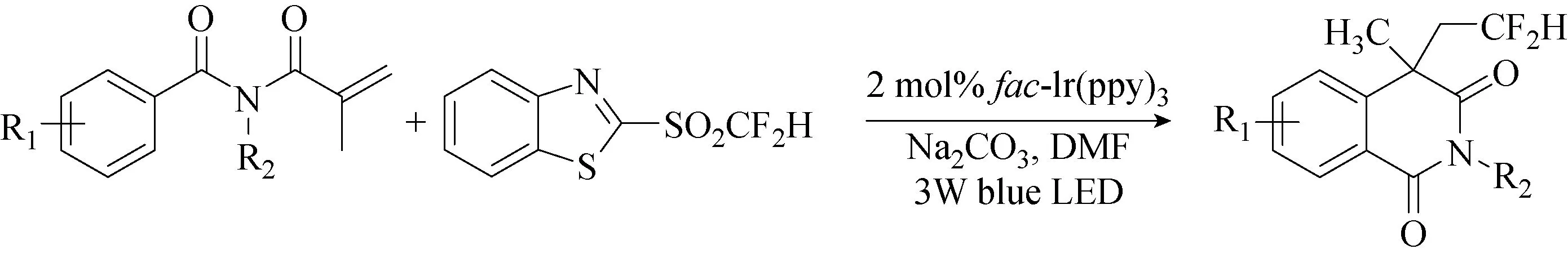
图39 可见光照射下甲基丙烯酰苯甲酰胺与二氟甲基砜的二氟甲基化反应[35]Fig.39 Difluoromethylation of methacryloyl benzamides with difluoromethy sulfone under visible irradiation[35]
2019年,Fun等[36]以二氟甲基砜为二氟甲基化试剂,成功地实现了可见光诱导的不饱和肟的二氟甲基化/环化反应。在中性条件下得到相应的二氟甲基异噁唑啉衍生物(见图40)。
5.2 HCF2SO2F进行O-二氟甲基化反应
在O-二氟甲基化反应的研究中,FSO2CF2CO2H由于其高反应效率,低价格和合成可用性,通常被认为是O-二氟甲基化的最佳选择试剂,特别是对于大规模合成。然而,环境友善的制备方法通常需要提高温度,与许多官能团不兼容,并且只在结构简单的底物上有效。

图40 可见光照射下β,γ-不饱和肟与二氟甲基砜的二氟甲基化反应[36]Fig.40 Difluoromethylation of β,γ-unsaturated oximes with difluoromethyl sulfone under visible light irradiation[36]
由于目前的方法具有上述限制,为了开发新的、简单的、将功能性醇转化为二氟甲基醚简单有效的方法,2016年,Levchenko等[37]通过CuI催化醇与FSO2CF2CO2H的反应,制备二氟甲基醚(见图41)。这一方法适用于各种功能性醇的O-二氟甲基化,FSO2CF2CO2H,是一种性能优越的二氟甲基化试剂,以CuI作为催化剂获得了产率较高的目标产物二氟甲基醚。
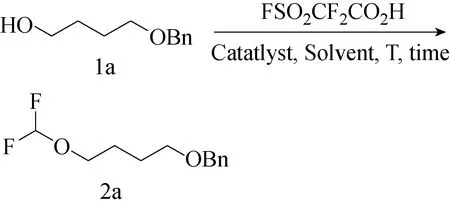
图41 2a的合成反应策略[37]Fig.41 Synthesis 2a reaction strategy[37]
5.3 CF2HSO2NHNHBoc试剂
5.3.1 CF2HSO2NHNHBoc对末端炔的二氟甲基化/环化反应
CF2HSO2NHNHBoc是一种新型二氟甲基化试剂[38-39],2018年,Xiong等[40]利用该试剂研究了炔烃自由基二氟甲基化反应(见图42)。该试剂性质稳定,可由CF2HSO2Cl和NH2NHBoc反应一步制备。通过二茂铁介导的电化学氧化产生的CF2H基团参与炔烃加成反应。

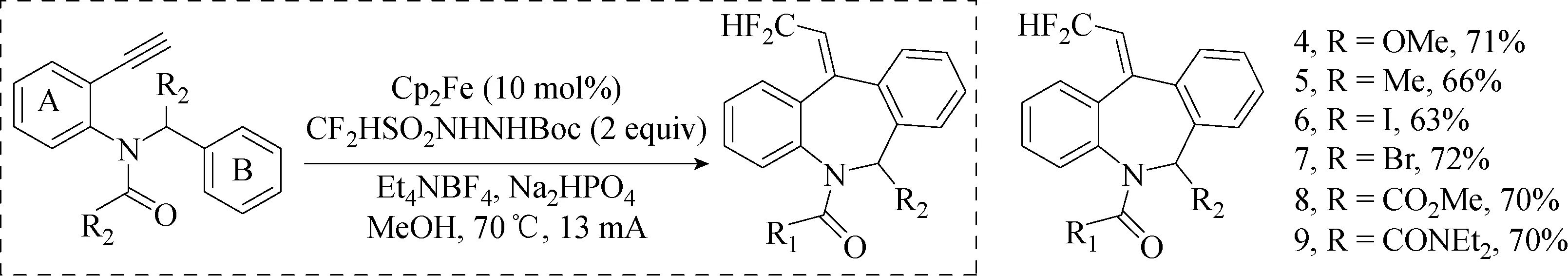
图42 炔烃的自由基二氟甲基化反应[40]Fig.42 Radical difluoromethylation of alkynes[40]
5.3.2 CF2HSO2NHNHBoc对烯烃的二氟甲基化反应
同样是使用CF2HSO2NHNHBoc作为CF2H基团来源,2019年Xu等[41]报道了电化学1,2-羟基二氟甲基化和丙烯酰胺的C-H二氟甲基化反应(见图43)。这些电氧化烯烃官能化反应不需要过渡金属催化剂和化学氧化剂,具体是发生1,2-二氢化反应还是C-H官能化反应,由丙烯酰胺的酰胺氮原子上的取代基决定。当仲N-芳基丙烯酰胺通过烯烃羟基二氟甲基化反应得到α-羟基酰胺时,叔丙烯酰胺发生烯烃C-H官能化反应(见图44)。
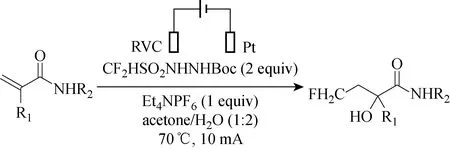
图43 吡咯烷类化合物的二氟甲基化反应[41]Fig.43 Difluoromethylation of pyrrolidine derivatives[41]

图44 叔丙烯酰胺C-H的二氟甲基化反应[41]Fig.44 Difluoromethylation of tert-acrylamide C-H[41]
5.4 HCF2SO2Na试剂
5.4.1 HCF2SO2Na对烯烃的二氟甲基化反应
N,N-二烷基腙不仅作为醛的合成等价物,而且作为进一步官能团转化的重要中间体,已被广泛用于有机化学合成中。与关于碳-碳π键的基团三氟甲基化或二氟烷基化的大量报道比,近年来,N,N-二烷基腙的直接二氟甲基或三氟甲基化反应报道相对较少。2017年,Xu等[42]报道了第一个无过渡金属和可扩展的N,N-二烷基腙的三-/二氟甲基化反应(见图45),使用易于处理和易得的HCF2SO2Na作为二氟甲基试剂,反应操作简单并在室温下进行,以较高收率得到产物。反应由二氟甲烷亚磺酸钠作为有效的氟代烷基自由基前体,引发自由基二氟甲基化反应,为进一步的可持续工业合成过程提供了基础。反应的特点在于氟化试剂二氟甲烷亚磺酸钠的经济有效,且无需过渡金属催化可直接制备二氟甲基化芳香醛腙,所得高度官能化的二氟甲基化的N,N-二烷基腙也可用作其他反应的二氟甲基合成子。
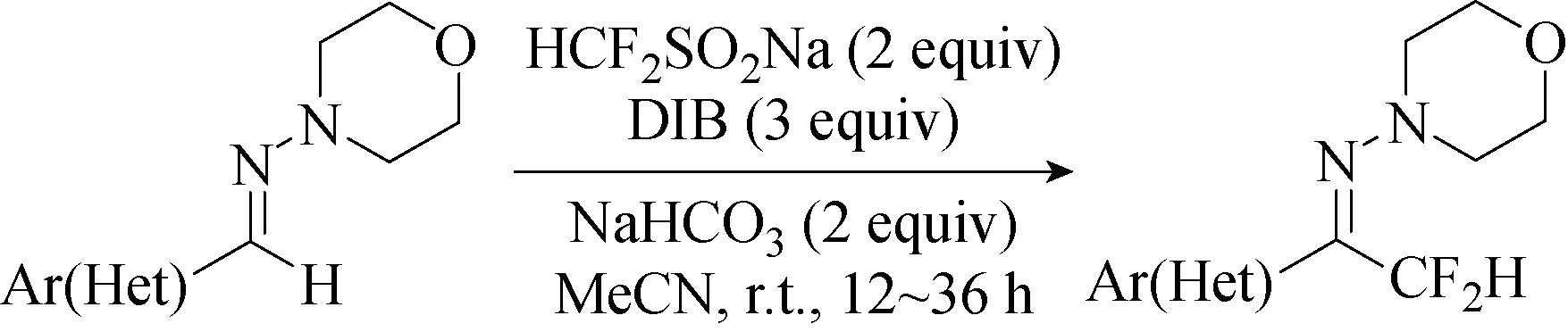
图45 N,N-二烷基腙的二氟甲基化反应[42]Fig.45 Difluoromethylation of N,N-dialkylhydrazones[42]
5.4.2 HCF2SO2Na对杂芳环的二氟甲基化反应
使用Zn(SO2CHF2)2作为二氟甲基自由基的Minisci反应,是将CF2H基团直接引入杂芳族化合物的最有效率方法之一。但该方法存在缺点是实验室难以合成Zn(SO2CHF2)2试剂。在Minisci反应机理的基础上,可以使用更易获得且更便宜的试剂,二氟甲基亚磺酸钠HCF2SO2Na也能够根据自由基机理使氮杂环二氟甲基化。2017年,Lytkina等[43]在室温下在两相体系(二氯甲烷-水)中使用HCF2SO2Na与叔丁基氢过氧化物的组合,完成了质子化杂芳族碱的自由基二氟甲基化反应(见图46),并以制备规模获得甲基吡啶-4-羧酸酯、吡啶-4-甲腈和2-氨基-1,3,4-噻二唑的二氟甲基化产物。在杂芳族碱的二氟甲基化反应试剂的应用中,该此方法重复性良好。
5.4.3 HCF2SO2Na进行烯烃的二氟甲基化/内酯化反应
2019年,Zhang等[44]报道了电引发烯烃二氟甲基化内酯化反应(见图47),使用HCF2SO2Na作为二氟甲基化试剂,以中等产率获得新型的含CF2H内酯,在额外的支持电解质和催化剂的条件下还可获得多种含CF3的内酯。这一方法也适用于不含金属催化剂,化学氧化剂和其他电解质情况下的含CF2H内酯药物分子的制备。
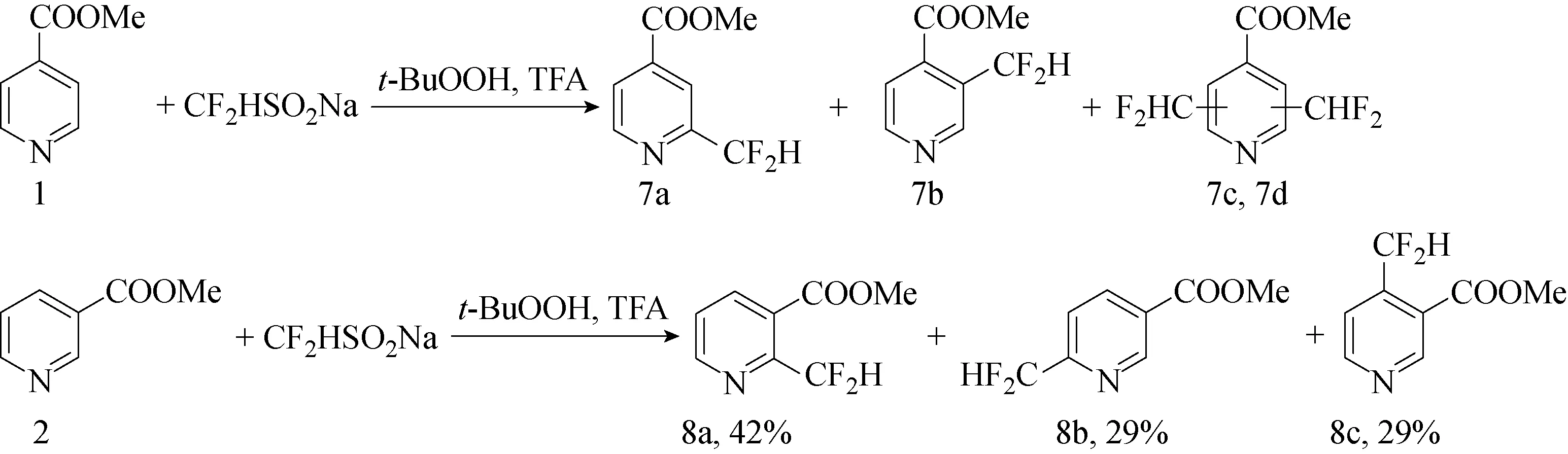
图46 质子化杂环碱与二氟甲基亚磺酸钠的二氟甲基化反应[43]Fig.46 Difluoromethylation of protonated heterocyclic bases with sodium difluoromethylsulfinate[43]

图47 烯烃的电化学二氟甲基化反应[44]Fig.47 Electrochemical difluoromethylation of olefins[44]
6 二氟甲基金属试剂
过渡金属介导/催化温和条件下的三氟甲基化方法成为了研究热点,最近报道很多,但目前报道的引入二氟甲基金属试剂直接生成二氟甲基化合物的方法却相对较少,此类试剂仍有待进一步研究。
6.1 二氟甲基银试剂
6.1.1 [(SIPr)Ag(CF2H)] 对酰氯进行二氟甲基化反应
与芳基底物的过渡金属催化的三氟甲基化反应的众多研究形成鲜明对比的是,芳基底物直接形成二氟甲基化合物的方法少得多。2015年,沈其龙课题组[45]利用具有热稳定、良好固化的NHC-连接的二氟甲基化银络合物[(SIPr)Ag(CF2H)],在存在或不存在CuI的情况下,[(SIPr)Ag(CF2H)]与各种活化的亲电试剂如二芳基碘鎓盐,乙烯基(芳基)碘鎓盐,芳基重氮盐和酰氯的反应在室温下稳定地反应(见图48),获得具有良好收率的二氟甲基化物。
尽管许多研究取得了令人瞩目的成就,但以前报道的大多数二氟甲基化方法主要集中在C(sp2)-CF2H键的构建上,而能够构建非杂原子连接的 C(sp3)-CF2H 键的方法基本上还没有探索,仍然是一项紧迫的任务。

图48 制备NHC-连接的二氟甲基化银配合物[(SIPr)Ag(CF2H)]和[(IPr)Ag(CF2H)]及CuI催化的酰氯二甲基化与[(SIPr)Ag(CF2H)]的反应[45]Fig.48 Preparation of the NHC-ligated difluoromethylated silver complexes [(SIPr)Ag(CF2H)] and [(IPr)Ag(CF2H)] and reaction for CuI-catalyzed difluoromethylation of acid chlorides with [(SIPr)Ag(CF2H)][45]
6.1.2 [(SIPr)Ag(CF2H)] 进行烯丙位的二氟甲基化反应
2017年,沈其龙课题组[46]在铜催化剂存在下,继续利用(SIPr)Ag(CF2H)在温和条件下与各种烯丙基氯化物/溴化物和炔丙基溴反应(见图49)。更重要的是,通过筛选不同配体,能够产生具有优异区域选择性的α-或γ-二氟甲基化物。当使用5,6-二甲基-1,10-菲咯啉作为配体时,仅获得α-二氟甲基化产物,而当使用N-杂环卡宾-SAPr作为配体时,产生γ-选择性二氟甲基化产物。同样,在类似的铜催化剂存在下,对于炔丙基溴的反应,实现了α-与γ-的高选择性。
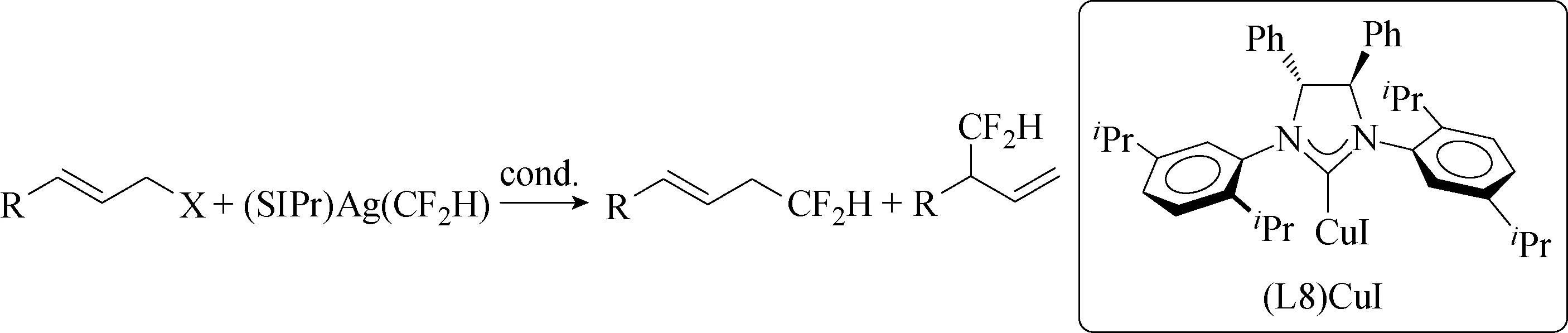
图49 Cu催化的烯丙基氯化物和溴化物的区域选择二氟甲基化反应扩展[46]Fig.49 Scope of Cu-catalyzed region-divergent difluoromethylation of allyl chlorides and bromides[46]
6.1.3 [(SIPr)Ag(CF2H)] 对芳杂环进行二氟甲基化反应
对于芳杂环上的C-H的二氟甲基化反应,2017年沈其龙课题组[47]在温和条件下利用银的二氟甲基化试剂在钯催化作用下对一系列杂芳基氯化物,溴化物和碘化物进行二氟甲基化反应(见图50)。各种缺电子的溴取代的含氮杂芳烃的二氟甲基化在温和条件下顺利进行并获得相应的二氟甲基化杂芳烃(见图51)。该研究代表了二氟甲基特异性引入杂芳烃部分位点的一种通用方法。

图50 钯催化的杂芳基溴化物二氟甲基化反应[47]Fig.50 Reaction of the palladium-catalyzed difluoromethylation of heteroaryl bromides[47]
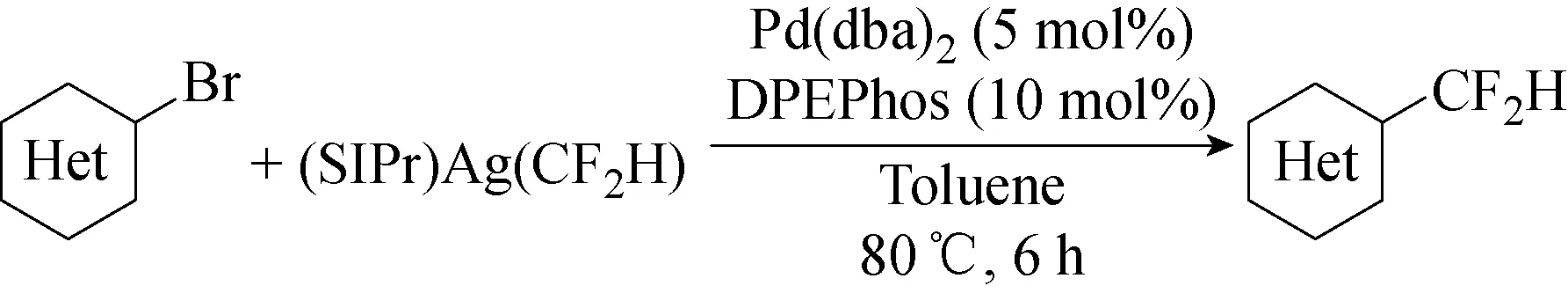
图51 钯催化的杂芳基溴化物的二氟甲基化反应[47]Fig.51 Reaction of the palladium-catalyzed difluoromethylation of heteroayl bromides[47]
2018年,该课题组[48]继续研究了一种N-杂环卡宾(NHC)连接的二氟甲基化银络合物[(SIPr)Ag(CF2H)]2,作为二氟甲基化试剂。在钯催化剂存在下,它与芳基溴化物或碘化物充分反应(见图52)。
然而,将二氟甲基化延伸到反应性较低的芳基氯化物的试验仅有部分成功。在Pd(dba)2/4,5-双二苯基膦-9,9-二甲基氧杂蒽(Xantphos)的组合使用下(见图53),活化的杂芳基氯化物如2-氯吡啶或其衍生物可与[(SIPr)Ag(CF2H)]2反应,得到相应可观产率的二氟甲基化吡啶衍生物,而未活化的芳基氯化物完全没有反应。当催化剂为Pd[3]、连接配体为X-phos时,产物具有90%收率(见图54)。预催化剂和Xphos的组合使用,为药物合成中的分子后期修饰提供了新的途径。
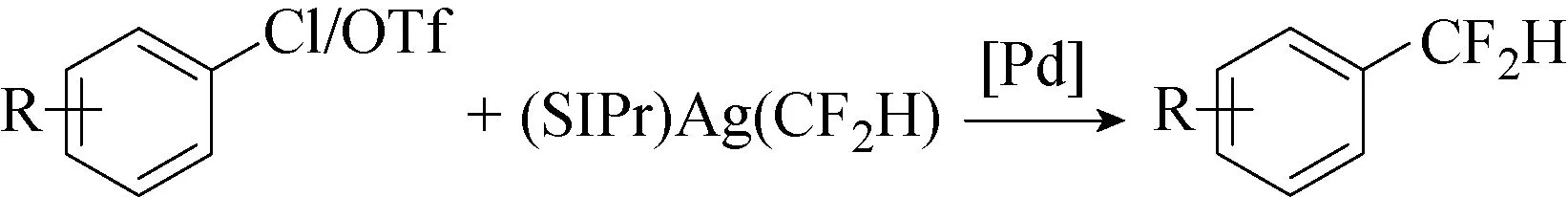
图52 钯催化的二氟甲基化反应[48]Fig.52 Reaction of the palladium-catalyzed difluoromethylation[48]
6.2 铜试剂参与的二氟甲基化反应
6.2.1 [Cu(O2CCF3)(phen)] 对芳杂环进行二氟甲基化反应
2016年,Lin等[49]利用易得和廉价的原料合成了新型铜二氟甲基化试剂[Cu(O2CCF3)(phen)](1a)和[Cu(phen)2] [O2CCF2Cl](2c)(见图55)。

图53 钯催化的4-叔丁基氯苯的二氟甲基化反应[48]Fig.53 Palladium-catalyzed difluoromethylation of 4-tert-butyl-chlorobezene[48]

图54 钯催化的芳基氯化物或三氟甲磺酸的二氟甲基化反应[48]Fig.54 Reaction of the palladium-catalyzed difluoromethylation of aryl chlorides or triflates[48]
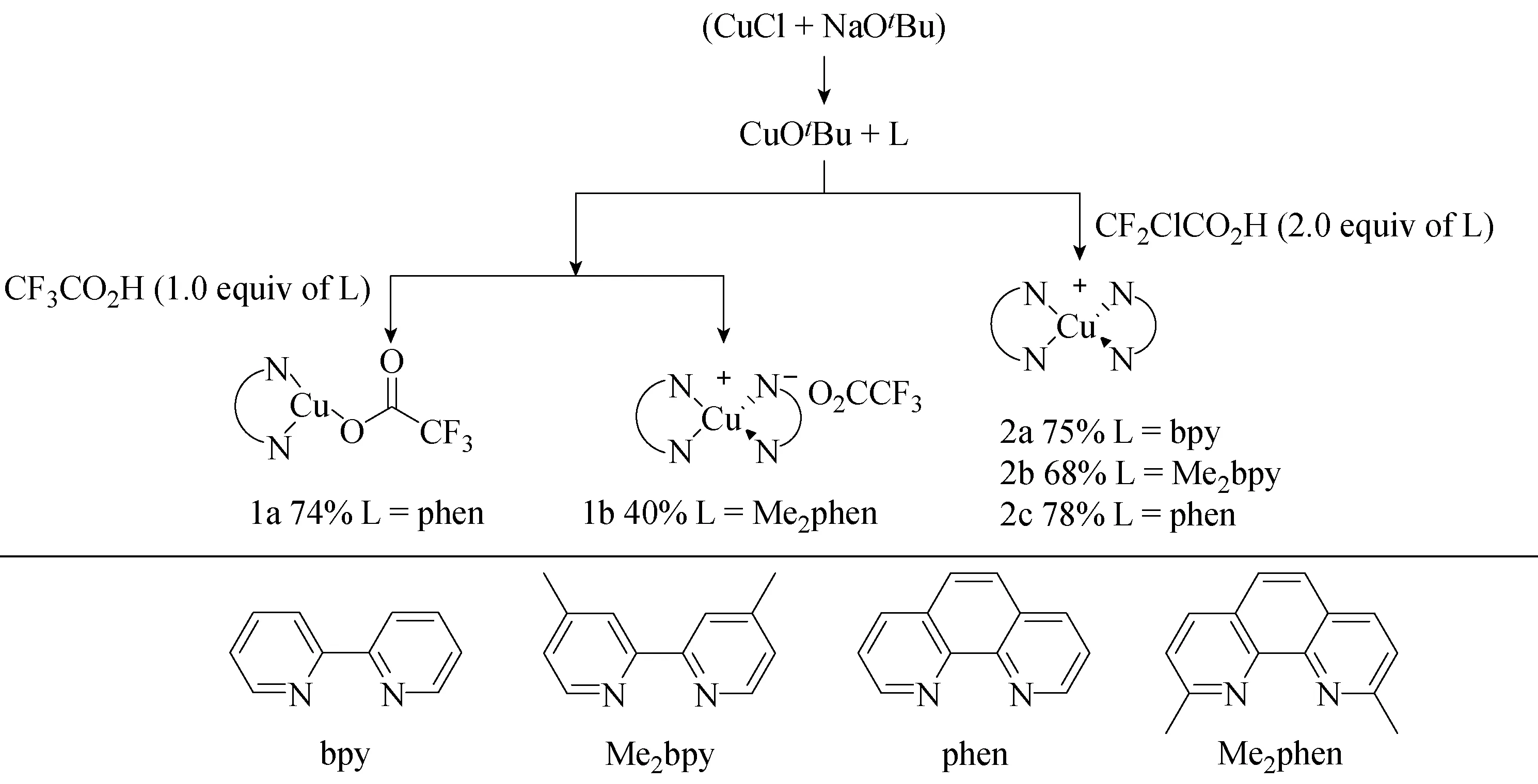
图55 三氟乙酸铜和铜-氯二氟乙酸盐配合物的合成[49]Fig.55 Synthesis of copper-trifluoroacetate and copper-chloeodifluoro-acetate complex[49]
性质稳定的络合物作为有效的三氟甲基化试剂,用于(杂)芳基卤化物三氟甲基(杂)芳烃的三氟甲基化反应(见图56),或作为二氟卡宾前体,用于苯酚和羟基吡啶的二氟甲基化,分别形成(杂)芳基二氟甲基醚。

图56 芳基碘的三氟甲基化反应[49]Fig.56 Reaction of the trifluoromethylation of aryl iodide[49]
6.2.2 (NHC)Cu(CHF2)对芳杂环进行二氟甲基化反应
[Cu(CF2H)]配合物在-30 ℃以上的温度下迅速分解,生成四氟乙烷和顺式-二氟乙烯的混合物。这些副产物暗示着双分子分解途径的存在,可能通过加入空间大位阻的配体如N-杂环卡宾(NHC)的方式来稳定[Cu(CF2H)]配合物。2017年,Bour等[50]利用(NHC)Cu(CHF2)络合物作为CHF2供体,得到4-(二氟甲基)苄腈的合成图(见图57)。可以选择适当的铜配合物,且这些配合物溶液在室温下能稳定至少24 h。

图57 (NHC)Cu(CHF2)配合物的通用合成方法[50]Fig.57 General synthetic procedure for (NHC)Cu(CHF2)complexes[50]
过滤反应混合物并随后从最小体积的THF中重结晶,分离出复合物2-IPr,收率为51%,以及复合物(SIPr)Cu(CHF2)(2-SIPr;SIPr = 1,3-双(2,6-二异丙基苯基)咪唑烷-2-亚基),收率82%。在室温下2-IPr或2SIPr与4-碘苄腈之间未观察到反应发生。
当将这些反应混合物加热至90 ℃反应20 h时,得到4-(二氟甲基)苄腈,产率分别为>98%及33%,报道发现带有庞大IPr配体的铜(I)化合物在室温下在溶液中表现出高稳定性。证明(IPr)Cu(CHF2)与各种芳基亲电试剂反应成二氟甲基化芳烃。此外,实验表明这些研究可以转化为(IPr)CuCl催化的芳基碘化物的二氟甲基化,且对于富电子芳族底物效果更佳。
6.2.3 (bpy)CuSCF3对芳杂环进行二氟甲基化反应
已知三氟甲硫醇盐阴离子在加热时容易分解形成碳硫代二氟化物(S=CF2)和氟阴离子。2018年,Zhang等[51]研究发现,三氟甲硫醇阴离子在加热时易于分解,形成硫代二氟化硫(S=CF2)和氟化物阴离子,这一特性可应用在三氟甲基化反应中。醇与AgSCF3和三氟甲磺酰胺能直接发生三氟甲基硫醇化反应(见图58),三氟甲硫醇阴离子还可应用于杂环化合物的二氟甲基化反应。利用硫代二氟甲基在形成氧硫杂环戊烷的同时引入二氟亚甲基,成为合成二氟化杂环的新方法,向含有氧硫的五元杂环化合物中引入二氟亚甲基,可使用硫代二氟化碳在与底物成环的同时作为二氟亚甲基合成源。根据这一构想,使用铜(I)三氟甲基硫醇盐络合物(bpy)CuSCF3作为二氟亚甲基供体,用3溴-4-羟基苄腈作为底物,利用KF作为碱,一锅法得到2,2-二氟-1,3-苯并氧硫杂环戊烷(见图59)。其中分子间加成和分子内偶联反应选择性C—O和C—S键合。由三氟甲硫醇盐分解产生的原位碳硫代二氟化物被用作形成2,2-二氟-1,3-苯并氧硫杂环戊烷的合成子。该一锅法方法与多种底物相容,并且能够实现几种功能相近的药样邻溴苯酚的后期二氟亚甲基化。
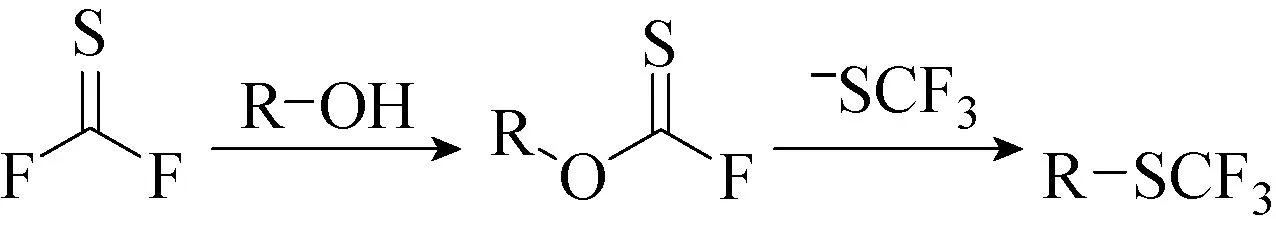
图58 Qing 和 Billard的三氟甲基化工作[51]Fig.58 Qing and Billard’s trifluoromethylation work[51]

图59 利用(bpy)CuSCF3制备二氟苯并氧硫杂环戊烷[51]Fig.59 Preparation of difluorobenzotrioxalane from (bpy)CuSCF3[51]
6.3 锌试剂参与的二氟甲基化反应
常用的二氟甲基锌试剂有(DMF)2Zn(CF2H)2、(DMPU)Zn(CF2H)2、(TMEDA)Zn(CF2H)2和(diamine)Zn(CF2H)2等[52],具有较好的稳定性,可由二氟碘甲烷与二乙基锌反应,再与配体络合,得到相应的二氟甲基锌试剂(见图60)。

图60 (二氟甲基)锌试剂的制备[52]Fig.60 Preparation of (difluoromethyl)zinc reagents[52]
6.3.1 [(DMPU)2Zn(CF2H)2]对芳杂环进行二氟甲基化反应
2016年,Xu等[52]报道二氟甲基锌试剂 [(DMPU)2Zn(CF2H)2]在镍催化剂下,在室温下即可与芳基碘化物、溴化物和三氟甲磺酸酯发生交叉偶联反应二氟甲基化反应。如果对膦配体加以修饰,还可更好地实现富电子芳基卤化物底物的二氟甲基化反应,镍催化的芳基和杂芳基碘的二氟甲基化可扩展至碘代及溴代底物(见图61)。该项研究中的锌试剂不仅性质稳定,还可与碱金属组合使用,以催化芳基碘化物、溴化物的二氟甲基化反应。同时,在金属催化剂如镍催化剂作用下有较好的底物扩展范围。此外,如果在金属镍所介导这些反应的膦配体加以修饰,还可更好地实现富电子芳基卤化物底物的二氟甲基化反应。
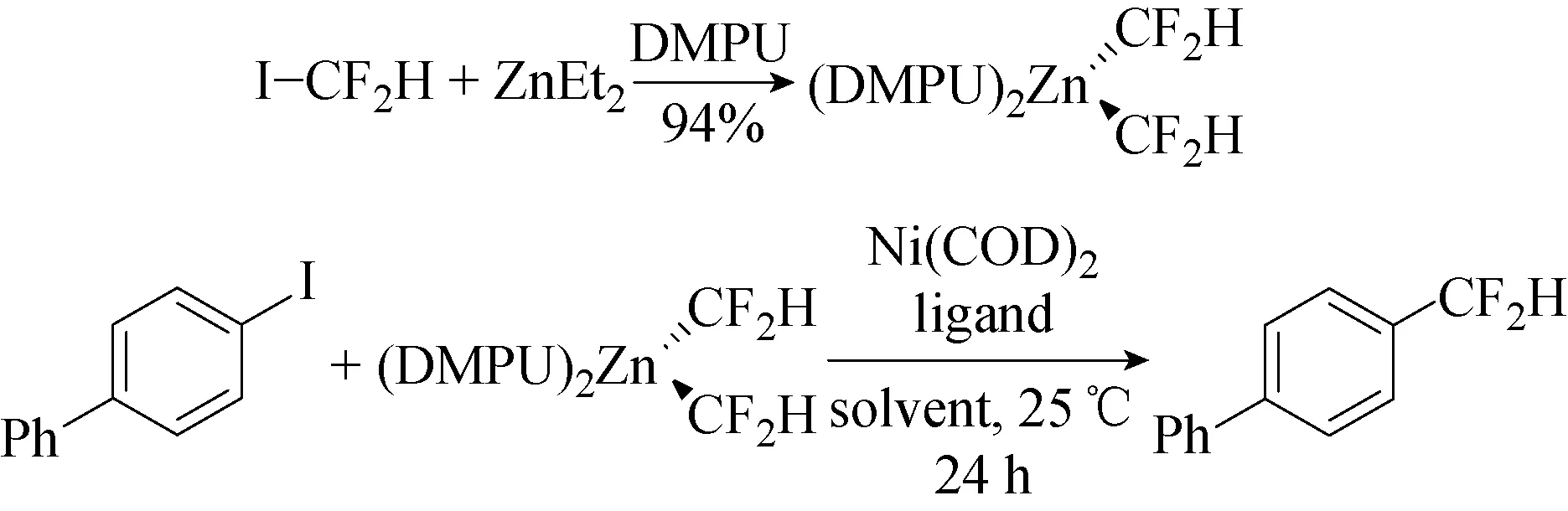
图61 镍催化的芳基和杂芳基碘的二氟甲基化反应[52]Fig.61 Nickel-catalyzed difluoromethylation of aryl and heteroaryl iodides[52]
6.3.2 (TMEDA)Zn(CF2H)2对芳杂环进行二氟甲基化反应
2016年,Aikawa等[53]利用钯催化的Negishi交叉偶联方法,将芳基碘化物与含有二胺化合物如TMEDA的(二氟甲基)锌试剂(见图62)共同反应,二氟甲基的转移可在没有活化剂存在的情况下进行。为了验证锌试剂二氟甲基化的底物适用性,作者研究了含有不同官能团取代的芳基卤化物二氟甲基化反应(见图63)。从锌试剂到钯催化剂的CF2H基团的转移均在没有活化剂的情况下有效地进行。

图62 碘/溴化芳烃的催化二氟甲基化反应[53]Fig.62 Catalytic difluoromethylation of iodine/brominated aromatic hydrocarbons[53]

图63 不同官能团取代的底物扩展[53]Fig.63 Substrate scope and functional-group tolerance[53]
6.3.3 (DMPU)2Zn(CF2H)2对烯丙位进行手性二氟甲基化反应
2017年,Aikawa等[54]报道在碘化亚铜催化下二氟甲基锌试剂[(DMPU)2Zn(CF2H)2]可与苯丙烯碳酸酯底物进行烯丙化反应引入二氟甲基(见图64),反应区域选择性好,收率良好,对于手性底物,所获得的手性烯丙基二氟甲基化物构型翻转。该工艺使用铜盐作为催化剂,实现烯丙基碳酸酯与(二氟甲基)锌试剂催化的烯丙基二氟甲基化,(二氟甲基)锌试剂可以通过二氟碘甲烷与二乙基锌的碘-锌交换反应制备,证明该反应具有立体选择性。

图64 铜催化下烯丙基碳酸酯与(二氟甲基)锌试剂的烯丙基二氟甲基化反应[54]Fig.64 Copper-catalyzed allylic difluoromethylation of allyl carbonates with (difluoromethyl)zinc reagent[54]
2017年,Serizawa等[55]同样使用(DMPU)2Zn(CF2H)2试剂(见图65)实现了芳基碘化物与锌试剂在铜催化下的二氟甲基化反应,以制备二氟甲基化的芳烃(见图66)。还证明了即使在室温下,CF2H基团从锌试剂到铜催化剂的转移也可以很好地进行,说明产生的不是中性的CuCF2H而是铜酸盐[Cu(CF2H)2]-。

图65 双(二氟甲基)锌试剂的制备[55]Fig.65 Preparation of bis(difluoromethyl)zinc reagents[55]
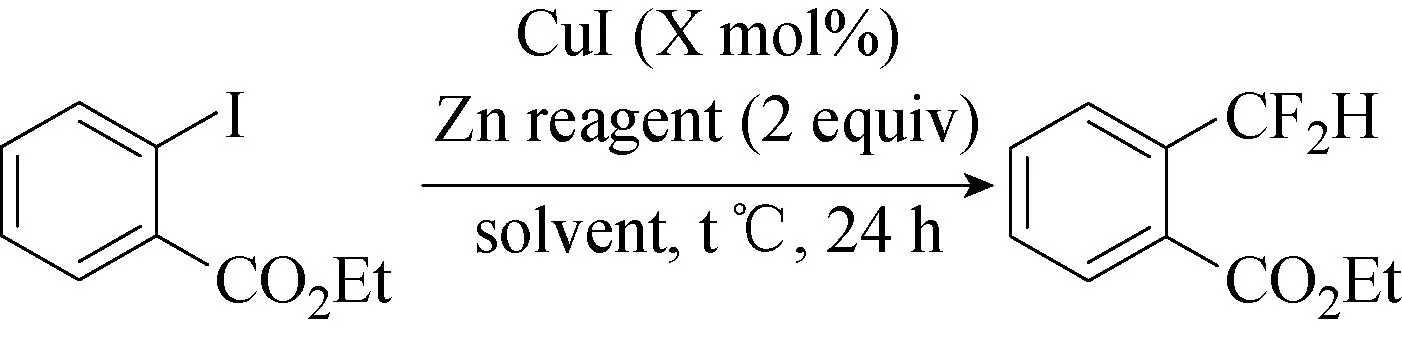
图66 铜催化的芳基碘化物的二氟甲基化反应[55]Fig.66 Copper-catalyzed difluoromethylation of aryl iodide[55]
7 其他二氟甲基化试剂
7.1 TFEDMA对杂芳烃的二氟酰化反应
2015年,Schmitt等[56]将TFEDMA(氟代烷基氨基试剂)用于芳烃、杂芳烃和C-H酸性化合物的二氟甲基化和二氟代酰化反应(见图67)。这种方法可以高效地获得高附加值的二氟甲基化产物,并具有良好的产率。实验发现,在存在路易斯酸的活化作用时,TFEDMA(1,1,2,2-四氟-N,N-二甲基乙-1-胺)与烷基或甲硅烷基烯醇醚能够发生有效反应,C-H酸性衍生物如丙二醇和氰基乙酸盐都是重要的合成结构片段。

图67 TFEDMA的制备及使用TFEDMA作为芳烃二氟酰化剂的二氟甲酰化反应[56]Fig.67 Preparation of TFEDMA and the use of TFEDMA as a difluoroformylation reaction of an aromatic difluoro acylating agent[56]
7.2 [双(二氟乙酰氧基)碘]苯对杂芳烃的二氟甲基化反应
2017年,Sakamoto等[57]报道二氟乙酸碘苯试剂在可见光(400 nm)照射下可产生二氟甲基自由基与甲基咪唑类化合物反应在其2-位引入二氟甲基,收率可达75%。通过将其他氟代烷基引入到聚合物中进一步证明了该方法的实用性(见图68)。

图68 以咖啡因为底物,对氟烷基化试剂羧酸配体的选择[57]Fig.68 Scope with respect to the carboxylic acid ligands in the fluoroalkylation reagents,using caffeine as a model substrate[57]
7.3 S-二氟甲基锍盐进行O-二氟甲基化反应
通常,O-二氟甲基化反应构建HCF2O-官能团主要限于酚类和醇类底物的转化。2016年,Yue等[58]描述了1,3-二酮与S-二氟甲基锍盐的O-二氟甲基化反应(见图69)。机理研究表明,环状和非环状1,3-二酮与S-二氟甲基锍盐的O-二氟甲基化反应可在室温下顺利进行,在该反应中,S-二氟甲基锍盐既作为直接二氟甲基化剂又作为二氟卡宾前体。

图69 1,3-二酮的O-二氟甲基化反应[58]Fig.69 Reaction of O-difluoromethylation of 1,3-dione[58]
7.4 S-二氟甲基-S-二(对二甲苯基)锍四氟硼酸盐进行区域选择性氨基-二氟甲基化反应
2017年,Noto等[59]发现,芳族烯烃的区域选择性氨基-二氟甲基化反应,可在可见光光氧还原催化中一步反应实现(见图70),通过C(sp3)-CF2H和C(C3)-N键与C=C的反应实现。该课题组开发的新型S-(二氟甲基)锍盐和聚乙烯催化剂的组合使得芳香族烯烃的氨基-二氟甲基化能够通过自由基过程容易地进行。
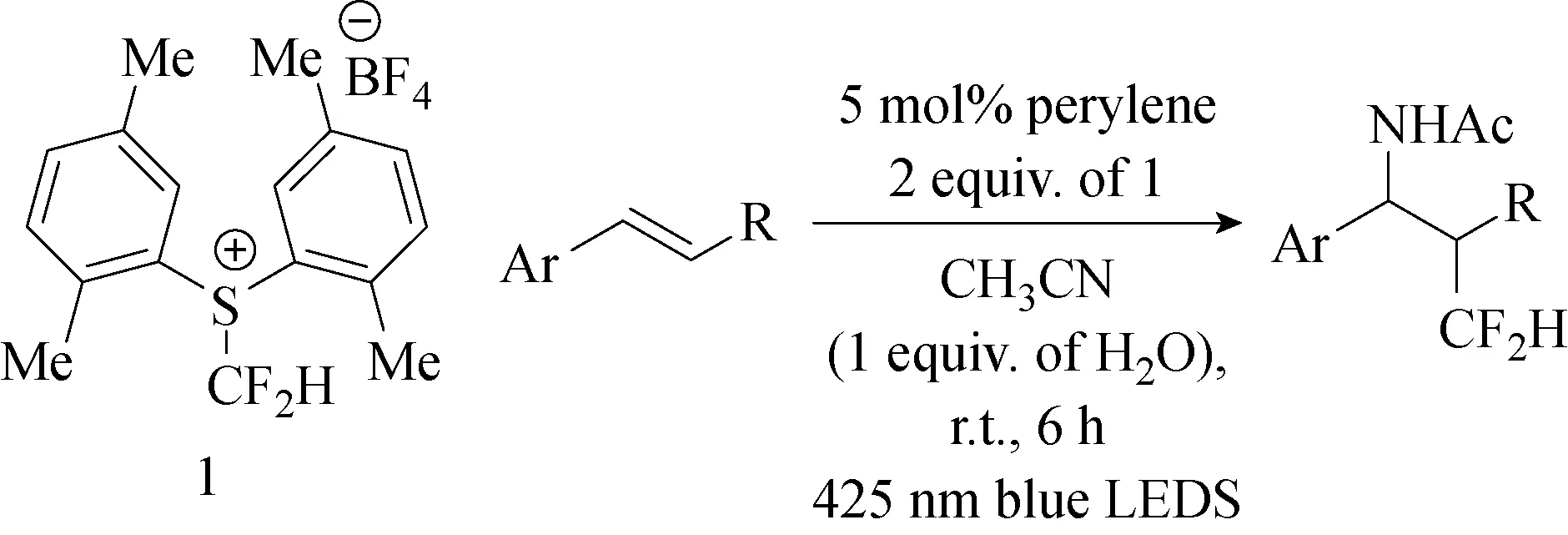
图70 烯烃的催化氨基二氟甲基化反应[59]Fig.70 Catalytic aminodifluoromethylation of olefins[59]
7.5 双-甲硅烷基化二氟烯胺
2018年,Kobayashi 等[60]利用Mg(0)/Me3SiCl体系制备了新型氟化二价阴离子等价物。在一锅反应中三氟亚氨代乙酰氯还原性裂解(见图71),得到双-甲硅烷基化二氟烯胺。其后双(甲硅烷基)烯胺与两种亲电试剂的碳-碳键反应形成各种二氟化亚胺(见图72)。一锅裂解法以及两个甲硅烷基的引入及其各自的转化对合成有机化学中氟化反应结构单元进行了拓展。
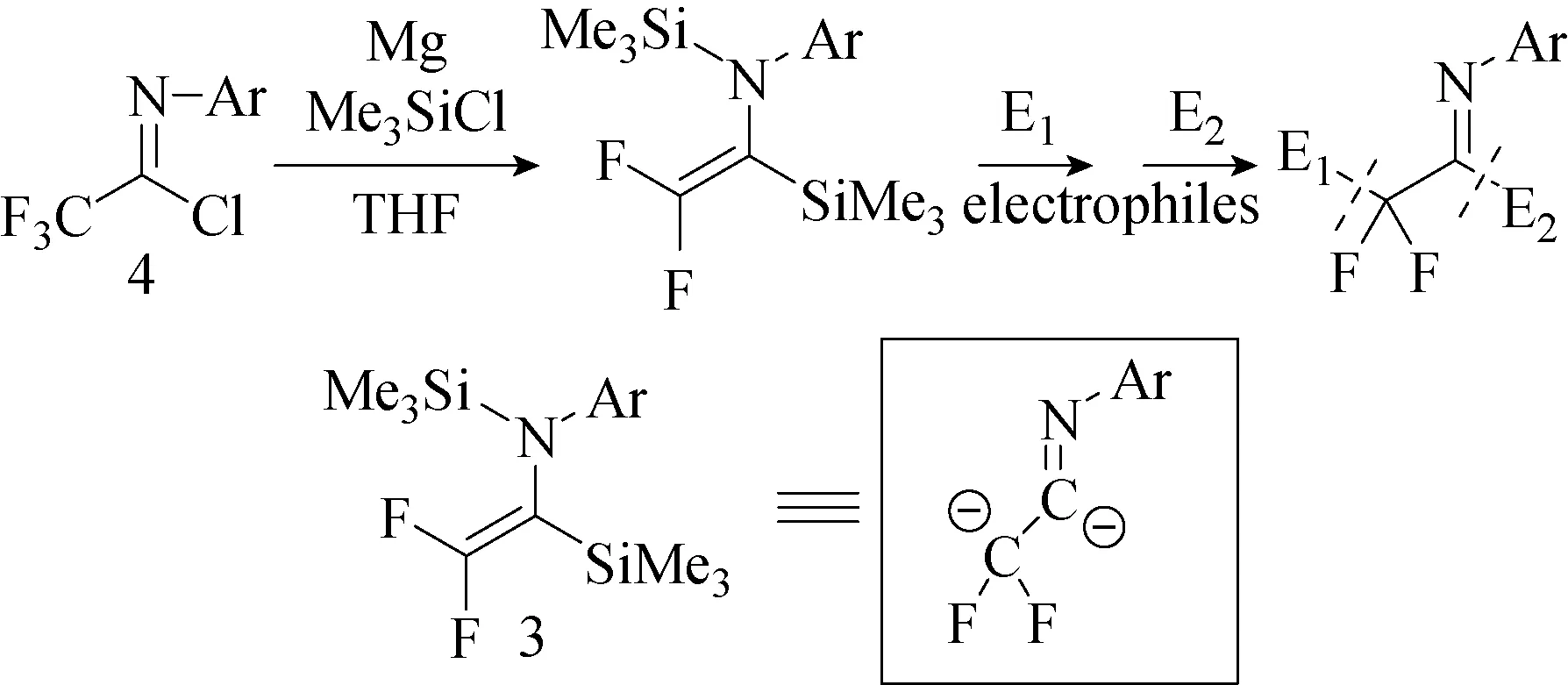
图71 一锅法制备新的偕-二氟化二价阴离子[60]Fig.71 A one-pot preparation of new gem-difluorinated dianion equivalents[60]

图72 双甲硅烷基化二氟烯胺的制备[60]Fig.72 Preparation of disilylated difluoroenamine[60]
8 结 语
总的来看,在目前的各类二氟甲基化试剂中,TMS类试剂作为一类传统二氟甲基化试剂,凭借其经济易得、稳定、易操作、易活化和反应条件温和的特点而广泛应用于各类二氟甲基化反应,例如TMSCF3或TMSCF2Br与重氮化合物发生自由交叉偶联反应[8]、以及TMSCF3对各种腈化合物的sp3碳进行二氟甲基化反应[7],都是对TMS类试剂应用的优秀实例。另外,使用含氟砜类试剂HCF2SO2Cl制备的各种二氟甲基化的酮类和二氟甲基异噁唑啉衍生物,也补充了目前制备二氟甲基化杂环较为少见的实例。二氟甲基金属类试剂也是二氟甲基试剂中的一大亮点,例如铜(I)三氟甲基硫醇盐络合物(bpy)CuSCF3[51]、[(DMPU)2Zn(CF2H)2][52]等。
尽管本文将二氟甲基化试剂做出新的分类,就其反应机理来看,仍是属于亲核二氟甲基化试剂、亲电二氟甲基化试剂以及二氟甲基自由基供体的试剂。目前,应用最为广泛的二氟甲基化试剂为亲和性二氟甲基化试剂,其试剂种类较为丰富,基本能完成各类二氟甲基化反应的需要,但是存在着部分试剂昂贵,毒性大,难以购买,环境有害等问题,因而,亲电型二氟甲基化试剂、二氟甲基自由基供体试剂就是对二氟甲基化试剂家族的最好补充,他们相互弥补了各类试剂存在的不足,为二氟甲基化反应的发展做出了巨大贡献。
结合现状来看,是否能在直接二氟甲基化反应中解决不使用成本昂贵的金属络合物、能否开发一种广泛适用的二氟甲基化途径或试剂、能否对复杂分子进行低成本高效率的二氟甲基化策略,将是未来全世界科研工作者共同的研究目标。

