桥联二茂稀土胺化物催化甲基丙烯酸甲酯聚合
沙 麟,胡 文,袁福根
(苏州科技大学 化学生物与材料工程学院,江苏 苏州215009)
二茂基稀土胺化物Cp2LnNR2是近年来稀土配位催化研究中的一个活跃领域。这类化合物一方面在结构上保持了单一催化活性中心(唯一的Ln-N 活性键),另一方面它的合成比经典稀土有机(Ln-C 活性键)化合物要方便得多。通过改变茂环上取代基以及胺基上的取代基,对二茂基稀土胺化物结构和性能进行调控,揭示稀土化合物结构和性能的关系[1-2],是稀土金属有机化学研究的重要内容。
沈琪课题组对茂基稀土胺化物进行了系统研究。合成了含不同茂基、 不同胺基的稀土金属化合物Cp2LnNR2(如 Cp=MeC5H4、tBuC5H4、C5Me5,NR2=NiPr2、NPh2、C5H10N,Ln=Yb、Y、Er 等),系统考察了它们对甲基丙烯酸甲酯(MMA)的催化聚合活性。结果发现,稀土胺化物的催化活性随茂基体积的增大而降低。例如同样二苯胺基稀土化合物,MeC5H4、tBuC5H4、C5Me5这三种茂基配体的催化活性顺序为 MeC5H4>tBuC5H4>C5Me5[3-4]。而不同胺基的催化活性也随胺基体积减小而增大。例如甲基环戊二烯为配体,NiPr2、NPh2、C5H10N 这三种取代胺基的催化活性顺序为 NPh2<NiPr2<C5H10N[5]。
由此可知,二茂基稀土胺化物的催化活性受茂基体积和胺基体积等影响较大,小配体对稀土胺化物催化活性有利。但是采用小体积的环戊二烯配体(如MeC5H4)后,就无法考察轻稀土元素的催化性质,因为由小配体配位的稀土胺化物因空间配位不饱和而不能稳定,有的会歧化为离子型化合物。为了全面考察稀土元素,尤其是轻稀土对稀土胺化物催化性能的影响规律,笔者合成了桥联二茂配体。将两个茂基连接起来,可稳定轻稀土胺化物,避免歧化反应的发生。选择环己基桥联二茂配体(CH2)5C(C5H5)2,这个配体的金属配合物在催化烯烃聚合方面表现出了优越的活性[6],并且笔者有过合成的经验[7]。通过 LnCl3、(CH2)5C(C5H4Na)2和NaN(TMS)2(TMS=Si(CH3)3)按照 1∶1∶1 摩尔比反应,合成了[(CH2)5C(C5H4)2]LnN(TMS)2(Ln=Nd,Sm,Er),选择轻、中、重三种稀土元素,研究了它们对甲基丙烯酸甲酯催化聚合反应性能。结果表明,稀土元素对催化活性有很大影响,[(CH2)5C(C5H4)2]ErN(TMS)2的催化活性比[Me2Si(C13H8)(C5H4)]ErN(TMS)2要高些,并且在75 ℃仍表现出较好的催化活性。
1 实验部分
1.1 试剂与仪器
所有操作均在无水无氧条件下采用Schlenk 技术进行。溶剂四氢呋喃(THF)和甲苯经无水氯化钙干燥一周后,经二苯甲酮-钠回流至兰紫色蒸出。MMA 经氯化钙干燥处理后减压蒸出。无水LnCl3从相应的氧化物出发按文献[8]方法制备。NaN(TMS)2从百灵威公司购得。环己基桥联双茂钠盐(CH2)5C(C5H4Na)2根据文献[7]方法制备。稀土离子含量用EDTA 络合滴定法测定。聚合物产率通过称重法获得。PMMA 分子量及其分布在PL-GPC50 凝胶渗透色谱仪上测定,温度40 ℃,四氢呋喃为流动相,流速l mL·min-1,标样为聚苯乙烯。
1.2 环己基桥联二茂稀土胺化物的合成
环己基桥联二茂稀土胺化物[(CH2)5C(C5H4)2]LnN (TMS)2(Ln=Nd,Sm,Er)的合成参考文献[9]中Ph2C(C13H8)(C5H4)LuN(TMS)2的合成方法进行。以(CH2)5C(C5H4)2ErN(TMS)2的合成为例,具体过程如下:在一个经脱水脱氧处理的反应烧瓶中,称入无水ErCl3(0.539 g,1.97 mmol),添加约25 mL 的THF 溶剂,磁力搅拌形成粉红浑浊液。用干燥针筒注入(CH2)5C(C5H4Na)2的 THF 溶液 1.97 mmol(3.5 mL,浓度 0.563 mol·L-1),反应液慢慢变成咖啡色。室温搅拌反应24 h 后,向反应烧瓶中注入NaNTMS2的THF 溶液1.97 mmol(1.9 mL,浓度为1.038 mol·L-1),反应混和液慢慢变成橘黄色浑浊。继续搅拌反应24 h 后,离心获得棕红色清液(固体沉淀用THF 洗涤3 遍,清液合并)。将清液在真空下脱溶剂进行浓缩,然后放冰箱-20 ℃冷冻5 d,析出大量亮棕红色晶体。移除母液,晶体部分加入适量甲苯溶解,得催化剂溶液,浓度通过EDTA 滴定稀土含量确定。反应方程式如式(1)所示。
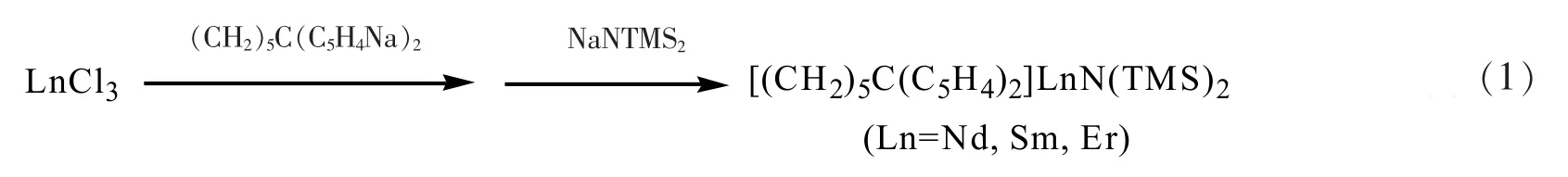
1.3 聚合反应过程
在脱水脱氧的小烧瓶中,先后加入计量的甲苯和MMA 单体,置于恒温油浴中搅拌(大约需要10 min),然后用注射器添加所需量的催化剂溶液。搅拌一段时间后,转子搅拌速度明显变慢,溶液变粘。聚合结束,用含少量盐酸的酒精终止反应,再加入大量酒精,PMMA 会沉淀析出。聚合物从聚合烧瓶中取出、剪细,用酒精充分浸泡、洗涤,最后在45 ℃真空干燥24 h 后收集,做称重和GPC 分析。
2 结果与讨论
2.1 稀土元素的影响
尽管稀土胺化物的研究报道已有很多,但关于轻稀土元素的胺化物以及桥联二茂稀土胺化物催化MMA聚合的报道并不多。Marks 等[10]最早报道了[(R)-(neomanthyl)C5H4]2LaN(TMS)2催化 MMA 聚合反应,可得到等规立构PMMA,但催化反应活性较低,0 ℃ 160 h 转化率仅36%。Lee 等[11]合成了芴和四甲基茂通过Si 桥联的稀土胺化物[Me2Si(C13H8)(C5Me4)]YN(TMS)2,发现催化 MMA 聚合活性也很低(0 ℃ 10 h 转化率 4.2%),推测原因是稀土金属周围的配位环境比较拥挤以及Ln-N(TMS)2键反应活性较低造成的。钱长涛等[12]合成了芴和无取代茂通过 Si 桥联的稀土胺化物[Me2Si(C13H8)(C5H4)]LnN(TMS)2(Ln=Dy,Er),发现催化 MMA 聚合活性有了较大的提高,这证明Lee 等推测是正确的。由此进一步推测,将两个无取代的环戊二烯相连接,相应的稀土胺化物催化活性可能更高。
环己基桥联双茂稀土胺化物[(CH2)5C(C5H4)2]LnN(TMS)2(Ln=Nd,Sm,Er)催化 MMA 聚合结果列于表1中。由表1 可知,不同稀土元素的桥联二茂稀土胺化物都能催化MMA 聚合,但它们的活性却有很大的差异。例如同样单体浓度、催化剂用量,0 ℃聚合反应120 min 的条件下,Sm 和Nd 配合物的催化产率分别为15.1%(实验2)和88.4%(实验5),而Er 配合物催化反应30 min,产率就达93.3%(实验9)。轻稀土元素配合物活性居中,Er 配合物的催化活性最好。三种配合物的催化活性顺序为Er>Nd>Sm。
[Me2Si(C13H8)(C5H4)]LnN(TMS)2(Ln=Dy,Er)在相同聚合反应条件下,Dy 配合物催化反应 60 min,聚合产率为 81.7%;Er 配合物催化反应 120 min,聚合产率为 67.5%[12]。显然,[(CH2)5C(C5H4)2]ErN(TMS)2的催化活性要比[Me2Si(C13H8)(C5H4)]ErN(TMS)2高很多,说明配体体积减小后,配合物催化活性的确有提高。
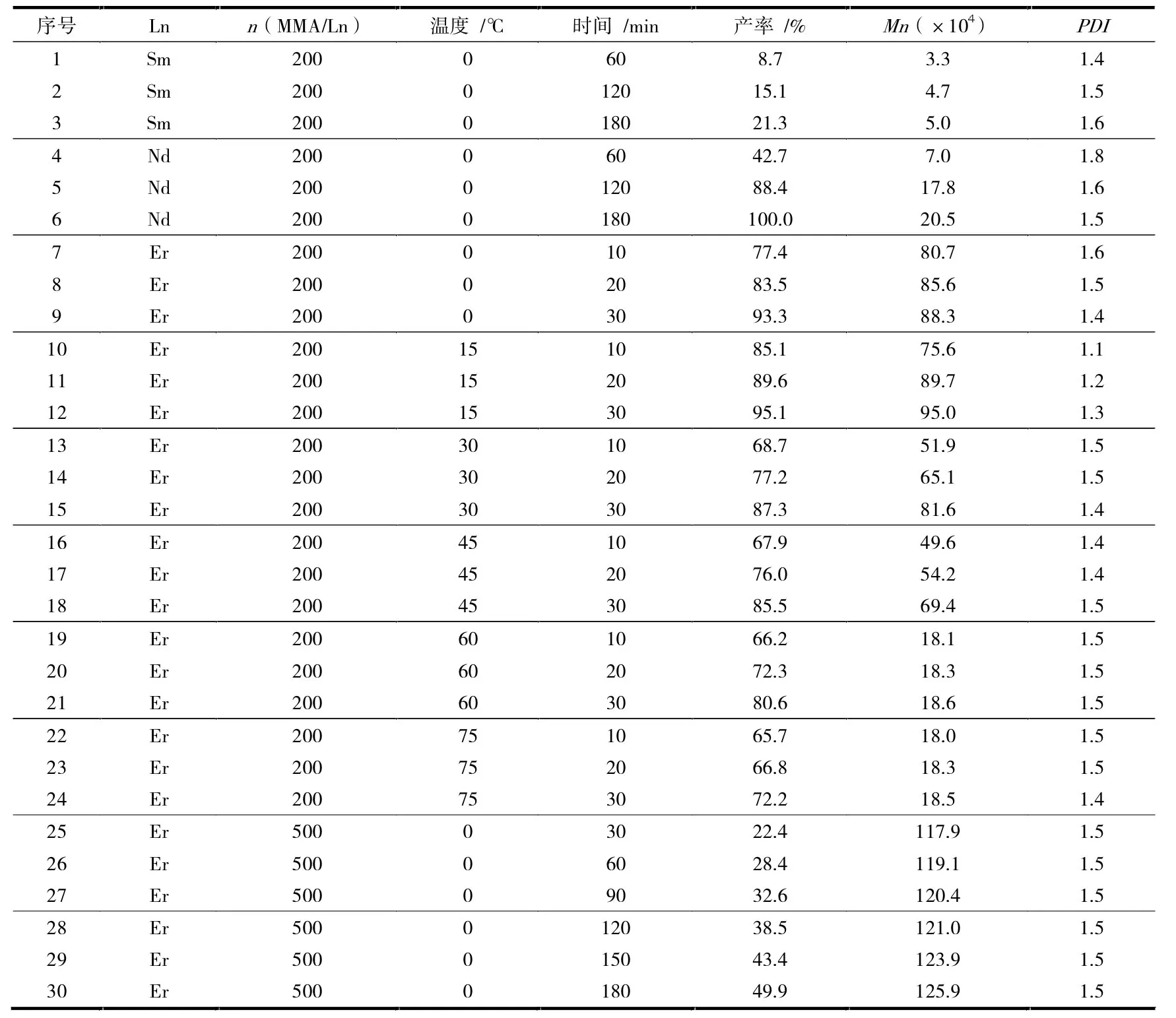
表1 环己基桥联双茂稀土胺化物催化催化MMA 聚合结果
2.2 聚合温度的影响
沈琪发现,二茂基稀土胺化物催化MMA 聚合时,催化活性受聚合温度影响极大。一般低温(如-78 ℃)能显示很高催化活性,但是当温度升高到40 ℃时,催化活性会明显降低,如(MeC5H4)2YbNiPr2(THF)在温度从0 ℃升到40 ℃时,聚合产率由96.2%下降到了45.2%[13]。
由表1 可见,温度对环己基桥联二茂稀土胺化物催化MMA 聚合也有很大影响。Er 配合物在0、15 、30、45 ℃时同样催化聚合 30 min,得到的产率分别为 93.3%(实验 9)、95.1%(实验 12)、87.3%(实验 15)、85.5%(实验18)。聚合反应在15 ℃具有最高的聚合产率。温度偏高或者偏低均不利。此现象跟芳氧基稀土硼氢化物催化MMA 聚合时现象一致。芳氧基稀土硼氢化物催化MMA 聚合时,0 ℃是其催化反应的最佳温度[14]。
值得注意的是,环己基桥联二茂稀土胺化物即使在75 ℃也有较好的催化活性,例如Er 配合物在75 ℃催化反应30 min,聚合产率达到72.2%(实验24)。这个温度比文献报道的失活温度(40 ℃)[13]要高很多。推测原因是,一方面桥联配体增加了催化剂的热稳定性,另一方面标题配合物的Ln-N(TMS)2键拥有两个大体积的三甲基硅基,这阻碍和影响了它跟MMA 酯基进行亲核取代反应(此反应被认为是催化剂失活的原因[15]),从而提高了其失活温度。
2.3 聚合时间的影响
聚合产率随聚合时间的延长而增加。当催化剂用量为单体的1/200 时,聚合反应速率很高。当降低催化剂用量为单体的1/500 时,聚合速率明显降低。详细考察了0 ℃下不同聚合时间的PMMA 产率 (实验25~30),换算成单体浓度随反应时间的变化,见图1。由图1 可见,ln([M]0/[M])对聚合时间t 基本呈线性关系,说明聚合反应速率对单体浓度呈一级反应动力学关系。回归方程为ln([M]0/[M])=0.002t+0.156,相关系数r 为0.994,相关系数临界值为r(0.01,4)为0.917,r 大于临界值,回归方程有意义。测得聚合物分子量分布指数在1.1~1.6。此分布指数比催化剂[Ph2C(C13H8)(C5H4)]LuN(TMS)2[9]所报道的 2.2 要窄一些。
3 结语
[(CH2)5C(C5H4)2]LnN(TMS)2(Ln=Nd,Sm,Er)可以中等速率催化MMA 聚合反应,稀土元素活性顺序为Er>Nd>Sm。[(CH2)5C(C5H4)2]ErN(TMS)2的催化活性比[Me2Si(C13H8)(C5H4)]ErN(TMS)2要高。催化聚合反应在15 ℃时有最高的反应速率。这类稀土胺化物失活温度可达75 ℃。聚合反应服从一级反应动力学。
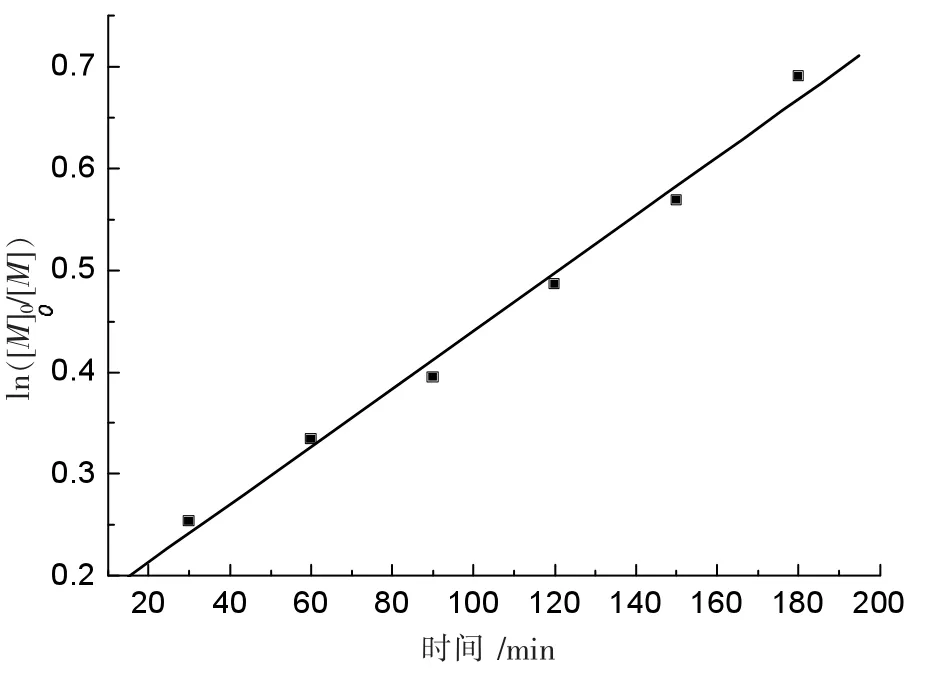
图1 ln([M]0/[M])和聚合时间 t 的关系

