顺铂联合紫杉醇或伊立替康治疗晚期宫颈癌的疗效分析
郭冰心,孙付霞
(河南省驻马店中医院,河南 驻马店 463000)
宫颈癌是发病率仅次于乳腺癌的女性恶性肿瘤,全球每年约有50万例新发病例,死亡病例达25万例[1],其中大部分病例发生在发展中国家,我国的宫颈癌病例数占全球85%左右,死亡率约占全球的1/3[2]。早期宫颈癌通过子宫全切术或放射治疗,5年生存率可达80%~90%,但晚期宫颈癌(ⅡB期~ⅣA期)患者的生存率较低,治疗失败率增加到40%~60%,复发的宫颈癌患者化疗缓解率介于20%~36%,生存期小于1年[3-4]。
目前,以铂类为基础的化疗是晚期宫颈癌患者的标准治疗方案[5]。铂类是宫颈癌化疗中最有效的化疗药物之一,常作为联合化疗的主要药物,与紫杉醇、吉西他滨、异环磷酰胺、伊立替康等联合使用[6]。紫杉醇和伊立替康在化疗中的应用效果已得到肯定,本研究旨在比较顺铂联合紫杉醇和顺铂联合伊立替康化疗治疗晚期宫颈癌的效果,从而为晚期宫颈癌的化疗用药提供参考。
1 资料与方法
1.1 一般资料
纳入标准:①病理学检查确诊为宫颈癌;②影像学检查显示盆腔外脏器或淋巴结转移;③无妊娠、无脑转移,有可测量的肿瘤病灶;④美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)体能状况(performance status,PS)0~ 2分;⑤治疗前 1个月未接受过化疗、放疗和手术治疗。排除标准:①合并其它部位恶性肿瘤者;②伴心脏或肝肾功能异常者;③血常规和心电图异常者;④不能耐受化疗者;⑤同时使用其它抗肿瘤药物者;⑥认知障碍无法配合治疗者;⑦不同意参与本研究者。
选择2014年6月—2016年6月我院收治的60例晚期宫颈癌患者,采用随机数字表法分为两组,各30例。其中一组接受紫杉醇联合顺铂治疗(taxol +platinum,TP 组),年龄 25~69岁,平均年龄(54.5±8.3)岁;另一组接受伊立替康联合顺铂治疗(irinotecan +platinum,IP组),年龄27~69岁,平均年龄(56.2±7.6)岁。两组患者年龄、病理类型、ECOG评分等一般资料比较,差异无统计学意义(P<0.05),具有可比性。见表1。
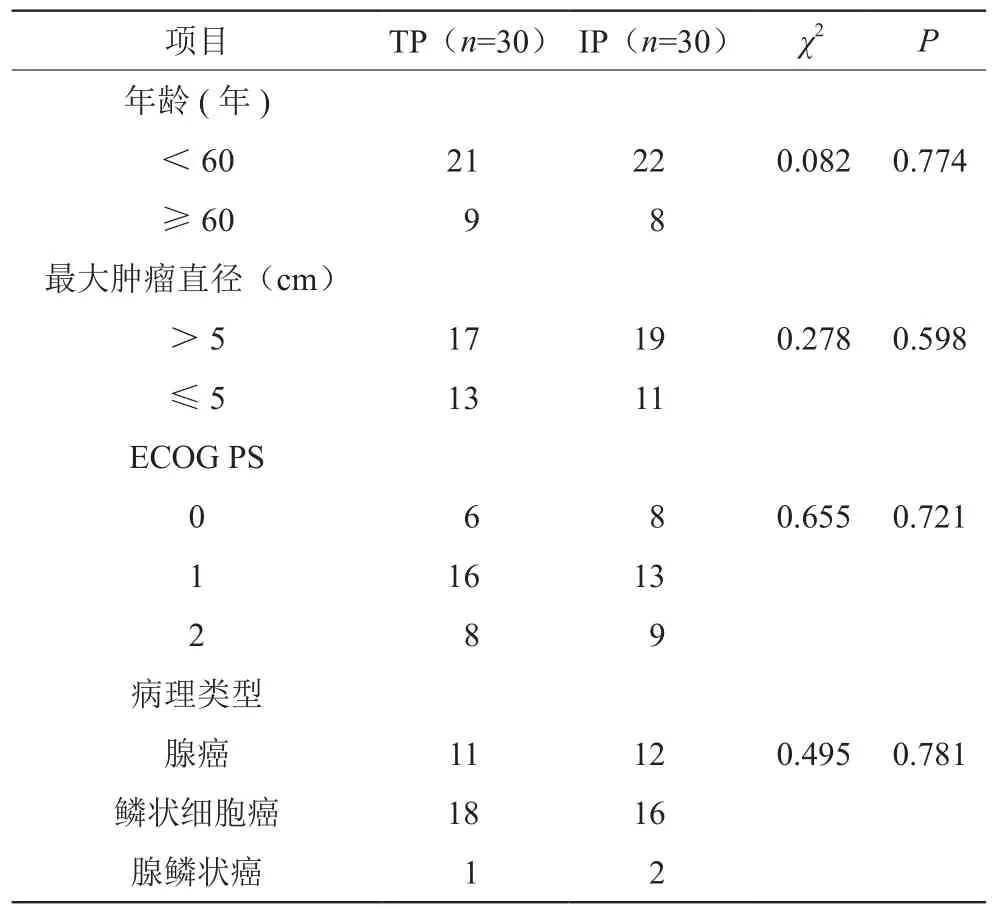
表1 两组一般资料比较
1.2 治疗方案
TP组患者采用紫杉醇135 mg/m2,第1天;顺铂80 mg/m2,第2天,静脉滴注,21 d为一个周期,至少2个周期。IP组采用伊立替康90 mg/m2,第1、8天;顺铂80 mg/m2,第2天,静脉滴注,21 d为一个周期,至少2个周期。化疗期间常规止吐、护胃处理,对白细胞下降者给予粒细胞集落刺激因子治疗,每周复查血常规,每4周复查血生化及肝肾功能,治疗前及2个周期治疗后全面复查,记录两组接受治疗至疾病进展或出现不能耐受的不良反应。
1.3 评价标准
1.3.1 近期疗效评估依据WHO实体瘤疗效评定标准[7],于治疗前及治疗后对患者进行影像学检查,并评估治疗效果:完全缓解(complete remission,CR),所有可见靶病灶完全消失;部分缓解(partial remission,PR),肿瘤靶病灶的最大横径与最大垂直径的乘积缩小50%以上;疾病稳定(stable disease,SD),肿瘤病灶变化介于PR和PD之间;疾病进展(progression of disease,PD),肿瘤靶病灶的最大横径与最大垂直径的乘积增加25%或有新发肿瘤出现;其中CR和PR至少持续4周。
客观缓解率(ORR)=(CR+PR)/总例数×100%。
疾病控制率(DCR)=(CR+PR+ SD)/总例数×100%。
1.3.2 远期疗效治疗结束后,每2个月随访1次,随访截止至2017年10月30日。记录患者总生存期(overall survival,OS)和无进展生存期(progression free survival,PFS)。OS为患者自治疗开始至死亡或末次随访的时间,PFS为患者自治疗开始至疾病进展或其他原因死亡的时间。
1.3.3 安全性评价每个治疗周期记录不良反应的发生情况,不良反应按照常见不良反应事件评价标准4.0版本进行评价[8]。
1.4 统计方法
采用统计软件SPSS 19.0处理数据,计数资料采取χ2检验或秩和检验,PFS和OS生存分析采用Kaplan-Meier法,两组间生存时间的比较采用Logrank检验,P<0.05为差别有统计学意义。
2 结果
2.1 近期疗效
TP组CR 1例、PR 12例、SD 10例、PD 7例,IP组CR 1例、PR 16例、SD 8例、PD 5例;TP组和IP组患者的ORR分别为43.3%和56.7%,DCR分别为76.7%和83.3%。两组ORR和DCR比较,差异无统计学意义(P>0.05)。见表2。

表2 两组近期疗效比较
2.2 远期疗效
截止至2017年10月30日,TP组患者的随访时间为2~12个月,中位随访时间为6个月,IP组患者的随访时间为1~13个月,中位随访时间为6.5个月;TP组和IP组患者的OS分别为8.7个月和10.4个月,95%可信区间(confidence interval,CI)分别为7.2~10.2个月和8.8~12.1个月,两组比较差异无统计学意义(P=0.274)(图1);TP组和IP组患者的PFS分别为5.5个月和7.5个月,95% CI分别为4.6~6.4个月和6.7~8.3个月,IP组高于TP组,差异有统计学意义(P=0.015)(图2)。

图1 两组患者的总生存曲线

图2 两组患者的无进展生存曲线
2.3 不良反应
化疗期间,两组白细胞减少、血小板减少及贫血发生率比较,差异无统计学意义(P>0.05);TP组肝肾功能异常及脱发发生率高于IP组,差异有统计学意义(P=0.018);两组恶心呕吐和腹泻等非血液学不良反应发生率比较,差异无统计学意义(P>0.05)。见表3。

表3 两组不良反应发生率比较
3 讨论
晚期宫颈癌患者通常已经失去手术机会,而系统地化疗可有效降低肿瘤的转移和复发,提高患者的生存率。近年来,越来越多的研究集中于晚期宫颈癌化疗药物的探索,并取得了一定的进展,但晚期宫颈癌患者治疗失败率仍较高,平均生存期只有7~12个月,因此需要寻找新的化疗方案或治疗药物。
伊立替康为半合成水溶性喜树碱衍生物,是拓扑异构酶Ⅰ抑制剂,主要作用于肿瘤细胞周期的S期,高浓度伊立替康可引起DNA双链断裂,并通过转化为7-乙基-10羟基喜树碱活性产物而发挥抗肿瘤作用[9]。同时伊立替康也能使周围正常细胞死亡,所导致的不良反应主要有胃肠道反应、骨髓抑制、肝肾功能损害和胆碱能综合征等,并且随着药物浓度的增加不良反应的发生率也随之增加,应根据实验室检查结果及时调整用量或停止用药[10]。有研究显示,伊立替康单独用于局部晚期宫颈癌化疗有效率可达70%,但与铂类、吉西他滨、氟尿嘧啶等联合应用可提高总有效率[11],本研究采用顺铂联合伊立替康化疗治疗晚期宫颈癌。
紫杉醇联合顺铂是目前临床治疗宫颈癌的一线化疗方案,紫杉醇具有广泛的抗肿瘤作用,它主要作用于细胞微管系统,促进微管蛋白聚合,抑制微管有丝分裂过程,从而阻止肿瘤细胞分裂、增殖,促使肿瘤细胞凋亡。由于紫杉醇不溶于水,使用时常采用聚氧乙烯蓖麻油等辅料助溶,而该物质在体内降解时可释放组胺从而导致严重的过敏反应,临床应用时需给予患者地塞米松及H2受体拮抗剂预处理,以减轻过敏反应。
本研究选择了60例晚期宫颈癌患者,分别采用TP和IP方案治疗,并比较这两种方案的效果,结果显示,两组ORR、DCR、OS比较差异无统计学意义,IP组PFS显著高于TP组(P=0.015),说明两种方案治疗晚期宫颈癌的疗效相当,但IP方案可改善患者的PFS。
治疗过程中发生的不良反应主要为骨髓抑制、胃肠道反应、肝肾功能损伤和脱发,其中骨髓抑制主要表现为中性粒细胞减少、血小板减少和贫血,两组发生率比较差异无统计学意义(P>0.05);胃肠道反应主要为恶心呕吐和腹泻,两组发生率比较差异无统计学意义(P>0.05);TP组肝肾功能损伤和脱发发生率明显高于IP组(P<0.05)。两组患者均无失访及治疗相关的死亡事件发生,说明IP方案的安全性更好。
IP方案与TP方案治疗晚期宫颈癌的近期疗效相当,但IP方案的安全性更高,且可明显改善患者的无进展生存时间,值得临床应用和推广。本研究样本量较小且研究时间有限,两种方案在近期疗效和总生存期方面的优劣需要多中心、大样本的前瞻性临床研究来进一步验证和探讨。

