注射用血塞通(冻干)治疗脑梗死后遗症期瘀血阻滞证的临床有效性研究
田文杨 李楠楠 孟繁兴 高芳 李学军 马丽珍 蔡英丽 陈志刚


摘要 目的:评价注射用血塞通(冻干)治疗脑梗死后遗症瘀血阻滞证的安全性和有效性。方法:本研究以灯盏细辛注射液为阳性对照,采用随机、盲法、阳性药对照、多中心临床研究,选取2015年1月至2017年1月7个分中心收治的脑梗死后遗症期瘀血阻滞证患者108例作为研究对象,随机分为观察组(n=72)和对照组(n=36)。2组均使用阿司匹林作为基础用药,给药周期为15 d。分别在基线点和试验终点对安全性及有效性指标进行评定。结果:观察组不良事件发生率为4.17%,對照组不良事件发生率为5.71%。2组间不良事件发生率比较差异无统计学意义(P>0.05)。主要疗效指标:1)观察组中医证候疗效、总有效率和愈显率均优于对照组,2组比较差异有统计学意义(P<0.05);2)美国国立卫生研究所卒中量表(NIHSS)评分疗效:2组试验前后患者肢体功能均有所改善,但2组比较差异均无统计学意义(P>0.05);3)2组间改良Rankin量表评分比较差异均无统计学意义(P>0.05)。次要疗效指标,1)单项症状疗效统计分析显示:口舌歪斜、舌强言謇或不语、偏身麻木、头晕等症状比较,组间比较差异均有统计学意义(P<0.05),观察组疗效优于对照组;上肢不遂、下肢不遂、头痛、口唇紫暗等组间比较,差异均无统计学意义(P>0.05);2)Barthel指数疗效分析结果显示,用药后Barthel指数及基线与用药后Barthel指数差值和变化率,2组比较差异均无统计学意义(P>0.05)。结论:注射用血塞通(冻干)治疗脑梗死(后遗症期)(瘀血阻滞证)疗效确切,能有效改善患者的中医症状及单项症状,疗效优于灯盏细辛注射液,且本品能有效改善患者的肢体功能和生命质量;临床使用安全,临床不良反应为轻度,无严重的不良事件发生。
关键词 血塞通;缺血性中风;瘀血阻滞证;脑梗死后遗症期;临床研究;随机对照;多中心;有效性
Clinical Efficacy of Freeze-Dried Xuesaitong Injection in the Treatment of Sequelae of Cerebral Infarction with Blood Stasis Syndrome
Tian Wenyang1, Li Nannan2, Meng Fanxing2, Gao Fang2, Li Xuejun2, Ma Lizhen2, Cai Yingli2, Chen Zhigang2
(1 Beijing University of Chinese Medicine, Beijing 100029, China; 2 Department of Encephalopathy, Dongfang Hospital, Beijing University of Chinese Medicine, Beijing 100078, China)
Abstract Objective:To evaluate the efficacy and safety of freeze-dried Xuesaitong Injection in the treatment of sequelae cerebral infarction with blood stasis syndrome.Methods:In this study, Dengzhan Xixin Injection was used as a positive control.A randomized, blind method, a positive drug control, and a multicenter clinical study were used.A total of 108 cases of patients with sequelae cerebral infarction with blood stasis syndrome from 7 centers during January 2015 to January 2017 were selected and randomly divided into an experimental group(Xuesaitong Injection)and a control group(Dengzhan Xixin Injection).Aspirin was used as a base drug in both groups, with a course of treatment of 15 days.Safety and efficacy indexes were evaluated at baseline and at the end of the test.Results:In terms of safety evaluation, the incidence of adverse events was 4.17% in the experimental group and 5.71% in the control group.The incidence of adverse reactions showed no statistical differences among each group(P>0.05).In terms of efficacy evaluation, the primary outcome:The efficacy of TCM syndromes(efficacy of TCM syndromes, total effective rate and increasing apparent rate)in the experiential group was better than that in the control group, and there was statistically significant difference in both groups(P<0.05).The results in National Institutes of Health Stroke Scale(NIHSS)score showed that the limb function of patients in both groups improved, but no statistical differences between two groups(P>0.05).Modified Rankin Scale(mRS)score showed that there was no statistically significant difference between the 2 groups(P>0.05).The secondary outcome:The results of single symptom efficacy showed that comparing the secondary symptom of dizzy and the main symptom of hemianesthesia, deviation of the eye and mouth, stiff tongue of the 2 groups, the difference was statistically significant(P<0.05), and the efficacy of the experimental group was better than that of the control group.Comparing the primary symptoms of motor impairment of the upper/lower limbs and secondary symptoms of headache, purple lips of the 2 groups, the differences were not statistically significant(P>0.05).The results of the Barthel index efficacy analysis showed that there was no statistically significant difference in the Barthel index and the difference and change rate between the baseline and post-dose Barthel index after treatment(P>0.05).Conclusion:Application of freeze-dried Xuesaitong Injection in the treatment of sequelae cerebral infarction with blood stasis syndrome presents certain efficacy in the improvement of TCM syndromes and single symptoms.The efficacy was better than the control group of Dengzhan Xixin Injection.It can effectively improve the limb function and life of quality, and it has high safety in clinical use, with mild adverse reactions and no serious adverse events.
Key Words Xuesaitong; Ischemic stroke; Blood stasis syndrome; Sequelae of cerebral infarction; Clinical research; Randomized control; Multicenter; Effectiveness
中图分类号:R255.2文献标识码:Adoi:10.3969/j.issn.1673-7202.2019.12.031
脑梗死是指因脑部血液循环障碍,缺血、缺氧所致的局限性脑组织的缺血性坏死或软化,而出现相应的神经功能缺损。在中医学中属于“中风病”的范畴,以猝然昏仆、口舌歪斜、半身不遂、语言不利为主要表现[1]。临床分期上,我们将脑梗死发病6个月以上的时期称为脑梗死后遗症期。这一时期根据脑组织缺血病灶所在部位的不同,可出现不同的神经功能缺损症状,若影响运动神经,则可导致肢体偏瘫后遗症;若影响语言中枢,则可导致言语功能障碍等。减少脑组织缺血灶的形成或清除病灶,改善脑梗死后遗症期遗留症状,提高患者生命质量是脑梗死后遗症的治疗关键。针对这一问题,本研究以灯盏细辛注射液为阳性对照,采用随机、盲法、阳性药对照、多中心临床研究,观察三七制剂血塞通(冻干)治疗脑梗死后遗症瘀血阻滞证的安全性和有效性。
1 资料与方法
1.1 一般资料 选取2015年1月至2017年1月北京中医药大学东方医院、钦州市中医院、临沂市人民医院、襄阳市中心医院、驻马店市中医院、重庆市第九人民医院及廊坊市中医医院等7家分中心的脑梗死后遗症期瘀血阻滞证住院患者108例作为研究对象,随机分为观察组(n=72)和对照组(n=36)。本研究经过伦理委员会审批[京东方(伦)审批号:2012081504-2]。
1.2 诊断标准
1.2.1 西医诊断标准 大动脉粥样硬化性脑卒中(Largearteryatherosclerosis,LAA),参照目前国际公认对缺血性脑血管病的病因学TOAST亚型分类标准拟定。临床上通过颈动脉超声波扫描或多普勒扫描发现颈动脉闭塞或狭窄(狭窄达到动脉横断面的50%);通过血管造影或MRA发现颈动脉、大脑前动脉、大脑中动脉、大脑后动脉、椎基底动脉狭窄达到动脉横断面的50%;其发生可能由于脑动脉粥样硬化所致。临床上如出现以下表现,对诊断LAA有重要价值。1)患者病史中曾出现多次的短暂脑缺血发作(TIAs),且多为同一条动脉供应区内的多次发作;2)临床上出现失语、忽视、运动功能受损症状或有小脑、脑干受损症状;3)临床检查可发现颈动脉听诊有杂音,脉搏减弱、血压双侧不对称等;4)脑CT或MRI扫描可发现有皮质或小脑损害,或皮质下、脑干损害大于1.5 cm,可能为潜在的大动脉粥样硬化所致的缺血性脑卒中;5)彩色多普勒超声、TCD、MRA或DSA检查可发现相关的颅内或颅外动脉及其分支狭窄、程度大于动脉横面的50%,或有闭塞;6)应排除心源性栓塞所致的脑卒中。
1.2.2 中医诊断标准
1)中风病诊断标准:参照国家中医药管理局脑病急症科研协作组起草制订的《中风诊断疗效评定标准》(试行)拟定。主症:偏瘫、意识昏蒙、舌强言謇或不语、偏身感觉异常、口舌歪斜;次症:头痛,眩晕,瞳神变化,饮水发呛,目偏不瞬,共济失调;急性起病,发病前多有诱因,常有先兆症状;发病年龄多在40岁以上。具备2个主症以上,或1个主症2个次症,结合起病、诱因、先兆症状、年龄即可确诊;不具备上述条件,结合影像学检查结果亦可确诊。
2)中风病分期标准:参照《中药新药治疗中风病的临床研究指导原则》(2002年版)[3]。急性期:发病2周以内,中脏腑最长1个月;恢复期:发病2周至6个月;后遗症期:发病6个月后。
3)中风病中经络标准:中风病无神识昏蒙者。
4)瘀血阻滞证中风病中医辨证标准:根据注射用血塞通(冻干)的处方组成和功能主治,参照《中药新药治疗中风病的临床研究指导原则》(2002年版),选择瘀血阻滞证作为观察证型。主症:a.半身不遂;b.口舌歪斜;c.舌強言謇或不语;d.偏身麻木。次症:a.头痛;b.头晕;c.口唇紫暗。舌脉:舌质紫暗或有瘀斑、瘀点;脉沉涩。中风病诊断成立,兼见上述主症2项,次症1项,结合舌象、脉象即可确定入选。
1.3 纳入标准 1)符合西医对大动脉粥样硬化性脑梗死的诊断标准;2)符合中医中风-中经络瘀血阻滞证的证候辨证标准;3)经诊断为前循环障碍者;4)病程在6~9个月以内(含6个月、9个月);5)神经功能缺损(NIHSS)评分>7分且<21分患者;5)年龄在35~75岁(包括35、75岁)之间;6)签署知情同意书者。
1.4 排除标准 1)经诊断为短暂性脑缺血发作、脑出血、脑栓塞、腔隙性梗死、蛛网膜下腔出血者;2)脑梗死急性期及恢复期;3)既往有脑出血病史;4)经检查证实由脑肿瘤、脑外伤,脑寄生虫病,代谢障碍,风湿性心脏病、冠心病及其它心脏病合并房颤引起脑栓塞者;5)有慢性肝、肾功能障碍者,其中肝功损害ALT、AST>正常上限2倍者,肾功损害血肌酐(Cr)>正常上限者;6)妊娠或哺乳期妇,对三七、酒精过敏或易过敏体质者;7)合并有严重心、肺、肝、肾疾病者;8)最近3个月内参加其他临床试验的患者。
1.5 脱落与剔除标准 1)出现过敏反应或严重不良事件,根据医生判断应停止试验者;2)试验过程中病情恶化,根据医生判断应该停止临床试验,接受其他有效治疗;3)受试者依从性差(依从性<80%或>120%),或自动中途换药或加用本方案禁止使用的中西药物者;4)各种原因的中途破盲病例;5)无论何种原因,患者不愿意或不可能继续进行临床试验,向主管医生提出退出试验要求而中止试验者;6)受试者虽未明确提出退出试验,但不再接受用药及检测而失访者。
1.6 治疗方法
1.6.1 试验用药 观察组:注射用血塞通(冻干)(昆明制药集团股份有限公司,国药准字Z20026438),注射用血塞通(冻干)400 mg,以0.9%氯化钠注射液250 mL稀释,缓慢静脉点注(20~40滴/min),1次/d。对照组:灯盏细辛注射液(云南生物谷灯盏花药业有限公司,国药准字Z53021569),灯盏细辛注射液40 mL,以0.9%氯化钠注射液250 mL稀释,缓慢静脉滴注(20~40滴/min),1次/d。基础用药:阿司匹林肠溶片(拜耳医药保健有限公司,国药准字:J20080078),口服,1片/次,1次/d(如有阿司匹林过敏患者,可改用其他同类型药物,并在合并用药中详细记录用法用量)。所有试验药品在输液前须用深色袋包装遮蔽,输液时使用深色输液器,以保证盲法实施。疗程为15 d。
1.6.2 盲法的实施 采用区组随机盲法、阳性药平行对照,多中心设计方法。专业统计人员(编盲者)负责用SAS软件产生中心编码分配随机数字、试验病例分配随机数字、处理组分配随机数字,以及试验病例随机编码表。在试验研究过程中对于符合入组标准的患者根据筛选合格的顺序先后分配药物编号,各中心护士长或药品管理员根据药物编号进行配液输液。在试验研究中试验药、对照药的注射剂均用深色纸袋包装遮蔽,由不参加试验的药房发药,护士按照药物编号进行配液输液,输液时用深色输液器输液。同时受试者均不知道所用何药,也不能问询有关药品的性状等可分辩出药物的问题,受试者回访也只谈和疗效、不良反应等相关内容。剩余药的回收由发药人负责。
1.7 观察指标
1.7.1 疗效性指标 1)美国国立卫生研究所卒中量表(NIHSS);2)改良Rankin量表;3)中医证候积分;4)单项症状疗效评定;5)Barthel指数。以NIHSS量表、改良Rankin量表及中医证候积分为主要评价指标。
1.7.2 安全性观察 1)试验中出现的不良事件(用药后随时观察);2)一般体检项目(包括体温、静息心率、呼吸、血压等);3)血常规、网织红细胞计数、尿常规、便常规、潜血、心电图和肝功能(AST、ALT、TBIL、γ-GT、ALP)、肾功能(BUN、Cr)、凝血四项等。以不良反应发生率为主要安全性评价指标。
1.7.3 观察时点 1)人口学资料、诊断性指标:基线点诊查,部分指标试验终点复查;2)中医证候和一般体检项目:每次就诊时诊查;3)试验中出现的不良事件:用药后随时观察;4)实验室指标:基线点、试验终点诊查。属于安全性指标疗前正常疗后异常且有临床意义者,应定期复查至随访终点。
1.8 疗效判定标准
1.8.1 病证疗效评价标准
1)主要疗效指标判定:参照1995年中华医学会第四次全国脑血管病学术会议通过的疗效评定标准制定。a.美国国立卫生研究所卒中量表(NIHSS)评价标准:基本痊愈:NIHSS量表评分减少≥90%;显著进步:NIHSS量表评分减少>45%<90%;进步:NIHSS量表评分减少≥18%≤45%;无变化:NIHSS量表评分减少或增加<18%;恶化:NIHSS量表评分增加>18%。组间NIHSS评分按0~1分、2~8分、≥9分、死亡4个级别例数分别占总病例数百分比进行统计。b.改良Rankin量表评价标准:采用相应的统计学方法对治疗前后不同级别(具体按0~1分、2~3分、4~5分、死亡四个级别)的构成比进行卡方分析,评价疗前疗后的差异和相应的趋势。c.中医证候疗效评定:疗效指数(n)=(治疗前总积分-治疗后总积分)/治疗前总积分×100%,临床痊愈:中医临床症状、体征消失或基本消失,症候积分减少≥95%;显效:中医临床症状、体征明显改善,症候积分减少≥70%且<95%;有效:中医临床症状、体征均有好转,症候积分减少≥30%且<70%;无效:中医临床症状、体征均无明显改善,甚或加重,症候积分减少不足30%。
2)次要疗效指标判定:
a.单项症状疗效评定标准:痊愈:症状消失;显效:症状明显好转(单项积分减少2个级别);有效:症状好转(单项积分减少1个级别);无效:症状无变化、或加重者。b.Barthel指数疗效判定标准:按95~100、55~90、0~50、死亡4个级别进行组间比较;以基线值为协变量,对治疗前后的差值及变化率进行方差分析,同时考虑中心效应的影响。
1.8.2 不良事件轻重程度判断标准 轻度:受试者可忍受,不影响治疗,不需要特别处理,对受试者康复无影响;中度:受试者难以忍受,需要撤药中止试验或做特殊处理,对受试者康复有直接影响;重度:危及受试者生命,致死或致残,需立即撤药或做紧急处理。
1.9 统计学方法 采用SPSS 21.0统计软件包对数据进行分析,计量资料以均数、標准差、例数、最小值和最大值,或加用中位数、上四分位数(Q1)、下四分位数(Q3)、95%可信区间描述,组间或组内治疗前后对比分析,先对变量分布进行正态检验,服从正态分布时,用t检验或自身t检验;非正态分布,用非参数统计方法。若考虑到中心或其他因素的影响,用协方差分析。计数资料以频数表、百分率或构成比描述,2组组间或组内治疗前后比较用χ2检验、Fisher精确概率法、Wilcoxon秩和检验或Wilcoxon符号秩和检验;两分类指标及等级指标的比较若考虑到中心或其他因素的影响,采用CMH-χ2检验。若考虑基线混杂因素的影响,采用logistic回归分析。除优效性检测外,假设检验统一使用双侧检验,取α=0.05,以P<0.05为差异有统计学意义。
2 结果
2.1 入组基线情况比较 本研究共纳入病例108例,数据完整患者共107例,其中观察组72例、对照组35例。对2组受试者入组时人口学资料(性别、年龄、体重、身高)、生命体征资料(静息心率、呼吸、血压、体温)、疾病基线情况(病程、发病次数、治疗药物、治疗手段、药物过敏史、目前患有其他疾病)、中医证候量化积分(中医证候总积分及单项症状积分)、卒中量表(NIHSS)、改良Rankin量表和Barthel指数基线情况比较,差异均无统计学意义(P>0.05),具有可比性。
2.2 疗效评价
2.2.1 主要疗效指标
1)NIHSS评分疗效比较:NIHSS评分构成统计分析结果显示,观察组0~1分2例,占2.78%;2~8分68例,占94.44%;≥9分2例,占2.78%;死亡0。对照组0~1分0例;2~8分33例,占94.29%;≥9分2例,占5.71%;死亡0。2组比较差异无统计学意义(P=0.638 7);2组NIHSS评分疗效评价比较,虽治疗前后患者肢体功能均有所改善,但2组比较差异无统计学意义(P=0.395 9)。见表1。
2)改良Rankin量表疗效构成比较:用药后2组改良Rankin量表疗效构成差异无统计学意义(P=0.275 7)。改良Rankin量表评分疗效构成统计分析结果显示,经过治疗后2组评分疗效构成比较差异无统计学意义(P=0.191 0)。见表2。
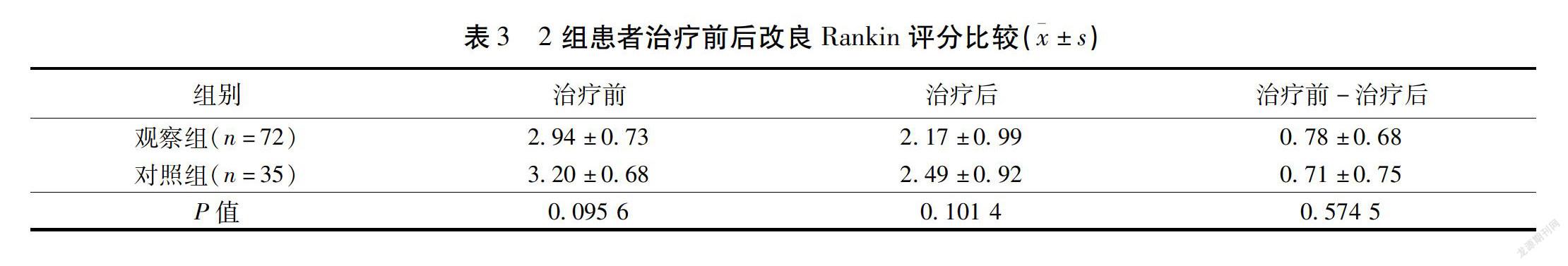
3)改良Rankin量表评分比较:2组治疗后改良Rankin评分及治疗前后评分差值比较差异均无统计学意义(P>0.05)。见表3。
4)中医证候疗效比较:2组中医证候疗效比较差异有统计学意义(P=0.002 5)。见表4。
2.2.2 次要疗效指标
1)单项症状疗效:2组主症“口舌歪斜”“舌强言謇或不语”“偏身麻木”和次症“头晕”比较,差异均有统计学意义(P<0.05);2组主症“上肢不遂”“下肢不遂”和次症“头痛”“口唇紫暗”比较,差异均无统计学意义(P>0.05)。
2)Barthel指数评分疗效评价:2组用药后Barthel指数及用药前后Barthel指数差值及变化率比较差异均无统计学意义(均P>0.05)。见表5。
2.3 安全性评价 本次临床试验共有5例不良事件发生,不良事件发生率为4.67%,其中观察组3例,不良事件发生率为4.17%,对照组有2例,不良事件发生率为5.71%。2组间不良事件发生率比较差异无统计学意义(P>0.05)。对受试者治疗前后生命体征和安全性实验室检查指标情况分析显示,注射用血塞通(冻干)对心、肝、肾、胃肠及血液系统等无不良影响,证明试验药物具有较好的安全性。
3 讨论
脑卒中主要分为缺血性脑卒中和出血性脑卒中两大类,其中缺血性脑卒中约占卒中患者总数的75%~85%[2],具有很高的發病率,同时存在高致残率和高复发率的特点。脑梗死发病6个月以上的时期为脑梗死后遗症期,根据病灶部位的不同,遗留不同程度的认知、情感和肢体功能障碍,严重者患者生活不能自理,给患者、家庭和社会带来沉重负担[3]。目前对于脑梗死的治疗以溶栓、血管介入治疗[4]、抗栓(抗血小板治疗、抗凝治疗)治疗、稳定斑块、改善脑侧支循环、脑保护等治疗为主,对于改善脑梗死遗留的不同程度的神经功能缺损症状具有一定局限性,目前国内外缺乏对于脑梗死后遗症期的标准治疗方案。中医药治疗脑梗死后遗症具有独特的优势。
中医学认为,本病属于“中风病”范畴,主要病机责之于阴阳失调、气血逆乱,病程日久,气虚渐甚,血液运行不畅、脉络瘀阻,瘀血阻滞肢体经络则见肢体活动不利、麻木,瘀血阻于舌窍则见言语不利,由此可见血瘀是后遗症期的主要病理因素。三七味甘、微苦、性温,归肝、胃经,治以散瘀止血,消肿定痛[5],《中国医药大辞典》记载:“三七功用补血,去瘀损,止血衄,能通能补,功效最良,是方药中之最珍贵者”。三七制剂可有效改善脑梗死患者神经功能损伤、提高患者生命质量以及恢复相关血液流变指标[6],三七可通过改善血液循环、脑衍生神经营养因子(BDNF)改善脑梗死大鼠的学习和记忆能力[7]。
本研究所用注射用血塞通(冻干)主要成分是三七总皂苷,三七总皂苷是三七的重要成分。三七总皂苷能促进急性缺血性中风病患者的白质纤维结构重塑,细胞毒性水肿及血管源性水肿得到改善,灰质功能得到恢复[8]。现代药理研究表明,三七总皂苷可通过抑制血小板活性、提高内皮祖细胞数量、促进纤维蛋白原活性、抑制炎性因子释放及清除氧自由基等机制改善动脉粥样硬化、抗血栓形成[9-10]。三七总皂苷改善脑梗死后神经受损情况[11-13],一方面调节促/抗炎因子的表达[14]、抑制兴奋性氨基酸毒性和Ca2+内流、抗自由基的毒性损伤改善脑梗后神经元细胞和脑组织的损伤;另一方面通过抑制凋亡调控基因,促进周围神经细胞再生保护脑组织[15]。研究[16]发现,三七总皂苷刺激骨髓中干细胞因子的产生,并通过降低粘附分子对骨髓间充质干细胞的黏附作用促进骨髓间充质干细胞向血浆的动员,改善梗死区的微环境,提高梗死区干细胞的存活率,促进干细胞分化为神经细胞,其作用机制与中医所说促进血液循环,消除血瘀的作用相一致。从药代动力学角度来说,三七总皂苷与阿司匹林联用时存在药代动力学药物-药物相互作用[17],不仅可增加三七总皂苷的吸收也可显著提高阿司匹林的浓度[18],同时抑制小肠吸收过程中阿司匹林的水解,从而提高其生物利用度[19]。脑梗死后遗症期患者需进行二级预防,三七总皂苷不仅具有良好的抗动脉粥样硬化、抗血栓形成作用、激活抗氧化剂保护大脑微血管内皮细胞[20],而且可增加阿司匹林的浓度,联用三七总皂苷制剂可使脑梗死后遗症患者获得更大收益,与此同时,三七总皂苷可从减少脑组织损伤及增加神经元再生两方面保护脑组织,改善脑梗死后患者神经功能损伤,由此可知注射用血塞通改善脑梗死后遗症期患者症状证据充分。
本研究采用多中心、随机、双盲、阳性药平行对照临床研究,以行业公认中西医量表作为疗效评价标准,以临床广泛应用的灯盏细辛注射液作为对照药,结果表明,注射用血塞通(冻干)改善脑梗死(后遗症期)(瘀血阻滞证)患者中医临床证候疗效确切,能有效改善患者的中医症状及单项症状,疗效优于阳性对照组灯盏细辛注射液;能有效改善患者的肢体功能和生命质量;NIHSS评分、Barthel指数及改良Rankin评分方面,注射用血塞通组较对照组没有统计学差异,但是从分值比较上与对照组比较具有优势。临床安全性评价方面,临床不良反应为轻度不良反应,无严重的不良事件发生。因此,在脑梗死后遗症期瘀血阻滞证的临床治疗中,注射用血塞通(冻干)安全有效。
参考文献
[1]中国中西医结合学会神经科专业委员会.中国脑梗死中西医结合诊治指南(2017)[J].中国中西医结合杂志,2018,38(2):136-144.
[2]Wang Y,Cui L,Ji X,et al.The China National Stroke Registry for patients with acute cerebrovascular events:design,rationale,and baseline patient characteristics[J].Int J Stroke,2011,6(4):355-361.
[3]刘海涛,王波,刘德喜.养阴通络丸联合针刺治疗脑梗死后遗症的临床疗效观察[J].广州中医药大学学报,2015,32(1):23-26.
[4]Powers WJ,Derdeyn CP,Biller J,et al.2015 American Heart Association/American Stroke Association Focused Update of the 2013 Guidelines for the Early Management of Patients With Acute Ischemic Stroke Regarding Endovascular Treatment:A Guideline for Healthcare Professionals From the American Heart Association/American Stroke Association[J].Stroke,2015,46(10):3020-3035.
[5]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015:11-12.
[6]齐家.三七制剂治疗急性中风临床疗效的系统评价[D].北京:北京中医药大学,2016:55-57.
[7]Chuang CM,Hsieh CL,Lin HY,et al.Panax Notoginseng Burk attenuates impairment of learning and memory functions and increases ED1,BDNF and beta-secretase immunoreactive cells in chronic stage ischemia-reperfusion injured rats[J].Am J Chin Med,2008,36(4):685-93.
[8]任珊.结合功能磁共振评价联合三七总皂苷对中风病患者神经重塑的研究[D].北京:北京中医药大学,2017.
[9]方鹏飞,常丽霞,宋渊.三七总皂苷临床应用研究进展[J].中医药学报,2016,6(44):120-123.
[10]丁小明,许嵘.三七总皂苷对大鼠局灶性脑缺血再灌注后IL-10及TNF-α表达的影响[J].局解手术学杂志,2017,26(9):634-637.
[11]Liu L,Zhu L,Zou Y,et al.Panax notoginseng saponins promotes stroke recovery by influencing expression of Nogo-A,NgR and p75NGF,in vitro and in vivo[J].Biol Pharm Bull,2014,37(4):560-568.
[12]余昌東,邱雄泉,梅全喜.三七总皂苷对脑血管的药理作用研究新进展[J].中国医疗前沿,2008,3(14):37-39.
[13]聂娟,唐标.基于系统药理学分析三七总皂苷干预脑血管疾病的作用机制[J].湖南中医药大学学报,2018,38(9):1032-1037.
[14]Shi X,Yu W,Liu L,et al.Panax notoginseng saponins administration modulates pro-/anti-inflammatory factor expression and improves neurologic outcome following permanent MCAO in rats[J].Metab Brain Dis,2017,32(1):221-233.
[15]刘抒雯,刘敬霞,虎喜成,等.三七总皂苷治疗缺血性脑卒中研究进展[J].中国实验方剂学杂志,2015,21(15):217-220.
[16]Jin-sheng Zhang,Bao-xia Zhang,Mei-mei Du,et al.Chinese preparation Xuesaitong promotes the mobilization of bone marrow mesenchymal stem cells in rats with cerebral infarction[J].Neural Regen Res,2016,11(2):292-297.
[17]Tian Z,Pang H,Du S,et al.Effect of aspirin on the pharmacokinetics and absorption of panax notoginseng saponins[J].J Chromatogr B Analyt Technol Biomed Life Sci,2018,1074-1075:25-33.
[18]Tian Z,Pang H,Du S,et al.Effect of Panax notoginseng saponins on the pharmacokinetics of aspirin in rats[J].J Chromatogr B Analyt Technol Biomed Life Sci,2017,1040:136-143.
[19]Sun Z,Wu Y,Yang B,et al.Inhibitory Influence of Panax notoginseng Saponins on Aspirin Hydrolysis in Human Intestinal Caco-2 Cells[J].Molecules,2018,23(2):455.
[20]Hu S,Wu Y,Zhao B,et al.Panax notoginseng Saponins Protect Cerebral Microvascular Endothelial Cells against Oxygen-Glucose Deprivation/Reperfusion-Induced Barrier Dysfunction via Activation of PI3K/Akt/Nrf2 Antioxidant Signaling Pathway[J].Molecules,2018,23(11):2781.
(2019-01-06收稿 责任编辑:芮莉莉)

