基于传统煎药工艺的川牛膝饮片标准汤剂制备及质量评价方法研究
孙博 常阿倩 朱广伟 徐腾腾 曲缘章 李西文 李琦 杉田亨 友田健久


摘要 目的:制备来自于不同产地的15批次川牛膝饮片标准汤剂,并以其出膏率、指标成分含量及转移率、指纹图谱等数据为指征进行研究。方法:参照传统煎药工艺制备标准汤剂,采用UPLC-DAD法测定指标成分含量,计算转移率、出膏率及指纹图谱数据研究。结果:15批次川牛膝样品制成的标准汤剂中杯苋甾酮含量为0.066~0.210 mg/mL,转移率为61.27%~99.69%,平均轉移率为73.27%,标准偏差为11.88%。出膏率范围为17.66%~31.45%,平均出膏率为24.48%,标准偏差为4.54%。指纹图谱共有峰11个,确认1个,为杯苋甾酮(C29H44O8)。结论:本研究建立的制备工艺符合传统汤剂制备方法,且稳定可行,可用于川牛膝饮片标准汤剂的制备及质量评价,并为配方颗粒、经典名方研究及工业化生产提供基本的数据支撑和参考。
关键词 川牛膝;标准汤剂(标准煎液);配方颗粒;UPLC-DAD;指纹图谱;杯苋甾酮;转移率;经典名方
Study on Preparation and Quality Evaluation of the Standard Decoction of Radix Cyathulae Based on Traditional Decocting Process
Sun Bo1,2, Chang Aqian3, Zhu Guangwei1, Xu Tengteng4, Qu Yuanzhang4, Li Xiwen1, Li Qi5, Toru Sugita6, Takehisa Tomoda6
(1 Institute of Chinese Materia Medica, China Academy of Chinese Medical Sciences, Beijing 100700, China; 2 Harbin University of Commerce, Harbin 150076, China; 3 Beijing University of Chinese Medicine, Beijing 100102, China; 4 Shandong University of Traditional Chinese Medicine, Jinan 250355, China; 5 Shanghai Traditional Chinese Medicine Co., Ltd., Shanghai 200002, China; 6 Tsumura Corporation , Tokyo 107-8521, Japan)
Abstract Objective:To evaluate the extraction ration, content determination, transfer ration, and feature maps or fingerprints by establishing 15 batches of standard decoction of Radix Cyathulae from different places.Methods:The standard decoction was prepared based on the traditional decoction process, the content of index components, the extraction ration, the transfer ration and the fingerprints were evaluated by UPLC-DAD.Results:The determination of cyasterone in 15 batches of standard decoration was in the range of 0.066~0.210 mg/mL, the transfer rate of cyasterone was in the range of 61.27%~99.69%, the average transfer rate was 73.27%, and the standard deviation was 11.88%.The extraction rate was in the range of 17.66%~31.45%, the average extraction rate was 24.48% and the standard deviation was 4.54%.11 peaks of fingerprint were confirmed in this research, and cyasterone was identified as cyasterone(C29H44O8).Conclusion:The preparation method in this paper is consistent with the traditional preparation method, which is stable and feasible.It can be used for the standard preparation and quality evaluation of the standard decoction of Radix Cyathulae.It is also able to provide both basic data and reference in the research and industrial production of dispensing granule and classical prescription.
Key Words Radix Cyathulae; Standard decoction; Dispensing granules; UPLC-DAD; Fingerprint; Cyasterone; Transfer rate; Classic prescriptions
中图分类号:R944.6+1;R283.6;R927.11文献标识码:Adoi:10.3969/j.issn.1673-7202.2019.12.010
川牛膝为著名川产道地药材,是苋科植物川牛膝Cyathula officinalis Kuan的干燥根,主要分布于四川、河北等地。具有活血祛瘀,通利关节,利水通淋之功效。其主要化学成分为生物碱和甾酮类[1-3]。
作为传统中药的代表药材之一,川牛膝多与其他饮片配伍煎汤剂服用。近年来,随着人们生活节奏的不断加快,中药饮片传统用药形式越来越难以满足人们的生活需求,配方颗粒作为传统中药饮片的有益补充应运而生。中药配方颗粒是由单味中药饮片经水提、浓缩、干燥、制粒而成的中药免煎颗粒制剂,可直接用于临床,具有易携带,易服用,方便配伍等诸多优点。但中药配方颗粒使用的原料药材产地广泛,制备工艺多样,各个厂家产品质量良莠不齐,临床应用时对于剂量的使用也没有统一的参照标准,质量标准的无法统一一直是中药配方颗粒乃至整个中药发展的关键问题。
2016年4月,陈士林等发表了《中药饮片标准汤剂研究策略》一文,指出了中药配方颗粒等多种饮片用药形式存在的问题,并表示中药饮片标准汤剂可为标化不同临床用药形式提供研究基础,并有效促进临床用药规范,减轻患者服药压力,加快中药标准化研究进程,统一制造工艺,利于有关部门有效监管監督[4]。同年8月,标准汤剂首次在官方文件《中药配方颗粒质量控制与标准制定技术要求(征求意见稿)》中(以下简称《技术要求》)得到具体阐述。《技术要求》中指出标准汤剂的制备除考虑中药药性,用药部位和置地等因素外,其制备过程还应充分研究古今文献。原国家食品药品监督管理总局在2017年10月发布的《中药经典名方复方制剂简化注册审批管理规定(征求意见稿)》(以下简称《征求意见稿》)提出了“标准煎液”这一概念。该《征求意见稿》也明确指出“标准煎液”是将古代经典医学书籍中所记录的经典古代名方制备方法为依据制备而得的中药药用物质。由此可见只有将传统中医理论与现代制备工艺标准技术相结合才能将中药推向世界[5]。
我们课题组(陈士林等)在标准汤剂研究方面具有扎实基础,发表相关中英文论文数十篇,并编写出版了《中药饮片标准汤剂》第一卷、第二卷,明确了200余种中药饮片标准汤剂的相关质量评价数据,为广大配方颗粒生产企业提供有效数据支持,加快其发展速度[6-12]。
川牛膝饮片标准汤剂以15批市面上主要流通的川牛膝饮片为材料,采用全面标准化制备过程。经DNA条形码技术鉴定[13-14],所用15批川牛膝样品皆为苋科植物川牛膝(Cyathula officinalis Kuan)的干燥根饮片。本课题以杯苋甾酮为指标成分,考察其在饮片与标准汤剂中的含量,计算转移率与出膏率,并建立指纹图谱,为制定川牛膝饮片标准汤剂质量标准及其配方颗粒的研制提供思路与数据。
1 仪器与试药
1.1 仪器
Agilent 1290 InfinityⅡUPLC仪(美国安捷伦科技有限公司,G7167B型自动给样系统,G7166B型柱温箱,G7117A型DAD检测器);电子分析天平(北京市赛多利斯天平有限公司,型号:Sartorius-BS 210S);超声波清洗器(昆山超声仪器有限公司,型号:KQ-100E);电子天平(沈阳市龙腾电子有限公司,型号:LD510-2型);高速离心机(湖南省湘仪实验室仪器开发有限公司,型号:H1650-W);混合仪(杭州市米欧仪器有限公司,型号:MIX-25P);真空干燥箱(北京永光明医疗仪器有限公司,型号:DZF)。
1.2 试剂
杯苋甾酮对照品(成都普菲德,纯度≥98%,批号130745),甲醇为美国Fisher公司色谱级甲醇,乙腈为美国Fisher公司色谱级乙腈,水为纯净水(杭州娃哈哈集团有限公司)。
1.3 分析样品
收集2个产地,共15批川牛膝样品,分别购自北京华邈、樟树天齐堂、安国昌达、江中、新荷花池和路路通药材市场,经DNA条形码技术鉴定均为苋科植物川牛膝(Cyathula officinalis Kuan)的干燥根,样品信息见表1。
2 方法与结果
2.1 色谱条件
2.1.1 饮片色谱条件 Thermo Accucore C18色谱柱(2.1 mm×150 mm,2.6 μm);甲醇作为流动相A,水作为流动相B,梯度洗脱(0~5 min,10%A;5~15 min,10%~37%A;15~30 min,37%A;30~31 min,37%~100%A);柱温:30 ℃;流速:0.4 mL/min;检测波长为243 nm。
2.1.2 标准汤剂色谱条件 Thermo Accucore C18色谱柱(2.1 mm×150 mm,2.6 μm);0.1%醋酸水溶液作为流动相A,乙腈作为流动相B,梯度洗脱(0~5 min,5%~15% B;5~10 min,15~20% B;10~15 min,20%~30%B;15~20 min,30%~70%B)柱温:30 ℃;流速:0.4 mL/min;检测波长:243 nm。色谱图见图1。
2.2 对照品溶液的制备
取经五氧化二磷减压干燥器中干燥36 h的杯苋甾酮对照品(成都普菲德,纯度≥98%,批号130745)3.5 mg,置于10 mL容量瓶中,加甲醇定容,即得对照品溶液。
2.3 供试品溶液的制备
2.3.1 饮片供试品溶液制备 取本品粉末约1 g,精密称定,置于20 mL具塞锥形瓶中,移液管加入20 mL甲醇,称重,记录。电热套加热回流60 min,放至室温,再次称重,甲醇将其补足重量,摇匀后,使用0.22 μm滤膜过滤,取续滤液,即得饮片供试品溶液。
2.3.2 标准汤剂供试品溶液制备 取川牛膝饮片100 g,置于1 000 mL圆底烧瓶中,加7倍量纯化水,浸泡30 min,打开电热套,调至最高档加热至沸腾,再调至中火,保持沸腾30 min,200目筛网趁热过滤。残渣中再加6倍量纯化水,最高档加热至沸腾,再调至中火,保持沸腾20 min,再次趁热过滤,与第一次滤液合并,浓缩至500 mL,即得标准汤剂供试品溶液。
2.4 线性关系考察
移液枪吸取“2.2”中配置好的对照品溶液0.05 mL、0.1 mL、0.5 mL、1.0 mL、1.5 mL、2.0 mL加入到5 mL的容量瓶中,加甲醇定容至刻度。按照“2.1.2”下的色谱条件测定杯苋甾酮峰面积,以243 nm波长下杯苋甾酮峰面积为纵坐标(Y),杯苋甾酮对照品的进样量(μg)为横坐标(X),计算回归方程,得到标准曲线,回归方程为:Y=2 623 040.357 0x-5.145 4,R2=0.999 6。
2.5 精密度试验
取一份川牛膝饮片标准汤剂供试品溶液,按照“2.1.2”色谱条件进样,连续进样6次,并计算杯苋甾酮的峰面积,得到峰面积的RSD值为2.68%,说明仪器的精密度良好。
2.6 供试品溶液稳定性试验
配制一份标准汤剂供试品溶液,按照“2.1.2”项下色谱条件进样,分别在配制后的0 h、4 h、8 h、10 h、12 h、24 h后进样,计算杯苋甾酮峰面积,得到杯苋甾酮峰面积的RSD值为2.50%,说明24 h内供试品溶液的稳定性良好。
2.7 重复性试验
平行制备个6批次的标准汤剂供试品溶液,按照“2.1.2”下的色谱条件进样,计算杯苋甾酮峰面积,得到杯苋甾酮峰面积的RSD值为2.76%,说明此方法重复性良好。
2.8 回收率试验
向已知杯苋甾酮含量的供试品中,分别加入等量杯苋甾酮对照品,并按照“2.1.2”项下色谱条件测定峰面积,计算其含量,最终得到杯苋甾酮的平均回收率为98.71%,RSD值为2.36%。
2.9 样品测定结果
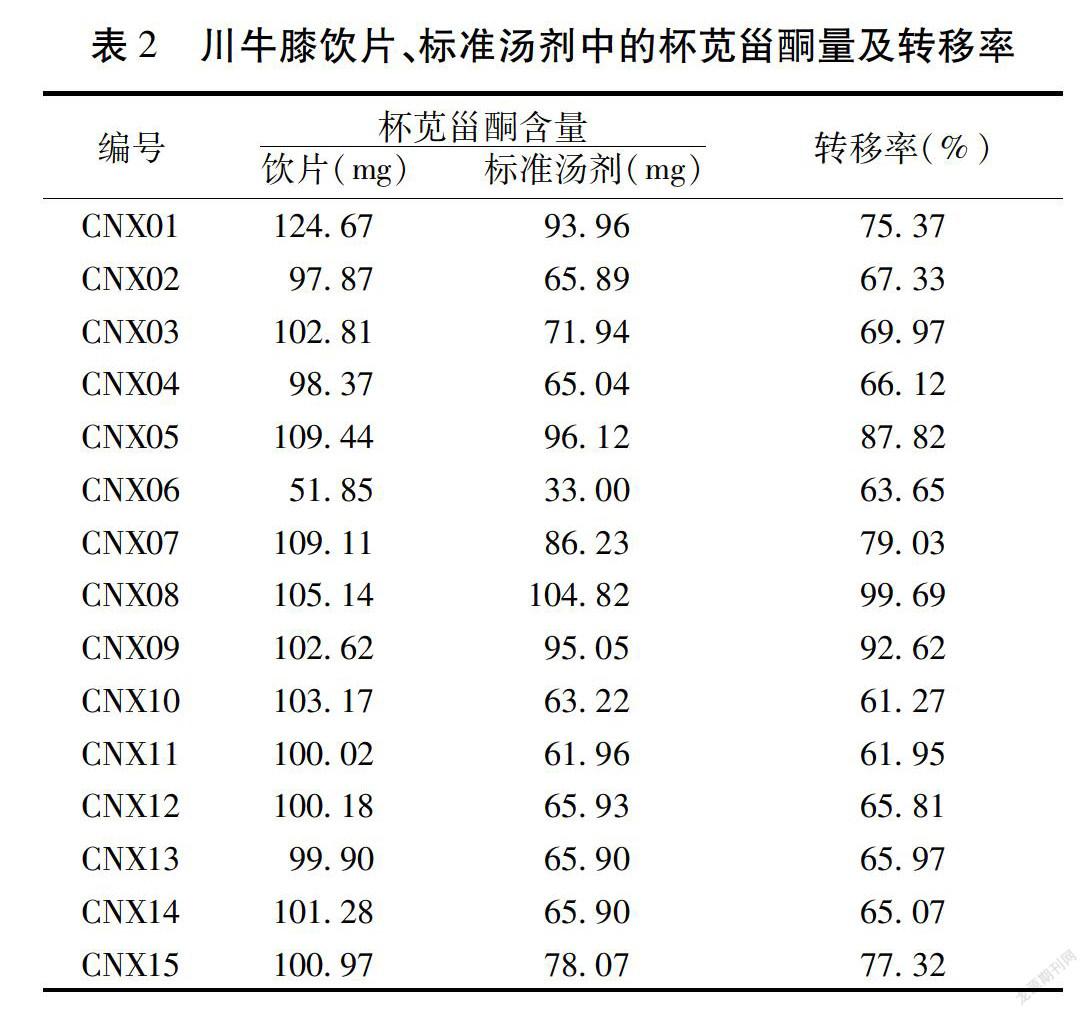
2.9.1 含量测定结果 分别精密吸取“2.3”下供试品溶液2 mL,加水1 mL稀释,超声5 min,12 000 r/min离心5 min,0.22 μm滤膜过滤,取续滤液,按照“2.1”下色谱条件进样5 μL,并测定峰面积,根据外标法计算川牛膝饮片及标准汤剂中杯苋甾酮含量,结果见表2。
2.9.2 转移率考察 根据“2.9.1”项下的测定结果,并按照转移率计算公式计算杯苋甾酮的转移率(表2),计算转移率的公式为:转移率(%)=W(mg)/M(mg)×100%(W表示汤剂中杯苋甾酮的含量,M表示饮片中杯苋甾酮的含量)。
2.9.3 出膏率考察 吸取“2.3.2”项下混合均匀的标准汤剂供试品溶液10 mL置于蒸发皿中,设置真空干燥箱温度为40 ℃,真空干燥至恒重,并称重,计算标准汤剂出膏率,出膏率公式:出膏率(%)=(w×V)/(v×M)×100%。(M为药材量,V为中药饮片标准汤剂体积,v为取样体积,w为取样所得干膏量),测得CNX01~CNX15出膏率结果最终为28.65%、21.54%、19.83%、17.98%、18.77%、23.55%、31.45%、27.87%、25.65%、17.66%、26.79%、23.53%、30.90%、25.43%、27.55%。
2.10 川牛膝标准汤剂指纹图谱研究
2.10.1 指纹图谱的建立及共有峰的标定 按照“2.1.2”项下的色谱条件,将15个批次的川牛膝饮片标准汤剂供试品溶液分别进样5 μL分析,并记录色谱峰信息,如图2;生成的对照指纹图谱,如图3。其中共有峰共有11个,指认1个。将6号峰杯苋甾酮作为参照峰。
2.10.2 相对保留时间及相对峰面积 对照指纹图谱中,以6号峰杯苋甾酮色谱峰的峰面积和保留时间为1,计算各峰的相对峰面积和相对保留时间,结果见表3。
2.10.3 指纹图谱相似度评价 采用“中药指纹图谱相似度评价系统(2004A)”版进行相似度分析,15个批次标准汤剂相似度全部大于0.9,均符合指纹图谱相似度要求。相似度依次为:S1:0.977;S2:
3 讨论
15批川牛膝指标成分含量测定的结果表明,各厂家提供的川牛膝饮片的杯苋甾酮含量相差较小,虽然不同厂家不同产地川牛膝饮片的杯苋甾酮含量具有一定差异,但波动范围小,品质相对稳定,且15批川牛膝的杯苋甾酮含量均达到药典要求(杯苋甾酮含量不低于0.030%)。其中杯苋甾酮转移率范围为61.27%~99.69%,平均转移率达到73.27%,标准偏差为11.88%。杯苋甾酮转移率处于《技术要求》要求的可接受转移率范围37.63%~108.91%(均值加减3SD)。出膏率范围为17.66%~31.45%,平均出膏率为24.48%,标准偏差为4.54%。川牛膝标准汤剂的出膏率也均符合《技术要求》所要求的可接受出膏率范围10.86%~38.11%(均值加减3SD),说明转移率和出膏率都具有较高集中度。
中药汤剂作为我国应用最早、最为广泛的剂型,傳承千年经久不衰。但数千年的历史朝代更迭,度量衡与制备工艺的不断变迁,致使中药汤剂质量参差不齐甚至出现不良反应,中药的质量疗效与安全再次面临挑战[15-18]。
为保障中药的安全与有效,加强中药药品质量标准化,规范中药制备工艺与标准。国家与地方在中药汤剂的煎煮工艺上先后出台多部中药煎煮管理规范,如《医疗机构中药煎药室管理规范》《上海中药行业零售药店中药煎药服务管理规范》《中药饮片煎煮规范》等。根据药材质地、药材部位以及功能主治分别对药材的浸泡时间、煎煮时间、煎煮次数和加水量等做出相关规定,极大减少了中药汤剂在临床应用时面对的问题与困难,加强了临床用药的一致性。但即使在此类管理规范的要求下人为因素所带来的不确定性仍然存在,质量依然无法保证[19]。
中药饮片标准汤剂遵循传统中医药理论,经规范化煎煮、固液分离、适当浓缩而制得。通过测定指标成分含量、转移率、出膏率、以及指纹图谱的建立对汤剂质量进行表征,充分体现了中药研究的复杂性和整体性。通过转移率分析指标成分的传递规律以明确影响成分传递规律的关键步骤;通过出膏率表达未知成分提取率;通过指纹或特征图谱的建立从整体的角度对中药饮片标准汤剂质量进行控制,进而将中药饮片标准汤剂作为一种基准标化临床各种饮片用药形式,尤其是质量标准仍较为模糊的中药配方颗粒[20-21]。
中药制剂多以复方为主,复杂的配伍与严格的煎煮工艺,使复方制剂质量标准更加难以统一,迫使中药新药审批环节复杂严苛。2007年中药新药申报数量首次出现断崖式下降,由2006年的1 798个下降到2007年的331个并且持续走低,这一现象无法满足公众用药需求。为加快促进中医药事业发展,2008年原国家食品药品监督管理总局在《中药注册管理补充规定》中首次提出部分源于古代经典名方的中药复方制剂在申报生产时可仅提供非临床安全性研究资料;2015年在《国务院关于改革药品医疗器械审评审批制度的意见》(国发〔2015〕44号)中再一次重申“简化来源于古代经典名方的复方制剂的审批”,并于2016年写入《中华人民共和国中医药法》。据此2018年6月国家药品监督管理局发布了《古代经典名方中药复方制剂简化注册审批管理规定》,对公布的古代经典名方目录(第一批)中的100首古代经典名方实施简化审批,可仅提供药学及非临床安全性资料[22-24]。
经典名方的研究与开发和中药复方标准汤剂的研究一脉相承,中药饮片标准汤剂与中药复方标准汤剂均可相互借鉴,无论在研究样品、指标成分的选择,还是检验方法、制备工艺的确定,以及质量标准主要参数的探讨上,饮片标准汤剂都为复方标准汤剂做出大量前期研究。饮片标准汤剂所得数据及经验均可作为参考应用于经典名方复方标准汤剂的研究中,为后续确定经典名方的制备工艺、确定经典名方质量参数提供数据支撑,缩短生产中试优化时间,从而降低研究成本[11-12]。
作为标准汤剂质量评价的重要依据,指标成分应具有权威性,多采用《中华人民共和国药典》中药材含量测定所规定的成分,但《中华人民共和国药典》中部分药材并无含量测定或某些药材指标成分含量极低(低于0.1%),饮片批次间成分含量差异较大,严重影响质量评价结果,此类药材需进一步研究确定合适的指标成分。可通过查阅文献将含量高、稳定性好的化学成分作为指标成分;为更准确掌握饮片中成分转移规律,也可确定2个指标成分,对药材进行更全面的把控。标准汤剂作为一种基准,更加注重指标成分转移率的稳定性而非高提取率,所以脂溶性或难溶于水的指标成分仍可以作为中药饮片标准汤剂的指标成分。
参考文献
[1]国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社,2015:38.
[2]童凯,李昭玲,闫燊,等.川牛膝酒炙和盐炙前后HPLC化学指纹图谱及其主要药效成分量变化研究[J].中草药,2016,47(4):580-584.
[3]黄丽婵,杨世奎,刘发元,等.川牛膝、怀牛膝治疗骨关节炎的药效物质基础探讨[J].风湿病与关节炎,2014,3(11):52-54.
[4]陈士林,刘安,李琦,等.中药饮片标准汤剂研究策略[J].中国中药杂志,2016,41(8):1367-1375.
[5]周蔚昕,刘涛,徐玉玲,等.对《中药配方颗粒质量控制与标准制定技术要求》(征求意见稿)部分内容的探讨[J].时珍国医国药,2017,28(10):2491-2493..
[6]刘安.中药饮片标准汤剂制备与质量标准研究方法概述[J].中国实验方剂学杂志,2017,23(7):1-1.
[7]杨立伟,王海南,耿莲,等.基于标准汤剂的中药整体质量控制模式探讨[J].中国实验方剂学杂志,2018,24(8):1-6.
[8]于小红,赵嵘,代云桃,等.党参标准汤剂质量评价的建立[J].中国实验方剂学杂志,2017,23(7):24-29.
[9]孙宝莹,郭涛,李西文,等.葛根饮片标准汤剂的研究[J].世界中医药,2016,11(8):1586-1589.
[10]刘冲,刘荫贞,乐智勇,等.桂枝饮片标准汤剂质量标准研究[J].中草药,2017,48(8):1577-1583.
[11]陈士林.中药饮片标准汤剂(第一卷)[M].北京:科学出版社,2018:3-14.
[12]陈士林,刘安.中药饮片标准汤剂(第二卷)[M].北京:科学出版社,2019:6-8,18-22.
[13]陈士林,姚辉,韩建萍,等.中药材DNA条形码分子鉴定指导原则[J].中国中药杂志,2013,38(2):141-148.
[14]陈士林.中国药典中药材DNA条形码标准序列[M].北京:科学出版社,2015:95-96.
[15]田军军,刘莹,冯广义.中药汤剂煎煮法和有效成分溶出率关系探讨[J].吉林中医药,2008,28(5):373-374.
[16]杨艳环,赵瑞华.中药煎服方法研究进展[J].辽宁中医药大学学报,2011,13(1):30-32.
[17]叶祖光,张广平.中药安全性评价的发展、现状及其对策[J].中国实验方剂学杂志,2014,20(16):1-6.
[18]朱葛馨,王丽霞,仝小林.中药安全性研究[J].长春中医药大学学报,2015,31(1):32-34.
[19]朱广伟,李西文,李琦,等.基于传统煎药工艺的龙胆饮片标准汤剂制备及质量评价方法研究[J].中草药,2017,48(20):4253-4260.
[20]朱广伟,李西文,陈士林.白芍饮片标準汤剂质量标准研究[J].世界中医药,2016,11(5):753-757.
[21]张鹏,邬兰,李西文,等.人参饮片标准汤剂的评价及应用探讨[J].中国实验方剂学杂志,2017:23(7):10-19.
[22]梁爱华,韩佳寅,陈士林,等.中药经典名方的质量与安全性考量[J].中国食品药品监管,2018:1(6):4-10.
[23]王智民,刘菊妍,刘晓谦,等.谈经典名方的化学、生产和质量控制研发和监管[J].中国中药杂志,2017,42(10):1819-1824.
[24]陈畅,程锦堂,刘安.经典名方研发策略[J].中国中药杂志,2017,42(9):1814-1818.
(2019-01-11收稿 责任编辑:苍宁)

