多西他赛解救治疗不同年龄组转移性乳腺癌的临床研究
马 焱 何 红 王赛男
乳腺癌作为女性最常见的恶性肿瘤,其发病率与死亡率逐年升高,已成为我国重大公共健康问题之一[1-3]。现阶段,化疗仍是乳腺癌患者的首选方案,临床上常用化疗药物有烷化剂类、蒽环类、紫杉类、抗代谢类等,单药或联合用药均有较好的疗效[4-5]。多西他赛单药治疗转移性乳腺癌疗效明确,成为复发转移性乳腺癌解救治疗重要选择之一[6]。老年肿瘤患者(≥60岁)作为一类特殊人群,其临床疗效及与之相伴的血液学毒性仍然值得关注。我们回顾性分析了200例多西他赛解救治疗复发转移性乳腺癌患者的临床资料,依照年龄分为≤45岁年龄组、46~59岁年龄组及≥60岁年龄组,对不同年龄组的多西他赛临床疗效及其血液学毒性进行了探讨分析,现将研究分析结果报告如下。
1 资料和方法
1.1 临床资料
回顾性分析我院2008年1月—2018年6月间收治的,病历资料相对完整的,且能够评定疗效和记录疾病进展时间(Time to progresstion,TTP)或治疗失败时间(Time to failure,TTF)的200例多西他赛治疗的复发转移性乳腺癌患者。全部病例均已病理证实。其中≤45岁组62例,中位年龄41(32~45)岁,46~59岁组98例,中位年龄53(47~58)岁,≥60岁组40例,中位年龄67(66~77)岁。各年龄组患者具体情况见表1。
患者随诊开始时间从乳腺癌确诊时计算,随访结束时间为确诊死亡或随诊截止时间2018年10月31日。
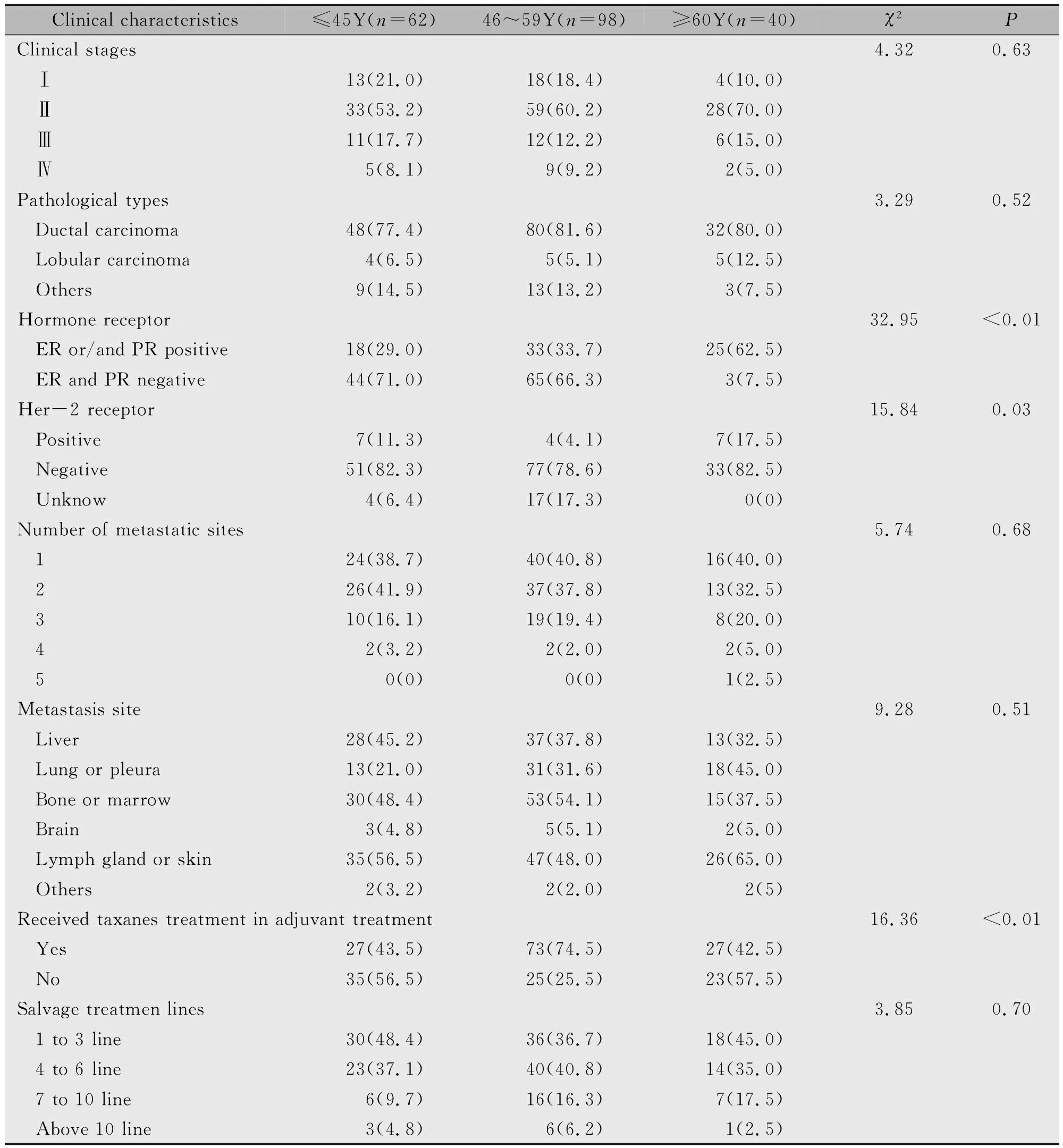
表1 200例不同年龄组患者基本情况[n(%)]
1.2 方法
1.2.1 治疗方法 依据NCCN指南中解救治疗的国际标准剂量,予以多西他赛60~100 mg/m2,静滴,d1,21天为1周期。有效者继续用药直至疾病进展或不良反应无法耐受。
1.2.2 观察指标 按照RECIST 1.1[7]将疗效评定分为完全缓解(CR)、部分缓解(PR)、稳定(SD)、进展(PD),CR+PR为客观缓解,CR+PR+SD(≥24周)为临床获益。
记录TTP或TTF及无进展生存期(Progression free survival,PFS)。
1.3 统计方法
全部数据采用SPSS 18.0统计软件进行分析,采用卡方检验分析定性资料;采用Kaplan-Meier法行生存分析,Log-rank检验进行单因素分析,多因素分析采用Cox回归模型,P<0.05为差异有统计学意义。
2 结果
2.1 不同年龄组多西他赛的客观缓解率(Objective reponse rate,ORR)和临床获益率(Clinical benefit rate,CBR)
200例多西他赛解救治疗复发转移性乳腺癌患者中,≤45岁年龄组的ORR为30.6%,CBR为38.7%,46~59岁年龄组ORR及CBR分别为27.6%和35.7%,而≥60岁年龄组ORR及CBR分别为20.0%和27.5%,三个年龄组患者的ORR及CBR无统计学差异(P=0.477,0.492)(表2)。

表2 不同年龄组多西他赛的ORR及CBR情况[n(%)]
2.2 不同年龄组多西他赛解救治疗的PFS
对接受多西他赛解救化疗的三个年龄组患者进行生存分析,结果显示≤45岁年龄组、46~59岁年龄组及≥60岁年龄组的中位PFS分别为6.0(2.9~9.1)个月、5.0(2.9~7.1)个月及4.0(3.3~4.7)个月,三个年龄组PFS无统计学差异(P=0.460)(图1)。
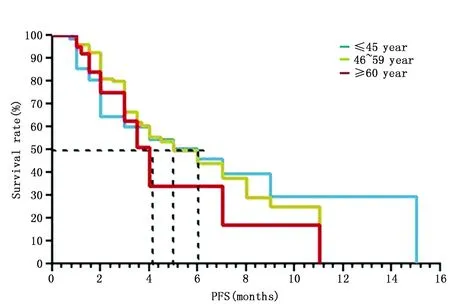
图1 多西他赛解救治疗不同年龄组转移性乳腺癌PFS的Kaplan-Meier曲线Figure 1 Kaplan-Meier curves of PFS for docetaxel rescue treatment in metastatic breast cancer patients of three different age groups
2.3 不同年龄组多西他赛解救治疗PFS的COX多因素分析
收集可能影响不同年龄组多西他赛解救治疗利用PFS的7项因素,以COX风险回归模型对不同年龄组多西他赛PFS进行分析。Cox回归模型基于最大估计后退法P>0.10为标准剔除变量,研究结果显示不同年龄组多西他赛PFS与临床分期、病理类型、同侧腋窝淋巴结转移数目、无病生存期、单位体表面积剂量、解救治疗线数、复发转移部位数目等因素均无关。
2.4 血液学毒性
200例患者临床资料显示主要的毒副作用为血液学毒性,其中有血常规检查结果者68例。多西他赛血液学毒性主要表现为白细胞及中性粒细胞下降,而对血红蛋白及血小板影响较小。≤45年龄组以白细胞下降Ⅱ度为主,占52.9%,而46~59年龄组及≥60年龄组白细胞下降则均以Ⅲ度为主,分别占56.1%及60.0%。≤45年龄组中性粒细胞抑制较轻,0度所占比例最高,达29.4%,而46~59年龄组及≥60年龄组均以Ⅳ度中性粒细胞抑制为主,分别占73.2%及60.0%(表3)。
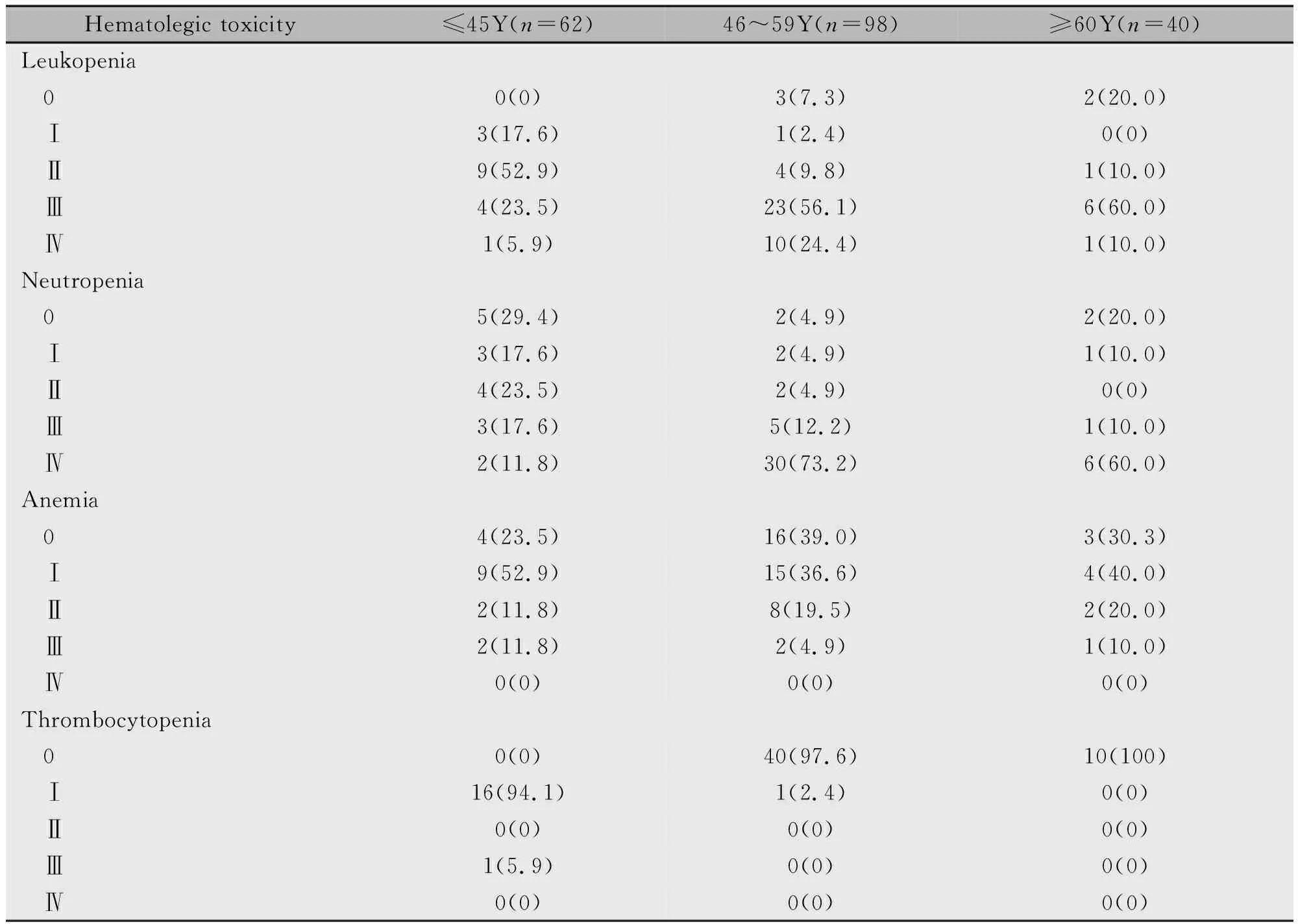
表3 多西他赛血液学毒性情况[n(%)]
3 讨论
多西他赛属紫杉类药物,其半衰期长、在细胞内浓度比紫杉醇高3倍且滞留时间长,具有更强的抗肿瘤作用[8],此外,与紫杉醇相比,多西他赛发生严重过敏反应几率较低,安全性更高[9],因此,被推荐用于治疗转移性乳腺癌[10],其通过加强微管蛋白聚合,同时通过抑制解聚过程使微管保持稳定状态,阻滞细胞于G2和M期,进而抑制癌细胞的有丝分裂和增殖,最终达到抗肿瘤效用[11]。
乳腺癌发病率与年龄呈正比[12],老年肿瘤患者体质弱,多数合并慢性基础疾病,不良反应耐受性差等特点,使其治疗方案的选择有一定难度。同时,乳腺癌目前尚无有效方法治愈,治疗着眼于延长生存时间及改善生活质量[13],鉴于老年乳腺癌患者自身特点,单药化疗成为此类人群的优选。据国外文献报道,多西他赛周疗治疗晚期乳腺癌疗效明确,耐受性良好,单药治疗一线失败的乳腺癌,疗效可达23%~65%[14]。因此,本研究依照年龄对患者进行分组,进一步研究了不同年龄段、三周疗多西他赛的临床疗效及血液学毒性的情况。
200例多西他赛解救治疗复发转移性乳腺癌患者中,≤45岁年龄组的客观缓解率及临床获益率分为30.6%及38.7%,46~59岁年龄组ORR及CBR分为27.6%和35.7%,而≥60岁年龄组ORR及CBR分为20.0%和27.5%。三年龄组ORR及CBR未见统计学差异(P=0.477,0.492),三组ORR及CBR情况与既往研究结果相似[6,15]。虽然不同年龄组多西他赛临床疗效未见明显差异,但是依照数据所示,仍可发现ORR及CBR的梯度变化,显现出≤45岁年龄组及46~59岁年龄组疗效优于≥60岁年龄组。同时,三年龄组中位PFS依次为6.0(2.9~9.1)月、5.0(2.9~7.1)月及4.0(3.3~4.7)月,结果仍未见统计学差异。Kaplan-Meier曲线显示,≤45岁年龄组及46~59岁年龄组重合部分较多,而≥60岁年龄组则较前两组重合部分较少,尤≤45岁年龄组与≥60岁年龄重合最少,显示年龄相近组PFS差异相对较少,而年龄相差大组间PFS差异相对较大。虽本研究三年龄组中位PFS未见统计学差异,但仍呈现出随年龄组增大而递减的变化趋势。鉴于本研究属于回顾性研究,患者均为多线化疗,临床疗效的干扰因素太多,各组病例数有限,尚需要更为科学设计的研究进行分析探讨。
此外,我们同时对不同年龄组多西他赛解救治疗PFS进行COX多因素分析,结果显示临床分期、病理类型、同侧腋窝淋巴结转移数目、无病生存期、单位体表面积剂量、解救治疗线数、复发转移部位数目等因素与不同年龄组多西他赛解救治疗的PFS无相关性。
多西他赛不良反应包括以中性粒细胞减少为主的血液学毒性、恶心、呕吐等消化道毒性反应、过敏反应、外周神经病变、脱发及体液潴留等,而本研究临床资料观察结果以血液学毒性为主,结果显示多西他赛血液学毒性主要表现为白细胞及中性粒细胞下降,而对血红蛋白及血小板影响较小,此结果与相关文献报道一致[15]。此外,本研究≤45岁年龄组及46~59岁年龄组白细胞及中性粒细胞抑制以Ⅲ度及Ⅳ度为主,而≤45岁年龄组仅白细胞出现Ⅱ度抑制。不同年龄组多西他赛血液学毒性差异考虑可能与年老者骨髓造血功能较差相关。
综上所述,虽然三年龄组的ORR、CBR及中位PFS均未见明显差异,但仍显现出随年龄增大,临床疗效递减且血液学毒性加重的变化趋势。

