LaCoO3对H2S选择氧化性能的影响
喻昕蕾, 潘伟童, 高 瑞, 高德志, 刘 霞, 代正华, 于广锁, 王辅臣
(华东理工大学 煤气化及能源化工教育部重点实验室, 上海 200237)
硫化氢(H2S)是一种有毒恶臭气体,微量即可对人体有害,主要来源于煤化工、石油化工、天然气加工等过程[1,2]。H2S无论是气态还是溶液,均为强腐蚀性介质,对管道和生产设施都具有极强的危害性[3]。H2S的脱除及回收利用对保障装置安全稳定运行、改善环境均有重要意义。目前,使用最广泛的H2S回收利用技术是克劳斯法,该法从含硫气体中回收元素硫,但由于受到热力学的限制,在含有三个Claus催化转化器的情况下,尾气中仍有较多的H2S气体[4],不能满足国家现有的气体排放标准。为处理未转化的H2S气体,可采用选择性催化氧化法,即在传统Claus装置后添加一个H2S选择性催化氧化反应器,用于除去前段剩余的浓度在5%以下的H2S气体,从而进一步提高硫回收率。目前,选择性催化氧化技术已经成功应用于工业化生产中,例如:荷兰Comprimo公司和VEG气体研究院与Utrecht大学合作开发的SuperClaus工艺[5]、德国Linde公司开发的Clinsulf-Do工艺[6]。
随着选择性催化氧化工艺的发展,新型高效催化剂的研发已成为研究热点。H2S选择性氧化催化剂主要有碳体系[7]、分子筛体系[8]、柱撑黏土体系[9]、氧化物体系[10]等。SiC 载体制备工艺复杂导致成本较高,故很难应用到工业上。分子筛体系虽然材料价廉易得,孔结构可选易控,易改性,但有稳定性、选择性和活性均较差,并且容易失活。钙钛矿氧化物是常见的无机功能材料,具有良好的氧化还原性能,其化学通式可用ABO3来表示,其中,A一般为碱土金属和稀土金属离子,位于晶胞体心并与12个氧离子配位;B一般为过渡金属离子,位于立方体的顶角并与六个氧离子配位[11]。钙钛矿氧化物的催化氧化性能取决于它的体相结构以及组成的物质,这其中包括缺陷、价态变化等作用。Zhang等[12]研究了掺杂Ce的LaFeO3催化剂对H2S选择性氧化的影响。LaCoO3对H2S选择性氧化催化性能的研究报道较少。Chen等[13]的研究表明,LaCoO3催化剂对NO氧化有良好活性。Seyfi等[14]的研究指出,改性LaCoO3钙钛矿催化剂对CO氧化有高催化活性。这些可能对LaCoO3对H2S选择性氧化催化性能研究有借鉴作用。因此,本研究以柠檬酸为络合剂使用溶胶-凝胶法制备了LaCoO3催化剂,采用相关测试手段对其物化性质进行了表征,考察了LaCoO3制备过程中煅烧温度、表面活性剂PEG-6000添加量和表面活性剂PEG-20000添加量对H2S选择性氧化反应的催化活性的影响。
1 实验部分
1.1 催化剂的制备
采用溶胶-凝胶法制备LaCoO3催化剂。所用原材料为分析纯的La(NO3)3·6H2O、Co(NO3)2·6H2O、表面活性剂PEG-6000、表面活性剂PEG-20000、无水柠檬酸等。称取0.02 mol La(NO3)3·6H2O与0.02 mol Co(NO3)2·6H2O用去离子水搅拌溶解,再加入络合剂柠檬酸,其中,柠檬酸和金属离子物质的量比为1∶1。将反应体系置于水浴加热锅中,80 ℃下不断搅拌,当溶液剩40 mL时加入适量的表面活性剂,形成湿凝胶后放入恒温干燥箱中干燥,于100 ℃下恒温脱水,得到干凝胶。然后将干凝胶研磨成粉,放入马弗炉中400 ℃煅烧1 h,后升至650 ℃煅烧5 h,即可得到粉体样品。
以此上述制备条件为基础,通过改变煅烧温度、表面活性剂PEG-6000含量及表面活性剂PEG-20000含量,制取了一系列催化剂样品,制备条件见表1。

表 1 LaCoO3催化剂的制备条件
1.2 催化剂的表征
催化剂的物相结构采用X射线衍射(XRD)进行测定,所用仪器为X-Pert Powder型X射线粉末衍射仪。该仪器采用CuKα射线,管电流40 mA,管电压40 kV,扫描速率为4(°)/min,10°-80°扫描。
催化剂的比表面积和孔结构在ASAP2020气体吸附仪上测定,测定前先在120 ℃下脱气10 h,以N2为吸附质,吸附过程在液氮温度(-196 ℃)进行。
催化剂的表面成分及化合态分析应用光电子能谱(XPS)法进行测定, 在ESCALAB 250Xi(Thermo Fisher Scientific,美国)上完成,采用条件为AlKα靶,电压14.0 kV,功率300 W。采集样品的0-1200 eV的全扫描谱,而后采集Re 4f金属以及C元素的窄扫描谱,以C 1s=284.8 eV为基准校正金属元素的结合能。
1.3 催化剂的活性评价
催化剂活性测试在自主搭建的固定床反应器(石英管直径10 mm,长550 mm)上进行。气体流量由质量流量计控制,反应器温度由可编程管式炉控制。反应器入口气体组成为5% H2S、2.5% O2、平衡气为N2的混合气,气体总流量为150 mL/min。催化剂活性测试温度为220-280 ℃,反应空速为5000 h-1。反应后的气体使用GC2060色谱仪进行分析。经色谱检测后的气体排空处理,未收集的气体通过NaOH洗瓶处理后排空。
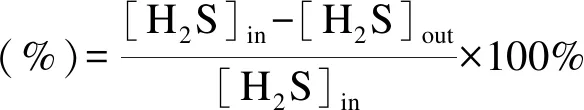
(1)
硫选择性(%)=

(2)
硫产率(%)=[H2S 转化率]×[硫选择性]
(3)
2 结果与讨论
2.1 催化剂的活性
2.1.1 催化剂煅烧温度的影响
催化剂的煅烧温度不仅影响最终所制备的催化剂的粒径,同时还会影响催化剂的晶型和结构。图1为不同煅烧温度下LaCoO3催化剂的H2S选择性氧化过程的转化率、 硫选择性和硫收率的变化。由图1可知,LaCoO3催化剂的煅烧温度对H2S选择性氧化有较大影响。随着煅烧温度的升高,LaCoO3催化剂的H2S转化率和硫选择性小幅增加,然而煅烧温度超过650 ℃后,催化剂的H2S转化率、硫选择性和硫收率均逐渐下降。与煅烧温度为650 ℃的催化剂相比,煅烧温度为750 ℃时催化剂的H2S转化率由88.43%逐渐下降到的82.57%,硫选择性由88.86%逐渐下降到的83.60%,这一现象可能是由于煅烧温度过高造成了催化剂的结构发生了变化。由上述分析可得,LaCoO3催化剂的最佳煅烧温度为650 ℃。

图 1 煅烧温度对LaCoO3催化剂的H2S选择性氧化活性的影响
2.1.2 表面活性剂PEG-6000含量的影响
添加表面活性剂会对催化剂的活性有一定影响,故在制备催化剂时添加一定量的PEG-6000以提高其活性。图2为添加不同含量的表面活性剂PEG-6000对LaCoO3催化剂的H2S选择性氧化过程的转化率、 硫选择性和硫收率的变化。由图2可知,添加表面活性剂PEG-6000能明显提高LaCoO3催化剂的活性。随着表面活性剂PEG-6000的添加量逐渐增加,LaCoO3催化剂的H2S转化率和硫选择性有所增加。与未添加表面活性剂PEG-6000的LaCoO3催化剂相比,PEG-6000添加量为0.45 g的催化剂的H2S的转化率由88.43%增加到了94.15%,然而其硫选择性并没有显著提高,仅从88.86%提高到了89.85%。此外,表面活性剂PEG-6000的添加量为0.45与0.60 g的LaCoO3催化剂的硫收率相差不大,分别为84.55%和84.06%。故表面活性剂PEG-6000的最佳添加量为0.45g。

图 2 PEG-6000含量对LaCoO3催化剂的H2S选择性氧化活性的影响
2.1.3 表面活性剂PEG-20000含量的影响
由2.1.2的实验结果可以看出,表面活性剂PEG-6000的添加并不能明显提高LaCoO3催化剂的硫选择性,故使用了另一种表面活性剂PEG-20000进行实验。图3为不同PEG-20000含量对LaCoO3催化剂的H2S选择性氧化过程的转化率、硫选择性和硫收率的变化。由图3可知,添加表面活性剂PEG-20000也能明显提高LaCoO3催化剂的活性。随着表面活性剂PEG-20000添加量的逐渐增加,LaCoO3催化剂的H2S转化率和硫选择性明显增加。当表面活性剂PEG-20000的添加量为0.30 g时,H2S的转化率提高到了96.10%,硫选择性也进一步提高到了93.77%。同时也可以发现,添加过量的PEG-20000会使催化剂的活性降低。当PEG-20000的添加量为0.60 g时,LaCoO3催化剂的H2S的转化率与添加量为0.30 g时相比差异不大,但其硫选择性下降到89.16%。发生这一现象的原因可能是过量添加PEG-20000不利于LaCoO3的形成,这与XRD的结果相一致。故表面活性剂PEG-20000的最佳添加量为0.30 g。
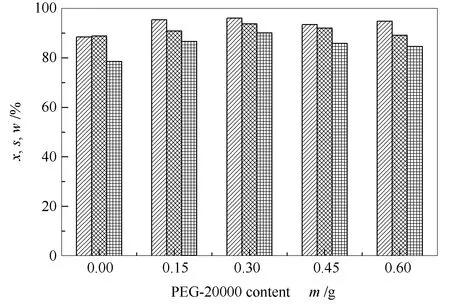
图 3 PEG-20000含量对LaCoO3催化剂的H2S选择性氧化活性的影响
2.1.4 反应温度的影响
综合2.1.1至2.1.3可以得出,表面活性剂PEG-20000添加量为0.30 g、煅烧温度为650 ℃的LaCoO3催化剂拥有最佳催化活性。众所周知,反应温度是影响催化剂活性的因素之一。图4为表面活性剂PEG-20000添加量为0.30 g、煅烧温度为650 ℃时LaCoO3催化剂的H2S选择性氧化过程转化率、硫选择性和硫收率随反应温度的变化。
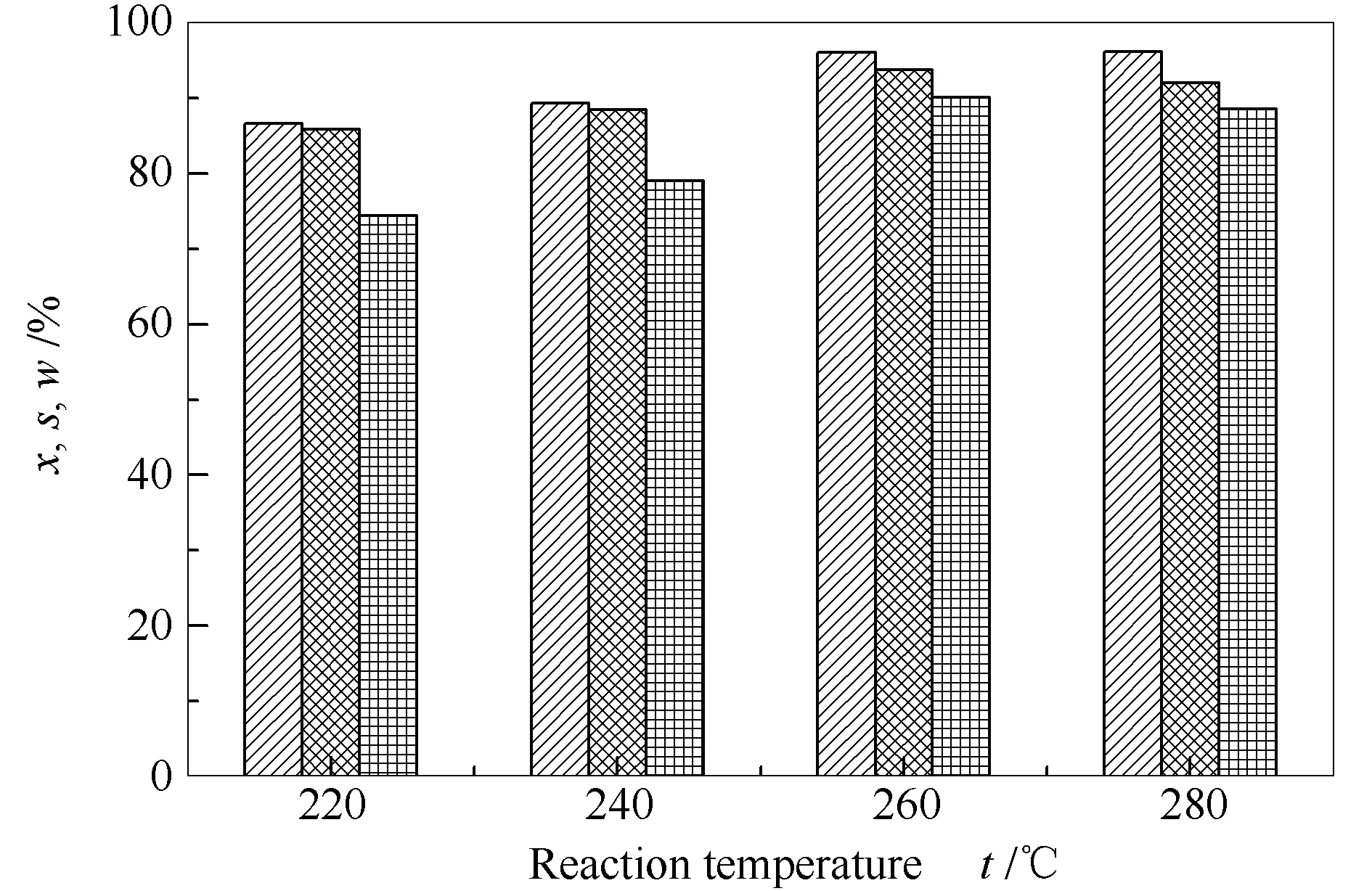
图 4 反应温度对LaCoO3催化剂H2S选择性氧化活性的影响
由图4可知,反应温度对催化剂活性有较大影响。随着反应温度的升高,LaCoO3催化剂的H2S转化率、硫选择性均呈现先增加后降低的趋势,均在反应温度为260 ℃时达到最高。与反应温度为220 ℃时相比,反应温度为260 ℃时催化剂的H2S转化率由86.68%提高到了96.10%,硫选择性由85.90%提高到了93.77%,而当反应温度达到280 ℃时,硫选择性会有细微下降,从而导致硫收率的下降。故LaCoO3催化剂最佳反应温度为260 ℃。
2.1.5 催化剂的稳定性
图5为煅烧温度为650 ℃、添加PEG-20000含量为0.30 g的LaCoO3催化剂的催化活性随时间的变化,其中,反应物组成为H2S∶O2∶N2=5∶2.5∶92.5,GHSV = 5000 h-1,反应温度为260 ℃。可以清楚地观察到5 h内催化剂的H2S转化率、硫选择性以及硫产率变化不大,H2S转化率从30 min时的97.02%缓慢下降到5 h时的96.10%,硫选择性从30 min时的95.19%缓慢下降到5 h时的93.77%。这说明该催化剂失活速率缓慢,具有一定的稳定性。

图 5 LaCoO3催化剂的稳定性能
2.2 催化剂的表征
2.2.1 XRD分析
X射线衍射(XRD)能确定催化剂的物相结构。本研究选择了不同煅烧温度和不同表面活性剂PEG-20000含量的LaCoO3催化剂进行XRD分析。图6为不同煅烧温度下LaCoO3催化剂的XRD谱图,与XRD谱库中的标准谱图对比,发现实验所得催化剂的XRD谱图上均出现LaCoO3钙钛矿晶体结构的特征衍射峰,这表明均形成了钙钛矿结构,且无杂相生成。随着煅烧温度的升高, 31.5°-35°的主峰由(1,-1,0)和(2,1,1)双峰向(1,1,0)单峰发生了转变,钙钛矿的晶体结构发生了畸变,从菱方相(Rhombohedral)转变成了立方相(Cubic),且当煅烧温度达到750℃时,特征衍射峰峰强减弱,这可能是由于温度过高造成了催化剂烧结团聚。图7为不同表面活性剂PEG-20000含量下LaCoO3催化剂的XRD谱图,与XRD谱库中的标准谱图对比,发现实验所得催化剂的XRD谱图上均出现LaCoO3钙钛矿晶体结构的特征衍射峰,但当表面活性剂PEG-20000添加量为0.60 g时,特征衍射峰峰强减弱,说明添加过量的表面活性剂PEG-20000不利于LaCoO3催化剂的形成。
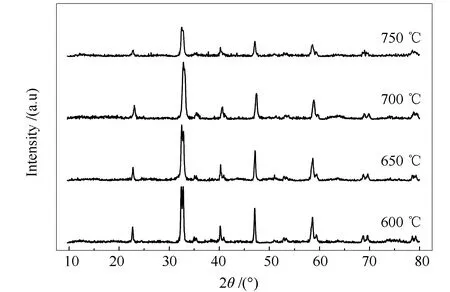
图 6 不同煅烧温度下LaCoO3的XRD谱图

图 7 不同PEG-20000含量下催化剂的XRD谱图
2.2.2 BET分析
本研究选择了煅烧温度为650 ℃时未添加表面活性剂、PEG-6000添加量为0.45 g以及PEG-20000添加量为0.30 g的LaCoO3催化剂,用BET分析测定其比表面积、平均孔径以及总孔容,具体见表2。

表 2 催化剂的比表面积以及平均粒径
由表2可知,加入0.45 g表面活性剂PEG-6000后,LaCoO3的比表面积从7.495 m2/g增加到8.543 m2/g,平均孔径由7.396 nm增加到了9.276 nm,总孔容再1.941×10-2cm3/g略微增加到了1.981×10-2cm3/g,而加入表面活性剂PEG-20000后,LaCoO3的比表面积、平均孔径、总孔容均进一步的增加。比表面积以及总孔容的增加提高了反应气体与催化剂的接触面,有利于H2S的氧化。这与实验结果相一致,也说明加入适量表面活性剂PEG-6000及PEG-20000有助于提高LaCoO3催化剂的性能。
2.2.3 XPS分析
X射线光电子能谱(XPS)能有效测定催化剂的元素组成和化合态。LaCoO3催化剂的XPS光谱与La 3d、Co 2p、O 1s的高分辨率XPS光谱见图8,所采用催化剂是煅烧温度为650 ℃、添加PEG-20000含量为0.30 g的LaCoO3催化剂。全谱图(图8(a))扫描说明催化剂主要由La、Co、O元素组成。La 3d的高分辨谱图(图8(b))显出在833.3、837.35和850.05、854.25 eV处有两对双峰,分别属于La 3d5/2和La 3d3/2,反映了了3d94f0和3d94f1结构,这是La3+化合物的典型特征[15]。从Co 2p的高分辨谱图(图8(c))可以看出,在键能为779.65和794.75 eV存在峰,前者属于Co 2p3/2,后者属于Co 2p1/2,这说明处于Co3+状态。图8(d)为O 1s的高分辨谱图。在键能为528.75和531.1 eV处存在峰,前者代表晶格氧(OL),后者代表化学吸附氧(OCA)[16]。从已有的文献中可知,化学吸附氧主要起到氧化的作用,与H2S的转化率和S 产率有直接的关系,而H2S氧化的选择性主要取决于有效的晶格氧[17]。LaCoO3催化剂中化学吸附氧和晶格氧的存在说明了该催化剂对H2S能起到选择性氧化的作用。
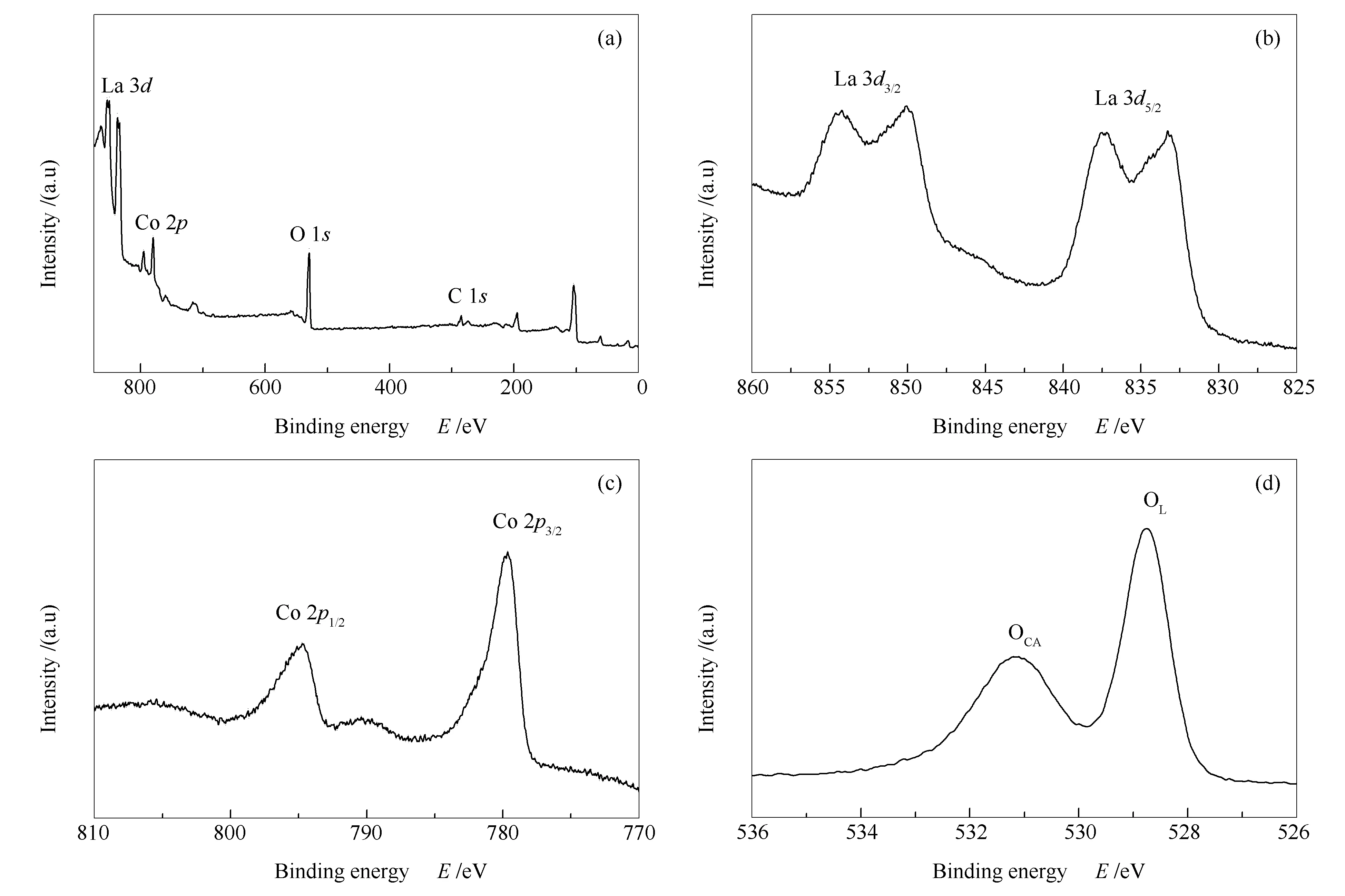
图 8 LaCoO3催化剂的XPS谱图
3 结 论
采用溶胶-凝胶法制备了一系列LaCoO3催化剂,该催化剂对H2S选择性氧化反应有较好的催化活性。催化剂制备过程中煅烧温度、表面活性剂PEG-6000和PEG-20000添加量对H2S选择性氧化反应的催化活性与稳定性有着较大的影响。实验结果表明,650 ℃为催化剂的最佳煅烧温度,表面活性剂PEG-6000的添加能提高催化剂的H2S转化率,表面活性剂PEG-20000的添加能提高催化剂的H2S转化率及硫收率。LaCoO3催化剂较好的制备条件为:煅烧温度为650 ℃、PEG-20000添加量为0.30 g,此时催化剂具有较高的催化活性,且反应温度为260 ℃时,H2S的转化率达到96.10%,硫选择性为93.77%。

