甲襞微循环检测对系统性红斑狼疮患者肺动脉高压的预测价值*
姜 波 徐 雪 王 春 耿林玉 冯学兵
系统性红斑狼疮(SLE)是一种常见的导致全身多脏器损害的自身免疫性疾病。肺动脉高压(PAH)为SLE严重并发症(定义为海平面静息状态下右心导管检测肺动脉平均压≥25mmHg[1]),此病以肺动脉压力进行性增高为特征,可引起右心衰竭甚至死亡,存活时间显著缩短。在SLE患者中PAH发生率为5%-14%,为SLE第三大致死原因[2],病程>3年的SLE住院患者中PAH高居死因首位[3],靶向药物上市前,SLE并发PAH的1年存活率仅45%。但因近半数PAH患者早期无症状,直至出现胸闷、气喘等严重心功能不全症状时才就诊,已错过治疗时机,猝死率很高,故寻找有效的预测方法,早期诊断及干预,是改善SLE并发PAH患者预后的关键措施。
电子甲襞毛细血管镜检查(又称甲襞微循环检查, NVC) 作为一种无创性的微血管检查方法,已在国际上越来越广泛用于系统性硬化症(SSc)患者的微血管病变评估,NVC的异常已被纳入美国风湿病学会/欧洲抗风湿病联盟2013年SSc分类标准中[4],其优点为操作简单,且费时少、无创、经济。而关于NVC在SSc之外的其它自身免疫病中应用意义的报道很少。为明确甲襞微循环异常与SLE患者并发PAH及继发心血管损害的相关性,判断其临床应用价值,本文分析了我科近期SLE患者NVC检测结果,现报道如下。
1 资料与方法
1.1 病例和分组
以2017-10—2018-10本科收入院的46例SLE患者为观察对象,所有患者均符合1997年美国风湿病学会制定的SLE分类标准[5]或2009年SLE国际临床协作组(SLICC)修订的美国风湿病学会 SLE分类标准[6],女45例,男1例,年龄19-67 岁,平均年龄34.25±11.97 岁,病程0.5-9 年。排除高龄(年龄≥70岁)、卧床、合并严重心肺疾病如心衰、呼衰、休克、心梗、手指畸形、手指外伤以及无法配合的患者。所有患者行经胸心脏超声(Philips iE33,荷兰)检查测定肺动脉压力(PAP),其中合并PAH患者17例(SLE-PAH组,心超检测PAP≥35 mmHg),平均PAP为56.60±14.25 mmHg;无PAH患者29例(SLE-non-PAH组)。依据是否伴发心血管并发症(包括心功能不全、高血压、先心病、心律失常和心包积液等),将患者分为SLE-无心血管损害组(n=30,年龄31.47±1.84岁,女29例)和SLE-有心血管损害组(n=16,年龄39.88±3.44岁,均女性)。10例健康女性(本院医护人员)作为正常对照组,平均年龄31.4±4.82 岁。本研究均取得受检者知情同意。
1.2 甲襞毛细血管镜检查
每组观察对象在NVC前至少4h内不吸烟或喝含咖啡因的饮料,并在22-23℃的房间内至少停留15min。于受检者双侧第三、第四指的甲襞皮肤滴石蜡油,由研究者采用200×的TR8000D型微循环显微检查仪(江苏同人医疗)进行常规检查和分析[7-9],连续取每手指甲襞中部1mm2的四个观测区域。应用专用软件(Videocap Scalar有限公司)存储及分析数字图像,分析参数包括:毛细血管的分布、形态、袢各分支直径、管袢长度、毛细血管密度即管袢数,不规则形态的毛细血管包括交叉管袢及畸形管袢、出血(表现为含铁血黄素沉积而形成的黑色团块)、流速等[10-12]。其中,输入支直径(μm)、输出支直径(μm)、袢顶直径(μm)、管袢长(μm)、管袢数(条/mm)以具体数值表示,其它形态学指标包括流速、出血、血色、畸形管袢数等以异常评分来评估[13]。
NVC检测的末梢毛细血管密度定义为每单位皮肤的毛细血管数量。正常甲襞毛细血管生理特点:(1)密度为9-13个毛细血管环/mm2皮肤;(2)毛细血管梳状有序排列;(3)传入支6-9μm,传出支8-21μm;(4)毛细管长度200-500μm。毛细血管管袢正常形态为发夹型或倒U型,正常情况下交叉管袢的比例不超过30%,畸形管袢不超过10%,超过此比例的交叉及畸形管袢积分大于0分。
1.3 实验室检查
采集SLE患者清晨空腹外周静脉血,分别加入EDTA抗凝管2ml和非抗凝管2ml收集血清,免疫比浊法检测血清补体C3、补体C4、免疫球蛋白IgG浓度,免疫荧光法定量检测抗凝血的BNP水平。
1.4 统计学处理
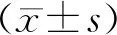
2 结 果
2.1 各组甲襞微循环比较
正常对照组甲襞毛细血管管袢数多数≥7条/ mm2,输入支、输出支及袢顶直径正常,血流速度正常,以线流为主,多数交叉管袢比例≤30%,畸形管袢比例≤10%,血色淡红,未见渗出及出血表现(图1、表1)。SLE-non-PAH组患者甲襞毛细血管表现为正常管袢减少,偶见管袢增粗、轻度畸形、散在出血(图2、表1)。SLE-PAH组患者甲襞毛细血管管袢数量明显减少,形态显著异常,血管畸形及出血明显增多,血色异常,毛细血管血流速度缓慢,以粒流或粒线流为主(图3、表1)。
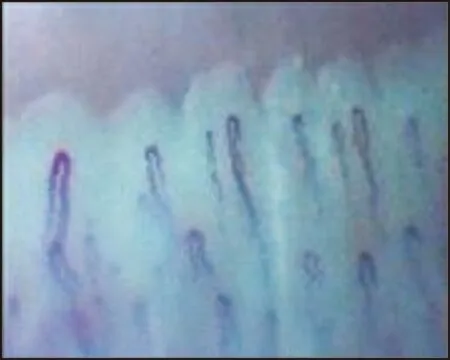
图1 正常对照组甲襞微循环表现(×200)

图2 SLE-non-PAH组甲襞微循环表现(×200)

图3 SLE-PAH组的甲襞微循环表现(×200)
与SLE-non-PAH组比较,SLE-PAH组管袢数显著减少(6.29±1.35 vs 5.41±1.57,P<0.05)。SLE-PAH组毛细血管的形态评分(3.589±0.556 vs 1.645±0.378,P<0.01)、流态评分(0.922±0.192 vs 0.282±0.089,P<0.01)、总评分(6.778±1.077 vs 3.293±0.628,P<0.01)和流速(0.564±0.103 vs 0.206±0.067,P<0.01)、红细胞聚集(0.200±0.076 vs 0.027±0.013,P<0.01)、血色(0.200±0.054 vs 0.048±0.018,P<0.01)等积分均显著高于SLE-non-PAH组。
SLE患者的输入支、输出支及袢顶直径均明显大于正常对照组,特别是SLE-PAH组,显著大于SLE-non-PAH组及正常对照组(P<0.05或P<0.01,表1)。SLE患者存在不同程度的交叉管袢和畸形管袢比例增加,其中SLE-PAH组患者严重异常形态的管袢比例高于SLE-non-PAH组,尽管未有统计学差异。NVC的综合评估显示,整体SLE人群的重度异常者占21.70%(10/46),其中SLE-PAH组占70.00% (7/10),在SLE-PAH组中以重度异常为主(41.20%),SLE-non-PAH组中以轻度异常为主(72.50%),两组患者的异常比例有统计学差异(P<0.05)。见表1。

表1 各组甲襞毛细血管管袢形态和异常管袢比例
注:与正常对照组比较,1)P<0.05,2)P<0.01;与SLE-non-PAH组比较,3)P<0.05
2.2 SLE-有心血管损害组患者NVC指标变化及与BNP水平的性关性
与SLE-无心血管损害组患者比较,SLE-有心血管损害组患者甲襞微循环管袢数明显减少(6.24±1.32 vs 5.28±1.69,P<0.05),而形态(3.263±0.583 vs 1.939±0.405,P<0.05)、流态(0.862±0.223 vs 0.354±0.090,P<0.05)和总积分(6.194±1.221 vs 3.819±0.650,P<0.05)、输出支管径(0.437±0.081 vs 0.260±0.060,P<0.05)、畸形管袢数(0.225±0.081 vs 0.080±0.026,P<0.05)、红细胞聚集(0.187±0.082 vs 0.040±0.014,P<0.05)和血色(0.200±0.057 vs 0.053±0.019,P<0.05)等积分显著高于SLE-无心血管损害组患者。
SLE-有心血管损害组患者的甲襞毛细血管的形态、流态、袢周积分和总积分、输入支直径、流速、血色、出血等评分及与心功能指标-血浆BNP水平呈正相关(r值在0.6394-0.7823之间,P<0.05或P<0.01),而管袢数与BNP水平呈负相关(r=-0.7520,P<0.01)。
2.3 NVC指标与SLE患者免疫指标的相关性
SLE患者输入支直径、输出支直径、袢顶直径、畸形管袢数、流速、血色等评分及形态积分、流态积分和总积分均与IgG水平呈正相关(r值在0.2918-0.4813之间,P<0.05或P<0.01),而毛细血管管袢数与IgG水平呈负相关(r=-0.3317,P<0.01)。在SLE-PAH组患者中,袢周积分、总积分与血清补体C3水平负相关(r=-0.5074、-0.3390,P<0.05),袢顶直径大小与补体C3呈正相关(r=0.4990,P<0.05),上述指标与补体C4水平无明显相关性。
3 讨 论
研究已证实,甲襞毛细血管检测异常反映了系统性硬化症-SSc的严重程度,特别是与心肺严重并发症相关,可作为预后判断的无创检测工具[14,15],但在SLE患者中的应用报道较少,而SLE为我国最常见的结缔组织病(300—700例/百万),发病率远高于SSc(10-50例/百万),在我国伴发PAH的结缔组织病中SLE也占第一位[16],且预后差、死亡率高,故探索NVC在SLE并发PAH及其它心血管并发症中的作用非常必要。SLE-PAH的病理机制以肺血管炎为主,表现为肺小血管的炎性充血水肿及随后的血管内壁增厚、血管重构狭窄,肺循环阻力明显升高,与SLE皮肤小血管的病变相似且多同步。NVC可清晰测量末梢毛细血管的数量、管径及形态、充血、血液流速等变化,故可能间接反映患者的肺血管病变程度,因此本文系统研究了SLE-PAH患者的NVC特点。
本文结果显示,SLE患者特别是SLE-PAH组患者的毛细血管镜下存在各种异常,包括管袢数减少、管径异常、形态、流态评分升高、交叉及畸形管袢等异常形态比例增加、流速减慢、红细胞聚集及出血等,且近半数SLE-PAH患者的NVC表现为重度异常,提示SLE在其肺动脉高压的发生发展过程中,伴随着末梢微血管数量的减少、直径及形态异常、血流减慢,验证了外周毛细血管与作为PAH发病基础的肺内微血管可能存在相似的病理生理变化,故而NVC的上述指标对SLE-PAH的早期预测发生具有重要的临床意义,可实时间接反映肺血管的病变程度。
本研究还发现,SLE患者甲襞毛细血管管袢数与IgG水平呈负相关,其管径、畸形管袢数、流速等与IgG水平呈正相关,而伴PAH患者的袢顶直径与补体C3呈正相关。C3 和IgG与SLE的活动程度及慢性病程相关,提示SLE急性活动时主要影响患者的毛细血管远端,如SLE病情长期控制不佳,将导致微血管的形态、结构、数量及血流变化,PAH的风险指数明显增加。甲襞毛细血管指标与补体C4无明显相关,可能因为C3比C4更能灵敏反映SLE疾病活动且下降更为明显[17,18]。因此NVC指标还可提示SLE及其PAH的病情活动性。
另外,本文结果还表明SLE伴发心血管并发症的患者甲襞毛细血管管袢数明显减少,而形态、管径、畸形管袢数、红细胞聚集等异常指标显著升高,且与心衰指标BNP呈正相关,提示NVC可作为SLE患者的心血管疾病特别是心功能不全发生及严重程度的预测指标和评估手段。
总之,SLE伴发PAH患者的NVC多项指标变化与病情活动及心血管并发症相关。2015年最新的中国SLE研究协作组制定的“中国成人SLE相关PAH诊治共识”中[19],关于SLE-PAH诊断评估的影像学手段主要为心脏超声和右心导管,尚未提到甲襞毛细血管镜。本研究证实了NVC对SLE-PAH具有预测及评估意义,且其操作简单、费用低、无明显禁忌症、可床边操作,提示NVC作为一项新兴的无创性检查手段,适用于初步筛查SLE患者,协助临床医生预测患者发生PAH及心血管事件的风险及预后。

