Fe3O4-COOH纳米材料的表征及富集能力检测
黄艳玲,程 杨,李春媛,刘鑫龙
(1.天津现代职业技术学院 天津 300350;2.天津市食品研究所有限公司 天津 301609;3.天津市林业果树研究所 天津 300384)
0 引 言
纳米技术是一项新的科学技术分支,已经发展到能源生产、工业生产及生物医学等方面[1]。在生物学和生物医学方面便是其中一个关键应用。纳米粒子(NP)可以被设计成具有独特的组成和功能,用以提供在生物医学研究中难以想象的新工具和技术[2]。
磁性 NP平台有多种类型,具有不同的大小、形状、组成和功能。此外,每种类型的纳米粒子都可能通过不同的技术制造出来,例如聚合物纳米粒子的纳米沉淀。虽然磁性 NP平台及其制造存在差异,但随着磁性纳米颗粒应用的多样化,在生物样品分离富集预处理中,它们提供更多的应用领域,而且减少对昂贵和费力的预处理方案(其主要瓶颈是生物分子的分离富集)的依赖。与传统色谱技术相比,生物分子磁性分离富集处理有许多优点[3],即:①快速分离;②处理步骤少;③蛋白质最小程度降解;④降低系统成本;⑤适宜复杂体系;⑥过程较温和缓慢;⑦可以保持高通量;⑧颗粒相容性高。这主要因为它们是超顺磁性的。超顺磁性纳米颗粒通常带有亲水涂层或其他生物相容性化合物的氧化铁核以提高其稳定性,磁铁矿(Fe3O4)或磁赤铁矿(γFe2O3)核心被广泛使用。这些磁性 NP表现出很大的依赖性使其在施加外部磁场时被磁化,而在去除外加磁场时表现出零净磁化,因此在生物技术领域被广泛研究[4]。
为了解决生物分子的分离富集问题,我们通过利用 Fe3O4-COOH纳米材料对微生物裂解液中的蛋白进行富集,以提高MALDI-TOF MS对蛋白检测的灵敏性与分辨率,通过增加质谱中蛋白检出的数量,以提高微生物指纹峰的数量,从而增强微生物鉴别的效果。对 Fe3O4-COOH纳米材料合成方法、表征及富集能力检测详见下文。
1 材料与方法
1.1 仪器
本章所涉及的实验仪器主要用于对磁性材料进行表征(表1),其中主要包括场发射扫描电子显微镜、傅里叶变换红外光谱仪、振动探针式磁强计,分别对 Fe3O4-COOH纳米材料的形貌特征、官能团与磁性大小进行分析。Milli-Q水纯化系统、超声波清洗器为实验辅助仪器,主要用于 Fe3O4-COOH磁性材料的合成。
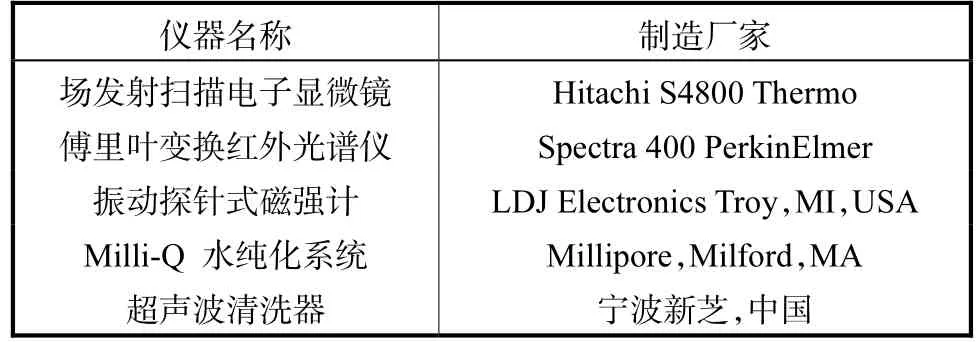
表1 主要实验仪器设备Tab.1 Experiment apparatus and equipment
1.2 材料
本实验所涉及的实验材料为分析纯,用于磁性材料的合成。主要实验材料见表2。

表2 试验药品Tab.2 Experiment reagents
1.3 实验方法
1.3.1 制备Fe3O4-COOH纳米材料
在 20mL乙二醇中,分别加入 FeCl3·6H2O 和Na3C6H5O7(柠檬酸钠),溶解并超声混匀,然后加入CH3COONa并搅拌混匀后,在200℃条件下,在高压反应釜中加热 8h得到黑色固体,再在外加磁场中,用超纯水与无水乙醇反复清洗,最后所得的黑色固体在真空干燥箱中60℃干燥过夜。
1.3.2 Fe3O4-COOH纳米材料的表征
主要利用场发射扫描电子显微镜、傅里叶变换红外光谱仪、振动探针式磁强计分别对 Fe3O4-COOH纳米材料的形貌特征、官能团与磁性大小进行分析,以判断Fe3O4-COOH纳米材料是否成功合成。
1.3.3 BSA的富集与检测
BSA用超纯水配制成 50mmol/L溶液,然后用序列级胰蛋白酶过夜水解,将所得水解液依次稀释成不同浓度,加入由 20mmol/L的醋酸钠溶液配制的Fe3O4-COOH 纳米颗粒悬浊液,取出 100µL Fe3O4-COOH悬浊液分别加入到不同浓度的 BSA水解液中,振荡 30min充分吸附后,磁性分离,用 10µL磷酸缓冲液与 10µL乙腈洗脱 10min,吸取 1µL洗脱液与1µL CHCA用于MALDI-TOF MS反射模式分析。将所得的质谱峰进行数据库检索,以确定所分析的BSA肽段。
MALDI-TOF MS反射模式分析具体参数如下:ion source 1,20kV;ion source 2,16.65kV;lens,8.73kV;pulsed ion extraction,150ns;matrix suppression,700Da.
BSA 多肽数据检索条件:digest used,Trypsin;maximum of missed cleavages,1;mass tolerance,±90mg/mL;fixed modifications,Carbamidomethyl(C);variable modifications,the oxidation of methionine。检索得分大于70分为显著。
2 结果与讨论
2.1 Fe3O4-COOH纳米材料的表征
Fe3O4-COOH纳米材料合成完毕,对其进行场发射扫描,电子显微镜、傅里叶变换红外光谱仪、振动探针式磁强计分别对 Fe3O4-COOH纳米材料的形貌特征、官能团与磁性大小进行分析。
从图1可以看出,图中所有 Fe3O4-COOH粒子接近于球形,同时显示制备的 Fe3O4-COOH磁性粒子的直径在 600nm左右。Fe3O4-COOH磁性粒子的FT-IR光谱图(图2)显示,Fe3O4-COOH 磁性粒子中-COOH 的-OH 强的红外特征峰在 1403cm-1,另外Fe3O4-COOH 粒子的-COO¯中 C=O 红外吸收在1626cm-1,而且在 587cm-1的 Fe-O 伸缩振动也在Fe3O4-COOH红外图中被发现,这表明 Fe3O4-COOH磁性粒子被成功合成。磁滞回线评价了Fe3O4-COOH粒子的磁响应特性,如图3所示。Fe3O4-COOH粒子的磁化值分别为46emμ/g,这可使磁性粒子在外加磁铁条件下,很容易地从水溶液中分离。这表明 Fe3O4-COOH磁性粒子已经具备了吸附蛋白的-COO¯官能团和很强的磁性。

图1 Fe3O4-COOH磁性颗粒扫描电镜图Fig.1 SEM image of Fe3O4-COOH particles
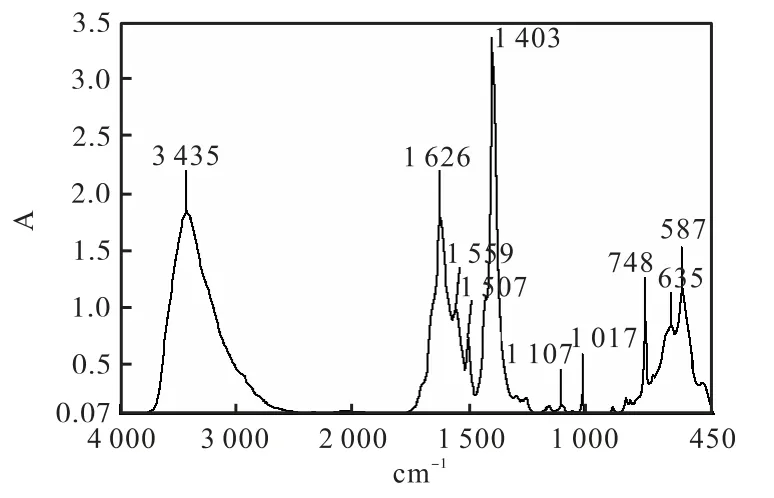
图2 Fe3O4-COOH磁性颗粒红外谱图Fig.2 FTIR spectrum of Fe3O4-COOH particles

图3 Fe3O4-COOH磁性颗粒磁滞回线图Fig.3 Hysteresis loops of Fe3O4-COOH particles
2.2 BSA的富集与MALDI-TOFMS
为了验证 Fe3O4-COOH磁性颗粒对蛋白的富集能力,BSA蛋白溶液被胰蛋白酶消化 18h,然后稀释成不同浓度 50fmol/µL和 5fmol/µL的 BSA 水解溶液,通过 Fe3O4-COOH磁性颗粒对其进行富集,观察Fe3O4-COOH磁性颗粒富集低丰度多肽的能力,在900~2100Da的质量范围内分析 BSA蛋白的酶裂解产物。BSA 的胰酶裂解产物(50fmol/µL)被 Fe3O4-COOH磁性颗粒富集的质谱图显示在图4(a)。经过Fe3O4-COOH磁性颗粒富集,13个匹配的多肽峰可以被质谱检测到,其序列覆盖度达到 20%。这些峰值的相应匹配序列显示在表3中。
当 BSA 胰蛋白酶消化的浓度降低到 5fmol/µL时,如图4(b)所示,在没有任何富集时,质谱中不能检测到任何多肽信号。而 Fe3O4-COOH磁性颗粒富集后,如图4(c)所示,仍有 4个匹配的肽段出现在MALDI-TOF MS质谱图中,4个匹配峰是:1283.7634、1478.4624、1494.4872、1567.6283m/z(图4c)。结果表明,Fe3O4-COOH磁性颗粒具有较强的低丰度多肽富集能力。

图4 BSA胰蛋白酶解多肽分别用 Fe3O4-COOH富集(100µL,10mg·mL-1)和不富集的 MALDI 谱图Fig.4 MALDI spectra of BSA trypsin digestion peptide without and with enrichment using Fe3O4-COOH(100µL,10mg·mL-1)
3 结 论
Fe3O4-COOH纳米颗粒具有合成简单、应用成本低的特点。本研究成功地合成 Fe3O4-COOH纳米颗粒,并对其进行表征,同时利用 Fe3O4-COOH纳米粒子对 BSA裂解液中的菌体蛋白进行富集,不仅可以提升MALDI/TOF MS检测的分辨率和灵敏性,而且可以增大BSA检测限。因此Fe3O4-COOH纳米颗粒富集菌体蛋白的方法有可能推广应用于致病菌菌株水平鉴别。
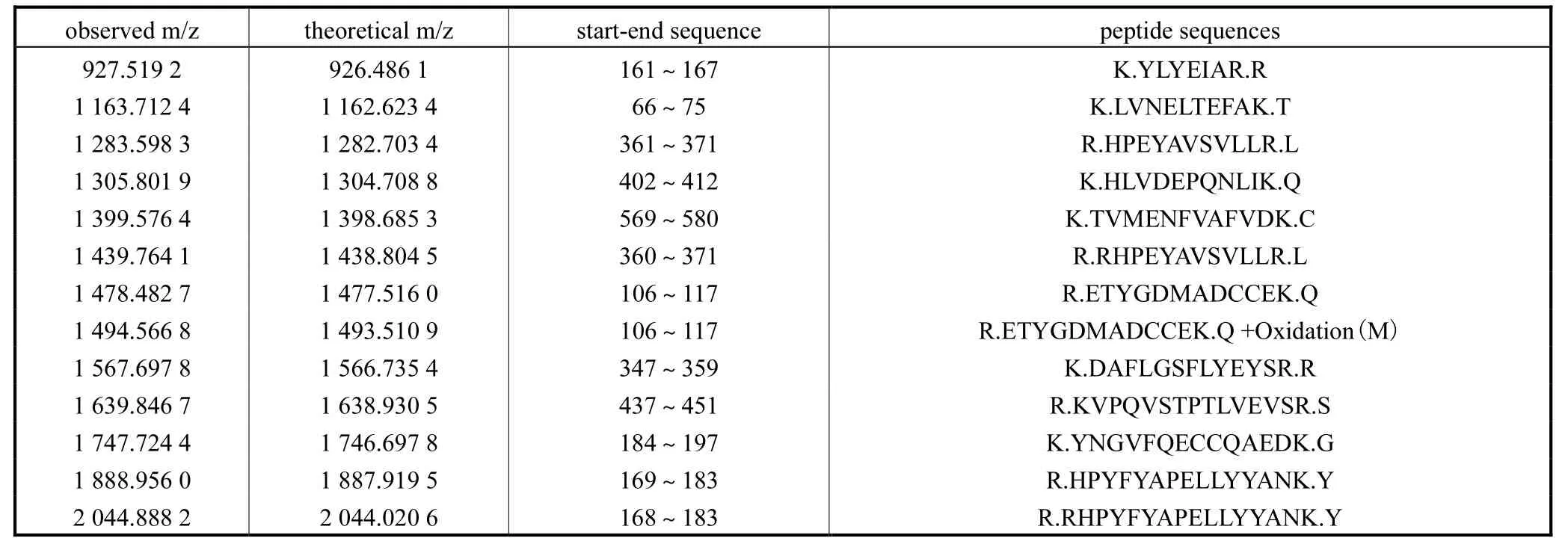
表3 BSA胰蛋白酶消解多肽(50 fmol·µL-1,5 fmol·µL-1)利用Fe3O4-COOH磁性颗粒富集的Mascot搜索结果Tab.3 Mascot search results for BSA(50 fmol·µL-1 and 5 fmol·µL-1)digested by trypsin with enrichment using Fe3O4-COOH particlesa

