超高压辅助低共熔溶剂提取复方双黄连有效成分
王慧,席小丽
(1.山西大学 分子科学研究所,山西 太原 030006;2.太原科技大学 化学与生物工程学院,山西 太原 030024)
0 引言
复方双黄连是由金银花、黄芩、连翘三味药材组成的复方制剂,主要用于治疗风热感冒发热、肺炎、呼吸道感染、扁桃体炎等疾病[1-2],对呼吸道感染及病毒性疾病有确切的疗效。
目前,复方双黄连有效成分的提取方法主要是传统的水提法,中华人民共和国药典方法(2015年版)需要对药物原料多次煎煮、反复浸提并多次过滤,操作工艺复杂,成本较高,生产周期较长。因此,为了进一步探讨更加经济绿色的提取技术,相关学者开始致力于研究超高压技术以及采用低共熔溶剂等新型溶剂应用于中药成分的提取。超高压提取技术(UPE)是最近几年才出现的一种全新的常温提取技术[3],超高压提取温度较低,有利于复方双黄连热敏感程度成分绿原酸和连翘苷的提取。
低共熔溶剂(Deep eutectic solvents,DESs) 是由2种或2种以上组分组成的低共熔体系,它有许多独特的性质,如较低的熔点,较高的表面张力,低的蒸汽压,相对高的热稳定性,良好的扩散速度,以及优良的溶解性,可溶解多种无机物质及难溶的有机物等。由于DESs 独特的理化性质,目前在中药提取、分离和分析等方面得到了广泛的应用,很多研究人员用低共熔溶剂来提取和分离天然产物中酚类、黄酮类、萜烯类、多糖、蛋白质等不同极性的化合物,并且取得了良好的效果[4-6]。氯化胆碱(Choline Chloride,ChCl)是动物生长不可缺少的一种水溶性维生素,在动物体内起着极其重要的作用,现已成为人类食品和动物饲料中的常用添加剂。乳酸(Lactic Acid,LA)是一种天然有机酸,由于酸性柔和且性质稳定,美国FDA将其确认为安全优良的防腐剂和腌渍剂,用于清凉饮料、糖果、糕点的生产当中。另外,乳酸水溶液还可以延长禽肉和鱼肉的保质期。前期的研究证明,用ChCl-LA作为溶剂提取黄芩苷达到了理想的效果[7]。另外据文献[8]报道组成DESs的单个成分无毒,则 DESs也无毒。
本文以ChCl-LA作为提取溶剂,结合超高压方法提取复方双黄连的3种有效成分;依据单因素实验结果,选取低共熔溶剂含水量、固液比、提取压力、提取时间4个因素,并且采用正交实验法优化了复方双黄连3种有效成分的提取条件;同时和药典提取方法进行对比。
1 实验部分
1.1 仪器和材料
Agilent 1260高效液相色谱仪(美国Agilent公司);HLM-100-300S食品高压加工机(山西三水银河科技有限公司);Sarturius.BS110S分析天平(北京赛多利斯天平有限公司);HH4恒温水浴锅(余姚市东方电工仪器厂)。
黄芩饮片(批号:1712035;规格:0.5 kg/袋)、连翘饮片(批号:1812071;规格:0.5 kg/袋)、金银花饮片(批号:1809004;规格:0.5 kg/袋)均购于安国市远光药业有限公司,均符合《中国药典》2015年版规定。黄芩苷标准品(批号:331C021)、绿原酸标准品(批号:516E021)、连翘苷标准品(批号:226A023)均由北京索莱宝科技有限公司提供,纯度均>98%;色谱甲醇(赛默飞世尔科技有限公司);所用水均为纯净水;其他试剂均为分析纯。
1.2 实验方法
1.2.1 DESs的合成和DESs水溶液制备
DESs的合成:将氯化胆碱与乳酸以摩尔比1∶1的比例混合放置在圆底烧瓶中,用磁力搅拌器90℃搅拌10 h左右,直至形成均一稳定的透明体系。待冷却至室温后,将所得DESs密封置于干燥器中以P2O5干燥至少14 d,备用。
DESs水溶液制备: 按照体积分数配制一定含水量(10%、20%、30%、40%、50%)的低共熔水溶液,充分摇匀、静置,得到均一、透明的低共熔水溶液。
1.2.2 样品提取
取黄芩饮片、连翘饮片、金银花饮片粉碎,过60目筛,称取黄芩(0.125 g),连翘(0.25 g),金银花(0.125 g),加入4 mL低共熔溶剂(ChCl-LA,摩尔比1∶1)混合置于聚乙烯袋(PE)内抽真空密封,将上述封装好的样品放入超高压设备中,设置提取条件(提取压力为400 MPa,提取时间为4 min)。提取完毕后,对其进行离心过滤,按照1.2.3.1色谱条件测定提取液中绿原酸、黄芩苷、连翘苷含量。
所得黄芩苷、连翘苷、绿原酸的含量计算公式为:
含量(mg/g)=CV/M
其中C表示样品溶液中被测物质的浓度(mg/mL);V表示样品溶液的体积(mL);M表示粉末的干重(g)。
1.2.3 含量测定
1.2.3.1 HPLC色谱条件
参考文献[9],金银花、黄芩、连翘中活性成分的含量测定使用安捷伦1260液相系统(安捷伦科技有限公司,美国),含在线真空脱气机、G1311C高压四元泵、G1329B 自动进样器、G1314B VWD检测器、GT-30 柱温箱。色谱柱:Venusil XBP-C18反相色谱柱(4.6 mm×250 mm 5 μm,100 Å),流速:1.0 mL/min,进样量:10 μL,检测波长:278 nm和324 nm,流动相:甲醇(A)和0.5%磷酸水溶液(B),洗脱条件:0~30 min,10%~35%(B);30~50 min,35%(B)。
1.2.3.2 对照品溶液的制备
精密称取绿原酸对照品14.5 mg,连翘苷对照品10.2 mg,黄芩苷对照品27.9 mg,于100 mL容量瓶,加入甲醇溶解定容,即得(即配即用)对照品贮备液。
1.2.3.3 标准曲线的绘制
分别精密量取对照品储备液1.0、3.0、5.0、7.0、9.0 mL至10 mL容量瓶并用甲醇稀释定容,在上述色谱分析条件下各测定3次。以分析所得峰面积为纵坐标(y),各个对照品溶液所对应浓度为横坐标(x),分别得到各对照品的标准曲线。
1.2.3.4 方法学考察
(1)精密度试验
取3种对照品溶液,1 d内各连续进样6次,计算各色谱峰的峰面积(A)和保留时间的RSD值,考察日内精密度。取同一供试品溶液,连续3 d,每天进样3次,测定日间精密度。
(2)重复性试验
将同一批金银花,连翘,黄芩饮片,按照正交试验优化所得的条件制备供试品溶液,取样品6份重复测定,得到3种主要有效成分的对应峰的峰面积和保留时间的RSD值。
(3)稳定性试验
按正交试验优化所得的条件制备供试品溶液,精密吸取供试品溶液分别于2、4、6、8、10、12、24 h进行分析测定,得到3种主要有效成分的对应峰的峰面积和保留时间的RSD值。
(4)准确度试验
利用加样回收法,称定黄芩饮片粉末(0.125 g),连翘饮片粉末(0.25 g),金银花饮片粉末(0.125 g),分别按3种物质质量百分含量的50%、100%、150%加入3种物质的标准品,按照优化所得到的最终条件提取样品,分析并计算3种物质的加样回收率及RSD值。
1.2.4 超高压提取的单因素试验
采用单因素试验法,以含水量(A)、提取压力(B)、提取时间(C)、固液比(D)为影响因素,绿原酸、黄芩苷、连翘苷含量为评价指标。
1.2.4.1 含水量筛选
称取黄芩饮片(0.125 g),连翘饮片(0.25 g),金银花饮片(0.125 g),配制5 mL含水量分别为10%、20%、30%、40%、50%的ChCl-LA低共熔溶剂,将药材和溶剂真空包装在PE袋中,将封装好的样品放入超高压设备中,设定保压时间4 min,提取压力400 MPa对其进行超高压处理,将处理后的样品进行离心过滤,按照1.2.3.1色谱条件测定提取液中绿原酸、黄芩苷、连翘苷含量。
1.2.4.2 提取时间考察
称取黄芩饮片(0.125 g),连翘饮片(0.25 g),金银花饮片(0.125 g),选择1.2.4.1中优化得到的40%的含水量,5 mL ChCl-LA作为溶剂,真空包装在PE袋中,将上述样品放入超高压仪器样品孔,固定保压时间1、2、4、5、6、8、10 min。设置提取压力为400 MPa对其进行超高压处理,将处理后的样品进行离心过滤,按照1.2.3.1色谱条件测定提取液中绿原酸、黄芩苷、连翘苷含量。
1.2.4.3 提取压力考察
称取黄芩饮片(0.125 g),连翘饮片(0.25 g),金银花饮片(0.125 g),选择1.2.4.1中优化得到的40%含水量,5 mL ChCl-LA作为溶剂,真空包装在PE袋中,将上述样品放入超高压仪器样品孔中,固定1.2.4.2中优化得到的保压时间4 min,设置提取压力分别为100、200、300、400、500、600 MPa对其进行超高压处理,将处理后的样品进行离心过滤,按照1.2.3.1色谱条件测定提取液中绿原酸、黄芩苷、连翘苷含量。
1.2.4.4 固液比筛选
称取黄芩饮片(0.125 g),连翘饮片(0.25 g),金银花饮片(0.125 g),选择1.2.4.1中优化得到的40%含水量,分别加入3、4、5、6、7、8、9 mL ChCl-LA低共熔溶剂,真空包装在PE袋中,将封装好的样品放入超高压设备中,设置提取压力为400 MPa,保压时间4 min,进行超高压处理,将处理后的样品进行离心过滤,按照1.2.3.1色谱条件测定提取液中绿原酸、黄芩苷、连翘苷含量。
1.2.5 正交试验
为进一步确定最佳超高压提取条件和各因素的影响顺序,选定低共熔含水量、提取压力、提取时间、固液比4个考察因素,各因素选择3个水平,按L9(34)正交表进行了实验。
1.2.6 提取方法比较研究
为验证优化所得提取方法的有效性,我们将其与药典法进行了比较。
1.2.6.1 药典提取方法(Pharmacopoeia)
称取黄芩饮片粉末5 g,连翘饮片粉末10 g,金银花饮片粉末5 g, 按照双黄连口服液的药典提取方法进行提取[10],将处理后的样品进行离心并过滤,计算各主要成分含量。
1.2.6.2 超高压辅助低共熔溶剂提取方法(DESs-UPE)
称取黄芩饮片粉末5 g,连翘饮片粉末10 g,金银花饮片粉末5 g,加入含水量为30%的低共熔溶剂(ChCl-LA,摩尔比1∶1)160 mL,混合置于聚乙烯袋(PE)内抽真空密封,将上述封装好的样品放入超高压设备中,设置提取条件(提取压力为400 MPa,提取时间为4 min)。提取完毕后,对其进行离心过滤,按照1.2.3.1色谱条件测定提取液中各主要成分含量。
2 结果与讨论
2.1 标准曲线的制备
结果表明(表1),3个提取化合物在测定范围内线性良好(r2> 0.999)。其中绿原酸的线性范围为0.014 5~0.145 0 μg/mL,连翘苷的线性范围为0.010 2~0.102 0 μg/mL,黄芩苷的线性范围为0.027 9~0.279 0 μg/mL。
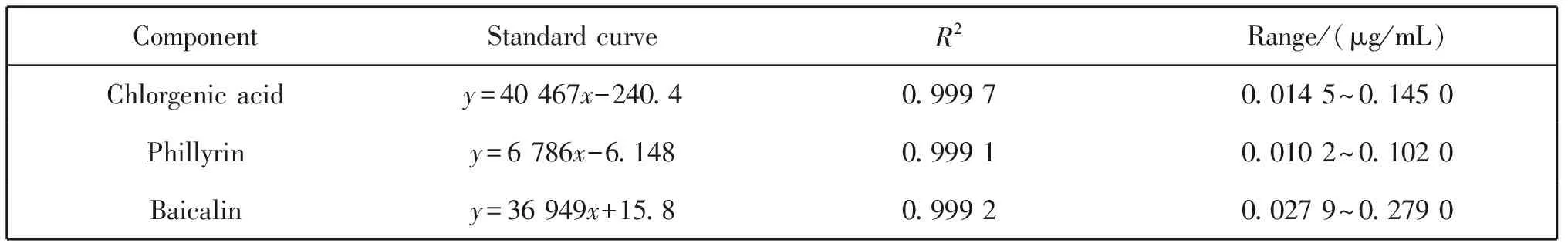
表1 3种活性成分标准曲线
2.2 方法学考察
2.2.1 精密度的考察
精密度试验结果表明(表2和表3),日内及日间精密度的相对标准偏差(RSD)都小于3%,说明该方法的精密度良好。
2.2.2 重复性考察
试验结果如表4所示,3种主要有效成分所得RSD都小于3%,表明试验重复性良好。
2.2.3 稳定性考察
稳定性结果表明(表5),3种主要有效成分所得RSD均小于3%,表明样品溶液在24 h内有良好的稳定性。
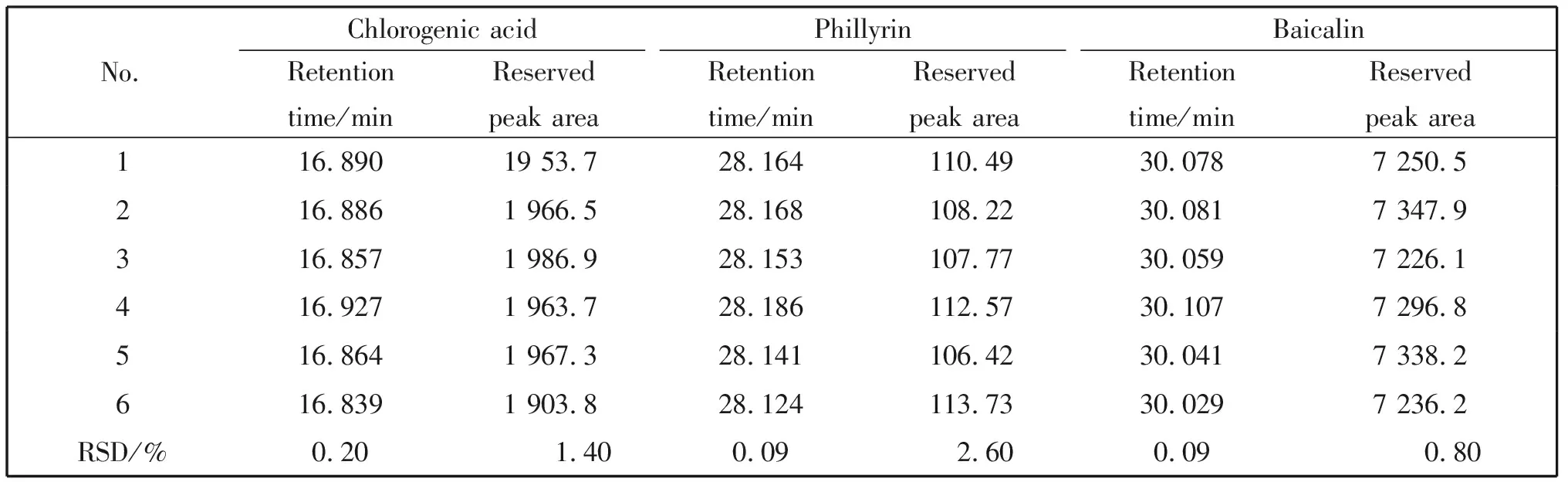
表2 考察日内精密度所得实验结果
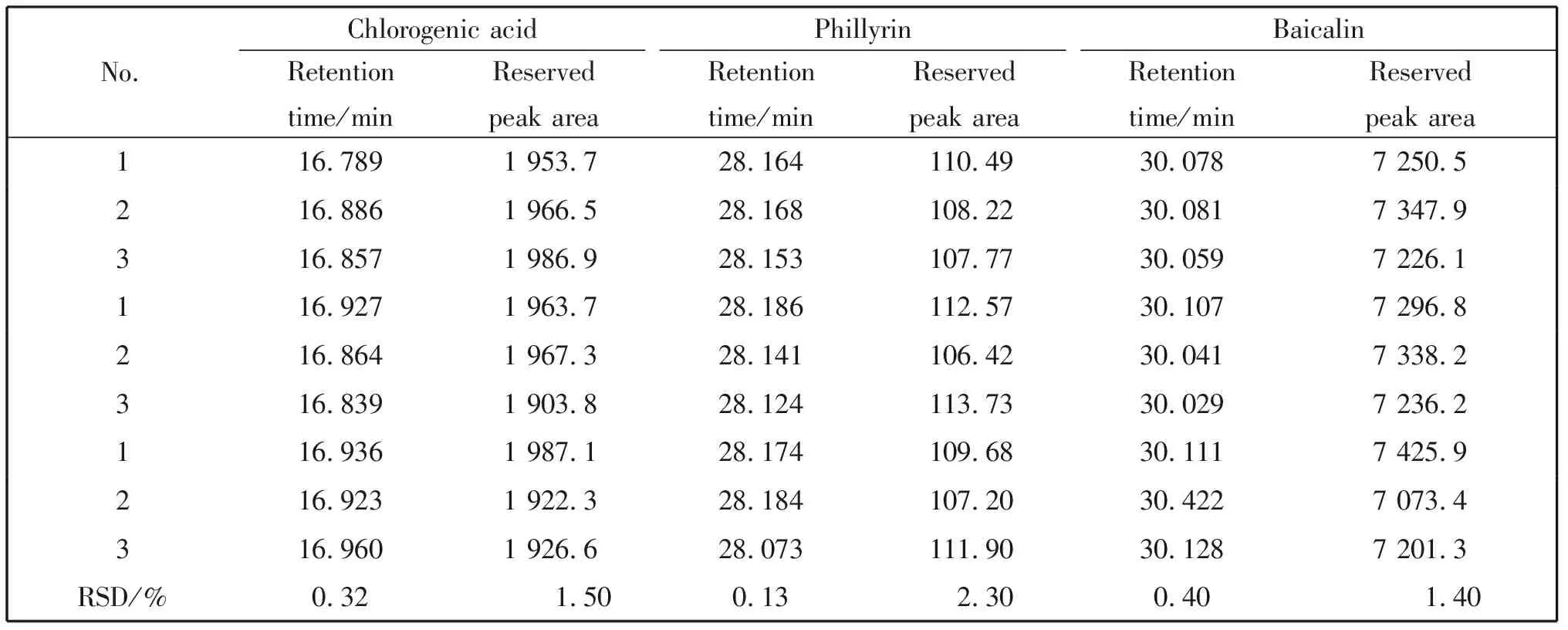
表3 考察日间精密度所得实验结果
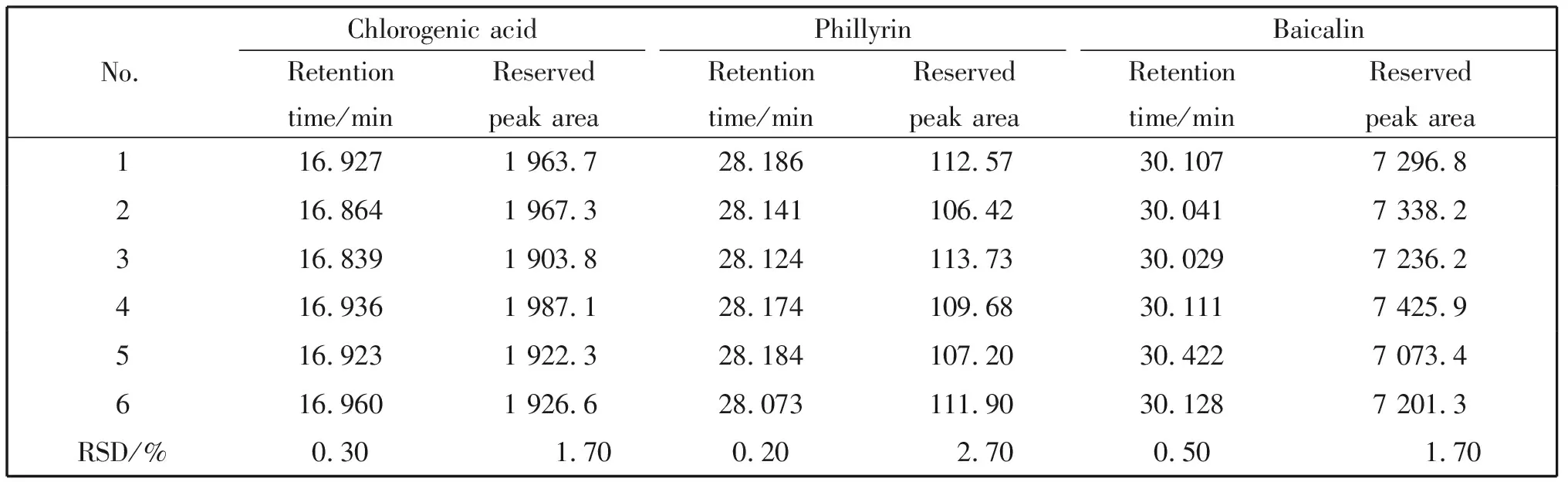
表4 重复性实验结果
2.2.4 准确度考察
加样回收率试验结果表明(见表6、表7、表8),由表中数据可知,3种活性成分的加样回收率均在95%~105%范围内,表明该方法回收率高,满足分析测定的要求。
2.3 单因素考察实验
2.3.1 含水量对提取液中黄芩苷、绿原酸、连翘苷含量的影响
含水量对低共熔溶剂的黏度、表面张力以及极性等起着很重要的作用,通过低共熔溶剂中添加水可以影响提取的效果。因此,我们考察了含水量分别为 10%、20%、30%、40%、50%的低共熔溶剂对3种活性成分提取效果的影响。图1结果表明,在相同的高压提取条件下,低共熔溶剂含水量为40% 时对绿原酸、连翘苷、黄芩苷3种活性成分的提取效果最好,分别为29.72 mg/g,5.9 mg/g,112.81 mg/g,这可能是因为加入水后低共熔溶剂的黏度减小、低共熔溶剂对样品的渗透作用增强,导致提取效率提高[11]。但当含水量超过40%时,3种活性成分的提取含量反而降低,这可能是由于加入过量的水,使低共熔溶剂极性增大,从而破坏了低共熔溶剂体系内部的氢键作用,导致目标成分溶解度降低[12]。所以后续实验选择了40%含水量的低共熔溶剂。
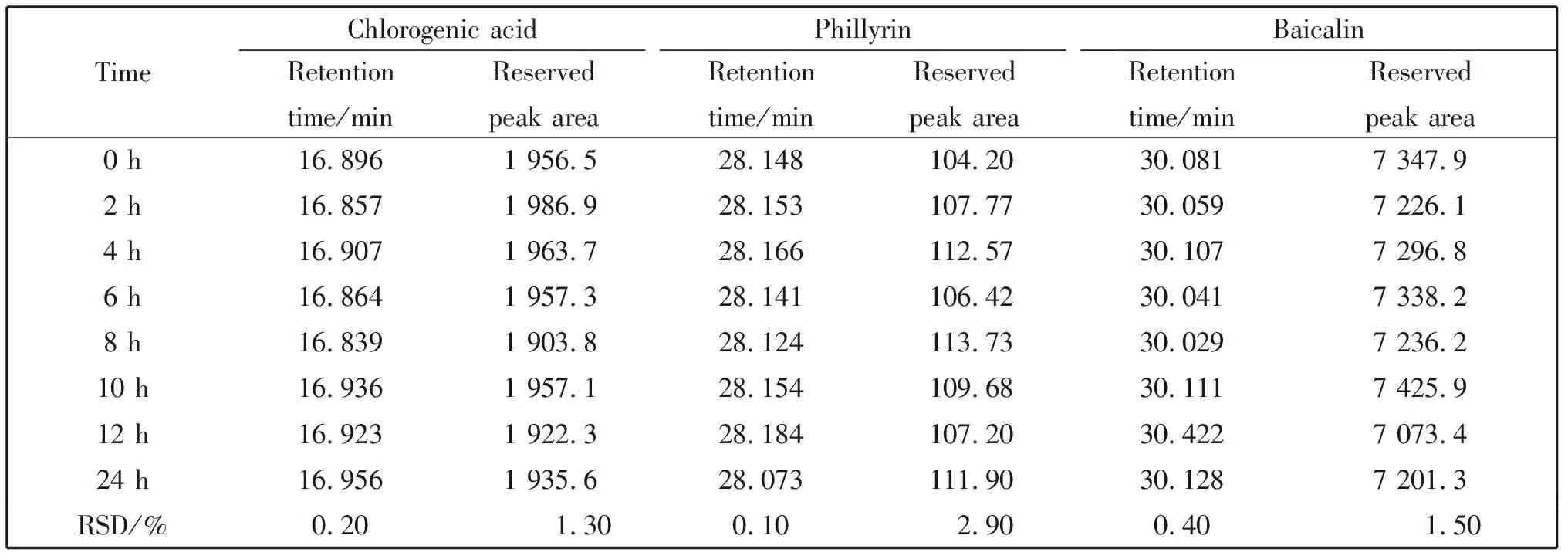
表5 稳定性实验结果
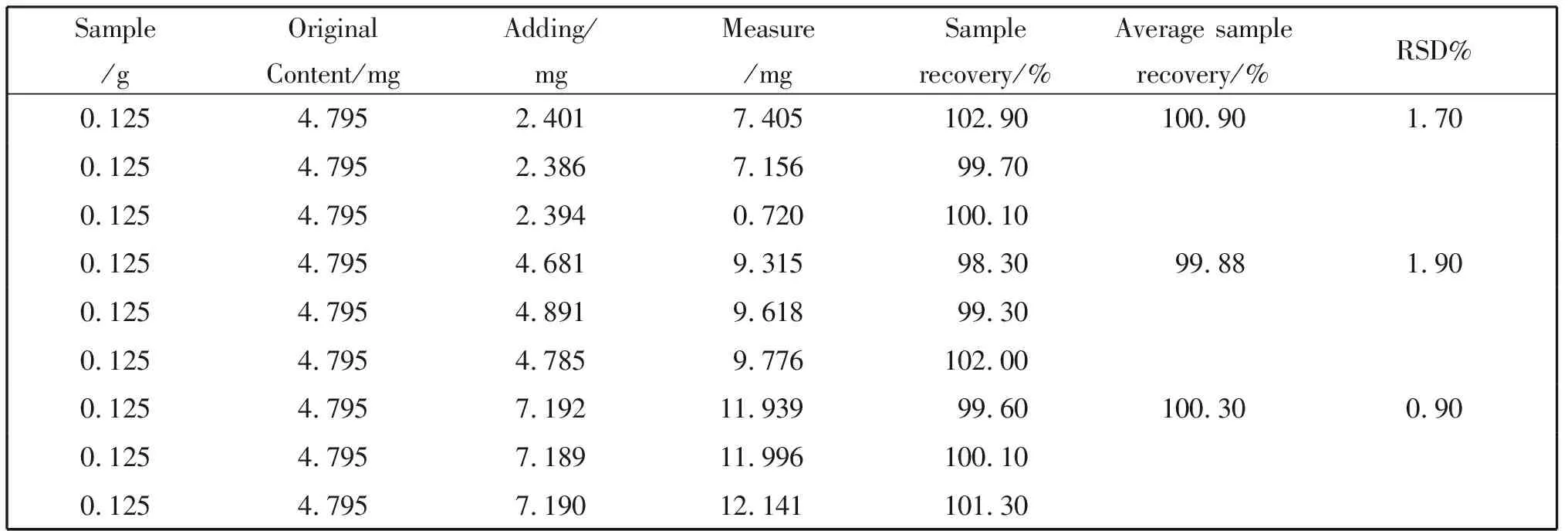
表6 绿原酸加样回收率
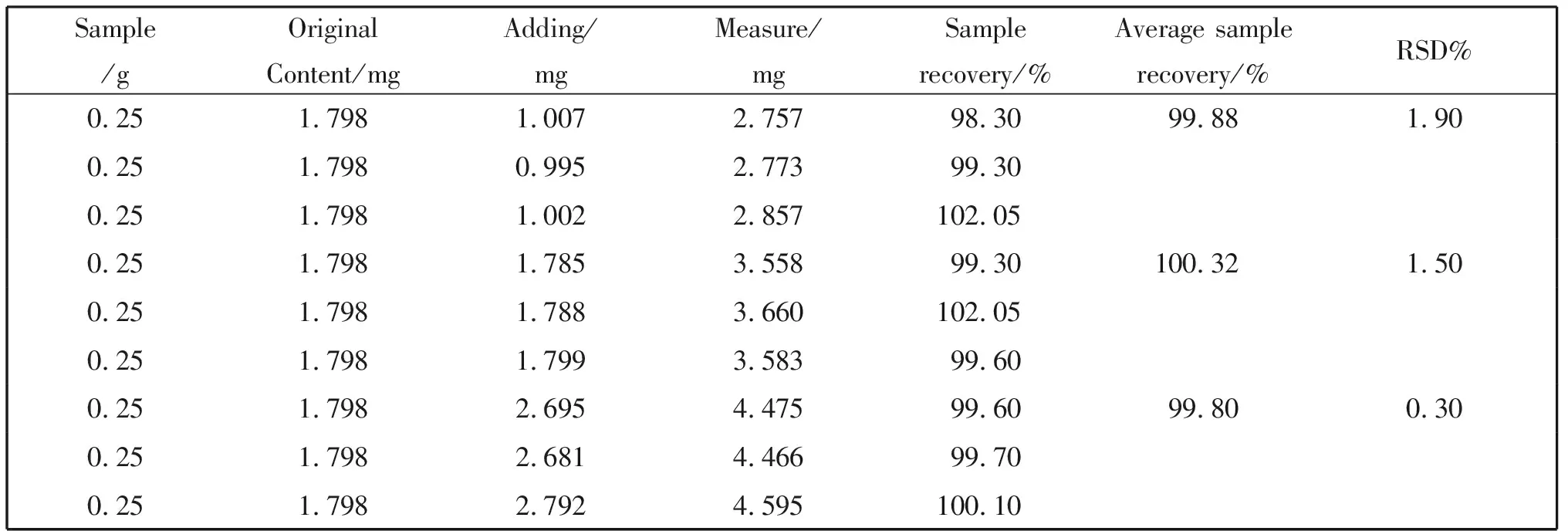
表7 连翘苷加样回收率

表8 黄芩苷加样回收率

Fig.1 Effect of water content in DESs on the extraction content图1 不同含水量的低共熔溶剂对提取含量的影响
2.3.2 保压时间对提取液中黄芩苷、绿原酸、连翘苷含量的影响
保压时间对3种活性成分提取含量的影响如图2所示,保压时间达到4 min时,3种有效成分的提取含量达到最高,当继续延长时间时对提取含量影响不大。这是因为超高压提取的过程是先增加压力,保持一段时间使植物细胞内外压力达到平衡后突然泄压,在增压过程中,细胞内外渗透压力突然增大,溶剂在高压下迅速渗透到细胞内,慢慢达到溶解平衡; 卸压过程中由于压力的突然降低,这导致有效成分能够穿过细胞的各种膜而转移到细胞外,从而达到高效提取的目的[13]。这表明植物细胞在400 MPa 高压下破裂很快,4 min时已充分破裂,细胞溶解已达到平衡,提取含量达到最高。故选择保压时间4 min进行下一步实验。
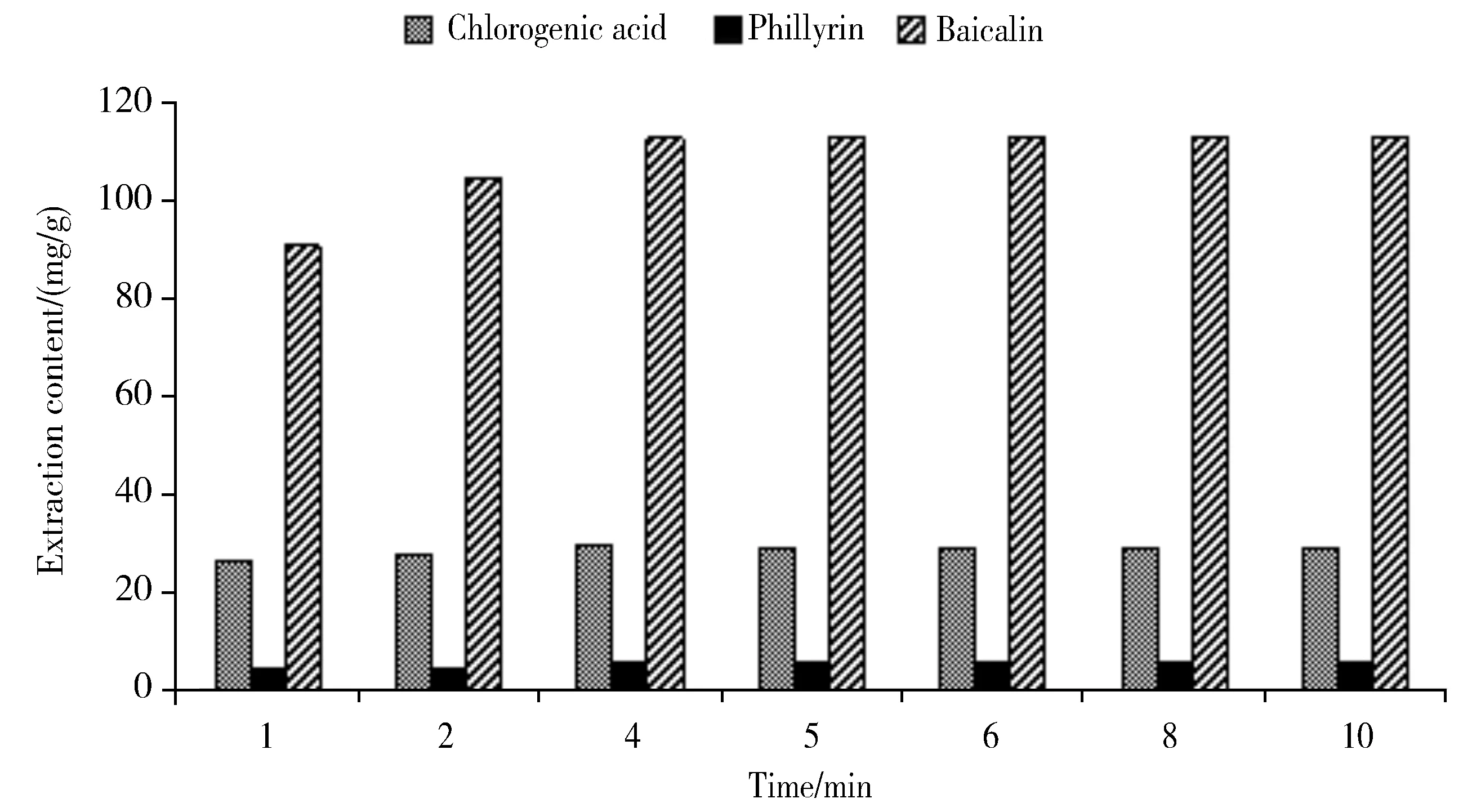
Fig.2 Effect of retention time of UPE on the extraction content图2 不同保压时间对提取含量的影响
2.3.3 提取压力对提取液中黄芩苷、绿原酸、连翘苷含量的影响
超高压提取压力对3种活性成分提取含量的影响如图3所示,在压力为100~400 MPa范围内,随着超高压压力的加大,3种活性成分的提取含量一直增加。在400 MPa时,各成分的提取含量达到最大,而在压力超过400 MPa后,有效成分提取含量反而呈现下降的趋势。可见,在一定范围内(100~400 MPa),超高压压力的增加对提取效率起着正向相关的作用。这与樊振江等和王居伟的提取效果相似[14-15],提高压力可以有助于溶剂扩散到物质细胞内部,使物质被溶剂浸润的速度加快,细胞壁和胞内各种膜被破坏,细胞内外平衡被打破,降低了有效成分的传质阻力,加快了有效物质向外扩散的速率[16]。而当压力大于400 MPa后,较大的压力使药材破碎的程度加大,形成过多的小颗粒堵塞了活性成分的溶出通道,同时部分活性成分被破碎的组织细胞所吸附,使得提取效率反而降低,因此,选择400 MPa作为合适的压力进行下一步实验。
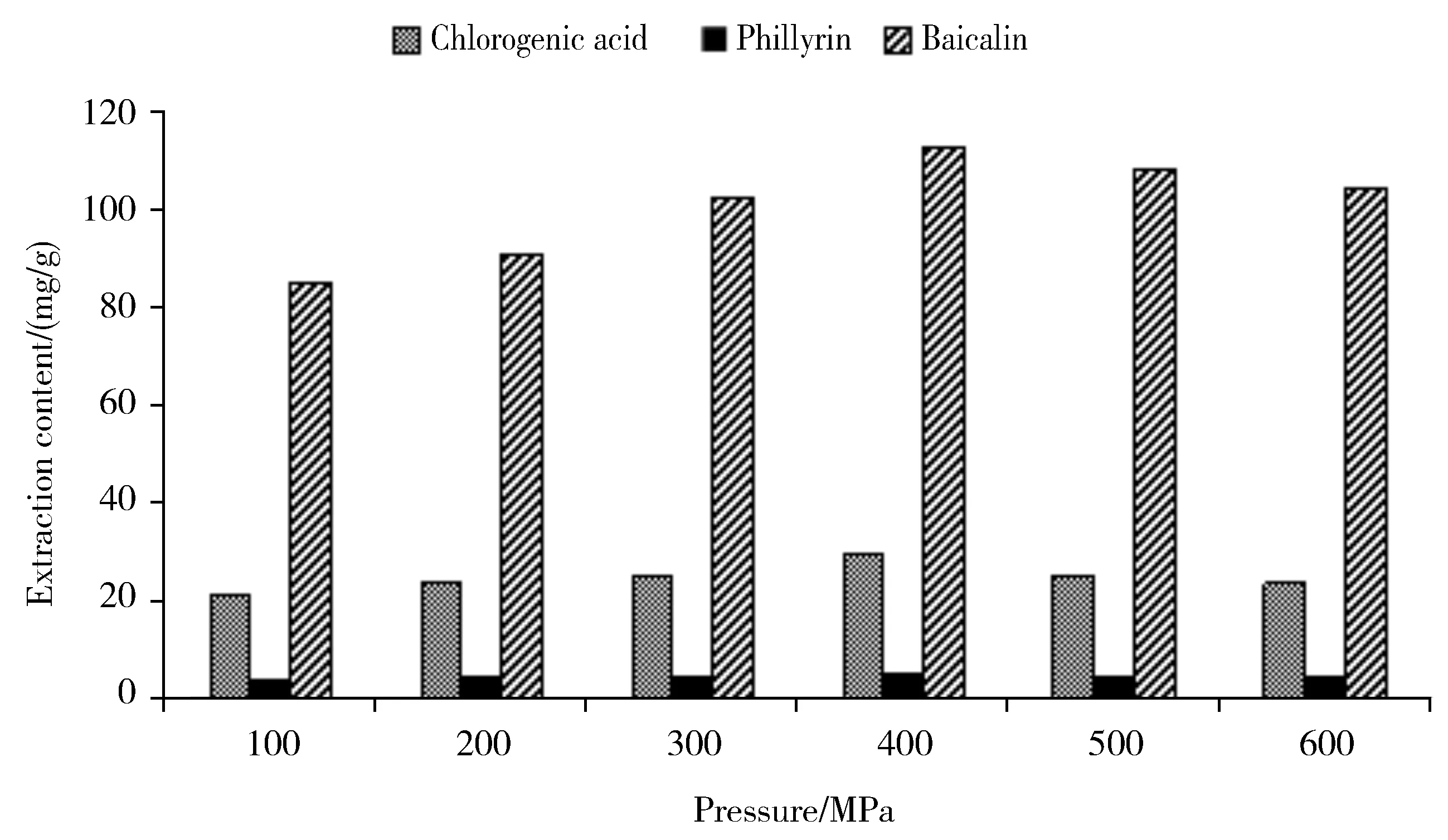
Fig.3 Effect of extracting ultrahigh pressure on the extraction content图3 不同压力对提取含量的影响
2.3.4 固液比对提取液中黄芩苷、绿原酸、连翘苷含量的影响
固液比对3种活性成分提取含量的影响如图4所示,由图4 看出,随着固液比的增大,即加入的溶剂量增加,提取含量增加,当固液比超过1∶8时,提取含量增加缓慢,趋于稳定。固液比对提取含量的影响主要是由于随着固液比的增大,有效成分从组织内向外溶出的过程中,浓度梯度和扩散速率也随之升高,有利于提取效率的提高。当有效成分达到一定溶出极限后,提取含量也不会再随着固液比的增加而升高[17]。所以我们选定1∶8作为最佳固液比进行下一步实验。
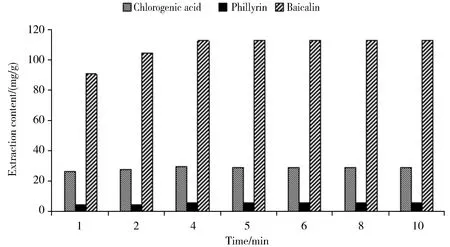
Fig.4 Effect of solid to liquid ratio on the extraction content图4 不同固液比对提取含量的影响
2.3.5 正交试验
在单因素试验的基础上,采用正交试验法对复方双黄连有效成分的提取条件进行优选,因素与水平的设计和试验结果分别见表9和表10,由极差分析结果可知,因素A对应K值为K1>K2>K3,因素B、D对应K值均为K2>K1>K3,因素C对应K值为K2>K3>K1,在极差R的比较中,发现影响3种有效成分提取效果的因素按主要程度排序为D(固液比)>A(含水量)>C(提取时间)>B(提取压力)。综合考虑单因素考察及正交试验结果,将超高压辅助低共熔溶剂提取复方双黄连有效成分的最佳提取条件定为:30%含水量,压力400 MPa,时间4 min,固液比1∶8。综合评分要以各指标的最大值为参照将数据进行归一化处理,再给出不同的权重。在本实验中,绿原酸、连翘苷及黄芩苷3种物质均为复方双黄连的主要成分,因此将其权重系数均设为0.33,进行加权求和,得综合评分(Y)=0.33X1/Xmax1+0.33X2/Xmax2+0.33X3/Xmax3,所得正交试验结果及极差分析如表10所示。
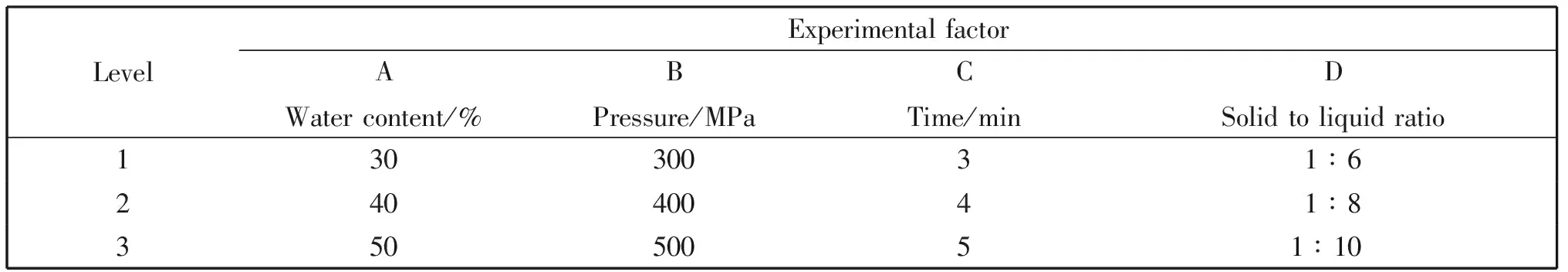
表9 正交试验因素水平表
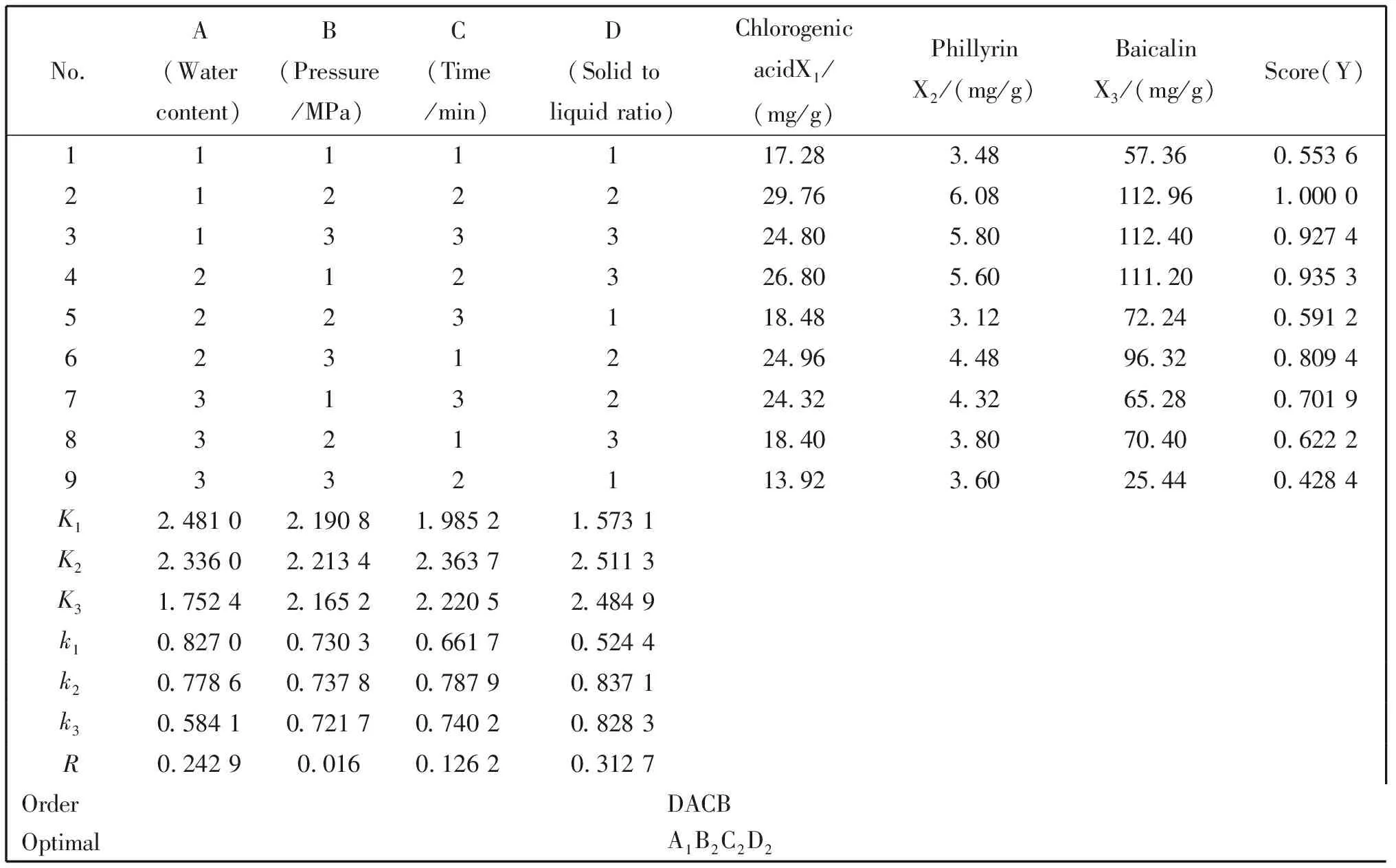
表10 L9(34)正交实验结果及极差分析表
2.3.6 正交试验验证
按正交实验所得的超高压提取的最佳条件A1B2C2D2,即30%含水量,压力400 MPa,时间4 min,固液比1∶8,平行做3组验证试验,结果为绿原酸含量为29.77 mg/g,黄芩苷含量为112.66 mg/g,连翘苷含量为5.99 mg/g。从表11中验证结果显示,绿原酸、连翘苷、黄芩苷各物质含量的RSD均小于3%,表明优化所得超高压辅助低共熔溶剂提取复方双黄连有效成分的条件合理可行。

表11 正交试验验证
2.4 与药典方法作比较
按照药典提取方法和1.2.6.2 超高压辅助低共熔溶剂提取方法,测得绿原酸、黄芩苷、连翘苷含量,结果列于表12。结果显示,超高压辅助低共熔溶剂法可以有效提取3种有效成分,与药典提取方法相比,绿原酸、黄芩苷、连翘苷含量均有所提高。

表12 提取方法比较(n=3)
3 结论
本文采用绿色、环保的低共熔溶剂ChCl-LA(1∶1)超高压辅助提取黄芩中的黄芩苷、连翘中的连翘苷、金银花中的绿原酸3种复方双黄连的有效成分,考察了低共熔溶剂的含水量以及超高压提取压力、固液比、提取时间等对活性成分含量的影响,并同时采用正交试验法对提取条件进行了优化,确定了最佳的提取参数。同时通过方法学考察对其含量测定方法进行了验证。结果表明,选定的低共熔溶剂含水量为30%,提取压力为400 MPa,提取时间为4 min,固液比为1∶8,在上述优化条件下进行了验证试验,绿原酸含量为29.77 mg/g,黄芩苷含量为112.66 mg/g,连翘苷含量为5.99 mg/g,此方法对提取液中有效成分的含量要高于药典提取法,为双黄连制剂的制备提供了新的思路,值得进一步推广。

