成人脊柱结核术后并发急性肾损伤的影响因素分析
李坤 罗太君 王菲 贾红彦 张宗德 刘伟
骨关节结核是比较常见的继发性肺外结核,其50%~60%为脊柱结核,且以椎体结核多见。脊柱结核可选择抗结核药物治疗,但由于病灶血供较差,药物起效时间缓慢,且对病灶破坏造成的脊髓或神经功能障碍、脊柱失稳等症状难以有效,导致临床上单纯抗结核药物治疗效果不佳。手术治疗可快速清除病灶,对解除脊髓、神经压迫,矫正后凸畸形以及重建脊柱稳定性等方面具有重要意义[1],故临床上多采取抗结核药物联合手术治疗。但需注意的是,手术治疗可引起多种术后并发症,明显影响患者的预后及生存质量,急性肾功能损伤(acute kidney injury, AKI)是其较严重的并发症之一,可明显延长住院时间,增加感染风险、术后病死率和医疗费用等[2]。目前,国内外对术后AKI危险因素的研究多集中在心脏手术方面,对脊柱结核的研究较少,且多为探讨脊柱结核手术方式、时机对疗效影响等方面的研究。本研究通过收集术前肾功能正常且行脊柱结核手术治疗的成人脊柱结核患者的临床资料,探讨此类患者术后发生AKI的相关影响因素,为临床诊治提供一定依据。
资料和方法
一、研究对象
1.患者选择:搜集2009—2018年首都医科大学附属北京胸科医院收治的年龄≥18岁、术前肾功能正常,且行脊柱结核手术(后路病灶清除+椎间植骨融合+内固定术)治疗的成人脊柱结核患者2535例,排除术前需要血液替代治疗、有严重感染或败血症、术中出现机械性肾损伤,以及一般临床资料、手术和麻醉记录单、术前和术后血肌酐(serum creatinine,Scr)、血尿素氮(blood urea nitrogen,BUN)、检查项目不全且无法填补者467例,最终纳入2068例患者。所有人口学基线统计数据和患者围手术期临床数据的采集均来自于北京胸科医院的电子病历系统和麻醉科数据库。
2.患者分组:(1)并发AKI组:从纳入的2068例患者中选择出术后发生AKI的31例患者作为并发AKI组,纳入患者AKI的发生率为1.49%。其中男15例(48.39%)、女16例(51.61%);胸椎结核12例(38.71%)、腰椎结核14例(45.16%)、胸腰椎结核3例(9.68%)、腰骶椎结核2例(6.45%);病变累及2个椎体29例(93.55%),累及3个椎体2例(6.45%)。(2)对照组:从剩余的2037例未发生AKI的患者中,参照并发AKI组患者的手术时间,按照1∶2的比例收集与此时间点最为接近的同病变部位、同手术方式的患者,如符合则纳入作为对照组,如不符合则将其排除,重复以上过程,直至为每例患者匹配到同期的2例对照患者;最终纳入62例脊柱结核患者作为对照组,其中男27例(43.55%)、女35例(56.45%)。分析两组患者的临床资料与术后发生AKI的相关性。所有患者均于麻醉前参照美国麻醉医师协会(American Society of Anesthesiologists,ASA) 根据患者体质状况和对手术危险性进行分类的分级标准[3](ASA分级标准)界定为Ⅱ、Ⅲ级患者。
二、临床观察指标
1.术前一般资料:包括年龄、性别、体质量指数(body mass index,BMI)、既往病史[高血压、糖尿病、心脏病、吸烟史、慢性阻塞性肺疾病(chronic obstructive pulmonary diseases, COPD)]、抗结核药物治疗时间等。
2.术前实验室检查:包括Scr、BUN、血红蛋白(Hb)、尿酸、白蛋白、C-反应蛋白(CRP)、术前估计肾小球滤过率(estimated glomerular filtration rate, eGFR)等。
3.术中观察项目:包括术中ASA分级、麻醉方式、有无高血压、有无低血压、手术时间、术中用药、胶体量(羟乙基淀粉130/0.4)、氯化钠注射液补液量、输血量、失血量、尿量等。
4.术后观察项目:包括肺部感染、术后住院时间、院内死亡例数等。
三、诊断标准
1.脊柱结核诊断标准[4]:(1)症状体征与影像学(包括X线、CT、MR检查)发现的局部结核病灶内的脓肿、死骨表现相符;(2)病灶标本的病理学检查提示为干酪样坏死及郎罕细胞肉芽肿;(3)病灶标本的微生物学检查提示为结核分枝杆菌感染;(4)规律抗结核药物治疗6个月以上,结核中毒症状及局部症状消失。符合以上任意2条即诊断为脊柱结核。
2.AKI诊断标准:依据全球改善肾脏病预后组织(kidney disease improving global outcomes, KDIGO)推荐指南[5],以术后48 h或7 d内Scr峰值较术前基线值上升≥26.4 mg/L或较基础值增加≥50%,和(或)尿量<0.5 ml·kg-1·h-1达到6 h为AKI诊断标准。
3.其他标准:(1)肾功能正常[6]:Scr≤97 μmol/L,BUN≤8.2 mmol/L。(2)eGFR:应用慢性肾脏病流行学合作组(chronic kidney disease epidemiology, CKD-EPI)提出的CKD-EPI公式[7]评估eGFR,当eGFR≥90 ml·min-1·(1.73 m2)-1时提示肾功能正常;当60 ml·min-1·(1.73 m2)-1≤eGFR<90 ml·min-1·(1.73 m2)-1时提示肾功能轻度损伤;当eGFR<60 ml·min-1·(1.73 m2)-1提示肾功能中重度损伤。(3)高尿酸血症:男性和绝经后女性>420 μmol/L,非绝经女性>360 μmol/L[8]。(4)贫血:血红蛋白(Hb)正常数值成年男性<130 g/L,成年女性<120 g/L[9]。(5)白蛋白参考值:35~51 g/L。
四、两组患者治疗情况
所有纳入患者均在术前以H-R-Z-E(H:异烟肼;R:利福平;Z:吡嗪酰胺;E:乙胺丁醇)方案进行3~12周规范抗结核药物治疗。待常规胸部X线摄影检查排除活动性肺结核,生命体征平稳,高血压、糖尿病等基础疾病得到控制,达到术前要求后择期行手术治疗。由于脊柱手术创伤较大、手术体位对呼吸有影响,为保证患者的安全,首选全身麻醉,麻醉方式采用静脉滴注麻醉和静脉滴注+吸入复合麻醉。手术方式均为后路病灶清除+椎间植骨融合+内固定手术。经麻醉前充分准备,积极预防并发症,所有患者手术、麻醉均顺利完成,术后无相关并发症发生。术后继续按照术前抗结核药物治疗方案给予化疗,待X线摄影检查显示植骨和内固定位置的螺钉固定良好、切口愈合良好、生命体征平稳后拆线出院。
五、统计学处理
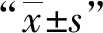
结 果
一、两组患者临床观察指标(变量)的检测水平及单因素分析
并发AKI组与对照组术前、术中、术后临床资料(因素)在两组患者中的统计及分布情况见表1~3。表1数据检测水平显示,两组患者在Scr和eGFR检测数值、失血量和输血量数量等方面的差异均有统计学意义(P值均<0.05)。表2、3单因素分析显示,在年龄、BMI,术前并发高血压、eGFR水平、高尿酸血症、贫血,术中使用右美托咪定、失血量等方面的分布差异均有统计学意义(P值均<0.05)。
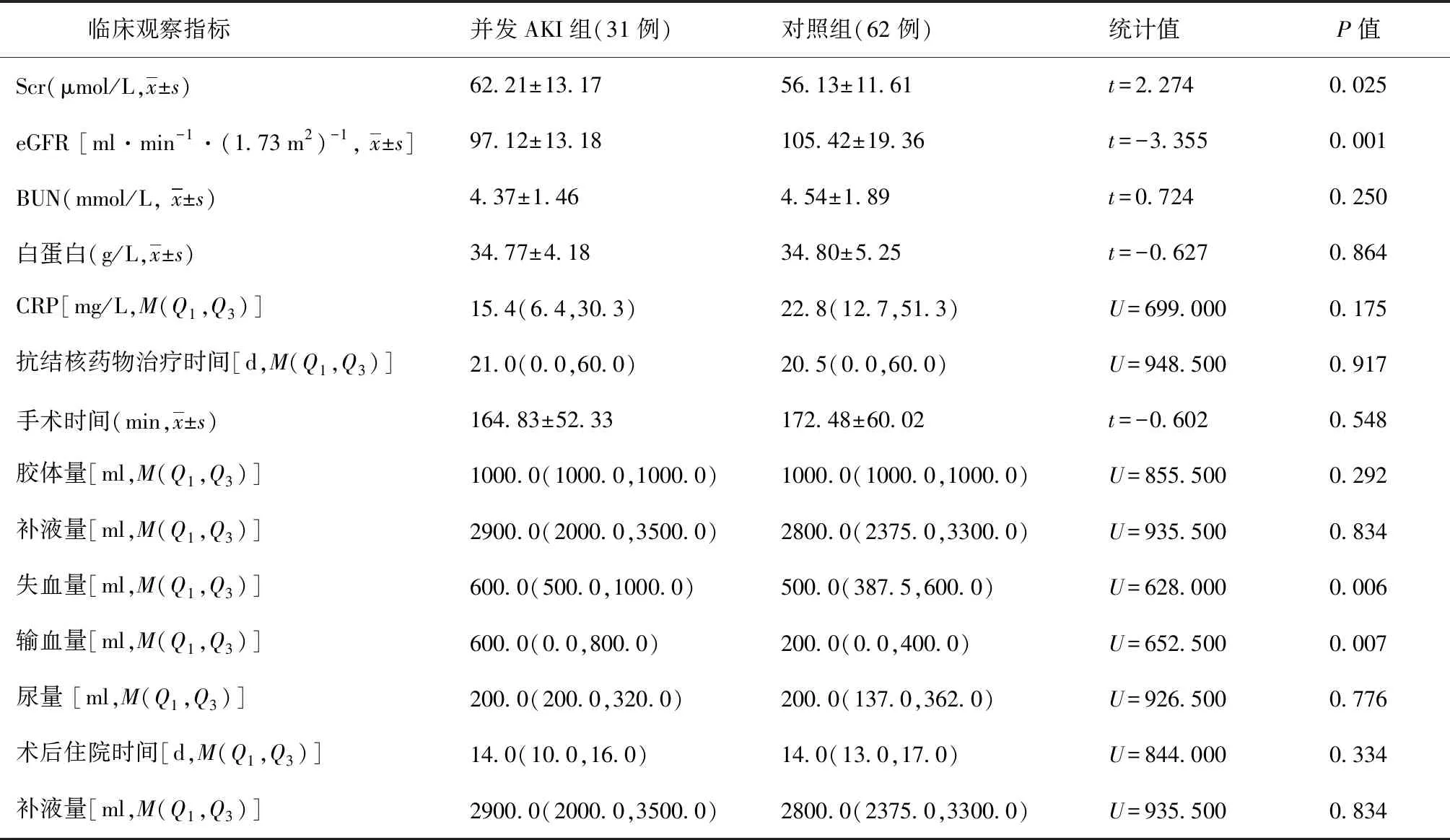
表1 术前部分临床观察指标在两组患者中的统计情况
注Scr:血肌酐;BUN:血尿素氮;eGFR:估计肾小球滤过率
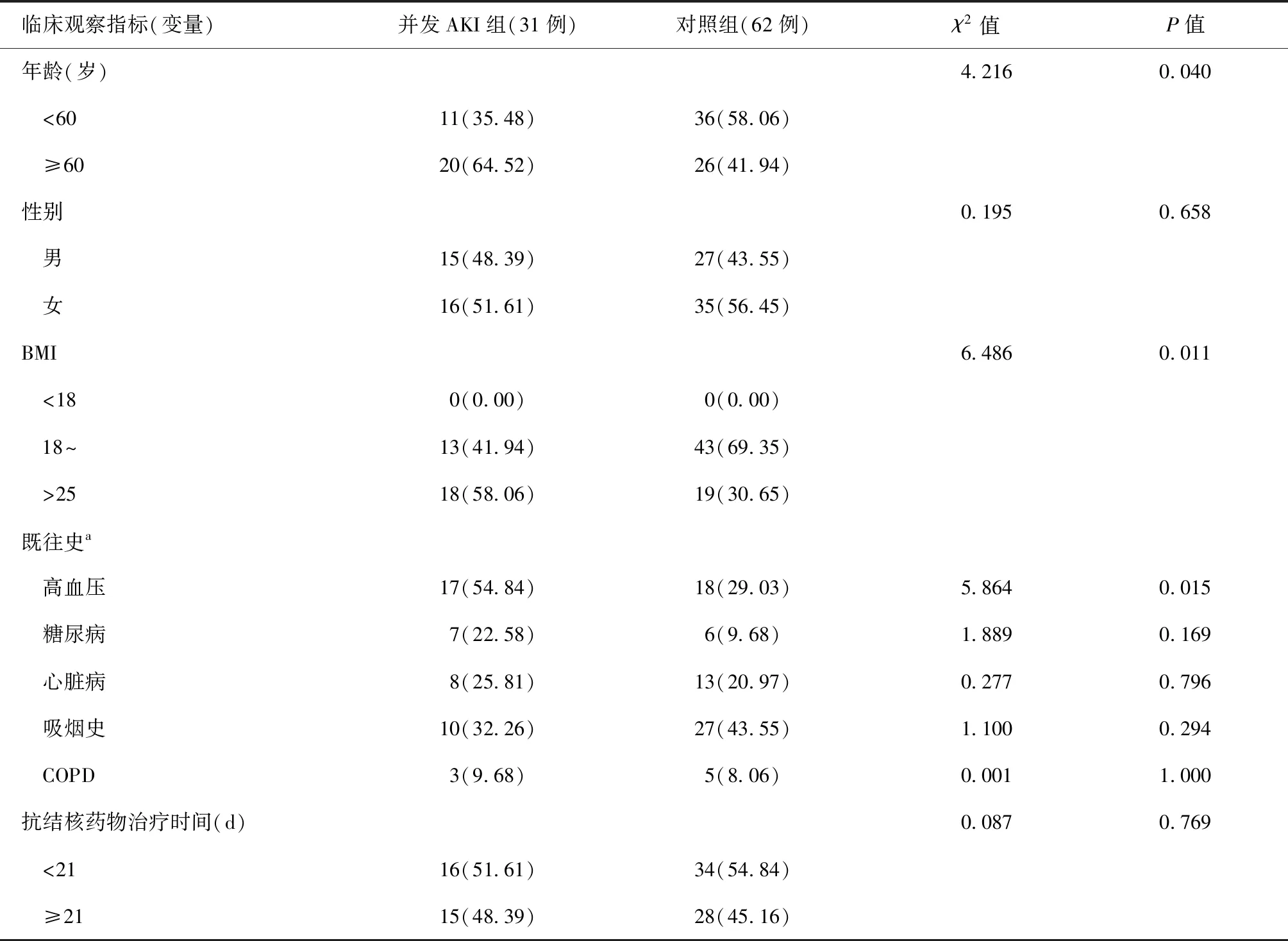
表2 术前不同临床观察指标(变量)在两组患者中的单因素分析
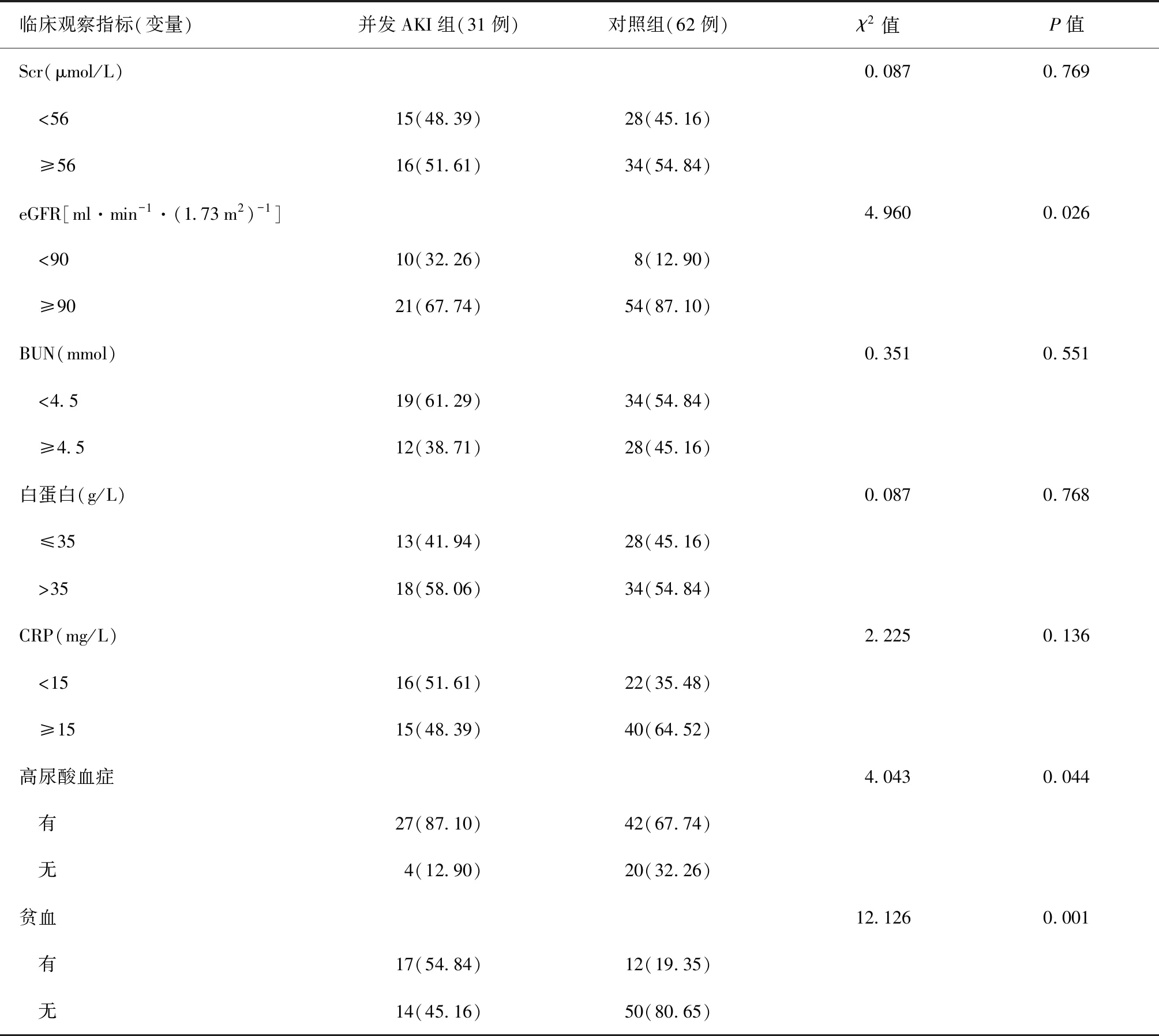
续表2
注括号外数值为“患者例数”,括号内数值为“构成比(%)”;a:既往病史发生率[例(发生率,%)];BMI:体质量指数;COPD:慢性阻塞性肺疾病;Scr:血肌酐;BUN:血尿素氮;eGFR:估计肾小球滤过率;CRP:C反应蛋白

表3 术中及术后不同临床观察指标(变量)在两组患者中的单因素分析
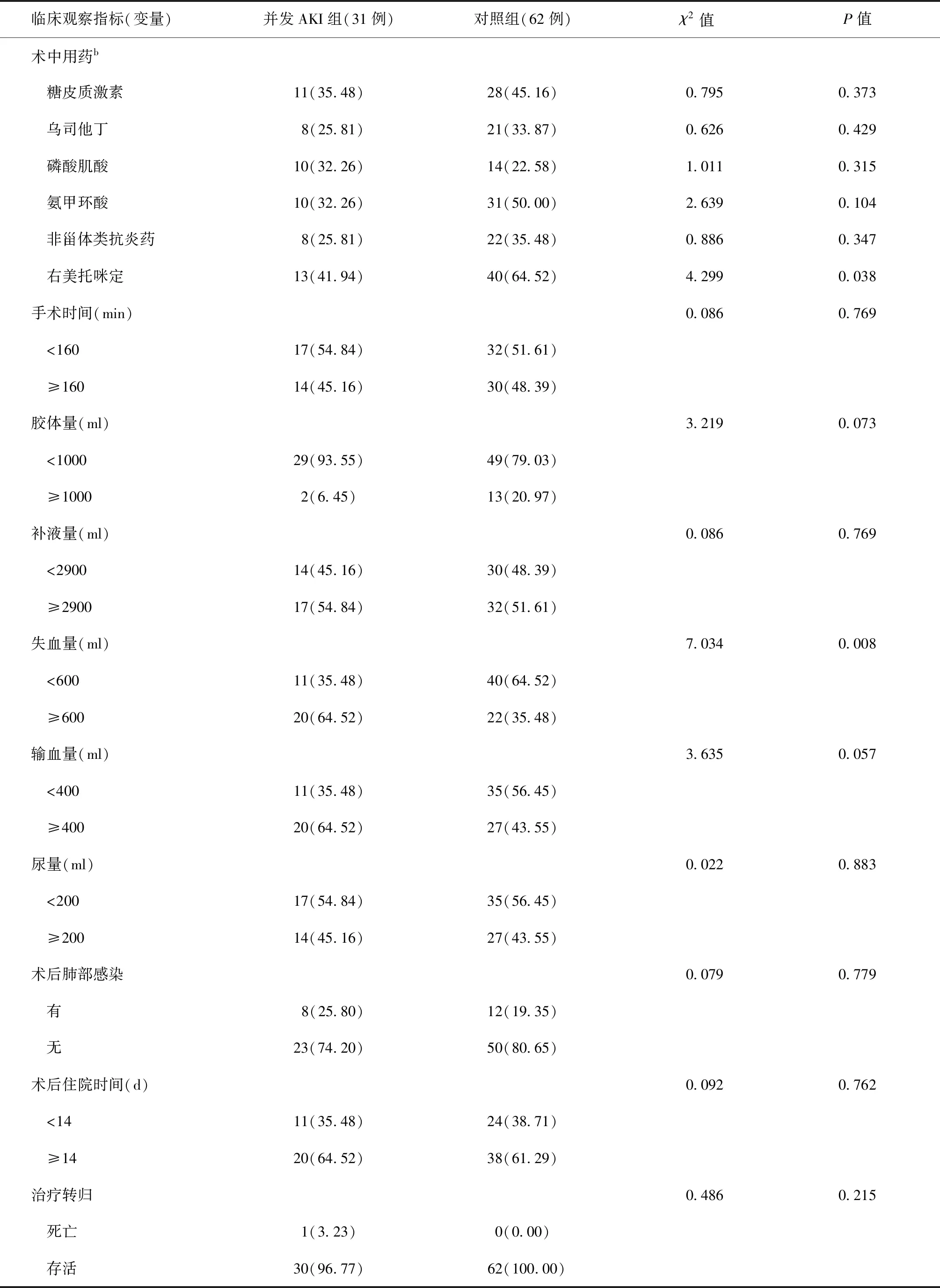
续表3
注括号外数值为“患者例数”,括号内数值为“构成比(%)”;a:单位为“例(发生率,%)”;b:单位为“例(使用率,%)”
二、术后发生AKI的多因素logistic分析
对单因素分析中的各项因素进一步行多因素logistic回归分析,结果显示术前BMI>25、并发高尿酸血症、贫血为术后发生AKI的独立危险因素[OR(95%CI)值分别为4.391 (1.187~16.238)、5.896 (1.126~30.874)、8.173(2.133~31.314)];术前较高的eGFR水平为术后发生AKI的保护性因素[OR(95%CI):0.213(0.049~0.921)],见表4、5。
讨 论
术后发生AKI是多种因素引起的以肾功能快速下降为主要表现的危急临床症状,是外科手术后严重并发症之一。有研究表明,心脏手术后出现AKI的发病率为18.7%,而骨科手术后为10.2%[10]。既往的研究多认为术后短暂、可逆的AKI患者预后良好[11],但最新的研究发现术后短暂、可逆的AKI同样会增加患者远期发生慢性肾脏病(chronic kidney disease, CKD)和终末期肾病(end-stage renal disease, ESRD)的风险[12-13],此类患者10年后肾功能进一步损伤的发生率仍可达61.1%[14]。故认为术后发生AKI可增加患者并发感染、肾功能预后不良、进展为慢性肾脏病的风险,早期发现、早期干预可有效避免AKI的发生、改善患者的预后、明显减少住院时间[15]。
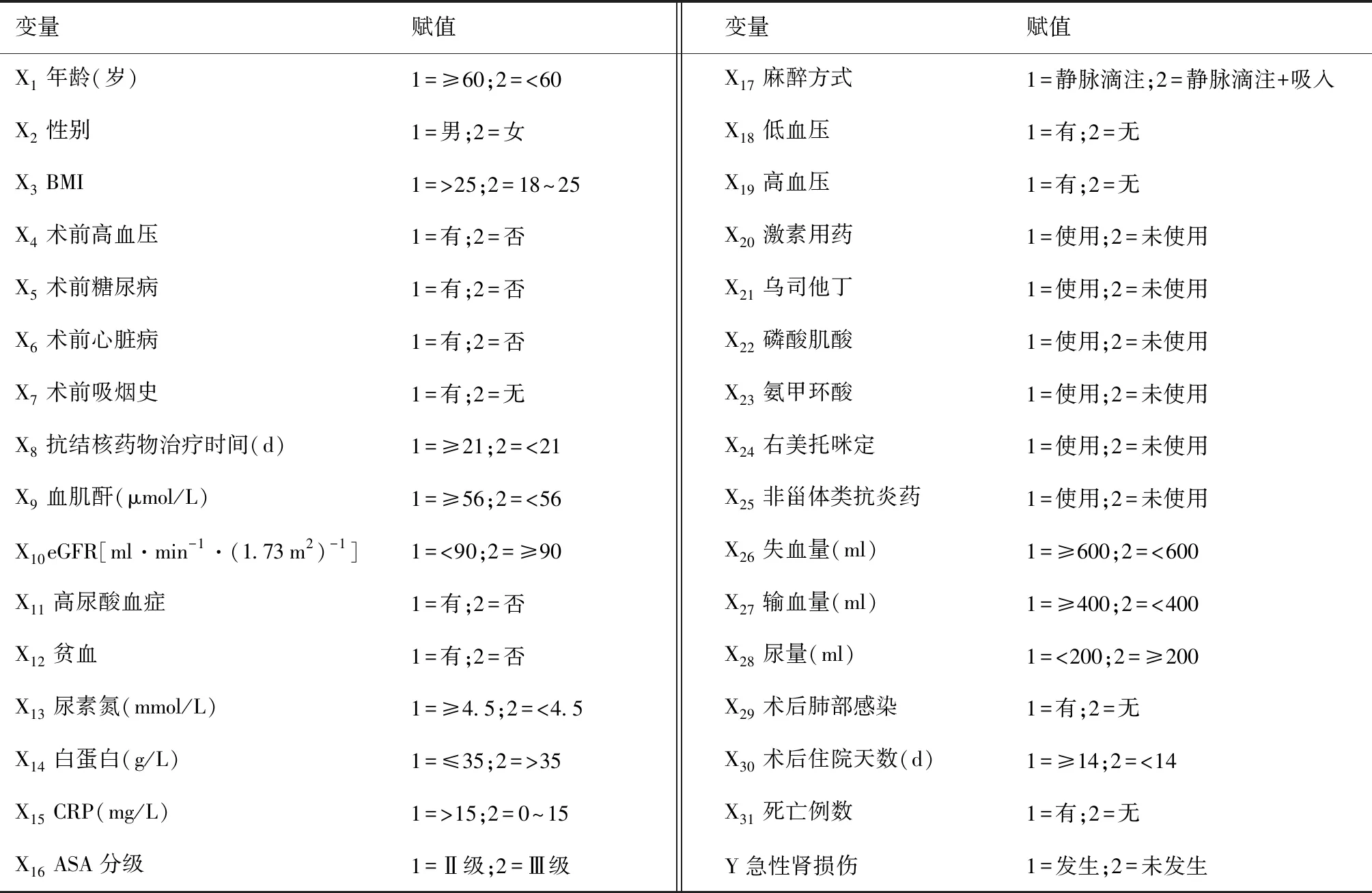
表4 术后发生AKI的多因素logistic回归分析赋值表
注赋值主要根据临床意义及中位数进行赋值
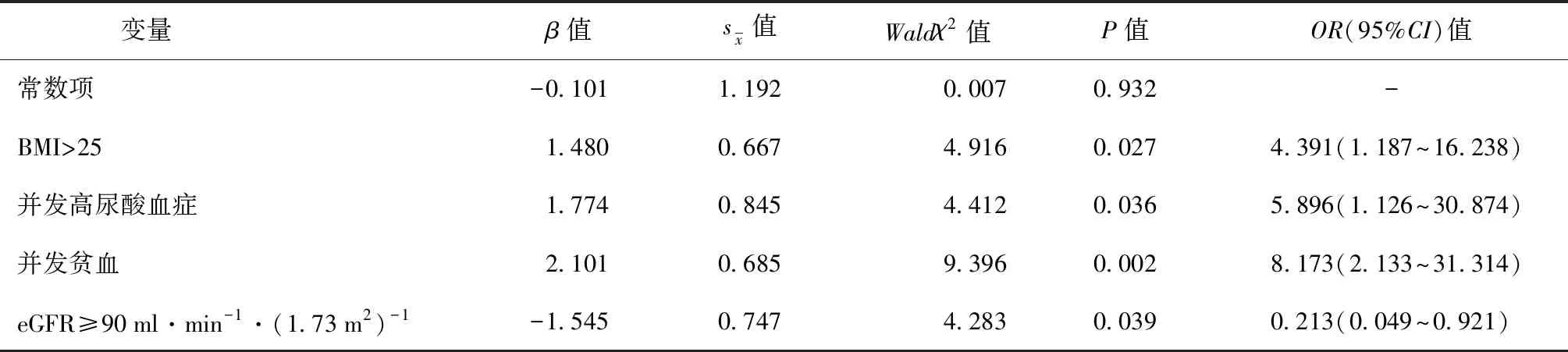
表5 影响术后发生AKI的多因素logistic回归分析
有研究表明,术前肾功能不全可能是术后发生AKI的危险因素[10],但缺少对脊柱结核患者术前肾功能正常而于术后发生AKI的危险因素的探讨。本研究采用2012年KDIGO相关指南,首次探讨术前肾功能正常脊柱结核患者在行椎体病灶清除+椎体间植骨融合+内固定术术后AKI的发生情况及危险因素,发现纳入患者术后AKI的发病率为1.49%(31/2068),低于Naik等[16][采用急性肾功能严重程度和转归分级标准(RIFLE标准,R:危险;I:损伤;F:衰竭;L:肾功能丧失;E:终末期肾病)]研究的AKI发生率(3.9%),可能与术前纳入患者类型、手术类型、术后AKI诊断标准不同有关。
术前高龄是患者术后发生AKI的危险因素已被许多研究证明[10, 13, 17],认为随着患者年龄的增加,其肾脏结构和功能可能发生进行性衰退,从而导致患者更易出现术后AKI。本研究显示并发AKI组患者的年龄明显高于对照组,与上述及Haanschoten等[18]的研究结果一致。另外,在其他研究中发现术前较高的BMI、高血压及糖尿病病史都可能与术后发生AKI相关[10, 13, 19-20],认为较高的BMI可能会导致患者肾脏结构隐匿性改变,如系膜细胞过多,足细胞肥大以及局灶性节段性肾小球硬化增加,从而增加患者术后发生AKI的风险;而术前并发高血压、糖尿病可能会影响肾脏血流自动调节功能,对术中缺血状态耐受性较差[10]。本研究单因素分析结果显示,术前BMI较高、并发高血压病史结果与上述研究一致,但由于本研究中所有患者术前的血糖水平均控制在正常范围,故结果中未体现出两组患者糖尿病方面的差异性。
对肾功能相关指标的研究表明,尿酸升高也是导致急性肾损伤的因素之一。尿酸在术后发生AKI中的发病机制可能为尿酸通过激活肾素-血管紧张素系统,刺激促炎症反应分子单核细胞趋化蛋白-1(MCP-1)、CRP及氧化剂的生成,最终引起肾血管内皮细胞损伤,破坏肾血管的自动调节机制[21]。在临床中对术前肾功能评估多采用Scr、BUN和eGFR指标,而尿酸增加对肾脏的损伤并未引起临床医生的足够重视[22]。本研究发现并发AKI组术前高尿酸血症患者明显高于对照组,与Kaufeld等[23]的研究结果相似,进一步提示术前高尿酸血症是术后发生AKI的独立危险因素。且Ejaz等[19]的研究认为,术前降低血清尿酸水平可能有利于预防术后AKI的发生,有助于患者术后肾功能的改善。另外,还有研究表明,肾功能损伤时Scr水平的升高往往滞后,在早期发现肾功能损伤方面检测eGFR较Scr更加敏感[24],能够较检测Scr更早期发现术后AKI的发生,可将eGFR水平作为评估肾功能的敏感指标。本研究结果显示,并发AKI组术前eGFR明显低于对照组,提示术前较高的eGFR水平是术后发生AKI的保护性因素,与Grams等[10]研究结果一致,这可能是由于较低的eGFR患者生理适应性较低,肾脏自动调节功能受损,不易耐受术中肾血流减少和其他肾毒性损伤,从而导致术后易发生AKI[25]。
本研究结果显示,并发AKI组术前贫血患者明显多于对照组,提示术前贫血是术后发生AKI的危险因素。有研究表明,86%的结核病患者并发贫血[26],且术前贫血不仅可加重结核病病情,还可增加结核病手术患者术后并发症的发生率[27]。Cho等[20]在股骨颈骨折患者术后发生AKI的危险因素分析中发现,术前较低的Hb是术后发生AKI的独立危险因素。认为其可能机制是术前贫血可引起术中氧气输送减少,造成机体缺氧状态,导致肾脏损伤;另外在贫血状态下,即使Scr正常,患者也可能存在亚临床肾脏疾病,肾小管耗氧量和氧化应激水平均增加,极易导致术后AKI的发生[28]。故认为对于术前贫血患者,仅在围手术期间输注红细胞并不会改善患者肾脏功能的预后,甚至会增加AKI、急性肾衰竭和术后死亡等并发症的风险[28],认为术中输血可能会导致血细胞比容增高,使局部血流流率及氧输送能力降低,造成游离铁大量聚集有关。故对于此类患者,可通过术前输血、服用药物,尽早纠正贫血状态,以预防术后发生AKI[29]。
本研究也存在一些局限性。一者,本研究为单中心回顾性病例对照研究,属于回顾性观察试验,结果数据代表性、科学性不足,需要进一步开展多中心大样本的前瞻性研究证实;二者,由于患者复诊率、依从性较差,大部分患者无法采集到随访资料,导致研究缺乏长期肾功能随访资料;三者,由于缺乏术前进行多次Scr检测的数据,仅选择距离手术时间最近的Scr值作为基线Scr值,可能会高估术后AKI的发生率。
综上所述,术前肾功能正常脊柱结核患者行结核病灶清除+椎体间植骨融合+内固定手术后,术前BMI>25、高尿酸血症和贫血是术后发生AKI的独立危险因素,而术前高eGFR水平可以减少患者术后AKI的发生。因此,针对术前肾功能正常的脊柱结核患者,术前应积极纠正患者贫血状态,降低术前尿酸水平,有助于降低患者围手术期AKI的发生,改善患者术后肾功能及预后。

