纤维素-碱木质素水凝胶的制备及其性能表征
赵 鑫,曹光辉,刘肖月,李琪微,于露露,孙 晨,胡英成
东北林业大学生物质材料科学与技术教育部重点实验室,黑龙江 哈尔滨 150040
水凝胶是一种在空间结构上三维网状结构的高分子材料,其具有亲水性而又不溶于水的特点,能够保持大量的水分,同时其生物学性质也表现出极好的效果,可用于药物释放的可控性操作[1]。天然高分子组成的水凝胶因其独特的吸水性和良好的生物相容性等优点而受到材料科学和生物医学领域的广泛应用和研
究。水凝胶在一些新型药物中的应用,能够有效提高药效,因此水凝胶在人体内控释、脉冲释放、触发式释放的领域具有广泛的应用前景[2]。
纤维素是由D-葡萄糖基构成的直链状高分子化合物,其分子链上具有多个可反应的羟基,制备得到纤维素水凝胶可以提高水凝胶的保水性能和生物相容性,改善生物降解性能[3]。木质素基水凝胶能在碱和乙醇溶液中溶胀的特性对于木质素基水凝胶在碱溶和醇溶性药物的载入方面具有较大优势,近年来含木质素水凝胶开始应用于药物的缓释。Nishida 等[4]将乙酸木质素溶解于NaOH 溶液中,用具有不同聚合度的聚乙二醇缩水甘油醚交联制备水凝胶,并对水凝胶的溶胀性能进行评价,结果表明当乙醇与水的体积分数为50%时,水凝胶在乙醇的水溶液中溶胀度最大。Raschip 等[5]以一年生纤维作物木质素与黄原胶混合,在NaOH溶液中用环氧氯丙烷直接交联制备了一种半互穿网络水凝胶,并研究了其对香草醛的控制释放。Ciolacu 等[6]将微晶纤维素和山杨木质素溶解于NaOH 溶液中,并在交联剂环氧氯丙烷的作用下制备含木质素-纤维素水凝胶,研究结果表明水凝胶在乙醇水(体积比1∶19)中的溶胀率随木质素含量的增加而增加。基于以上所述内容,本文以微晶纤维素、碱木质素为原料,制备出纤维素(cellulose,CL)水凝胶和纤维素-碱木质素(cellulose-alkali lignin,CAL)水凝胶,并且以杨木木粉为原料,基于离子液体体系反应得到离子液体木质素,进而制备出纤维素-离子液体木质素(cellulose-ionie liquid lignin,CIL)水凝胶。通过溶胀度测试、热重分析等表征方法,评价添加碱木质素以及离子液体木质素对水凝胶溶胀性能及热性能的影响。
1 实验部分
1.1 原料及设备
杨木木粉、1-丁基-3-甲基-咪唑硫酸氢盐([Bmim]HSO4)、1,4-丁二醇、微晶纤维素、碱木质素、环氧氯丙烷、氢氧化钠、无水乙醇、氯化钠;集热式恒温加热磁力搅拌器、恒温磁力搅拌器、电热鼓风干燥箱、冷冻干燥机、水热反应釜、循环水式多用真空泵。
1.2 实验步骤
1.2.1 CL 水凝胶的制备 配制质量分数6%NaOH和质量分数为4%尿素水溶液,然后用砂芯漏斗过滤后做为纤维素的溶剂[7]。将2 g 微晶纤维素分散在上述98 g 纤维素溶剂中,然后在室温下磁力搅拌10 min,混合均匀后将上述混合溶液放入冰箱中,在-7 ℃条件下冷冻12 h。样品在室温下解冻,磁力搅拌得到无色透明的纤维素溶液。将9 mL 环氧氯丙烷滴加到上述纤维素溶液中,在室温条件下磁力搅拌30 min,然后在80 ℃加热该混合物8 h,得到CL 水凝胶样品。
1.2.2 CAL 水凝胶的制备 将0.2 g 碱木质素和1.8 g 微晶纤维素分散在上述纤维素溶剂(98 g)中,并采用1.2.1 节中CL 水凝胶的制备方法制备CAL水凝胶样品。
1.2.3 CIL 水凝胶的制备 将杨木木粉利用实验室小型粉碎机进行粉碎处理,然后使用筛孔尺寸为0.15 mm 的筛网进行筛选,得到杨木木粉粉末。将筛选得到的杨木木粉粉末水洗60 min 后干燥,然后使用丙酮在90 ℃下进行索氏抽提4 h,抽提结束之后干燥备用,即得预处理后杨木木粉粉末样品。
量取24 mL 1,4-丁二醇和6 mL 蒸馏水,然后向其中加入1 g 1-丁基-3-甲基咪唑硫酸氢盐,搅拌使其混合均匀。称取1 g 预处理后杨木木粉样品,倒入水热反应釜中,同时加入上述混合均匀的溶液,不断搅拌以便除去反应体系中可能存在的气泡,随后拧紧反应釜将其密封,放入200 ℃恒温油浴锅中反应30 min[8]。反应结束后,待反应釜冷却至室温,打开反应釜,对反应物进行真空抽滤,实现固液分离,得到溶有木质素的滤液及不溶的综纤维素滤渣。向滤液中加入适量反向溶剂蒸馏水,木质素再生并析出,再次进行真空抽滤,抽滤所得到的滤渣放入烘箱中干燥,即得到离子液体木质素样品[9]。
取0.2 g 上一步制备得到的离子液体木质素,与1.8 g 微晶纤维素分散在1.2.1 中所述的纤维素溶剂(98 g)中,并采用1.2.1 节中CL 水凝胶的制备方法制备CIL 水凝胶样品。
1.3 表征方法
1.3.1 水凝胶溶胀率和再溶胀度的测定方法 水凝胶的溶胀率测定:将水凝胶分别浸泡在蒸馏水、乙醇水溶液(体积比1∶19)、生理盐水溶液中,浸泡24 h,以便水凝胶达到溶胀平衡。浸泡结束后,将水凝胶取出,用滤纸除去水凝胶表面残留的水分,称重得到水凝胶的湿重。水凝胶在60 ℃下干燥,待水凝胶质量恒定后称重,得到水凝胶的干重[10]。水凝胶的溶胀率(SR)通过以下公式计算得出:
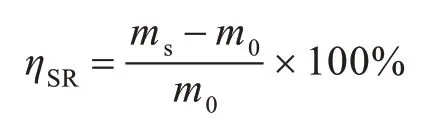
其中,ms代表水凝胶的湿重,m0代表水凝胶的干重。
水凝胶再溶胀度的测试:将干凝胶浸泡在蒸馏水、乙醇水溶液、生理盐水溶液中,经过一定时间间隔(t)后取出水凝胶,用滤纸吸去表面残留的水后称重,得到该时间下水凝胶的质量mt。水凝胶再溶胀度定义为:
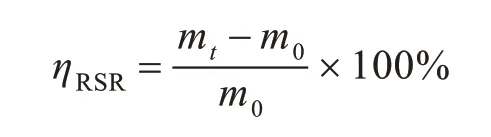
其中,mt代表一定时间间隔下水凝胶的湿重,m0代表水凝胶的干重。
1.3.2 扫描电子显微镜分析 样品的微观形貌通过美国FEI 公司的Quanta200 型扫描电子显微镜(scanning electron microscope,SEM)测定,加速电压为15 kV。
1.3.3 热重分析 为了评价样品的热稳定性,利用热重分析仪(PerkinElmer,STA 6000)对样品进行测定,测试过程中采取氮气保护,气体流速为20 mL/min,升温速率为10 ℃/min,测试温度范围为40~800 ℃。
2 结果与讨论
2.1 水凝胶在不同溶液中溶胀率及再溶胀度
图1 为CL、CAL 及CIL 在不同溶液中的溶胀性能测试结果。结果表明碱木质素以及离子液体木质素的添加均对纤维素水凝胶的溶胀性能有一定的影响。CL 水凝胶在乙醇水溶液中的溶胀率最高(6 813.9%),在蒸馏水中的溶胀率最低(1 457.4%),在生理盐水溶液中也具有较高的溶胀度(4 375.5%)。随着碱木质素或离子液体木质素的添加,CAL 和CIL 在乙醇水溶液和生理盐水溶液中的溶胀率均有一定程度的下降,并且CIL 下降的幅度更大。CAL 在这乙醇水溶液和生理盐水中的溶胀率分别为5 181.3%、3 868.6%,而CIL 的溶胀率则分别为4 643.3%和3 320.8%。在蒸馏水溶液中,CAL和CIL的溶胀率相比于CL有明显的提高,二者的溶胀率分别为6 134.8%和6 374.8%。可能原因是木质素中的羟基与环氧氯丙烷的环氧基团反应生成单醚,环氧氯丙烷中新生成的羟基和氯原子重排生成新的环氧基团,新形成的环氧基团和另一个木质素分子中的羟基反应形成凝胶,这种水凝胶的溶胀率会受羧基离子化程度的影响,也会受到水溶液中盐浓度或pH值的影响[11]。
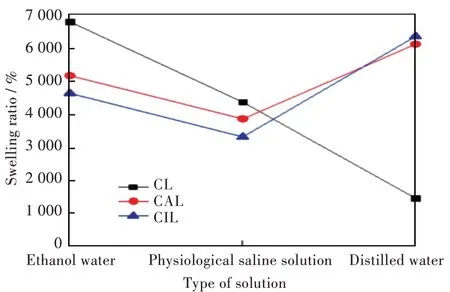
图1 三种水凝胶在不同溶液中的溶胀率Fig.1 Swelling ratios of three hydrogels in different solutions
水凝胶在不同溶液中的再溶胀能力直接影响水凝胶材料的循环使用和潜在应用。为了评价2 种水凝胶的再溶胀能力,分别在2、4、6、8、24 h对2 种干凝胶的吸能能力进行测试。图2 为25 ℃下CL、CAL 和CIL 在不同溶液中的再溶胀度。实验结果表明,CL 在乙醇水溶液中的再溶胀度最高,24 h 再溶胀度为2 233.3%。在蒸馏水中的再溶胀度最低,24 h 再溶胀度为809.3%,在生理盐水溶液中24 h 的再溶胀度为1 788.8%,这与CL 在3 种不同溶液中溶胀度测试结果相吻合。CAL 及CIL 在蒸馏水中的再溶胀性能最好,24 h 再溶胀度分别为1 459.1%和2 337.6%;在生理盐水溶液中的再溶胀性能最差,24 h 再溶胀度分别为847.9%和1 097.7%,在乙醇水溶液中24 h 的再溶胀度分别为1 305.6%和1 681.8%。再溶胀度测试结果也与CAL 和CIL 在3 种不同溶液中的溶胀度测试结果相吻合。水凝胶的溶胀可分为两个阶段:第一阶段是溶剂分子钻入凝胶中与大分子相互作用形成溶剂化层,第二个阶段是液体分子的继续渗透[12]。需要注意的是,图2(a)中显示CL 在生理盐水中的再溶胀度前期会出现先下降后上升的现象,这主要是因为生理盐水在CL 中溶胀的第二阶段进行较缓慢,而第一阶段溶剂分子所形成的溶剂化层在较短时间内达到饱和,从而抑制了水凝胶的继续溶胀,所以会出现再溶胀度先下降后上升的趋势。CAL 在乙醇水溶液表现出类似的现象也是由于该原因[13]。总体而言,碱木质素或离子液体木质素的添加使纤维素水凝胶的再溶胀能力有一定程度的下降。
2.2 水凝胶的形貌分析
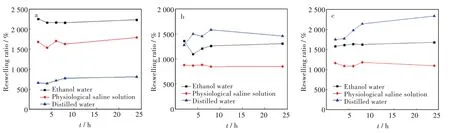
图2 三种水凝胶在不同溶液中的再溶胀度:(a)CL,(b)CAL,(c)CILFig.2 Reswelling ratios of three hydrogels in different solutions:(a)CL,(b)CAL,(c)CIL
加热法得到水凝胶的网络结构中既包括化学交联又包括物理交联,其中物理交联主要是由于纤维素分子去溶剂化引起的分子链缠结形成的聚集结构。基于威廉森醚化反应和烷氧基化作用,纤维素在NaOH/尿素水溶液中通过环氧氯丙烷交联形成水凝胶[14]。图3 为水凝胶的宏观照片及SEM 图,GEL-CL 呈无色透明状,随着木质素的添加,木质素-纤维素水凝胶呈棕色,CIL 水凝胶的颜色比CAL 水凝胶的颜色深,因为经过离子液体醇体系分离得到的木质素颜色比碱木质素颜色更深,同时可以看出CL 的透光率明显好于含有碱木质素的CAL 水凝胶。经过离子液体醇体系处理椰壳纤维得到的木质素与碱木质素添加对纤维素水凝胶的表面形貌无明显影响,3 种水凝胶的表面均呈现凹凸不平的褶皱,加大了水凝胶单位体积的表面积,有助于水分子扩散至其内部,使水凝胶具有较强的吸水和保水能力[15]。
2.3 热重分析

图 水凝胶宏观照片及 图:()() ,()() ,()()Fig.3 Photographs and SEM images of hydrogels adCLbeCALcfCIL

图 三种水凝胶:() 图,() 图Fig.4 Three hydrogels:(a)TG curves,(b)DTG curves
CL、CAL 和CIL 的热稳定性通过热重(thermogravimetric,TG)分析和微商热重(derivative thermogravimetry,DTG)分析进行评价,3 种水凝胶的TG 和DTG 曲线如图4 所示。3 种水凝胶均在100 ℃左右开始分解,主要是因为样品中结合水的蒸发带来的质量下降[16]。3 种水凝胶的热分解范围基本相同,在200 ℃左右开始分解,在220~280 ℃左右分解速度最快。与CL 相比,CAL 和CIL拥有较窄的热分解范围,而且其热分解速度减缓,CAL 在600 ℃高温炭化后固体残留量由32.6%提高到38.8%,CIL 在600 ℃高温炭化后固体残留量由32.6%提高到35.7%,木质素的加入对纤维素水凝胶的热稳定性有一定的提高,且三者中CAL的热稳定性最好。
3 结 语
在氢氧化钠/尿素水溶液体系下,以环氧氯丙烷做为交联剂,采用加热法分别制备出CL、CAL 水凝胶和CIL 水凝胶。CL 水凝胶在3 种溶液中溶胀度由大到小的顺序为乙醇水溶液>生理盐水溶液>蒸馏水,CAL 水凝胶在3 种溶液中溶胀度由大到小的顺序为蒸馏水>乙醇水溶液>生理盐水溶液,CIL水凝胶在3 种溶液中溶胀度由大到小的顺序为蒸馏水>乙醇水溶液>生理盐水溶液。木质素的添加有利于CL 水凝胶在蒸馏水溶液中的溶胀度,CIL水凝胶在3 种水凝胶中的再溶胀能力最高。
与CL 水凝胶相比,纤维素-木质素水凝胶热分解范围较窄且分解速度缓慢,木质素的加入对纤维素水凝胶的热稳定性有一定的提高,纤维素-木质素水凝胶具有良好的热力学稳定性。基于氢氧化钠/尿素水溶液体系在纤维素溶液的基础上掺杂木质素制备纤维素-木质素水凝胶,对于提高纤维素水凝胶热稳定性,实现生物质多组分高值化利用具有重要意义。

