葫芦巴碱对热应激致小鼠睾丸损伤的保护作用
吴 璟,郑 婕,金学琴,黎伟华*
(1.宁夏医科大学实验动物中心,银川 750004; 2.宁夏医科大学药学院,银川 750004)
葫芦巴碱(trigonelline)是从豆科蝶形花亚科葫芦巴中分离纯化的一种生物碱,主治温肾,祛寒,止痛[1]。现代医学研究表明其具有提高男性生育能力、抗氧化、保护心肾等作用[2-4]。本研究拟以单次热应激构建小鼠生殖损伤模型,给予不同剂量的葫芦巴碱进行干预,观察葫芦巴碱对热应激致小鼠睾丸损伤的保护作用。
1 材料和方法
1.1 实验动物
SPF级雄性ICR小鼠120只,8~10周龄,体重25~30 g,由宁夏医科大学实验动物中心提供[SCXK(宁)2015-0001]。饲养于宁夏医科大学实验动物中心屏障动物实验设施内[SYXK(宁)2015-0001],温度范围20~26℃,昼夜明暗交替(12/12 h),自由进水摄食。动物使用的伦理审批号为:IACUC-NYDWZX2018071。
1.2 主要试剂与仪器
葫芦巴碱盐酸盐(ST8270,≥ 98%,北京索莱宝科学技术有限公司),苏木素染液(716113,珠海贝索生物技术有限公司),伊红染液(716122,珠海贝索生物技术有限公司),水浴锅(DK600S,上海精宏实验设备有限公司),电子天平(PTY-C2200,福州华志科学仪器有限公司),全自动组织脱水机(ASP200S,德国Leica公司),包埋机(Leica HistoCore Arcadia,德国Leica公司),石蜡切片机(RM2245,德国Leica公司),正置荧光显微镜(NI-U,日本尼康),无水乙醇(20181110,北京市北联精细化学品开发有限公司),二甲苯(20171220,北京市北联精细化学品开发有限公司)。
1.3 实验方法
1.3.1 实验分组及药物干预
SPF级雄性ICR小鼠120只,随机分为正常对照组、模型组和葫芦巴碱药物干预组(分别给予25 mg/kg,50 mg/kg,100 mg/kg,分为低、中、高剂量组),每组24只。正常对照组及模型组给予生理盐水0.5 mL/20 g灌胃,葫芦巴碱药物干预组给予相应剂量葫芦巴碱预防灌胃给药一周后,单次热应激处理,继续给药14 d。
1.3.2 小鼠睾丸的局部热应激处理及标本采集
药物干预一周后,各组小鼠麻醉处理,正常对照组不予处理,其余各组小鼠用固定架固定,待小鼠睾丸下降至阴囊后将其下腹部浸入43℃恒温水浴15 min。随后取出小鼠,打开固定架,室温放置,待麻醉消除后放回鼠盒。各组继续给予相应药物灌胃14 d。并分别于1,7,10,14 d称重并处死动物。留取睾丸、附睾及精囊腺,吸干表面,称取重量,计算脏器系数。右侧睾丸用bouin液固定,左侧睾丸置于-80℃保存,备用。
睾丸系数(testicular coefficient)=
(双侧睾丸平均重量/体重) ×100%;
附睾系数(epididymis coefficient)=
(双侧附睾平均重量/体重) ×100%;
精囊腺系数(seminal vesicle coefficient)=
(精囊腺重量/体重) ×100%。
1.3.3 附睾精子数的检测[5]
将盛有5 mL生理盐水的培养皿置于恒温水浴箱内预热至37℃,将小鼠右侧附睾尾剪下称重并在培养皿中剪碎,摇匀,水浴5 min,待精子充分游离出来,用200目细胞筛过滤,然后取20 μL滤液滴于计数板上,在400倍光镜下计数血细胞计数板上4大格精子的数量,计算单位重量附睾尾精子数量,根据附睾重量,进一步计算出整个附睾平均精子数量。
每克附睾尾组织所含精子数量=四大格精子数量之和/4×原液体积(2 mL) ×10 000/组织块重量;
整个附睾平均精子数量=每克附睾尾组织所含精子数量×附睾重量。
1.3.4 小鼠睾丸组织切片的制备与观察
用Bouin液固定睾丸组织4~8 h后,用注射器扎破睾丸两端的鞘膜,确保固定液充分浸润组织达到固定效果。固定48 h后取材脱水,将睾丸组织从 Bouin固定液中取出,放入脱水盒内,脱水盒依次放入Leica ASP200S脱水机中以不同的梯度酒精脱水7.5 h,透明1.5 h,浸蜡2 h。石蜡包埋,置于4℃冷藏箱保存。用半自动石蜡切片机切片(片厚约5 μm),苏木素伊红染色,封片,晾干。用正置荧光显微镜观察睾丸组织切片中生精小管、生殖细胞的形态变化情况,并记录拍照。
1.4 统计学方法
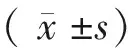
2 结果
2.1 葫芦巴碱对热应激致睾丸组织损伤的影响
热应激后第1天,与正常对照组比较,模型组附睾精子数量显著减少(P< 0.01)、附睾系数(P< 0.01)、精囊腺系数(P< 0.01)、睾丸系数(P< 0.05)明显降低;与模型组比较,中剂量葫芦巴碱药物干预组精子数量显著升高 (P< 0.05)。高剂量葫芦巴碱药物干预组精子数量显著升高(P< 0.05)、精囊腺系数(P< 0.01)显著升高。
热应激后第7天,与正常对照组比较,模型组附睾精子数量、睾丸系数、附睾系数、精囊腺系数均显著性降低 (P< 0.01);与模型组比较,葫芦巴碱各剂量组均能显著提高小鼠睾丸系数、附睾系数(P< 0.01)、精囊腺系数(P< 0.05)并增加精子数量,且呈剂量依赖性。
热应激后第10天,与正常对照组比较,模型组各脏器系数与附睾精子数量仍显著降低(P< 0.01);与模型组比较,低剂量给药组附睾精子数量(P< 0.05)、睾丸系数(P< 0.01)、附睾系数(P< 0.05)、精囊腺系数(P< 0.01)均明显增加。中、高剂量药物干预组各脏器系数与精子数均显著增加(P< 0.01),呈明显时间依赖性。
热应激后第14天,模型组部分自修复,但与正常对照组比较,各脏器系数与精子数仍有明显降低(P< 0.05);与模型组比较,中、低剂量给药组睾丸系数有明显升高(P<0.05),高剂量给药组睾丸系数(P< 0.01)、精子数(P< 0.05)均显著增加。结果见表1。
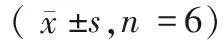
表1 葫芦巴碱对热应激致小鼠睾丸系数,附睾系数、精囊腺系数及附睾精子数的影响
注:模型组与正常对照组比较,*P< 0.05,**P< 0.01;药物干预组与模型组比较,#P< 0.05,##P< 0.01。
Note. Comparison between the model group and the normal control group,*P< 0.05,**P< 0.01. Comparison between the drug intervention group and the model group,#P< 0.05,##P< 0.01.
2.2 单次热应激对小鼠睾丸组织形态的影响
2.2.1 大体观察
正常对照组小鼠睾丸结构完整,睾丸组织紧实圆润,体积大,血管网清晰充盈可见。热应激第7天后,与正常对照组比较,模型组小鼠睾丸结构较完整,睾丸组织松驰,体积较小,血管网颜色变浅。与模型组比较,各剂量药物干预组睾丸组织紧实,体积较大,血管网清晰可见。
2.2.2 葫芦巴碱对热应激诱导的小鼠睾丸损伤模型中睾组织病理的影响
HE染色后镜下可见:正常对照组(图1:E1,E2,E3,E4)小鼠睾丸组织的生精小管排列紧密有序,细胞层数清晰完整,管周联系紧密,生精上皮可见精原细胞及各个发育阶段的精母细胞、精细胞、精子细胞,管腔中成形精子密集可见,睾丸的Leydig间质细胞规则有序。与正常对照组比较,模型组热应激后第1天(图2A)生精上皮层数减少,细胞排列松散,精细胞明显减少,管腔中成形精子显著减少,生精上皮变薄,管周联系不紧密。第7天(图3A),小鼠睾丸组织生精上皮明显空泡变性及萎缩,排列紊乱,生精细胞层数和数量明显减少,生殖细胞剥离,精子未可见,且间质空泡增多,间质细胞显著减少,胶原纤维增生,界膜增厚。第10天(图4A),除睾丸间质细胞数量稍有增加,其它损伤均未改善。第14天(图5A),小鼠睾丸组织生精上皮仍存在明显空泡变性及萎缩,排列较为整齐,生精细胞层数依然混乱,数量明显少,精子未可见。与模型组比较,葫芦巴碱各剂量药物干预组对热刺激致小鼠睾丸生精小管的损伤在不同时间段均有一定的恢复作用,其中以高剂量组在热应激后14 d效果最佳(图5D)。镜下可见生精小管各级层数清楚增多,空泡变性现象改善,生精细胞分布较为致密,排列整齐,精细胞和精子均可见,且管间联系紧密,间质细胞显著增多(图2~5:B,C,D)。
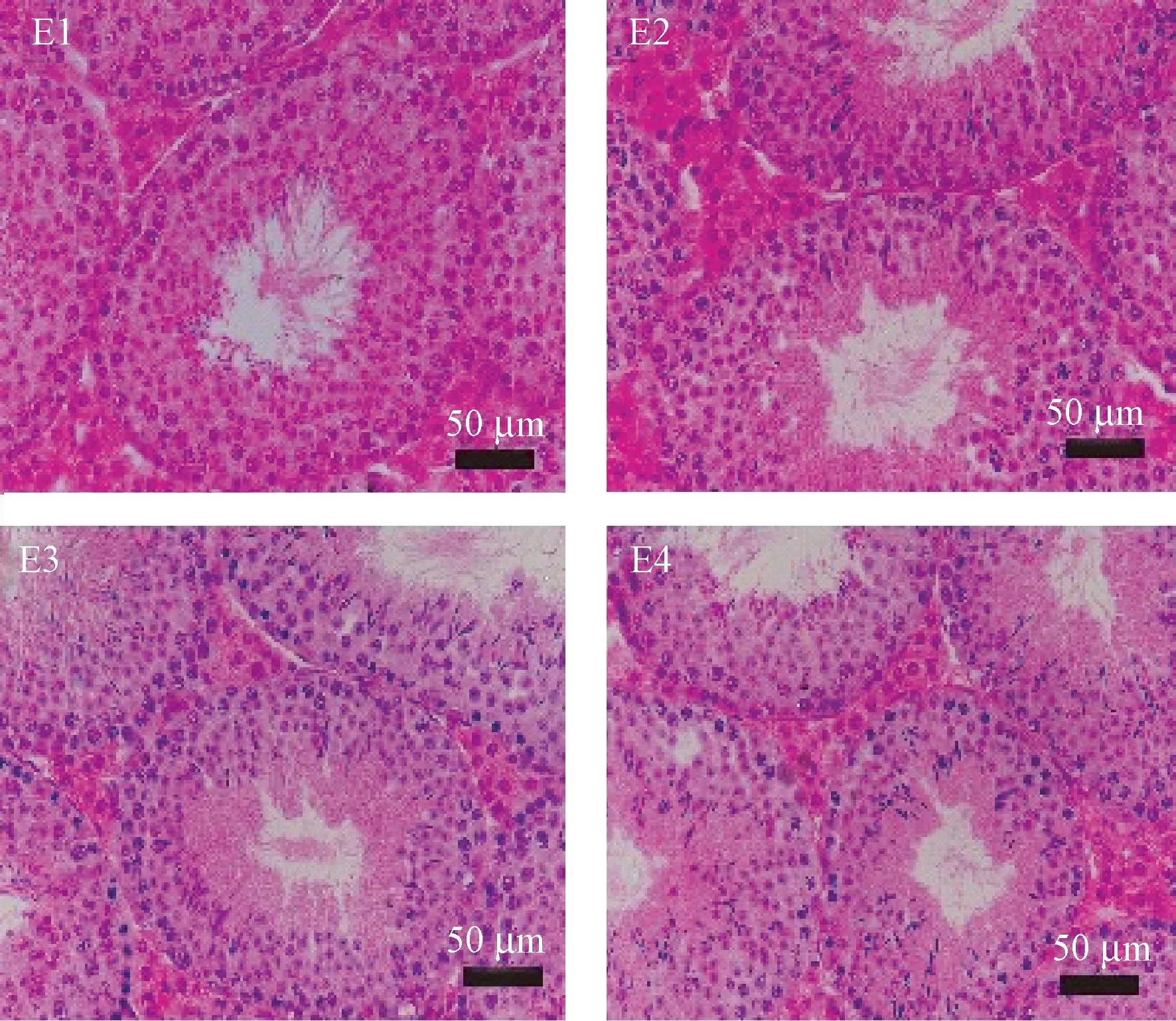
注:E1:第1天正常对照组;E2:第7天正常对照组;E3:第10天正常对照组;E4:第14天正常对照组。图1 正常对照组睾丸组织病理观察(HE染色,×400)Note. E1, Normal control group on the 1st day. E2, Normal control group on the 7th day. E3, Normal control group at the 10th day. E4, Normal control group on the 14th day.Figure 1 Pathological observation of the testis in the control group. HE staining
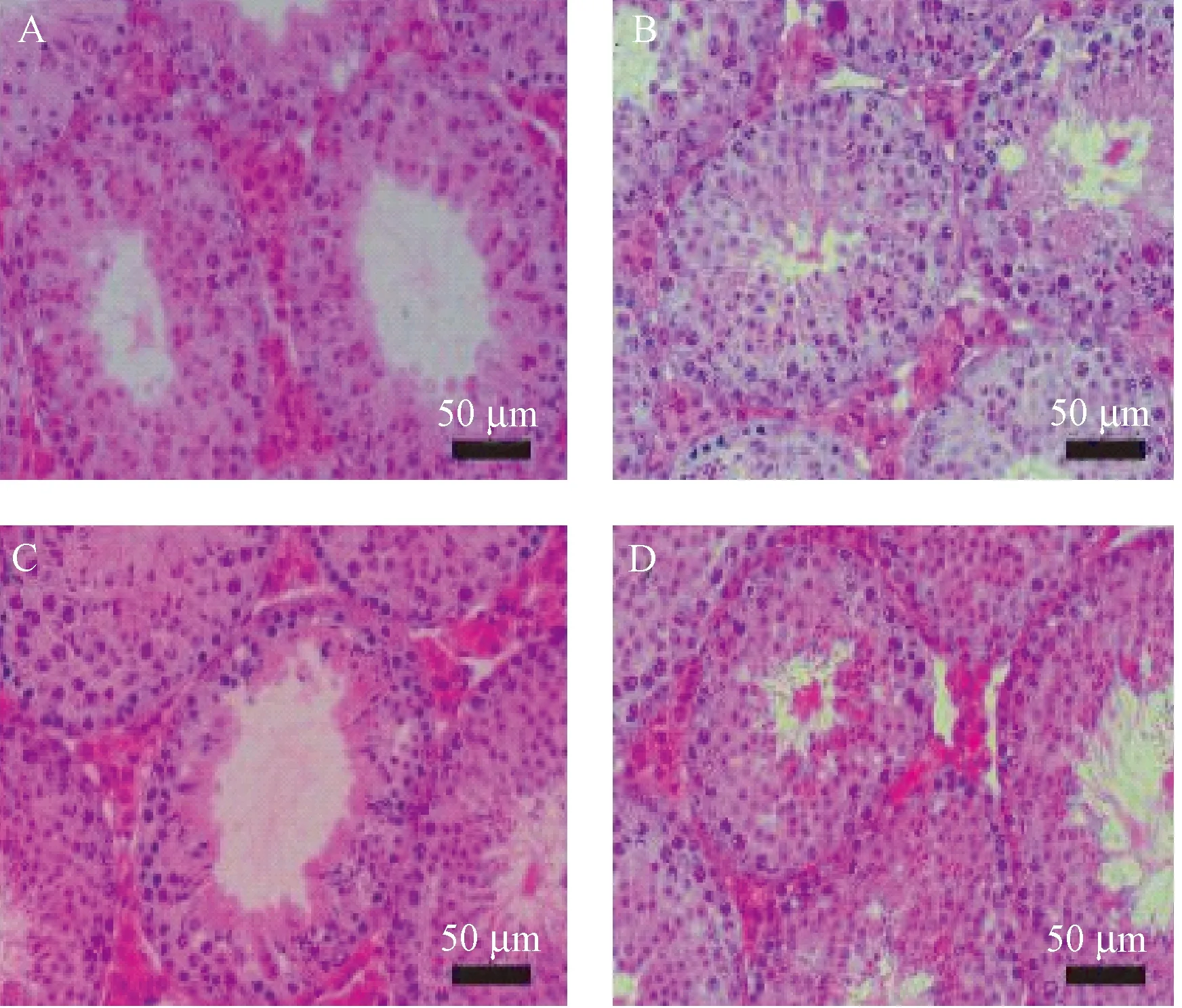
注:A:模型组;B:葫芦巴碱低剂量组;C:葫芦巴碱中剂量组;D:葫芦巴碱高剂量组。下图同。图2 热应激后第1天,模型组和葫芦巴碱干预组睾丸组织病理观察(HE染色,×400)Note. A, Model group. B, Low dose group of trigonelline. C, Medium dose group of trigonelline. D, High dose group of trigonelline. The same in the following figures.Figure 2 Pathological observation of the testis tissue in the model group and trigonelline group on the 1st day after heat stress. HE staining
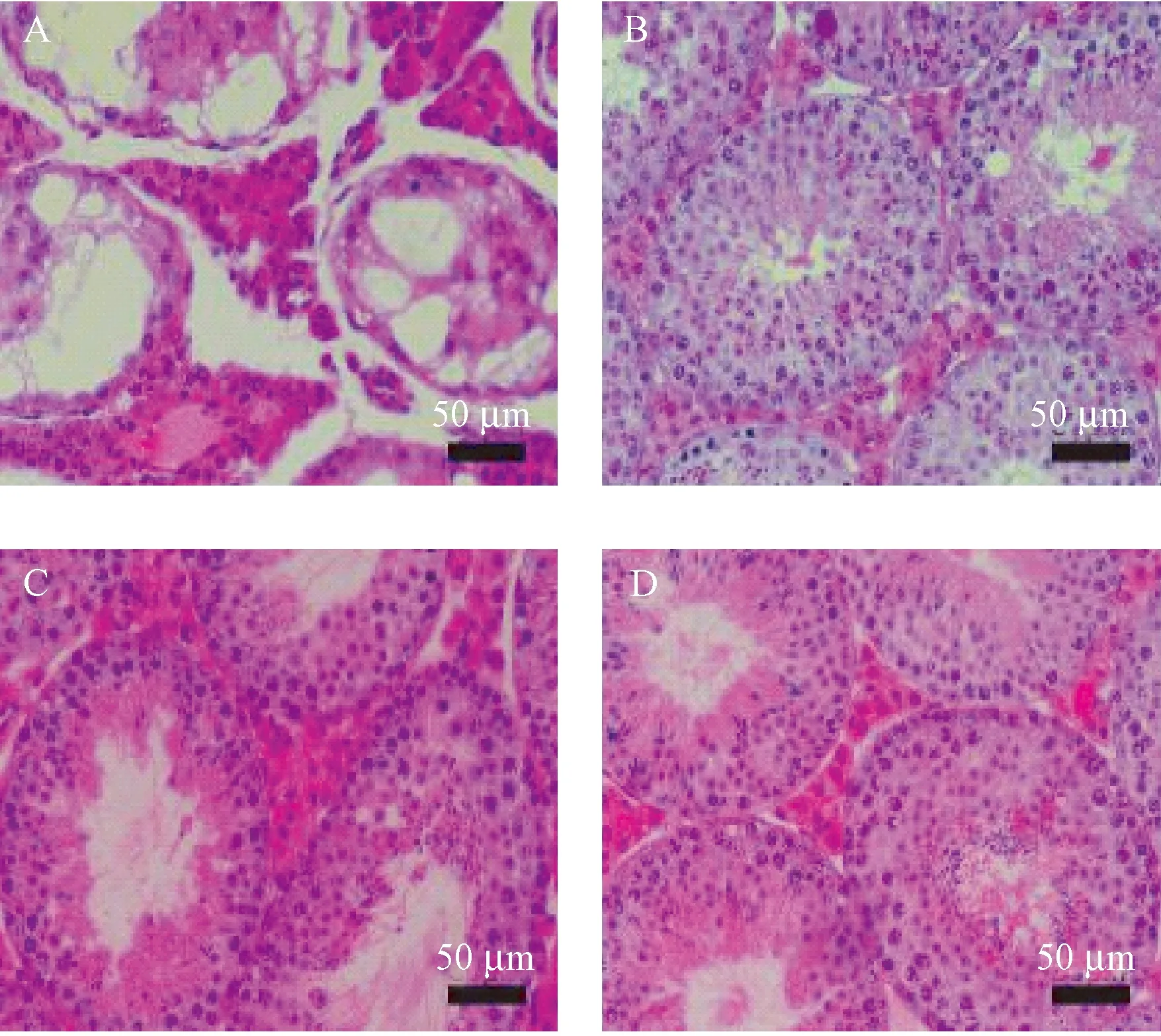
图3 热应激后第7天,模型组和葫芦巴碱干预组睾丸组织病理观察(HE染色,×400)Figure 3 Pathological observation of the testis tissue in the model group and trigonelline group on the 7th day after heat stress. HE staining
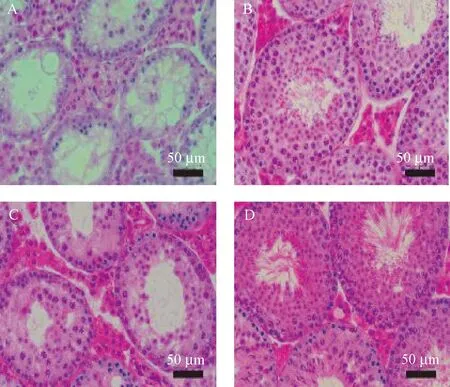
图4 热应激后第10天,模型组和葫芦巴碱干预组睾丸组织病理观察(HE染色,×400)Figure 4 Pathological observation of the testis tissue in the model group and trigonelline group on the 10th day after heat stress. HE staining
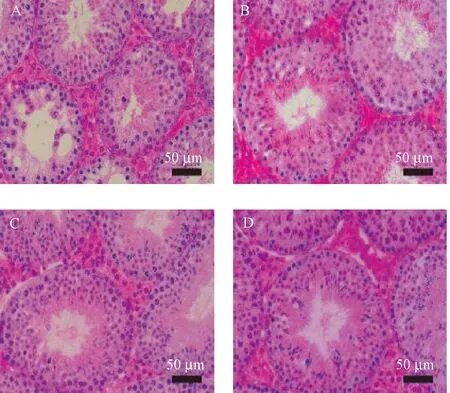
图5 热应激后第14天,模型组和葫芦巴碱干预组睾丸组织病理观察(HE染色,×400)Figure 5 Pathological observation of the testis tissue in the model group and trigonelline group on the 14th day after heat stress. HE staining
3 讨论
雄性小鼠生殖系统由睾丸(testis)、生殖管道、附属腺及外生殖器组成。睾丸能产生精子,分泌雄激素。附睾可暂存精子和促进精子成熟,也是运输精子的生殖管道[6-7]。睾丸包含生精小管,直精小管、睾丸网和Leydig间质细胞,其中生精细胞占多数,而生精小管由生精细胞(雄性的生殖细胞)和Sertoli支持细胞组成。精子是减数分裂后期形成的,其发生时生精细胞(包括A、B型精原细胞,初、次级精母细胞及早、晚期精子细胞和精子)从生精上皮的基底侧迁移到管腔侧,其间经过复杂的分裂再生过程[8]。本研究发现,睾丸组织损伤明显造成精子数的显著减少,且各生殖器官脏器系数显著降低。
中医学认为肾藏精,为先天生殖之本,肾能汇聚五脏六腑之精而藏之,肾气充盈,才能保障生殖功能及性功能正常。而精子发生、成熟与肾精充盈与否关系密切[9]。葫芦巴适生于宁夏、甘肃、青海、新疆、内蒙古等地,在宁夏境内分布尤为广泛,其干燥成熟种子作为常用中药收入中国药典[10]。用于治疗“肾脏虚冷”等多种虚损性疾病[11]。葫芦巴其它化学成分的研究已多有报道,但其葫芦巴碱在保护生殖器官损伤方面鲜有报道。
马文智等[12]报道热应激抑制了精原细胞的增值。丛霞等[13]研究热应激对雄鼠生殖器官及精子发生的影响。热应激温度的阈值决定了对生殖细胞造成的损害程度,43℃单次热应激处理15 min时可以明显诱导生殖损伤[14-18]。本研究以43℃热处理15 min成功诱导小鼠睾丸组织损伤,并进一步监测热应激后不同时间小鼠睾丸组织损伤情况以及自恢复情况。结果表明:与正常对照组比较,热应激后小鼠生殖器官脏器系数显著降低,精子数量明显减少,睾丸组织病理形态变化显著,并在观察期间没有完全的可逆性恢复。葫芦巴碱药物干预后,小鼠生殖器官脏器系数显著提高,精子数量明显增加,睾丸组织病理形态部分恢复,镜下可见生精小管界膜完整,各级生精细胞排列致密清楚,数量明显增多,空泡变性现象显著改善,大部分管腔内精细胞和精子均可见,结构逐渐恢复趋于正常,且呈剂量依赖性和时间依赖性。说明葫芦巴碱对热应激致小鼠睾丸组织损伤由明显的保护作用,其作用机制还有待于进一步研究。

