以粟米糠油为原料制备营养型人造奶油基料油的研究
孙塬,肖志刚,杨庆余,李芮芷,李佳楠,梁丹洋,段玉敏
(1.沈阳师范大学粮食学院,辽宁 沈阳 110034;2.沈阳师范大学学前与初等教育学院,辽宁 沈阳 110034)
粟米,又称谷子,是一年生草本植物,属于谷类。谷子是我国最古老的栽培作物之一,起源于黄河流域。粟米糠是谷子在脱壳过程中产生的米胚芽,糊粉层和种皮的混合物[1]。粟米糠油是从粟米糠中提取得到的油脂,是一种不需占用耕地,低成本的油类。粟米糠油的化学结构组成独特,非常符合人类膳食脂肪酸推荐标准,粟米糠油中不饱和脂肪酸可达80%以上,且以亚油酸含量最高[2]。亚油酸能降低胆固醇在血管壁上过多的沉积,可预防动脉粥样硬化,同时,粟米糠油中含有的维生素E、角鲨烯、活性脂肪酸酶、谷维素、植物甾醇等几十种天然生理活性成分,对调节人体机能、改善代谢功能都有很大作用[3]。粟米糠油价格低廉,有效利用粮食加工副产品,符合现代社会“节约,高效”的理念,具有较大的现实意义。
人造奶油是一种在精炼食物油中加水及乳化剂,经乳化,急冷,捏合成的具有类似天然奶油特点的一类可塑性油脂制品。随着人民经济消费水平的提升,人造奶油已经成为食品行业中不可缺少的重要产品,广泛应用于糕点,饼干,糖果,冷饮等食品的生产中。人造奶油最初是以动物油脂为基料油,但动物油脂作为基料油,有氧化稳定性差、结晶颗粒大、储存性能差、饱和脂肪酸含量过高和抗生素残留等缺点,导致奶油口感不佳,入口有黏腻感,影响食欲,且饱和脂肪酸过高,容易增加人体祸患心血管疾病及动脉粥样硬化的危险[4],严重危害人们身体健康。本文以粟米糠油和氢化大豆油为原料,采用酶法酯交换法确定制备人造奶油基料油的工艺条件,并对人造奶油基料油的性质进行分析。使用粟米糠油替换原有的动物油脂作为基料油,生产出熔点低、口感好、营养全面的新型植物型人造奶油,满足近年市场对营养健康型人造奶油的需求。
1 材料与方法
1.1 材料与试剂
粟米糠油:江西天然香料有限公司;极度氢化大豆油:丰益(上海)生物科技研发中心;Lipozyme TL IM 固定化脂肪酶(酶活250 IUN/g):诺维信生物技术有限公司。
1.2 仪器与设备
微波反应器(MCR-3):格兰仕微波炉有限公司;电子万用炉(DL-1):北京市永光明医疗仪器厂;烘箱(XLRF):柳州兴柳电气有限公司;恒温磁力搅拌器(RCT):艾卡(广州)仪器设备有限公司;制冰机(SNY-101):上海声阳电子有限公司;离心机(LD4-2):上海市安亭科学仪器厂;电子分析天平(DF110 型):中国轻工机械总公司常熟衡器工业公司;高效气相色谱仪(GC-2014):岛津企业管理(中国)有限公司;射线衍射仪(MPDDY2094 X):荷兰帕纳科公司。
1.3 试验方法
1.3.1 酶法酯交换反应
溶解氢化大豆油,使其与粟米糠油充分混合,加入一定比例的Lipozyme TL IM 固定化脂肪酶。在恒温磁力搅拌器中反应一段时间后,用离心机除去脂肪酶,得到酯交换产物。反应以熔点作为指标、对底物质量比、反应时间、酶添加量、反应温度分别进行单因素试验,确定工艺条件[5-6]。
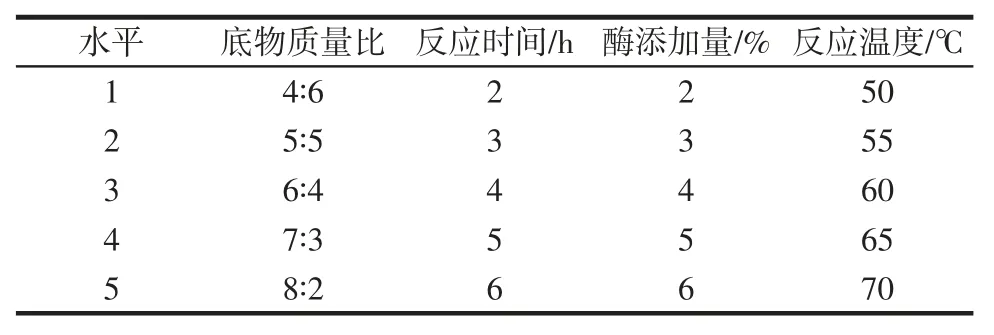
表1 酶法酯交换反应条件参数及水平Table 1 Conditions and parameters of enzymatic interesterified
1.3.2 熔点测定
采用毛细管法测量熔点。融化酯交换产物混合油脂,将毛细管插入油脂中,当油脂在毛细管中高度达到1 cm 左右时取出,放入冰水中使其迅速凝固,转移到4 ℃冰箱中冷藏15 h 后待测。
测量时将毛细管安装在温度计精确位置,控制加热速度适宜,注意观察并记录油脂的熔化瞬间水的温度,每个样品进行3 次平行测试,减小误差。
1.3.3 热性质的测定
油样融化结晶热性质分析采用差示扫描量热法(differential scanning calorimetry,DSC)。将保存在冰箱里的样品取出,精确称量油脂混合物6 mg~10 mg,记录并放入专用铝盒内,压紧密封,待测,检测时以空盒做参比。开始测定前先将样品升温80 ℃,稳定10 min,以消除历史记忆。测定条件:以10 ℃/min 降温至-20 ℃,稳定 5 min,然后从-20 ℃以 5 ℃/min 升温至 80 ℃[7]。
1.3.4 甘三酯组成分析
采用高温气相色谱法测定反应前后油脂甘三酯组成变化[8]。气相色谱条件:DB-1HT 毛细管柱(15 m×0.32 mm×0.1 μm),进样量 0.5 μL。进样器温度 380 ℃,检测器温度400 ℃,初始温度100 ℃,首先以50 ℃/min升温至 220 ℃,其次以 30 ℃/min 升温至 290 ℃,然后以20 ℃/min 升温至 330 ℃,保持 2 min,最后以 30 ℃/min升温至 380 ℃,保持 3 min[9]。
1.3.5 晶型的测定
采用X-射线衍射法进行测定酯交换前后油脂晶型的变化。将保存在冰箱里的样品取出,适量地平铺于玻璃片上的圆孔内,用X-射线衍射仪测定,工作电压 40 kV,电流 40 mA,温度 25 ℃左右,扫描角度:5°~50°,扫描速度为 5 °/min。
1.3.6 酯交换反应率(interesterification rate,IR)
根据反应前后气相色谱图,以酯交换反应前后混合油脂中变化最大的两种总碳数为指标,对酯交换反应率进行研究。酯交换反应率的计算公式如下[10]:
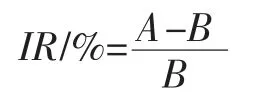
式中:A 为酯交换反应后变化最大的两种总碳数面积之和与反应后总面积的商,B 为反应前两种总碳数面积之后与反应前总面积的商。
2 结果与分析
2.1 酯交换反应指标的选择
气相色谱中可根据反应前后气相的出峰时间和出峰顺序的变化来推测甘三酯的组成变化和总碳数组成,采用高温气相可对甘三酯进行分离分析,并以C52 和C54 的变化为指标,对酶法酯交换反应前后甘三酯组成的变化进行分析,计算酯交换反应率[11]。
2.2 酯交换反应
2.2.1 底物质量比对酯交换反应的影响
在其他条件不变的情况下,底物质量比会从根本上影响反应结果。酶与底物的结合有先后顺序,因此只有在配比合适的情况下,酶才能最高效的催化反应,分解一定的最终产物,达到最优结果。
底物质量比对酯交换反应的影响见图1。
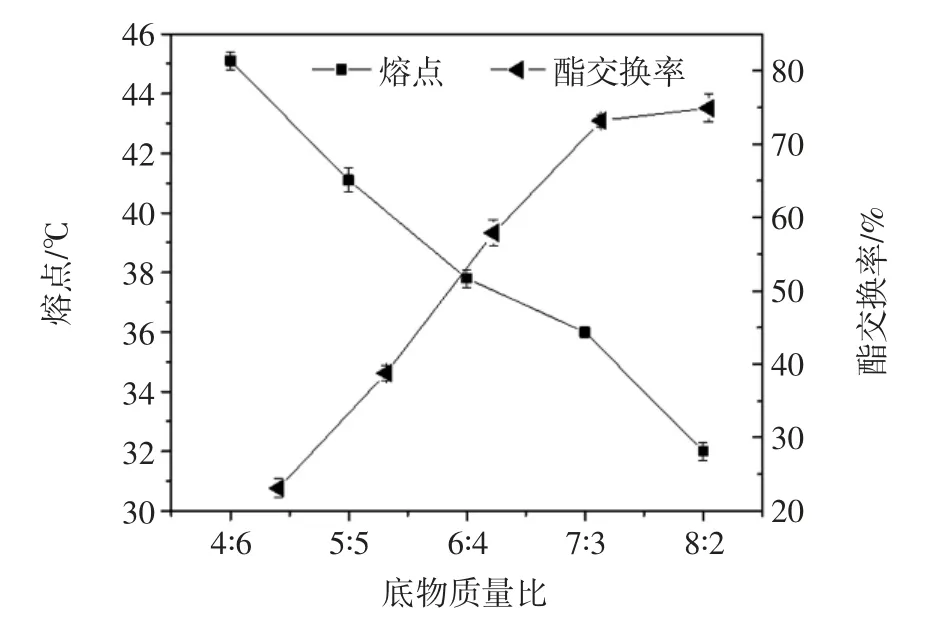
图1 底物质量比对酯交换反应的影响Fig.1 Influence ofsubstrate ratio temperature on interesterification
由图1可以看出,粟米糠油占底物质量比例越高,混合油脂熔点越低,酯交换率越高。这是由于氢化大豆油中含有高熔点的甘油三酯。如果氢化大豆油比例过高,熔点过高,酯交换率低,则奶油入口不易化、黏度大且延展性差、包裹空气能力不足;如果粟米糠油比例过高,则熔点过低、油脂密度小、塑性差[12]。当底物油脂比例适当时,酯交换率也趋于稳定,口感适宜。综合考虑,选取粟米糠油∶氢化大豆油质量比为7 ∶3。
2.2.2 反应时间对酯交换反应的影响
反应时间一定程度上影响酶的活性,反应初始时酶活性较高,随着反应时间的延长,酶逐渐失活,且开始发生副反应,因此,反应时间对酶催化反应的影响十分重要。
随着全面深化改革不断走向深入,国家不再全额供养地方科研院所,大量单位转制为国有科技型企业,这就不可避免的要直面市场竞争。难以融资、体制机制僵化、人才队伍更迭严重等问题更是加剧了地方科研院所的困难。具体到改革过程中,需要进行法人治理结构的单位正面临着理事会对单位的实际把控问题。行业性质的研究单位随着产业转移和更新转型压力更大,有一定规模的科研单位因二级法人单位业务、财务独立而难以有效集聚资源,完全按照政府部门的模式管理又导致科研单位体制机制僵化,致使盈收无法合法分配,这些问题有的是现实发展所致,有的是历史遗留问题。
反应时间对酯交换反应的影响见图2。
由图2可知,混合油脂的熔点随着反应时间增加而降低,反应时间越长,熔点越低,酯交换率越高。这是由于酯交换反应使油脂的低熔点甘油三酯和高熔点甘油三酯的含量发生改变,反应时间越长,酯交换率越高,酯交换反应越完全,若反应时间不足,酯交换反应则不充分。反应时间从2 h~5 h,反应产物的酯交换率升高,熔点逐渐降低,当反应时间达到6 h 后,与反应5 h 相比,产物熔点变化幅度不大,说明反应5 h基本可以反应完全。反应时间过长会使副反应产物增加,同时酰基转移的概率增加,所以时间不宜过长,考虑到生产成本和节约时间,选择反应时间为5 h[13]。
2.2.3 酶添加量对酯交换反应的影响
酶量添加低,不能高效催化反应,但酶量过高,不仅不利于生产成本的控制,同时多余的酶量也会开始发生逆反应[14],使反应不能高效有序的进行,因此,控制好酶的用量非常重要。
酶添加量对酯交换反应的影响见图3。
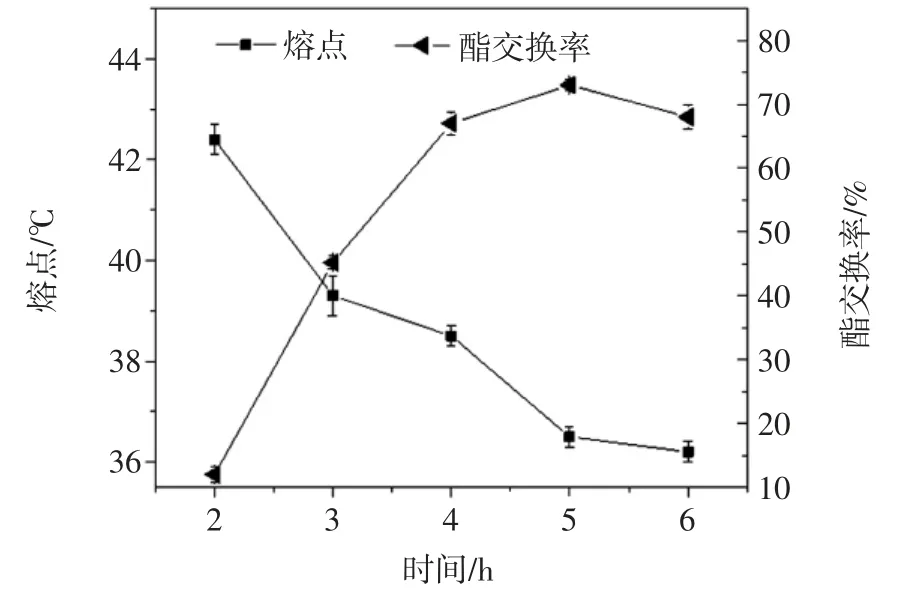
图2 反应时间对酯交换反应的影响Fig.2 Influence ofreaction time temperature on interesterification
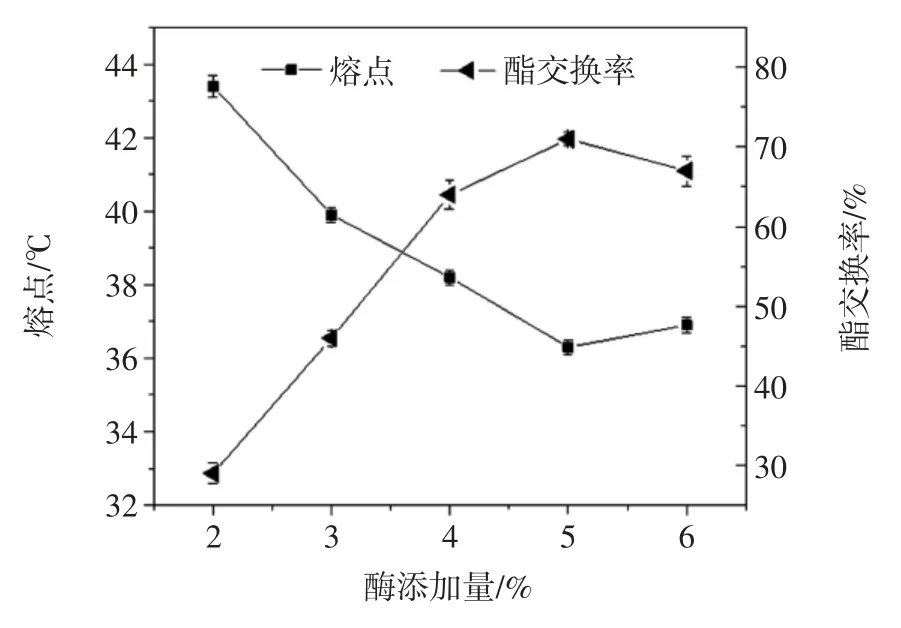
图3 酶添加量对酯交换反应的影响Fig.3 Influence of lipase dosage temperature on interesterification
由图3可知,在一定范围内,酶添加量越高,油脂熔点越低,酯交换率越高。这是因为随着酶添加量的增加,底物与酶的接触面积逐渐增加,酯交换反应速率提高,导致熔点逐渐下降。但酶添加量应当在适当范围,不宜过多,因为酶的反应是可逆的,当酶法酯交换反应基本完全时,增加酶量意义不大,且酯交换率有所下降,加之考虑酶的价格和生产成本,选择Lipozyme TL IM 固定化脂肪酶添加量为5%。
2.2.4 反应温度对酯交换反应的影响
温度对酯交换反应的转化率影响较大,温度低,转化率低,同时酯交换速率低,反应时间延长;温度过高则易使酶失活,酯交换率降低。
反应温度对酯交换反应的影响见图4。
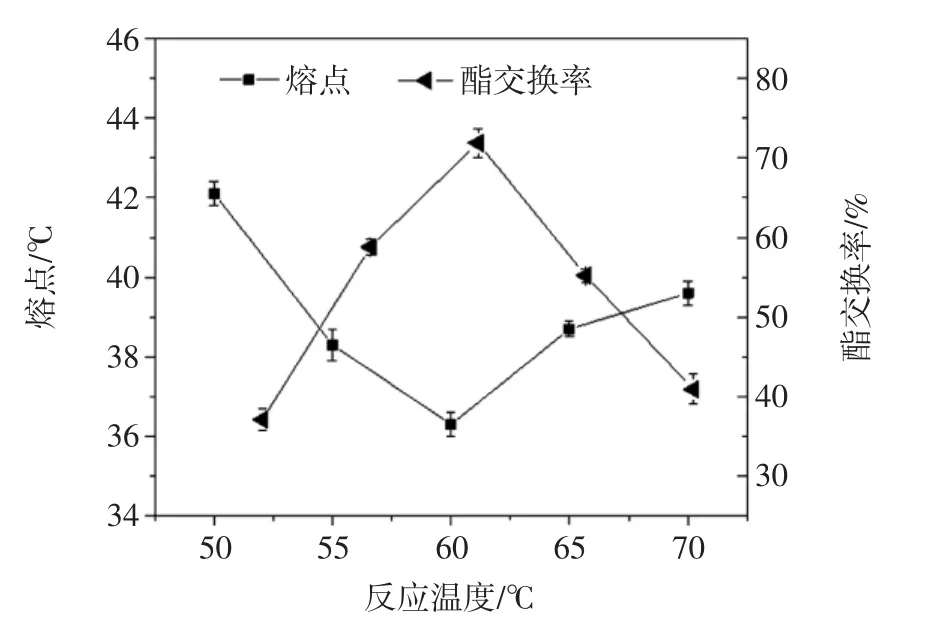
图4 反应温度对酯交换反应的影响Fig.4 Influence of reaction temperature on interesterification
2.3 热性质的测定
采用差示扫描量热法通过测定油脂中的热量变化来表明脂肪酸组成发生变化,可以通过对比反应前后的图像的变化,判定油样热性质的变化。
酯交换反应前后粟米糠油中脂肪酸的变化见图5。
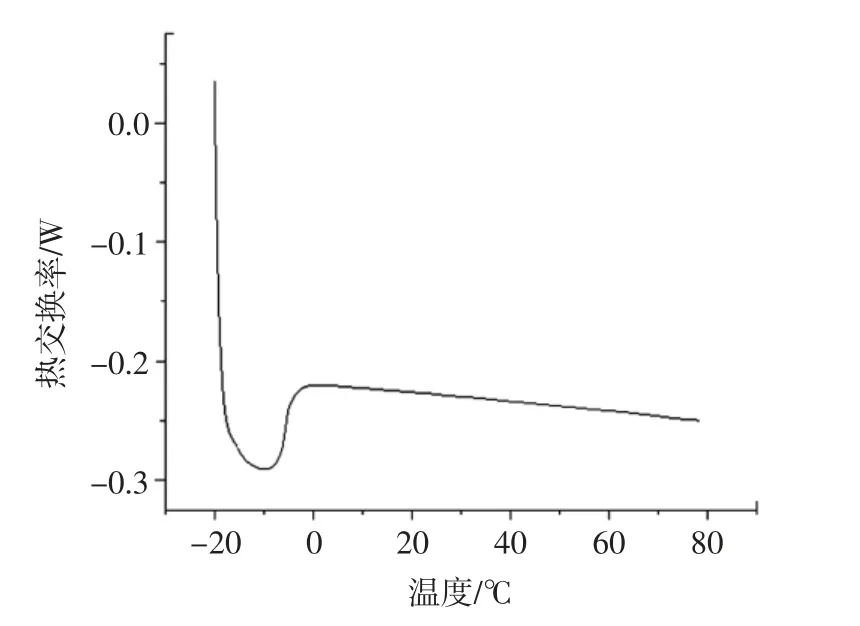
图5 粟米糠油DSC 图像Fig.5 DSC image of millet bran oil
图5在-10 ℃出现一个吸热峰,说明粟米糠油熔点很低,常温下为液态,这是由于粟米糠油中含有大量不饱和脂肪酸造成的,图像无放热峰,基线平稳,说明正常温度下油脂不会凝结。峰型圆钝,峰面积较大,说明其热交换速率较低[16]。因此粟米糠油须混合部分硬性油脂来综合熔点,使其在常温下能保持基料油形态,丰富营养,改善口感。
酯交换反应前后氢化大豆油中脂肪酸的变化见图6。
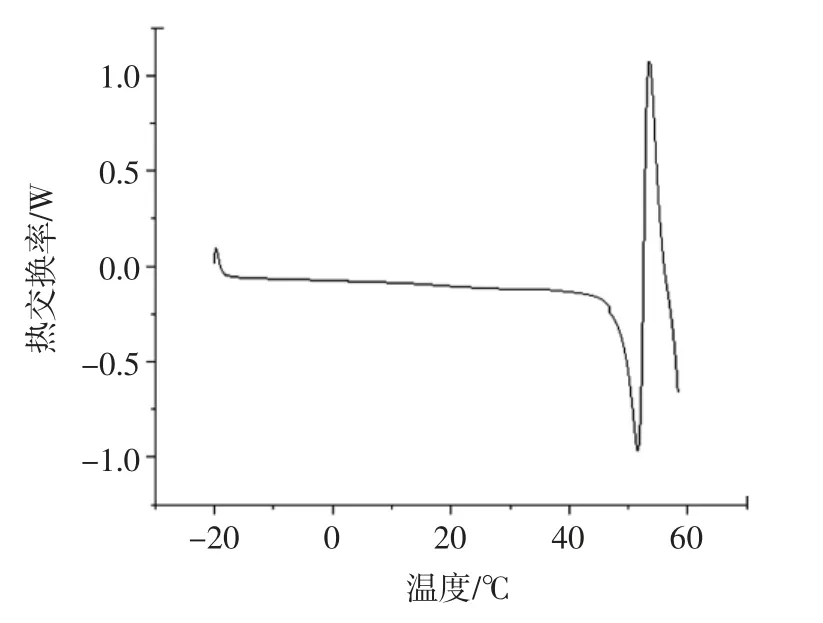
图6 氢化大豆油DSC 图像Fig.6 DSC image of hydrogenated soybean oil
由图6可以看出,氢化大豆油吸热峰放热峰均较为靠后,在60 ℃时样品热容增加,基线改变,说明氢化大豆油在温度较高时才会发生热反应,其峰尖锐,峰面积较窄,说明其吸热放热能力很强。且大豆油种植范围广,原料普遍,产量高,成本低廉。故符合与粟米糠油混合的条件。
酯交换反应前后混合油中脂肪酸的变化见图7。
由图7可以看出酯交换后峰型产生变化,混合油脂反应后与反应前相比,图像由3 个峰变为4 个峰,这是由于脂肪酸在甘油三酯骨架上重排引起的;反应后高温处的溶解峰波动变小,表明混合油脂中的饱和甘三酯含量下降。0 ℃溶解峰的存在是由于底物中含有粟米糠油,粟米糠油中丰富的不饱和脂肪酸使图像呈现低温溶解峰。反应后峰型趋于稳定,峰面积变小,峰型变窄,表明酯交换后油脂功能特性有所提高,且口感更加清爽不厚重。
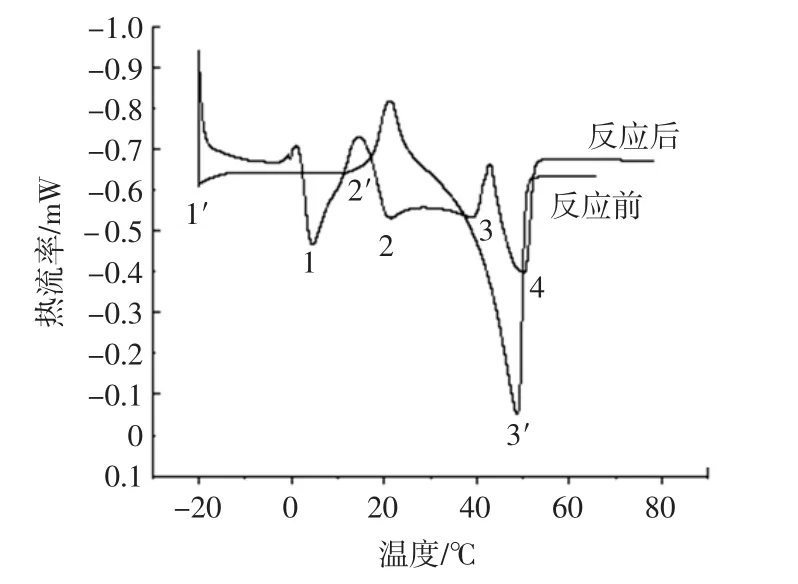
图7 酶法酯交换反应前后脂肪酸的变化Fig.7 Change of fatty acid before and after the enzymatic interesterified
2.4 甘三酯组成
甘三酯组成的改变对油脂的风味和口感有重要意义,在酯交换反应中,甘三酯在脂肪酶的作用下,生成甘油和脂肪酸。甘三酯的相对分子质量较高,沸点较高,因此反应所选色谱柱需要满足耐高温,柱长较短,柱内径细等条件[17]。
气相色谱中可根据反应前后气相的出峰时间和出峰顺序的变化来推测甘三酯的组成变化和总碳数组成。在该混合油脂中的气相检测主要表现为C52、C54 和C56 的变化。碳链越长,油脂熔点越高;碳链越短,油脂熔点越低。因此,C52 碳链长度最短,熔点最低;C56 碳链长度最长,熔点最高。
酯交换反应前混合油中甘三酯的变化见图8。酯交换反应后混合油中甘三酯的变化见图9。
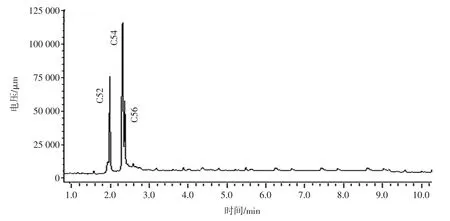
图8 酶法酯交换反应前甘油三酯的变化Fig.8 Change of triglyceride before enzymatic interesterified
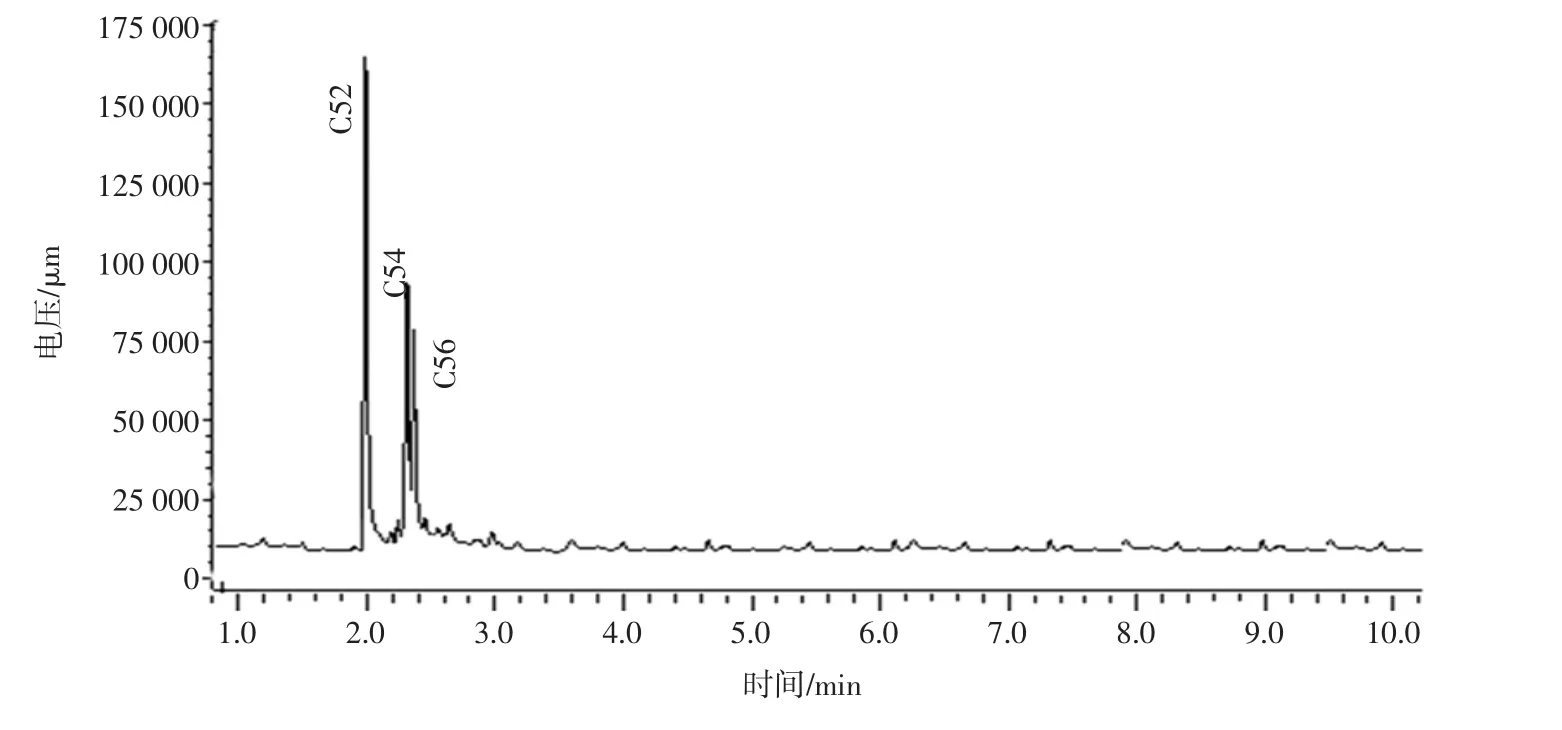
图9 酶法酯交换反应后甘油三酯的变化Fig.9 Change of triglyceride after enzymatic interesterified
图9酯交换后混合物甘三酯排布与图8反应前混合物的气相色谱图对比,反应后C56 含量变化不大,而C54 的含量减少,C52 含量显著增加,这说明油脂发生了酯交换反应且反应向碳数变低方向进行,总碳数发生改变,说明酯交换反应使甘三酯分子侧链上的脂肪酸发生重排,说明油脂甘三酯组成发生变化。长链甘三酯含量降低,短链甘三酯含量升高,表明油脂中的饱和脂肪酸已大部分转化为更加健康的不饱和脂肪酸。低熔点甘三酯增加,高熔点甘三酯降低,其熔点变得更加接近人体口腔,能达到入口即化,不黏腻的效果,其口感更佳,即比反应前更适合做人造奶油的基料油脂。
2.5 晶型分析
甘三酯的晶型会较大影响奶油的物理特性,如起泡性,润滑程度,涂抹性等。X-射线衍射法广泛应用于研究甘油三酯的晶型结构,脂肪结晶的晶型不同,则其短间距不同,可以通过短间距的差异判断其脂肪的不同[18]。油脂一般存在 3 种晶型:α 型,β 型和 β'型。短间距在4.15Å 的衍射峰代表α 型,α 型稳定性差且熔点较低;短间距在 3.8、4.2、4.27、4.35、3.97Å 属于 β'型,β'晶型较稳定,且能困住空气作为发酵气体,不仅口感好,也能起到增大体积的作用,因此β'型为一般情况下所需要的晶型;不符合α 型和β'型短间距的一般都可认作β 型,β 型结构为粗粒状,其包裹液相气相的能力都较差。
粟米糠油晶型结构见图10。
由图10可以看出粟米糠油只有一个峰,短间距在4.6Å,说明粟米糠油晶型组成单一,晶型为β 型。β 型油脂最为稳定,但颗粒大,在 25 μm~30 μm 之间,口感粗糙,因此需要对粟米糠油进行处理,将β 型转化为口感好,质量好的β'晶型,才能作为人造奶油的基料油。
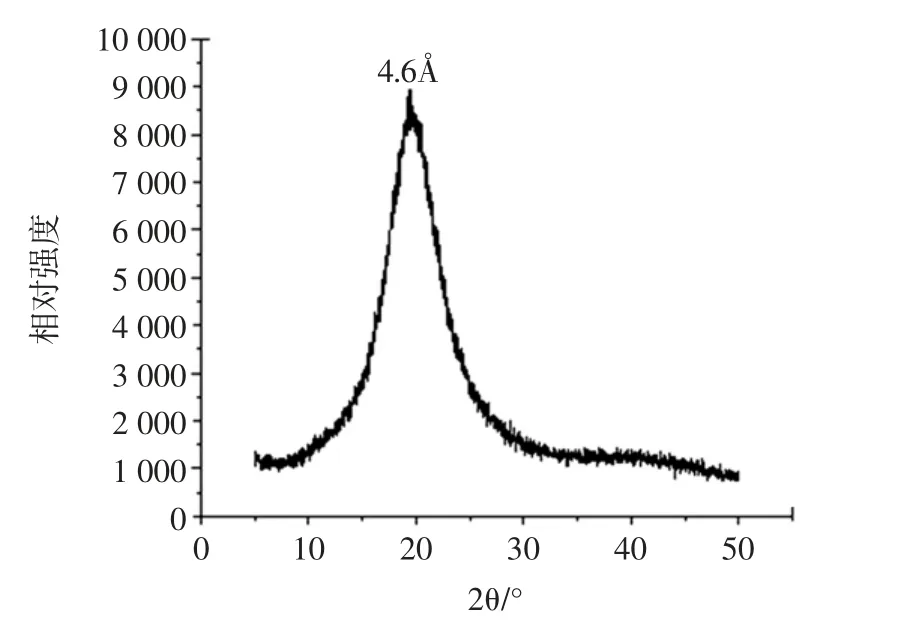
图10 粟米糠油晶型分析Fig.10 Crystal structure analysis of millet bran oil
氢化大豆油晶型结构见图11。
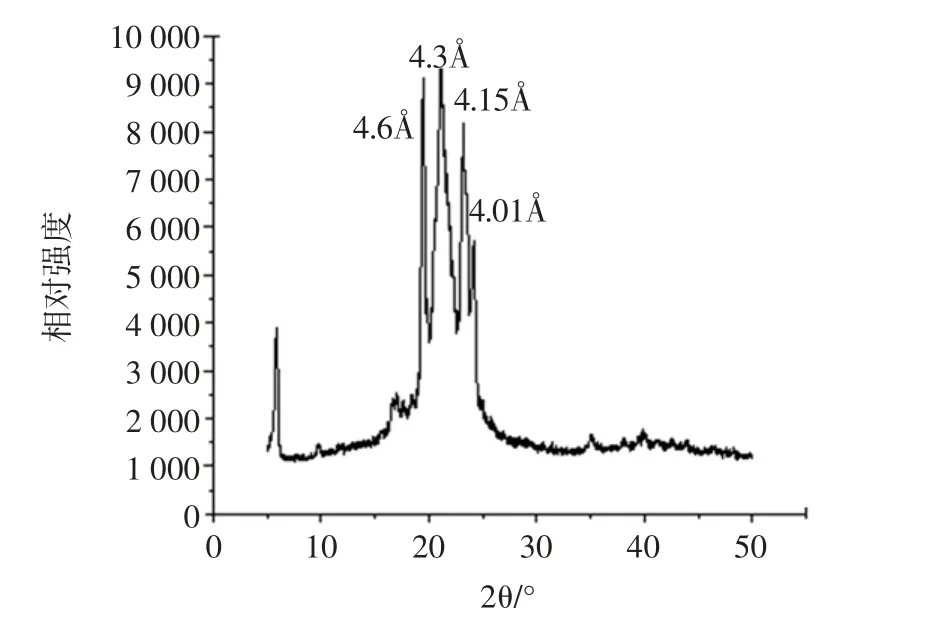
图11 氢化大豆油晶型分析Fig.11 Crystal structure analysis of hydrogenated soybean oil
由图11可以看出,氢化大豆油有4 个强吸收峰,分别为 4.6、4.3、4.15Å 和 4.01Å,其晶型组成为 α 型和β 型,且 β 型多于 α 型,但没有所需要的 β'型,说明反应前氢化大豆油和粟米糠油都不适合做人造奶油的基料油。
混合油脂晶型反应前后变化见图12。
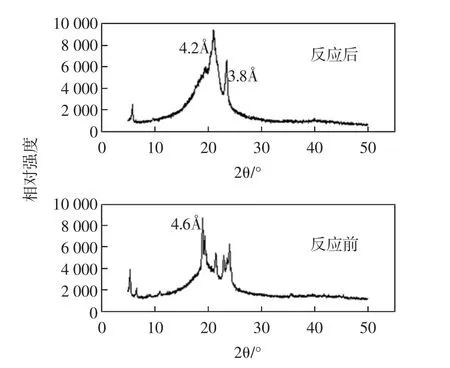
图12 混合油脂晶型分析Fig.12 Crystal structure analysis of mixed grease
由图12可以看出,反应前强吸收峰为4.6Å,反应后变为4.2Å 和3.8Å 处存在强吸收峰,说明酯交换反应后的油脂晶型向β'晶型转变。酯交换反应前后,油脂的晶型发生改变,是因为脂肪酶催化酯交换反应进行,改变了油脂的晶体结构[19],油脂的结构,口感,性能均发生改变。对于人造奶油,若产品中具有大量的β晶型,会使产品出现砂粒感和晶体不均匀的现象,导致人造奶油产品口感粗糙。β'晶型是一种可塑性好的细针状,是人造奶油期望的晶型。酯交换反应后油脂富含β'晶型,能够使制备出的人造奶油绵密,结构蓬松柔软[20],并具有良好的起泡性和塑性,能够达到期望的人造奶油基料油的要求。
3 结论
1)油脂的熔点以接近人体口腔温度为宜,约在37 ℃左右。而酯交换率越高,说明甘三酯的转化越充分。则通过单因素试验法可得出酶法酯交换的最佳反应条件为反应温度60 ℃,反应时间5 h,酶添加量为5%,底物中粟米糠油:氢化大豆油质量比为7 ∶3 时,得到产物的熔点为36.5 ℃。
2)酶法酯交换后,原底物中存在的β 晶型甘三酯大量转化为β'晶型,反应后油脂中含有较多β'晶型,β'晶型有针状结构,其口感柔软,组织绵密,起泡性和塑性更强,不仅改善口感,也能增加奶油体积,更适宜做人造奶油基料油。
3)与酯交换前相比,酯交换反应后甘三酯的组成发生改变,甘油三酯骨架上的脂肪酸发生重排,导致甘三酯结构发生改变,低熔点甘三酯含量增加,高熔点甘三酯含量下降,饱和脂肪酸大部分转化为不饱和脂肪酸,营养结构更加健康。酯交换反应后的混合油脂,更适宜做人造奶油基料油。

