γ-氨基丁酸键合硅胶毛细管色谱柱填料的绿色制备及其分析性能研究
赵双丽,罗菲菲,祝璐琪,王清江,何品刚
(华东师范大学 化学与分子工程学院,上海 200241)
色谱柱是色谱分离的核心,对填充毛细管色谱柱来说,色谱填料直接影响其对分析物的选择性和分离效率。目前,色谱固定相大多以多孔二氧化硅为基质进行表面化学修饰制备而成[1],根据所键合官能团的不同具有不同的色谱分离机制,进而为分离复杂样品提供多种选择。在以往研究中,合成色谱固定相所用溶剂往往是易挥发、有毒的有机溶剂(如甲苯[2-4]、甲醇[5-6]、氯仿[7-8]和N,N-二甲基甲酰胺(DMF)[9-10]等),但近年来随着环境问题越来越受到人们的关注,亟待建立不涉及有毒有害溶剂的“绿色化学”合成技术[11-12]。
γ-氨基丁酸(GABA)是一种广泛存在于生物体内的活性物质[13],其结构中所含氨基、羧基等极性基团具有亲水作用;此外,GABA是一种两性物质,还具有离子交换作用。本文在不含任何有机溶剂的水相条件下,通过一步反应绿色制备了GABA修饰的硅胶固定相(Sil-GABA),并将其用于不同类型分析物的色谱分离,结果表明,Sil-GABA固定相具有多种色谱分离模式的作用机理:在富水模式下可分离硝基氯苯位置异构体和7种磺胺,亲水模式下可分离4种苯甲酸类化合物,反相模式下可分离硝基苯胺位置异构体。目前尚未见SiO2表面键合GABA的色谱固定相报道。
1 实验部分
1.1 材料、试剂与仪器

Trisep-2100加压毛细管电色谱(pCEC)仪器(上海通微分析技术有限公司),配有紫外检测器;2400 Ⅱ元素分析仪(美国Perkin Elmer公司);Nicolet NEXUS 670傅立叶变换红外光谱仪(美国Perkin Elmer公司);Milli-Q超纯水系统(美国Millipore公司);高压输液泵(北京莱伯秦科仪器股份有限公司)。
1.2 Sil-GABA固定相的制备
硅胶在使用前需经活化处理[14]:称取一定质量硅胶均匀分散于10%的稀盐酸中,置于圆底烧瓶中回流加热30 min;冷却至室温,过滤悬浮液,超纯水洗涤至流出液呈中性;将过滤后的硅胶于180 ℃真空干燥4 h。
Sil-GABA的制备过程见图1。首先通过碱性条件下的开环反应实现GABA与硅烷化试剂的键合,然后再修饰到硅胶表面。具体步骤如下:称取0.01 g的GABA溶于20 mL超纯水中,用Na2CO3溶液调至pH 10.6,再滴加22 μL的GPS,混合液于冰水浴下以230 r/min磁力搅拌2 h;再采用CH3COOH调节反应后的溶液至pH 6.0后转移至含有0.5 g活化硅胶的圆底烧瓶中,于100 ℃下回流2 h。最后,过滤反应悬浮液,用超纯水洗涤滤饼,并于70 ℃真空干燥6 h,即制得Sil-GABA固定相。
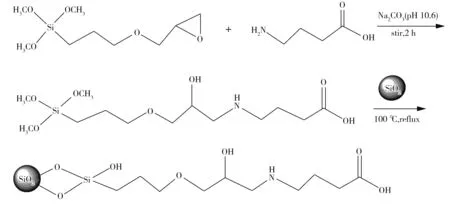
图1 Sil-GABA固定相的合成Fig.1 Synthesis of the Sil-GABA stationary phase
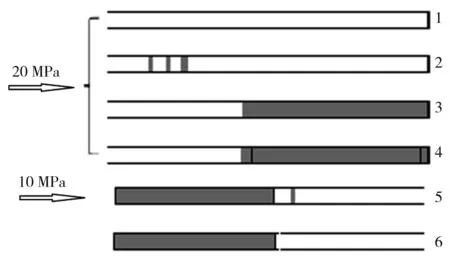
图2 Sil-GABA的填充示意图Fig.2 Schematic diagram of the Sil-GABA packing procedure1:preparation of a temporary frit;2,3:packing the capillary with the Sil-GABA;4:preparation of the permanent frits at both ends;5:elimination of the excess of packings;6:preparation of a detection window
1.3 毛细管柱的装填
截取50 cm石英毛细管,用1 mol/L NaOH处理0.5 h,再用超纯水洗涤至流出液呈中性;然后用0.1 mol/L HCl处理0.5 h,再用超纯水洗涤至流出液呈中性。将处理后的石英毛细管用于Sil-GABA固定相的装填(图2),毛细管一端吸取饱和硅酸钠溶液,于烧红的电炉丝上加热1~2 s,制得临时柱塞;另一端连接到装有固定相悬浮液(0.2 g Sil-GABA均匀分散于乙腈中)的不锈钢管中。以80%的甲醇为顶替液,在20 MPa的压力下将Sil-GABA填料填入毛细管中(为使填料更均匀致密,在整个装填过程中毛细管需置于超声浴中)。在距离临时柱塞约24 cm处,通过电炉丝加热Sil-GABA填料制得另一端柱塞,即永久柱塞(用同样的方法去除临时柱塞)。撤掉液相色谱泵的压力,取下毛细管,反向连接,在10 MPa的压力下去除多余的填料。最后,在靠近出口端柱塞处,通过去除毛细管外层涂料,制得1~2 mm左右的检测窗口。
1.4 色谱条件
实验所用石英毛细管色谱柱外径360 μm,内径100 μm,总长50 cm;Sil-GABA 固定相有效填充长度为24 cm;流动相所用溶剂为色谱纯的甲醇、乙腈;流动相流速0.02 mL/min;检测波长为254 nm;溶解样品所用溶剂均为甲醇、超纯水。

图3 硅胶和Sil-GABA的红外光谱图Fig.3 FT-IR spectra of silica and Sil-GABAa.SiO2,b.Sil-GABA
2 结果与讨论
2.1 固定相的表征

固定相中各元素含量的分析结果表明:活化SiO2中C含量为0.294%,H为0.784%,未检出N;而Sil-GABA中C含量为3.888%,H为1.116%,N为0.345%。与未修饰的SiO2相比,制备的固定相中C、H含量明显增加,且在其表面检出N元素,进一步表明已成功制备了Sil-GABA。由元素分析中N含量计算得GABA在SiO2表面的覆盖程度为0.87 μmol/m2。
2.2 Sil-GABA作用机理及色谱性能评价
2.2.1 富水模式色谱富水模式色谱流动相中水占有很高的比例(70%~100%),可减少有机溶剂的使用[15]。作为一种绿色色谱分析方法,富水模式色谱可替代亲水色谱用于一些极性物质的分离。本研究通过对硝基氯苯位置异构体和磺胺类物质的色谱分离,研究Sil-GABA固定相在富水模式下的分离特性。
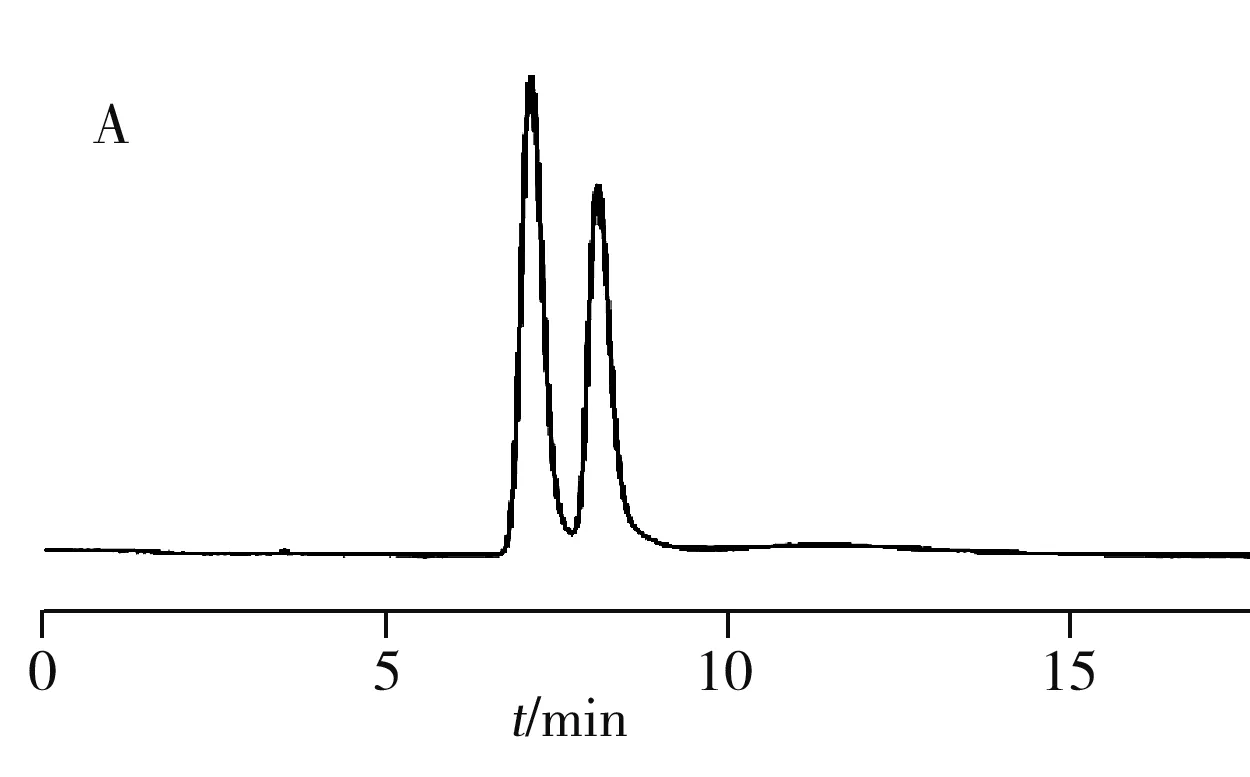
(1)硝基氯苯位置异构体的分离:硝基氯苯具有一定的极性,其位置异构体的分离色谱图见图4,流动相采用20 mmol/L乙酸铵水溶液-乙腈。结果显示,流动相中20 mmol/L乙酸铵水溶液与乙腈的体积比为80∶20时,异构体的保留时间相同,色谱峰重叠;当20 mmol/L乙酸铵的体积分数由80%增至90%时,流动相极性增强,保留时间增加;继续升高20 mmol/L乙酸铵水溶液的体积分数为100%时,邻、间、对硝基氯苯在25 min内可实现基线分离,保留因子分别为0.145、0.456、0.754,分离度分别为3.2、1.56。表明Sil-GABA固定相对硝基氯苯具有良好的选择性,在富水色谱模式下可用于硝基氯苯位置异构体的分离。
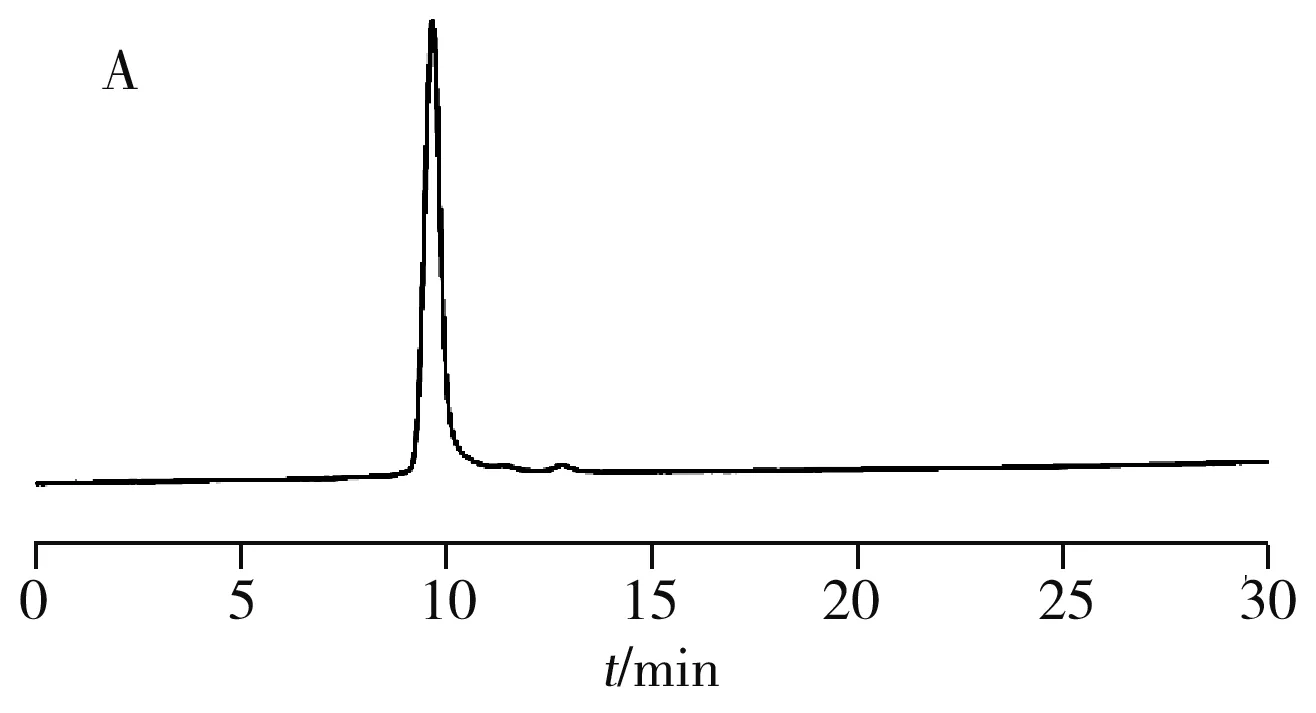
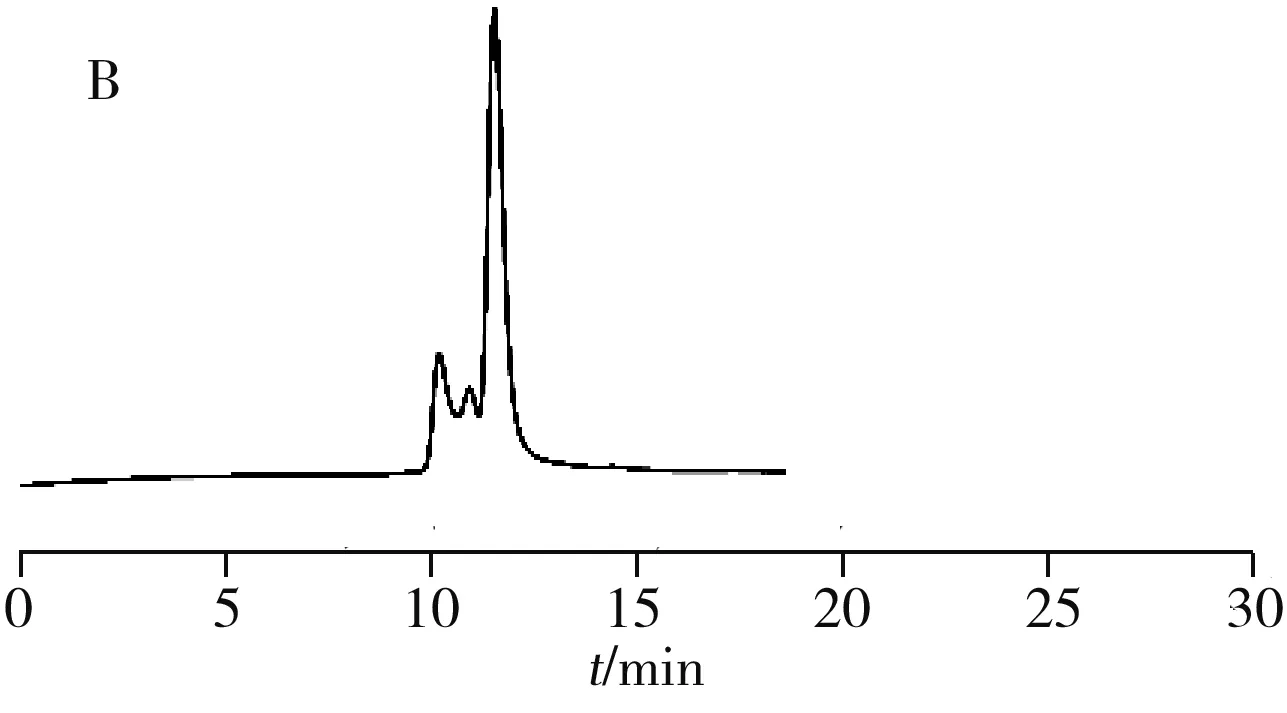
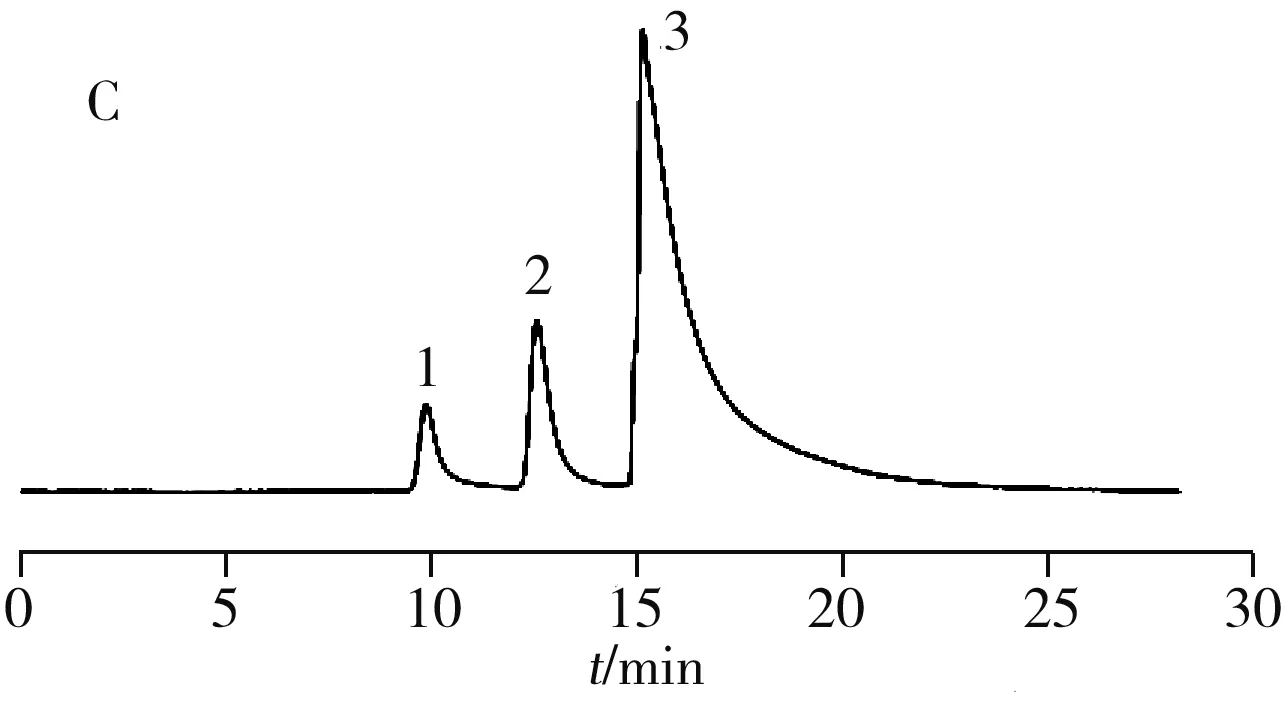
图4 硝基氯苯位置异构体的分离色谱图Fig.4 Chromatograms of nitrochlorobenzene isomersA,B,C:ammonium acetate-acetonitrile was 80∶20,90∶10,100∶0(by volume);1.m-nitrochlorobenzene,2.o-nitrochlorobenzene,3.p-nitrochlorobenzene

图5 7种磺胺的分离色谱图Fig.5 Chromatograms of seven sulfonamidesmobile phase:20 mmol/L ammonium acetate(pH 4.0);1.SG,2.SD,3.SM1,4.SM2,5.SMZ,6.SDM,7.SQ
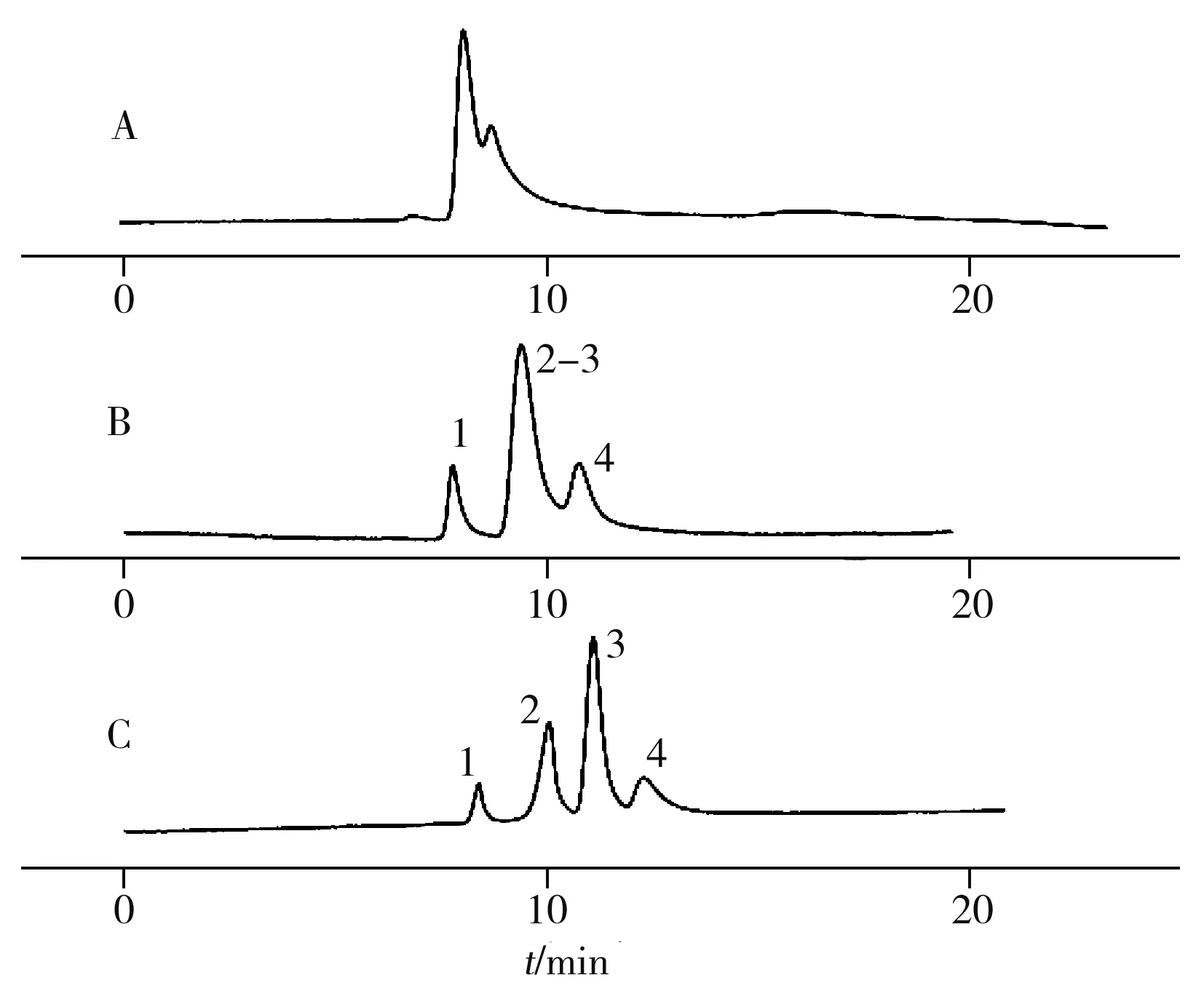
图6 4种苯甲酸类化合物的分离色谱图Fig.6 Chromatograms of four benzoic acid compoundsmobile phase:20 mmol/L ammonium acetate,A,B,C:water-acetonitrile was 40∶60,30∶70,20∶80(by volume);1.2,3-dihydroxybenzoic acid,2.benzoic acid,3.3,4-dihydroxybenzoic acid,4.4-hydroxybenzoic acid
(2)磺胺类药物的分离:以7种磺胺(SG、SD、SM1、SM2、SMZ、SDM、SQ)为分离对象,20 mmol/L乙酸铵水溶液为流动相探讨了在富水色谱模式下的分离条件。由于GABA是一种两性离子化合物,流动相pH值和浓度会影响分析物在固定相上的保留情况,因此实验考察了pH值分别为3.0、4.0、5.0、6.0、8.0时7种磺胺的保留情况。结果表明,随着pH值增大,SG的保留时间基本不变,但其余6种磺胺在Sil-GABA固定相上的保留时间都有所增加。这是因为GABA的等电点为7.19,随着流动相pH值的增加,越来越多的GABA会以负离子形式存在,固定相与磺胺的相互作用增强,造成保留时间延长。另外,乙酸铵的浓度也会改变溶剂的离子强度,进而影响分析物在固定相上的峰形和分离效率[16]。因此实验还考察了乙酸铵浓度分别为10、20、40、50、100 mmol/L时对磺胺保留的影响,结果发现随着乙酸铵浓度的增加,7种磺胺在Sil-GABA固定相上的保留减弱,这是因为溶液离子强度增加,缩短了保留时间。
在流动相为20 mmol/L乙酸铵(pH 4.0)的条件下,除SM2、SMZ外,其余5种磺胺都实现了良好的分离(图5)。
2.2.2 亲水模式色谱在高亲水性有机溶剂乙腈为流动相的条件下,考察了4-羟基苯甲酸、3,4-二羟基苯甲酸、2,3-二羟基苯甲酸、苯甲酸在Sil-GABA固定相上的保留特征(图6)。结果显示,随着流动相中乙腈含量的增加,上述化合物保留增强,分离度增大,与亲水模式色谱的保留机理一致。当乙腈体积分数增至80%时,4种苯甲酸类化合物实现了良好的分离,出峰顺序依次为2,3-二羟基苯甲酸(pKa=2.96)、苯甲酸(pKa=4.20)、3,4-二羟基苯甲酸(pKa=4.45)、4-羟基苯甲酸(pKa=4.57),与其pKa值由小到大的顺序一致。这是因为键合GABA后硅胶表面的羧基具有弱阳离子交换作用,离子交换是其完成色谱分离的主要机制。
2.2.3 反相模式色谱以甲醇-水为流动相,以硝基苯胺位置异构体为分离对象,探究Sil-GABA固定相的反相色谱模式,邻、间、对位硝基苯胺的色谱分离图见图7。流动相中甲醇体积分数为20%时,邻、对硝基苯胺的色谱峰重叠,当甲醇体积分数由20%降至10%时,从色谱图上可以观察到邻硝基苯胺的色谱峰;当甲醇体积分数降至5%时,各分析物的保留增强,3个异构体之间的分离度增加,可在20 min内实现分离,保留因子分别为0.966、1.228、1.448,分离度分别为2.15、1.60。由此可见,Sil-GABA具有反相色谱的保留特性。但色谱峰出峰顺序为间位(LgP=1.338)、对位(LgP=1.195)、邻位(LgP=1.669),与疏水性顺序不一致,表明Sil-GABA存在多种保留机理。
2.3 重复性试验
以磺胺类药物为分析物,考察了该色谱柱的重复性,实验结果见表1。结果显示,7种磺胺保留时间的日内和日间相对标准偏差(RSD)分别为0.42%~1.3%、0.49%~3.2%。在整个分析测试期间,重复进样色谱峰的峰形和分离效率均无明显变化,表明此毛细管填充柱具有良好的分析重现性和稳定性。

表1 磺胺的重复性试验Table 1 Repeatability test of seven sulfonamides
3 结 论
本文在水相溶剂中绿色制备了Sil-GABA色谱填料,采用红外光谱、元素分析对其结构进行了表征,发现该填料具有多种保留机理,可用于磺胺、硝基氯苯位置异构体、苯甲酸类化合物和硝基苯胺位置异构体的分离,且具有良好的稳定性和重现性。该Sil-GABA填料制备方法简单、绿色无毒,作为色谱填料在毛细管液相色谱中有潜在的应用价值。

