阿帕替尼联合奥沙利铂和替吉奥在局部晚期胃癌新辅助化疗中的应用效果
骆 杨,霍 亮,许家亮,欧 龙,胡 伟
(1.信阳市中心医院肿瘤外科,河南 信阳 464000;2.信阳市中心医院肿瘤内科,河南 信阳 464000;3.河南省信阳市中心医院药学部,河南 信阳 464000)
我国恶性肿瘤患者中,胃癌的发病率位居第2位,死亡率居第3位[1]。局部晚期胃癌是临床上常见的胃癌类型,通常可行根治性手术治疗。既往的研究[2]证实,对于T3~4、N+期的局部晚期胃癌,新辅助化疗是有益的,但在具体的药物选择、最佳周期数、安全性、评价模式和疗效等方面尚未达成共识与标准。奥沙利铂和替吉奥方案已经在胃癌的新辅助及术后化疗中得以广泛应用,而阿帕替尼作为新型小分子血管内皮生长因子受体抑制剂,已被广泛应用于晚期胃癌的治疗中[3]。上述方案的联合应用也已经在晚期胃癌的辅助化疗中有了一定的应用研究[4]。本文初步研究了阿帕替尼联合奥沙利铂和替吉奥方案在局部晚期胃癌新辅助化疗中的临床疗效及安全性,现报道如下。
1 资料与方法
1.1 一般资料选取2017年1月至2018年8月我院收治的局部晚期胃癌患者35例,其中男21例,女14例;年龄38~72岁,中位年龄57岁。所有患者均经胃镜下留取活组织标本明确病理诊断为腺癌,术后大体标本行常规免疫组化检查。病理类型:高分化腺癌7例,中分化腺癌3例,中-低分化腺癌11例,低分化腺癌7例,黏液腺癌5例,印戒细胞癌2例。免疫组化检查示表皮生长因子受体均为阳性。B超、CT主要确定腹腔淋巴结有无转移和病灶浸润程度及重要脏器转移情况,进而对肿瘤进行分期。TNM分期:Ⅲ期28例,Ⅳa期7例。入选条件:经病理诊断;KPS评分≥60分,预计生存时间≥3个月,有可监测指标评疗效;血常规、肝功能、肾功能、心电图正常;既往未接受过化疗。常规检测治疗前后癌胚抗原、糖类抗原(CA)19-9和CA72-4。所有患者均签署化疗知情同意书,且经过我院伦理委员会批准。34例患者进行了手术治疗,余1例患者拒绝手术治疗。
1.2 化疗方案入组患者采用阿帕替尼联合奥沙利铂和替吉奥方案治疗。奥沙利铂(商品名:艾恒,江苏连云港恒瑞医药股份有限公司,批准文号:国药准字H20000337,规格:50 mg、100 mg)130 mg·m-2静脉滴注,化疗第1天使用,21d为1周期。替吉奥(齐鲁制药有限公司,批准文号:国药准字H20100150,规格:20 mg、25 mg)的使用剂量取决于体表面积(<1.25 m2者40 mg,2次/d;1.25~1.50 m2者50 mg,2次/d;>1.50 m2者60 mg,2次/d),早餐和晚餐后口服,化疗第1~14天应用。阿帕替尼(江苏恒瑞医药股份有限公司,批准文号:国药准字H20140103,规格:250 mg)500 mg·d-1,餐后0.5 h口服,自化疗第1天起,4周为1周期。2周期后进行近期疗效评价。每6周及新辅助化疗结束后2周复查腹部增强CT以评价疗效。符合手术切除要求时即进行手术。入组患者均行2~4周期新辅助化疗。
1.3 手术治疗入组患者化疗结束后2~3周由同一组医师行常规开腹手术或腹腔镜探查手术,根据术中情况决定手术方案。首选D2根治性切除,若局部癌灶无法根治性切除则选择姑息性切除和(或)消化道短路手术以达到减轻肿瘤负荷和改善患者临床症状的目的。
1.4 疗效及不良反应近期疗效参照实体瘤疗效评价标准(RECIST)1.1[5],分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)以及疾病进展(PD)。以CR+PR计算客观缓解率,以CR+PR+SD计算疾病控制率。化疗不良反应有骨髓抑制、胃肠道反应、乏力、口腔溃疡、高血压、蛋白尿、手足综合征等,参照WHO抗肿瘤药物不良反应评价标准分为0~Ⅳ度。
1.5 统计学处理采用SPSS 19.0进行数据分析,计数资料用百分数表示,比较用χ2检验,检验水准α=0.05。
2 结果
2.1 阿帕替尼联合奥沙利铂和替吉奥方案的近期疗效及手术情况入组35例患者中,CR 0例,PR 19例,SD 10例,PD 6例,客观缓解率为54.3%,疾病控制率为82.9%。术后病理分期:Ⅱa期6例,Ⅱb期4例,Ⅲ期22例,Ⅳa期3例。新辅助化疗后临床降期18例(51.4%)。除1例拒绝手术外,2例无法切除肿瘤仅行胃空肠吻合,3例因腹腔种植性转移或其他情况未达到D2根治性切除,手术切除率94.1%(32/34),D2根治性切除率85.3%(29/34)。入组患者无手术后死亡病例,手术后近期并发症主要有切口愈合不良3例、肺部感染2例、腹腔感染1例。
2.2 阿帕替尼联合奥沙利铂和替吉奥方案的不良反应35例患者均可评价化疗不良反应,无化疗相关死亡。常见的化疗不良反应有骨髓抑制、胃肠道反应、周围神经毒性、口腔溃疡、乏力等。Ⅲ、Ⅳ度骨髓抑制发生率为11.4%、Ⅲ、Ⅳ度胃肠道反应8.6%、Ⅲ、Ⅳ度口腔溃疡5.7%,Ⅲ、Ⅳ度乏力8.6%,其余不良反应均为Ⅰ、Ⅱ度,患者可耐受。见表1。
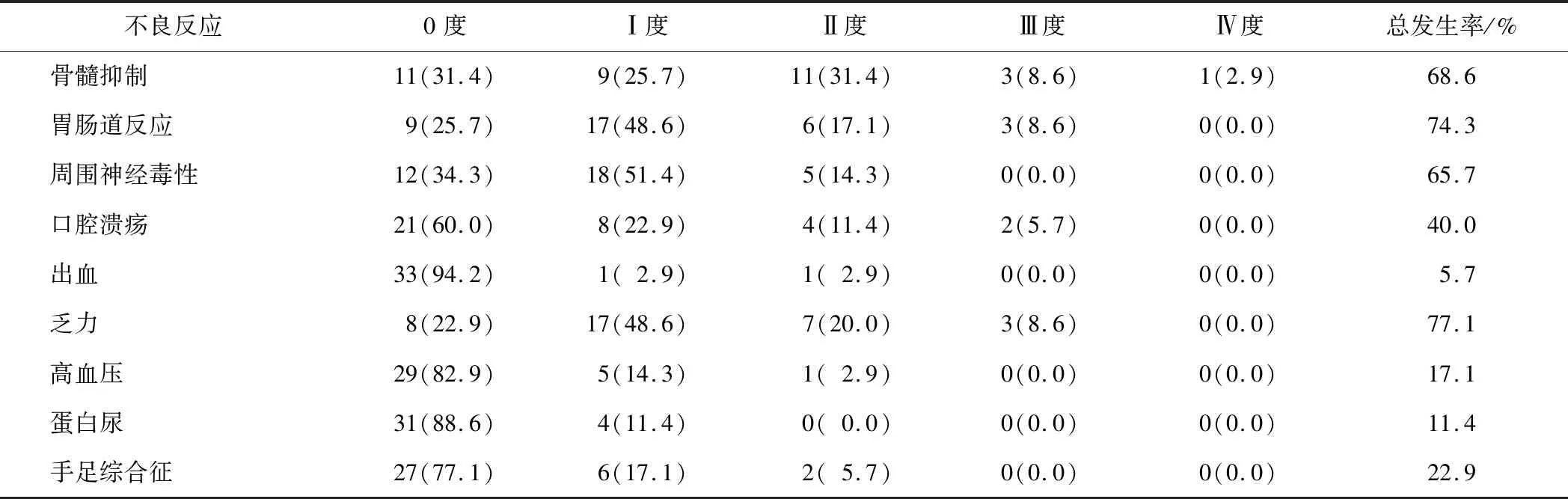
表1 阿帕替尼联合奥沙利铂和替吉奥方案的不良反应 n(%)
3 讨论
局部晚期胃癌定义范围较广,肿瘤异质性较强,目前其手术、放疗和化疗最佳个体化综合治疗模式仍然存在较大差异,是临床上较为棘手的难题。对于局部晚期胃癌的治疗,目前已经达成2个共识:单纯手术无法根治,姑息切除好于未做手术;2个目标:提高根治率,提高切除率,即以提高R0切除率,降低复发与转移为治疗的最终目的。新辅助化疗理念的基本原理是术前使用化疗药物后使肿瘤体积缩小、降期并杀灭休眠中的肿瘤细胞,预期可使手术切除更彻底,降低肿瘤复发率,延长患者生存时间。美国NCCN指南已经推荐胃癌新辅助化疗作为Ⅰ级证据。我国最新制定的胃癌诊疗规范亦将无远处转移的局部晚期胃癌列为新辅助化疗的适应证。
替吉奥是由替加氟、吉美嘧啶和奥替拉西钾构成的复合制剂,是新一代氟尿嘧啶类口服药物[6]。奥沙利铂作为第3代铂类药物,与氟尿嘧啶具有协同作用,且无肾毒性、耳毒性等不良反应,应用时不需水化[7]。目前,临床上认为奥沙利铂和替吉奥方案具有高效、低毒、耐受性好等优点,已成为进展期胃癌患者辅助化疗的一线方案和化疗的研究热点[8-9]。阿帕替尼作为抗肿瘤血管生成的新药,其本身是一种血管内皮生长因子受体2的酪氨酸激酶抑制剂[10],通过竞争性结合血管内皮生长因子受体2的酪氨酸ATP结合位点阻断血管内皮生长因子的信号转导,达到减少肿瘤血管生成的目的[11]。此外,阿帕替尼对血小板生成因子受体β和c-kit存在抑制效应,本身也具有抗肿瘤作用[12]。已在大多数肿瘤中发现血管内皮生长因子过表达,研究认为,血管内皮生长因子与肿瘤生长、复发、转移有关[13]。阿帕替尼使用后安全性较高,主要原因是其代谢很快,使用96 h后体内只存在23.3%,大部分通过肠道排出体外,小部分以尿液形式排出[14]。目前,阿帕替尼已获国家批准用于晚期胃癌患者的三线及三线以上的治疗[15]。
本研究采用阿帕替尼联合奥沙利铂和替吉奥方案对35例局部晚期胃癌患者进行新辅助化疗,结果显示,客观缓解率为54.3%,疾病控制率为82.9%,远高于文献报道的未进行新辅助化疗的患者[16]。化疗的不良反应主要为主要为骨髓抑制、胃肠道反应、周围神经毒性、口腔溃疡、乏力等。骨髓抑制以白细胞减少为主,胃肠道反应主要表现为恶心、呕吐、腹泻,多为Ⅰ、Ⅱ度,可耐受。周围神经毒性、口腔溃疡等也较轻微,停药后可缓解,无明显的肝、肾功能损害。上述不良反应发生率并未超过文献报道的单纯应用奥沙利铂和替吉奥方案者。出血、乏力、高血压、蛋白尿、手足综合征等的发生率较文献报道的单纯应用奥沙利铂和替吉奥方案者高,但由于多为Ⅰ、Ⅱ度,较容易控制,并未影响到其临床使用。经过新辅助化疗,有18例患者达到肿瘤降期,治疗后降期率为51.4%,D2根治性切除率为85.3%(29/34),手术切除率为94.1%(32/34),高于文献报道的进展期胃癌60%~70%的手术切除率。本研究中没有患者在接受新辅助化疗后达到CR,可能是入组患者分期均较晚的缘故。国外一项荟萃分析研究[17]发现,经过新辅助化疗后达到CR的进展期胃癌患者3 a和5 a总生存率分别为96%和85%,提示今后的研究可以适当入组分期更早的患者。
综上所述,局部晚期胃癌患者应用阿帕替尼联合奥沙利铂和替吉奥方案进行新辅助化疗,能明显降低肿瘤临床分期,提高手术切除率和D2根治切除率,且不良反应与单纯奥沙利铂和替吉奥方案相近,患者可耐受,值得临床上推广应用。

