胫骨骨折手术前后关节内炎症因子的变化分析
陈荣 孙志波 李相伟 禹志宏 刘幸卉
创伤性关节炎 ( posttraumatic osteoarthritis,PTOA )是关节创伤后骨性关节炎 ( osteoarthritis,OA ),以软骨破坏退变、软骨下骨硬化、关节周围骨质增生为主要病理改变,临床上以反复疼痛及关节功能障碍为主要表现。与老年性原发性 OA 不同的是 PTOA 有明显关节外伤病史,以关节内骨折、前交叉韧带撕裂、半月板损伤为主,发病年龄以中青年居多 ( 18~44 岁 ),严重影响患者工作和生活质量,且加重国家医疗负担[1]。
近年来,虽然骨折复位固定技术不断改进及加强对软骨损伤的重视,但关节内骨折导致 PTOA 的发病率依然高达 75% ( 胫骨远端 ),胫骨平台骨折为 23%~44%[2]。急性胫骨平台骨折关节内有明显的炎症反应,与未受伤膝关节相比,白细胞介素-1β( interleukin-1β,IL-1β )、IL-6、IL-8、IL-10、白细胞介素-1 受体拮抗剂 ( interleukin-1 receptor antagonist,IL-1ra ) 和单核细胞趋化蛋白-1 ( monocyte chemotactic protein-1,MCP-1 ) 高表达[3]。OA 患者软骨内 IL-1β、TNF-α 高表达,而 IL-1β 抑制蛋白聚糖及 II 型胶原蛋白的合成,促进软骨退变[4-6]。手术治疗是恢复关节面平整及关节稳定的关键,但术后关节内炎症的变化情况及术后炎症增高是否表明远期创伤性关节炎发生的可能性较大尚无研究。
Punzi 等[7]在综述中指出关节内炎症在 PTOA 发生发展过程中起关键作用,但如何预测或评估 PTOA风险性尚无法确定。PTOA 有明确起始时间,即关节创伤后当时损伤及关节内微环境变化可能导致远期 PTOA,若早期预测 PTOA 发生而进行相关性干预,可能降低 PTOA 发病率。因此本研究通过分析胫骨骨折不同时间点手术前后关节内炎症变化,为减少关节内炎症反应提供手术时间依据,为创伤性关节炎的研究奠定基础。
资料与方法
一、纳入与排除标准
1. 纳入标准:( 1 ) X 线片或 CT 检查为单侧胫骨平台骨折者;( 2 ) 行手术治疗及关节腔穿刺者。
2. 排除标准:( 1 ) 严重类风湿性关节炎等自身免疫性疾病、骨结核、骨肿瘤者;( 2 ) 年龄>65 岁者;( 3 ) 术后 4 天白细胞计数异常者;( 4 ) 膝关节骨性关节炎,定期使用非甾体类抗炎药者;( 5 ) 开放性骨折,关节面粉碎严重难以恢复平整,继发骨筋膜室综合征者;( 6 ) 前后交叉韧带损伤需重建手术,半叶板损伤需切除或二次手术,对侧膝关节损伤者。
二、一般资料
本组 46 例,其中 2 例拒绝术后关节腔穿刺( Schatzker I、IV 型 ),1 例前交叉韧带需二次重建 ( Schatzker VI 型 ),2 例术中行半叶板次全切( Schatzker II、V 型 )。共纳入 41 例。A 组:36 例,受伤至手术时间平均 5.2 ( 3~7 ) 天,手术时间平均149.9 ( 90~219 ) min;B 组:5 例,受伤至手术时间平均 12.6 ( 12~14 ) 天,手术时间平均 198 ( 150~230 ) min。骨折按 Schatzker 分型:I 型 9 例,II 型7 例,III 型 6 例,IV 型 4 例,V 型 7 例,VI 型8 例;按受伤至手术时间不同分组,A 组:36 例,受伤至手术时间为 3~7 天,平均 5.2 天;B 组:5 例,受伤至手术时间为 12~14 天,平均 12.6 天。
三、治疗方法
入院后完善相关检查,术前准备充分后行手术治疗。根据术前 X 线片、CT 等影像学资料评估关节骨折情况及骨折 Schatzker 分型,明确手术入路、钢板放置位置及数量。关节囊切开前注射器抽吸关节腔内积液,术中生理盐水冲洗关节腔,术中 C 型臂透视下恢复关节面平整,关节面塌陷需常规植入自体髂骨或人工异体骨压实,Schatzker I~IV 型采用单钢板,Schatzker V、VI 型采用双钢板固定,此外根据后柱骨折移位稳定情况,进行相关固定。术后引流管 2 天拔除,术前 30 min 及手术时间超过 3 h常规使用抗生素,术后继续使用 3 天,第 4 天关节穿刺抽取积液,患者平卧位,以髌骨内上缘为穿刺点,助手协助挤压膝关节,测量并记录抽出的所有关节腔积液。
四、关节腔积液 ELISA 检测
收集关节腔积液后立即离心 15 min,转速为3000 rpm,收集上清液并分装,于 -80 ℃ 保存。根据 ELISA 检测试剂盒 ( 沛瑜生物科技有限公司 ) 步骤检测 IL-1β、TNF-α、IL-6、抗酒石酸性磷酸酶( tartrate-resistant acid phosphatase,TRAP ) 的表达情况。用 Excel 表作标准曲线,以吸光值作为纵坐标,以浓度作为横坐标。根据样品的吸光值在坐标上找出对应的浓度。实验重复 3 次,取均值。
五、统计学处理
结 果
一、手术前后 X 线片及关节腔积液量
术前总共 46 例入选,A 组 2 例拒绝术后关节腔穿刺 ( Schatzker I、IV 型 ),B 组 1 例前交叉韧带需二次重建 ( Schatzker VI 型 ),B 组 2 例术中行半叶板次全切 ( Schatzker II、V 型 )。A 组:36 例,受伤至手术时间 3~7 天,平均 5.2 天,手术时间 90~219 min,平均 149.9 min;B 组:5 例,受伤至手术时间 12~14 天,平均 12.6 天,手术时间 150~230 min,平均 198 min。术前 X 线片见 Schatzker III及 IV 型骨折移位较轻,而 Schatzker II 及 VI 型较严重。术后 2 天,白细胞计数>10×109/ L 有 11 例( Schatzker VI 型 4 例,Schatzker II、IV 型各 3 例,Schatzker V 型 1 例 ) ,术后 4 天白细胞恢复正常,所有患者均无伤口感染。术前关节腔积液粘稠度高,呈暗红色,术后大多数为红色水样积液,个别为暗红色,粘稠度低,A 组术后关节腔积液量为 4~16 ml,平均 8.33 ml;B 组为 5~15 ml,平均 8.4 ml( 图 1~6 )。

图 1 患者,女,43 岁,车祸致右侧胫骨平台 Schatzker I 型骨折 a:术前正位 X 线片;b:术后正位 X 线片图 2 患者,男,40 岁,1 m 高处摔伤致右侧胫骨平台 Schatzker II 型骨折 a:术前正位 X 线片;b:术后正位 X 线片Fig.1 Female, 43-year-old, Schatzker I fracture of the right tibial plateau caused by a traffic accident. a: Pre-operative X-ray film; b: Post-operative X-ray filmFig.2 Male, 40-year-old, Schatzker II fracture of the right tibial plateau caused by a high fall of 1m a: Pre-operative X-ray film; b: Post-operative X-ray film
二、手术前不同 Schatzker 分型骨折关节腔积液中 IL-1β、TNF-α、TRAP、IL-6 的表达情况
Schatzker III 型骨折关节腔积液中 IL-1β 表达较其它 4 型都低 (P=0.001,P=0.000,P=0.001,P=0.000 ),与 Schatzker IV 型胫骨平台骨折中比较,差异无统计学意义 (P=0.607 );IL-1β 在 Schatzker II 及VI 型骨折关节腔积液中的表达高于 Schatzker III 及IV 型,差异有统计学意义 (P=0.001,P=0.003 )。Schatzker III 型骨折关节腔积液中 TRAP 的表达较其它 4 型都低 (P=0.003,P=0.042,P=0.017,P=0.032 ),与 Schatzker IV 型骨折相比,差异无统计学意义 (P=0.173 )。Schatzker III 型骨折关节腔积液中 IL-6 的表达较其它 5 型都低 (P=0.000,P=0.000,P=0.001,P=0.000,P=0.000 );IL-6 在 Schatzker II 型骨折关节腔积液中的表达高于 Schatzker I、III、IV 及 V 型,差异有统计学意义 (P=0.008,P=0.000,P=0.038,P=0.015 );IL-6 在 Schatzker VI 型骨折关节腔积液中的表达高于 Schatzker I、III 及 V 型,差异有统计学意义 (P=0.027,P=0.000,P=0.046 )。然而 TNF-α 在各分型中的表达,差异无统计学意义 (P=0.134 ) ( 图 7 )。

图 3 患者,男,39 岁,1 m 高处摔伤致右侧胫骨平台 Schatzker III 型骨折 a:术前正位 X 线片;b:术后正位 X 线片图 4 患者,男,37 岁,车祸致左侧胫骨平台 Schatzker IV 型骨折 a:术前正位 X 线片;b:术后正位 X 线片图 5 患者,女,45 岁,车祸致右侧胫骨平台 Schatzker V 型骨折 a:术前正位 X 线片;b:术后正位 X 线片图 6 患者,男,42 岁,高处坠落致左侧胫骨平台 Schatzker VI 型骨折 a:术前正位 X 线片;b:术后正位 X 线片Fig.3 Male, 39-year-old, Schatzker III fracture of the right tibial plateau caused by a high fall of more than 1m while working a: Pre-operative X-ray film; b: Post-operative X-rayfilmFig.4 Male, 37-year-old, Schatzker IV fracture of the left tibial plateau caused by a traffic accident a: Pre-operative X-ray film; b: Post-operative X-ray filmFig.5 Female, 45-year-old, Schatzker V fracture of the right tibial plateau caused by a traffic accident a: Pre-operative X-ray film; b: Postoperative X-ray filmFig.6 Male, 42-year-old, Schatzker VI fracture of the left tibial plateau caused by a high fall a: Pre-operative X-ray film; b: Post-operative X-ray film
三、手术前后关节腔积液中 IL-1β、TNF-α、TRAP、IL-6 的表达情况
A 组和 B 组术后关节腔内 IL-6 的表达量均较术前增高,A 组术后关节腔内 IL-1β、TNF-α、TRAP的表达水平较术前降低,而 B 组术后反而增高( 表 1~2 )。

表 1 A 组手术前后关节腔积液中 IL-1β、TNF-α、TRAP、IL-6的表达情况Tab.1 Pre- and post-operative expressions of IL-1β, TNF-α, TRAP and IL-6 in the articular effusion of Group A
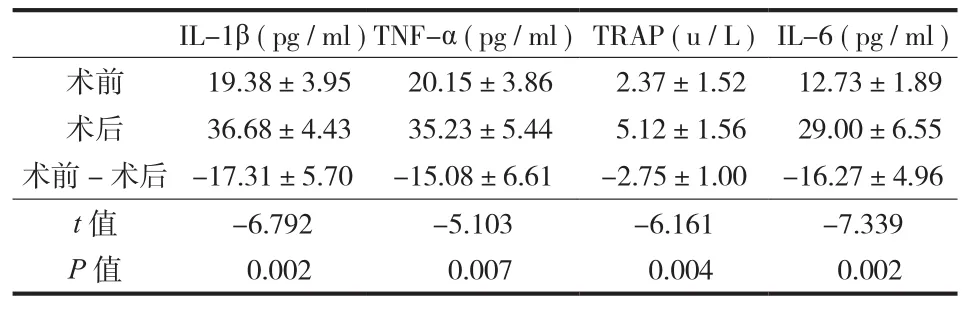
表 2 B 组手术前后关节腔积液中 IL-1β、TNF-α、TRAP、IL-6的表达情况Tab.2 Pre- and post-operative expressions of IL-1β, TNF-α, TRAP and IL-6 in the articular effusion of Group B

图 7 不同 Schatzker 分型术前关节腔积液中 IL-1β、TNF-α、TRAP、IL-6 的表达情况 ( 注:*#与其它组相比,差异有统计学意义,P < 0.05 )Fig.7 Expressions of IL-1β, TNF-α, TRAP and IL-6 in the articular effusion before operation in different Schatzker types ( Notice: *#Compared with other groups, P < 0.05 )
讨 论
炎症在 OA 疾病病理发展过程中起关键性作用,促炎症因子加剧软骨退变、加重滑膜炎及关节疼痛[4-5,8]。PTOA 是有明确起始时间及创伤因素的OA,Lieberthal 等[9]认为关节内炎症在其疾病发生发展过程中起关键作用。关节内骨折导致创伤性关节炎是多因素引起的,最主要包括两个方面:一方面是关节软骨急性损伤 ( 包括暴力损伤及炎症损伤 ),另一方面是由于关节面不平整、关节不稳及关节力线不良引起的慢性关节超负荷[2]。Haller 等[3]对胫骨平台 Schatzker 6 种分型根据受伤能量分为低能量组( Schatzker I、II、III 型 ) 和高能量组 ( Schatzker IV、V、VI 型 ),发现低能量组与高能量组间关节内炎症无明显差异。本课题研究发现关节内炎症高表达是Schatzker II 和 VI 型,而低表达是 Schatzker III 和 IV型,这可能与关节面软骨损伤情况及髓腔内容物渗入关节腔加重关节内炎症有关。Lewis 等[10]通过小鼠膝关节内骨折研究发现严重关节面损伤将加重滑膜炎症。有学者利用兔膝关节 PTOA 模型发现关节内非负重区钻孔可引起关节内积血及髓腔内容物渗出,促进滑膜炎症发展,髓腔渗出某些成分可引起机体免疫反应,进一步损伤软骨,最终导致 PTOA[11]。
无论是 OA[8]还是急性关节损伤[12],关节腔积液中炎性因子增高,尤其是 IL-1β、TNF-α 通过抑制软骨细胞外基质形成或促进其降解导致软骨退变[5-6]。Sward 等[12]收集膝关节损伤后 0~23 天不同时间点关节腔积液,检测发现伤后 1 天炎性因子如IL-1β、TNF-α、IL-6 等达到高峰,后续逐渐下降。笔者在后续研究发现合并有软骨骨折的膝关节急性损伤关节腔积液 TNF-α 表达较高[13]。受伤后 7 天以内 ( A 组 ) 手术的大多数患者术后 IL-1β、TNF-α 较术前表达水平降低,除外个别患者表达增高,回顾性分析发现这些患者复位固定后术中发现关节软骨面部分缺损或者关节面骨折缝隙较大,此外,受伤后 12 天以上 ( B 组 ) 行手术治疗患者术后关节腔内炎性因子 IL-1β、TNF-α 表达较术前增高,可能是由于手术复位困难创伤增大或复位不理想。创伤后疼痛是关节功能康复锻炼的最大障碍,而关节内炎症增高直接或间接导致疼痛,例如 IL-1β 通过增加环氧化酶-2 ( cyclooxygenase-2,COX-2 ) 及前列腺E 合酶 1 ( prostate E synthase 1,mPGES-1 ) 合成间接导致疼痛[14]或直接作用于疼痛感受器产生疼痛过敏[15]。因此关节内 IL-1β、TNF-α 增高不仅促进软骨退变导致关节炎作用,而且增加患者疼痛,影响关节功能恢复,对于术后关节内 IL-1β、TNF-α 表达能否作为创伤性关节炎高风险人群筛查指标仍需进一步研究。
IL-6 由巨噬细胞或成纤维细胞产生,在免疫调节、炎症甚至肿瘤发生中具有多重和本质的功能,是许多慢性炎症或自身免疫性疾病发展的关键因素;它可促进炎症相关的 B 细胞和 Th17 细胞的分化以及急性期蛋白的合成,与 IL-1 共同诱导金属蛋白酶 ( metalloproteinases,MMPs ) 的产生,降解软骨细胞外基质,此外诱导破骨细胞 ( osteoclast,OC ) 分化,造成关节骨质损伤[16-18]。Hwang 等[19]研究发现IL-6 和 IL-8 分泌增高可通过促进破骨细胞活化导致骨吸收。本研究发现术后所有患者关节内 IL-6 表达较术前增高,这可能与手术应激再次创伤有关,虽然 IL-6 目前认为具有抗炎及促炎双向作用,但在关节炎症方面研究侧重引起关节退变等作用。Haller等[3]对平均受伤 9.5 ( 3~21 ) 天胫骨平台骨折患者研究发现,关节内 IL-6 表达较未受伤膝关节仍明显增高,认为其在关节炎症反应中作用时间长。Adams等[20]对踝关节骨折 6 个月患者研究发现,关节内滑膜积液 IL-6、IL-8 等仍高表达,并提出针对这些因子治疗可能预防 PTOA。OC 来源于骨髓中造血干细胞、巨噬细胞等,活化的 OC 在酸性环境下促进骨内无机矿物质丢失,骨基质内的胶原纤维裸露,有利于各种组织蛋白酶充分接触骨外基质,导致骨质吸收疏松。IL-1β、TNF-α、IL-6 等炎性因子通过影响核因子 κB 受体活化因子配体 ( receptor activator of nuclear factor-κB ligand,RANKL ) 或直接作用于 OC前体细胞,促进 OC 增殖活化及增强其功能[21]。关节内骨折后关节腔内髓腔内渗出物中 OC 前体细胞及渗出的巨噬细胞将是破骨细胞活化的来源,而活化的 OC 可通过骨折缝隙进入骨内,破环骨质再生与吸收之间平衡,从而导致骨或软骨退变。TRAP是 OC 及其前体细胞的细胞标志物之一,TRAP 阳性表达的多核细胞具有破骨细胞功能[22]。本研究发现术后关节内 TRAP 表达较术前降低,这可能与手术恢复骨折完整性减少髓腔内容物渗出及关节内积血有关;而受伤后 12 天以上 ( B 组 ) 术后 TRAP 升高,可能是由关节内增高的炎性因子所活化或者是骨折复位不理想仍有较多髓腔内容物渗入关节腔所致。Bertuglia 等[23]研究认为钙化软骨微裂缝及退变将通过软骨 RANKL 促进 OC 聚集,而 OC 分泌组织蛋白酶 K 降解关节软骨,促进软骨退变。
综上所述,提示受伤后 7 天内 ( A 组 ) 手术,术后关节内炎症较术前降低,因为手术恢复骨折完整性,清除关节腔渗出的髓腔内容物及积血,减少后续髓腔内容物渗出及关节内积血,从而降低关节内炎症,但是受伤后 12 天以上 ( B 组 ) 手术将导致关节再次发生炎症反应。但是本研究也存在一些不足,如样本量较小,仍需增加其它因子检测如 MCP-1、IL-1RA,术后炎症增高的患者后续疼痛、功能情况以及是否发展为创伤性关节炎尚需跟踪随访。

