NFE2L3在直肠癌中的表达及预后意义
赛 恺,余昌俊
直肠癌(rectal cancer, RC)是常见的恶性消化道肿瘤,当前根治性手术仍然是其主要的治疗方法,但仍有40%~50%的患者因术后复发或转移而死亡[1]。寻找预测预后的有效生物学指标是当下RC诊疗的研究热点。转录因子(nuclear factor-erythroid 2,NF-E2)相关因子3(NF-E2-related factor 3,NFE2L3,又称Nrf3)是NF-E2家族的第三个家族成员,主要的生物学作用是诱导抗氧化作用基因的表达[2]。近期有研究表明[3-5],NFE2L3在血液系统、乳腺癌等多种恶性肿瘤中呈显著高表达,且与患者预后有着密切关系,但NFE2L3在RC中的表达及预后意义目前仍未见明确报道。该研究利用免疫组化验证结合生物信息学预测的方法探讨NFE2L3在RC中的表达水平及其与临床预后指标的相关性。
1 材料与方法
1.1 生物信息学预测选择癌症相关数据库(gene expression profiling interactive analysis,GEPIA)[6]和Oncomine[7]进行生物信息学预测,具体实施步骤如下:输入基因名称“NFE2L3”和癌症类型中选择“直肠腺癌”检索分析NFE2L3基因mRNA的相对表达水平,按其表达水平高低降序排列,排名前50%定义为NFE2L3高表达(46例),余下定义为NFE2L3低表达(46例)。运用Kaplan-Meier法绘制“NFE2L3基因表达水平-患者的总生存期(overall survival,OS)关联曲线。
1.2 RC标本及患者相关临床信息回顾性收集2008年4月~2016年12月在安徽医科大学第一附属医院普外科的RC患者癌、配对癌旁组织石蜡标本66对,术后病理均证实直肠腺癌。患者相关的临床信息见表2。本研究已经安徽医科大学伦理委员会审批,所有患者已签署知情同意书。
1.3 免疫组化及结果判读相关标本应用链霉菌抗生物素蛋白-过氧化物酶连接法(streptavidin-perosidade,SP)对进行检测。一抗为NFE2L3兔多克隆抗体(货号:HPA055889)购自美国Sigma公司,工作浓度为1∶200。染色结果:利用盲法测定,两名病理医师对每一张切片进行独立判断,参照此前已报道的判读方法[8],根据染色阳性细胞数(percentage of positive cells,PP)乘以染色强度(staining intensity,SI)的百分比计算免疫反应性评分(immunoreactive score,IRS),评分标准为:SI(0~3分):0为阴性,1为弱阳性,2为中度阳性,3为强阳性;PP(0~4分):0为阴性,1为1%~25%,2为26%~50%,3为51%~75%,4为76%~100%。结合IRS评分范围为0 ~12分,若IRS> 4分,定义为NFE2L3高表达;若IRS≤4分,评为NFE2L3低表达。
1.4 统计学处理采用SPSS19.0软件进行统计分析。RC与正常对照组之间阳性表达率的比较采用χ2检验。Kaplan-Meier法(log-rank test)进行单因素生存分析,而后将在单因素生存分析有意义的因素代入进行Cox多因素生存分析。P<0.05为差异有统计学意义。
2 结果
2.1 NFE2L3在RC中呈显著高表达GEPIA数据库中共检索到含有NFE2L3基因表达信息的RC 92例,正常对照318例见图1A;其中共有5项关于“直肠癌vs正常对照组”的研究在Oncomine数据库中检索到,该研究涉及到有NFE2L3基因表达水平的信息见图1B,结果均显示:与正常对照组比较,NFE2L3基因mRNA在RC中呈现显著高表达,差异有统计学意义(P均<0.05)。经免疫组化SP法进一步验证上述结果显示,NFE2L3蛋白主要表达于RC细胞核中,在RC中表达呈现高表达(66.7%)显著低于配对癌旁正常组织(15.2%),见图2,差异有统计学意义(P<0.001),见表1。此蛋白表达结果与利用癌症相关数据库预测的mRNA表达结果相一致。
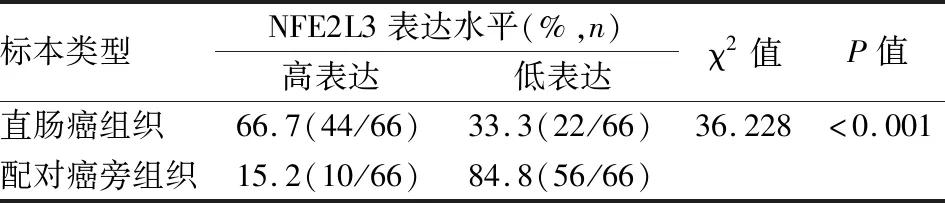
表1 NFE2L3在RC及配对癌旁组织中的蛋白表达水平
2.2 NFE2L3表达与RC患者临床病理参数的关系随后,对RC中NFE2L3差异表达水平与患者的各项临床病理参数的关系进行检测,见表2。 NFE2L3的差异表达水平仅与有无脉管侵犯有关,差异有统计学意义(P=0.013),而与患者性别、年龄、有无淋巴结侵犯、组织学分级、肿瘤大小、TNM分期及浸润深度无关。
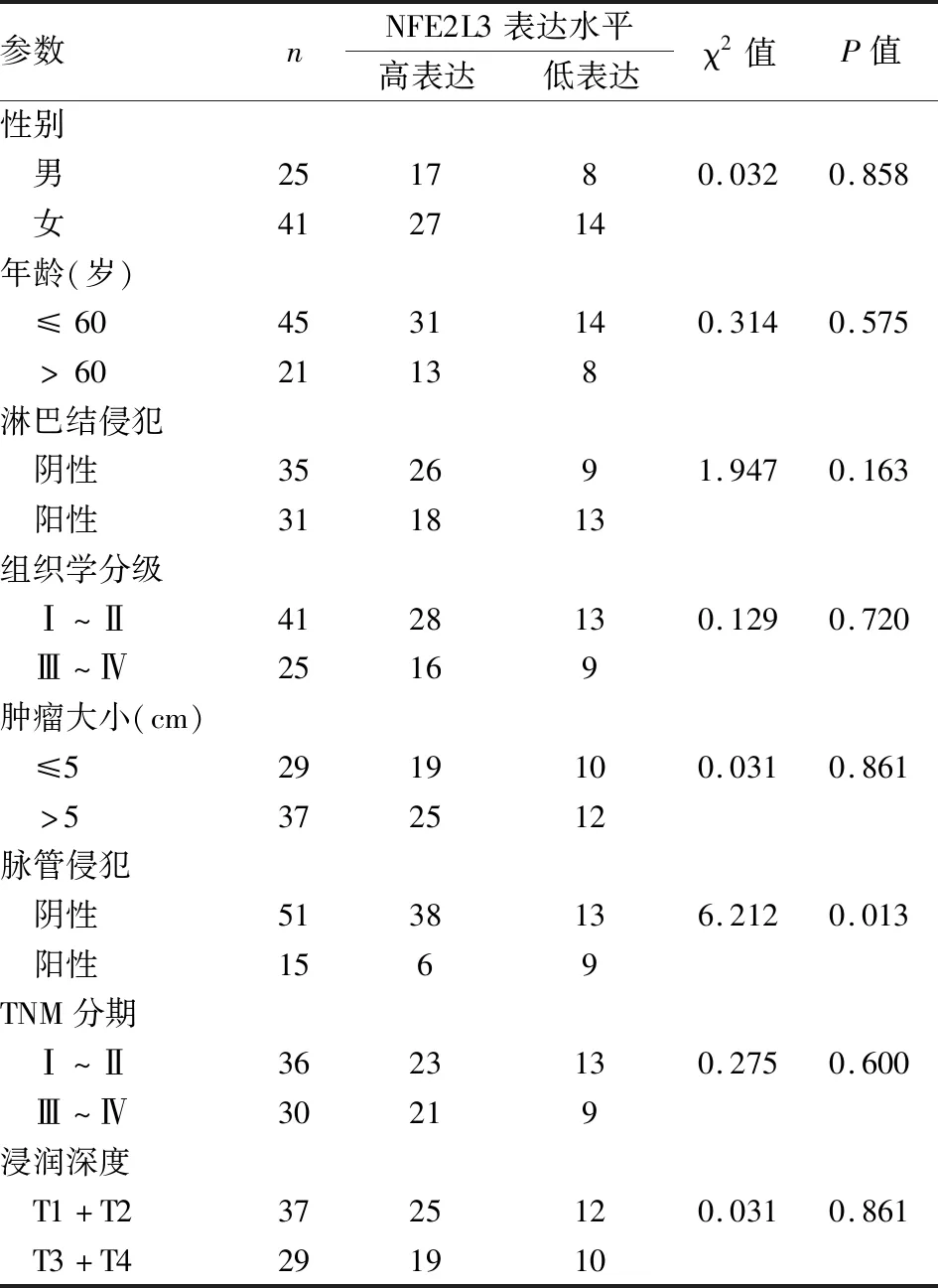
表2 NFE2L3差异表达水平与RC患者各临床病理参数的关系

图1 癌症相关数据库预测NFE2L3基因在RC中高表达A:GEPIA数据库预测结果;B:Oncomine数据库预测结果;与正常对照组比较:*P<0.05
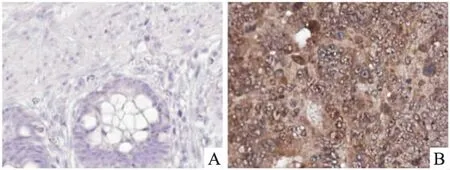
图2 免疫组化法检测NFE2L3在RC及癌旁正常组织的蛋白表达水平 SP×100
A:NFE2L3在癌旁正常组织中低表达;B:NFE2L3在RC组织中高表达
2.3 NFE2L3预测RC患者临床预后的价值随后对RC患者的预后与NFE2L3基因的差异表达水平的关系进行研究。GEPIA数据库预测显示:RC患者中NFE2L3基因mRNA高表达者的预后显著好于其低表达患者(P=0.041),见图3A,经进一步免疫组化SP法检测得到相似的结论,RC患者中NFE2L3蛋白高表达者的总生存时间显著好于其低表达者,差异有统计学意义(P=0.009),见图3B;Kaplan-Meier单因素生存分析结果示:NFE2L3差异表达水平、脉管侵犯、TNM分期及浸润深度是决定RC患者总生存时间差异的关键因素,见表3;将该4个单因素代入Cox多因素生存分析后,显示如下:NFE2L3表达水平可作为RC患者预后的独立预测因子(P=0.012)。见表4。
表3 RC患者的Kaplan-Meier单因素生存分析
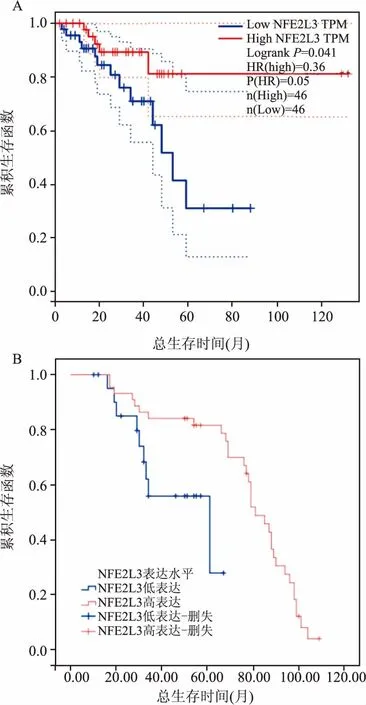
图3 基于NFE2L3表达水平差异绘制总生存曲线
A:NFE2L3 mRNA表达水平与总生存期曲线(Kaplan-Meier法);B:NFE2L3蛋白表达水平与总生存曲线(Kaplan-Meier法)

表4 RC患者的Cox多因素生存分析值
3 讨论
目前在霍奇金淋巴瘤、非霍奇金淋巴瘤、乳腺癌、大肠癌、睾丸癌、胰腺癌等多种恶性肿瘤中均发现NFE2L3呈现显著高表达水平[3-5, 9-10],但有关该基因到底扮演着促癌基因还是抑癌基因的角色却存在着不同的研究发现。Chevillard et al[11]最早利用NFE2L3基因缺陷的小鼠模型发现,该基因缺失后的小鼠对致癌物苯并芘的敏感性高度增加,其T细胞淋巴母细胞淋巴瘤的发病率显著升高,且死亡率亦增加,提示该转录因子在造血系统恶性肿瘤中具有保护作用,发挥着抑癌基因的角色。另一方面,Wang et al[10]证实NFE2L3在胰腺癌中呈明显高表达,并与患者淋巴结转移及TNM分期呈正相关性,且高表达NFE2L3的患者生存期更短,其机制与其调控血管内皮生长因子A表达促进肿瘤血管生成有关,该结果提示NFE2L3又具有促癌基因的角色。而在大肠癌的研究中出现了更为有趣的现象:国内学者[12-14]利用全基因组寡核苷酸技术筛选出NFE2L3为大肠癌高表达基因,并在体外实验中发现NFE2L3可抑制大肠癌细胞株LoVo和肝癌细胞株SMMC-7721的细胞生长,但对细胞凋亡无明显影响;国外Chowdhury et al[15]通过实验证实NFE2L3可通过刺激U2AF同源基序激酶1基因的表达在体外促进大肠癌细胞株DLD-1的细胞增殖,但它们在另一种大肠癌细胞株HCT116中也发现NFE2L3可显著抑制其细胞增殖。本实验采用生物信息学的方法预测到NFE2L3基因在RC组织中的表达明显高于正常对照组(P均<0.05);进一步应用免疫组化SP法对66例RC及配对的癌旁组织进行检测显示:NFE2L3蛋白在RC组织中显著升高,且与配对癌旁边组织相比,差异有统计学意义(P<0.001)。这一真实数据结果与生物信息学预测结果相一致,同时也与NFE2L3基因在前述其它恶性肿瘤中的高表达情况相吻合。该结果提示:NFE2L3基因在恶性肿瘤发展、发生等生物学进程中起着关键的作用。
继而对NFE2L3表达水平与RC预后进行研究,经相关性分析显示:NFE2L3的差异表达与RC患者有无脉管侵犯有关;经Cox多因素生存分析显示:NFE2L3基金的高表达可作为预测RC患者预后良好的独立预测因子,该结果与利用GEPIA公共数据库直肠癌数据预测的生存分析结果相一致,提示NFE2L3高表达与RC患者预后良好相关,该基因可能参与RC转移、生长等过程并发挥重要调节作用。
而针对NFE2L3在上述不同恶性肿瘤中既有发挥促癌基因的作用亦有抑癌基因的作用,甚至在大肠癌不同细胞株中扮演着相反的角色,这一现象也提示:NFE2L3在肿瘤中所发挥的调控作用存在着较大的异质性,未来仍需要进一步深入探索,剖析其在具体瘤种中的特异性作用及其分子机制。

