柴黄口服液对靶动物鸡安全性试验研究
刘 毅张国荣耿智霞贾 兴瞿红颖刘 欣∗宋婷婷刘 静魏丽娟刘 欣史万玉
(1.河北远征药业有限公司,石家庄050041;2.河北省兽药工程技术研究中心,石家庄050041;3.黄骅市农业局,沧州061100;4.河北农业大学,保定071001)
我国大部分地区每年夏季都会出现持续性高温、高湿天气,如果外界环境温、湿度过高,特别是通风不良等,鸡体散热困难,体内新陈代谢和生理机能紊乱,严重影响到鸡的采食量、生产繁殖性能、饲料利用率以及产品质量下降,并可导致鸡在短时间内大量死亡。长期以来,高温、高湿给畜禽业带来不可忽视的经济损失[1-3],因此,如何有效的缓解由高温、高湿引起的疾病,已经引起国内外学者们的高度重视,而进一步开发和研究能够缓解或修复动物由高温、高湿引起的疾病损伤的安全型药物将对畜禽生产具有重要的现实意义。
柴黄口服液由柴胡、黄芩两味药材提取组成,具有清热燥湿的作用,拟临床用于预防高温、高湿引起的鸡群发热,精神不振,食欲下降。为了全面评价本制剂在临床上使用的安全性,研究根据《兽药研究技术指导原则汇编》[4],通过靶动物安全试考察其用于靶动物鸡的的安全性及安全剂量范围,为临床试验给药方案的制定提供依据。
1 材料与方法
1.1 材料
1.1.1 试验动物及饲料 1日龄体重相差±5 g 的罗斯308 肉雏鸡:购自河北大午农牧集团种禽公司,严格按照管理标准进行饲养。
饲料:购自河北大午农牧集团生产的雏鸡全价饲料。
1.1.2 供试药品及试剂 柴黄口服液:河北远征药业有限公司生(含量:每1 mL 相当于原生药1 g,批号:150312)。
门冬氨酸氨基转移酶试剂盒、丙氨酸氨基转移酶试剂盒、尿素氮试剂盒、肌酐试剂盒购于北京北化康泰临床试剂有限公司。
1.1.3 仪器设备 TBA-120FR 全自动生化分析仪(日本东芝);08-230-2C 型滑走切片机(日本爱尔玛公司);S-35 型羽毛刀片(日本爱尔玛公司)。
1.2 方法
1.2.1 动物分组与处理 根据《兽用中药、天然药物临床试验技术指导原则》中对靶动物安全试验的分组要求,从新购进的1日龄体重相差±5 g 的罗斯308 肉雏鸡中选取健康活泼的雏鸡80 只,随机分为四组,每组20 只。其中1~3 组为试验组,分别在饮水中全程添加拟推荐剂量(1 mL/L)1 倍、3 倍和5倍的柴黄口服液;4 组为不用药对照组,全程饮用新鲜自来水。试验期6 周,每天观察并记录各组鸡的临床体征,每周末称重1 次,6 周末试验结束时心脏采血,用全自动血液细胞分析仪测定白细胞计数及分类、红细胞计数、血红蛋白含量测定各组鸡的血液学指标,分离血清,用门冬氨酸氨基转移酶试剂盒、丙氨酸氨基转移酶试剂盒、尿素氮试剂盒和肌酐试剂盒测定AST、ALT、BUN 和CRE 等血液生化指标。同时进行剖检,观察各脏器有无眼观和显微结构上的变化。
1.2.2 检测指标及方法 临床体征变化观察:试验过程中,每天观察并记录各组鸡的临床体征,比较各组鸡群之间有无异常变化。
体重测定:试验过程中,每周末测定各组鸡的体重变化情况,比较各组鸡群之间的体重有无异常变化。
血液生理指标的测定:6 周末试验结束时各组鸡心脏采血,测定各组鸡的血液生理指标的变化情况。
①红细胞总数的测定 采用试管法,即将供检血稀释200 倍后,用血细胞计数板计数一定容积内的红细胞数,最后计算出每升血液中的红细胞数。红细胞总数的计算公式:红细胞总数(×1012个/L)=X/100×1012。式中的X为5 个中方格的红细胞总数。
②白细胞总数的测定 采用试管法,即将供检血稀释20 倍后,用血细胞计数板计数一定容积内的白细胞数,最后计算出每升血液中的白细胞数。白细胞总数的计算公式:白细胞总数(×109个/L)=X×50×106。式中的X为4个大方格中的白细胞总数。
③血红蛋白含量的测定 采用比色法。红细胞遇酸溶解后会游离出血红蛋白,并被酸化为褐色的酸性血红素,稀释后与标准比色柱比色,即可求得血红蛋白的含量。
④淋巴细胞比例的测定 用未抗凝血,制作血涂片,姬姆萨染色法染色,采用白细胞胞分类法对白细胞计数,计算淋巴细胞比例。
血液生化指标的测定:试验组在饮水中以推荐剂量的1 倍、3 倍、5 倍剂量加入柴黄口服液饮喂雏鸡,对照组正常饮水,6 周后,剖杀取血液制备血清,测定肝功能指标门冬氨酸氨基转移酶(AST)及丙氨酸氨基转移酶(ALT)和肾脏功能指标尿素氮(BUN)、肌酐(CRE)。
剖检变化观察:6 周末试验结束后,将各组鸡进行剖检,观察其眼观剖检变化。
组织切片观察:取肝脏、肾脏、脾脏、心脏固定,石蜡切片,H-E 染色并观察。
1.3 数据处理及统计 应用SPSS17.0 软件对数据进行单因素方差分析。
2 结果与分析
2.1 临床表现 在整个试验过程中,1 倍、3 倍、5倍剂量试验组和对照组的雏鸡,活泼好动,能自由摄食、饮水,粪便正常。整个试验过程所有雏鸡均存活,未出现中毒性临床症状。
2.2 体重变化 由表1可知,肉鸡在试验期前3 周内各组间的平均体重均无显著性差异(P>0.05)。只是在42日龄试验结束时,1 倍剂量组和3 倍剂量组肉鸡的体重均显著高于5 倍剂量组和不用药对照组(P<0.05);而1 倍剂量组和3 倍剂量组间,以及5 倍剂量组和对照组间均无显著性差异(P>0.05) 。
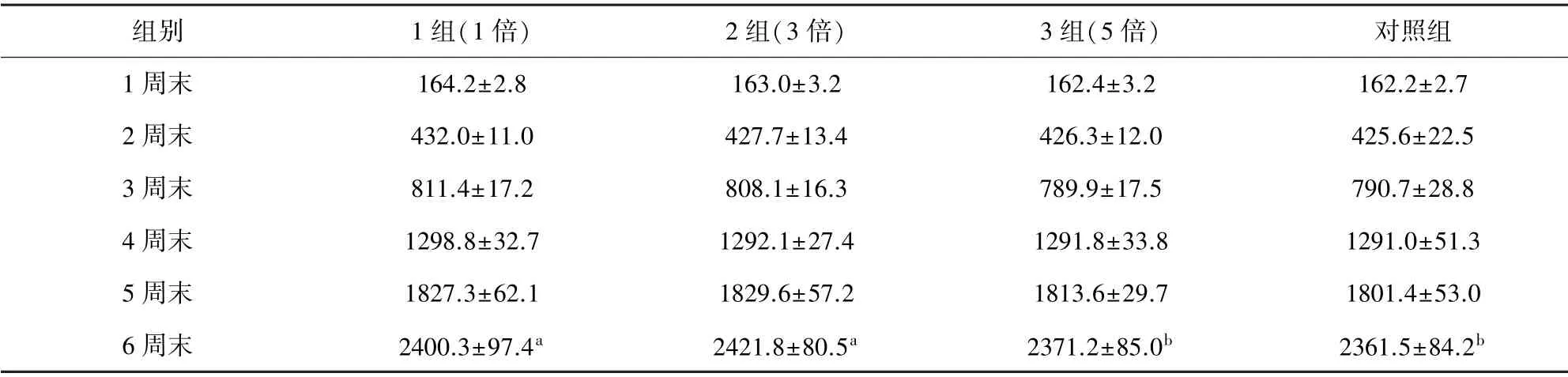
表1 试验各组体重情况( ±SD) (g/只)Tab 1 Weight of each group in the trial( ±SD)
2.3 血液生理指标变化 由表2可知,各试验组与对照组的红细胞总数,血红蛋白含量、白细胞总数均差异不显著(P>0.05),各试验组之间的淋巴细胞比例也均无显著差异(P>0.05)。

表2 各组雏鸡血液生理指标( ±SD)Tab 2 Blood physiological indexes of chickens in each group
2.4 血液生化指标变化情况 由表3可知,试验组雏鸡血清中门冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)、尿素氮(BUN)和肌酐(CRE)的含量均与对照组差异不显著(P>0.05 ),且各试验组各剂量水平之间差异也不显著(P>0.05)。
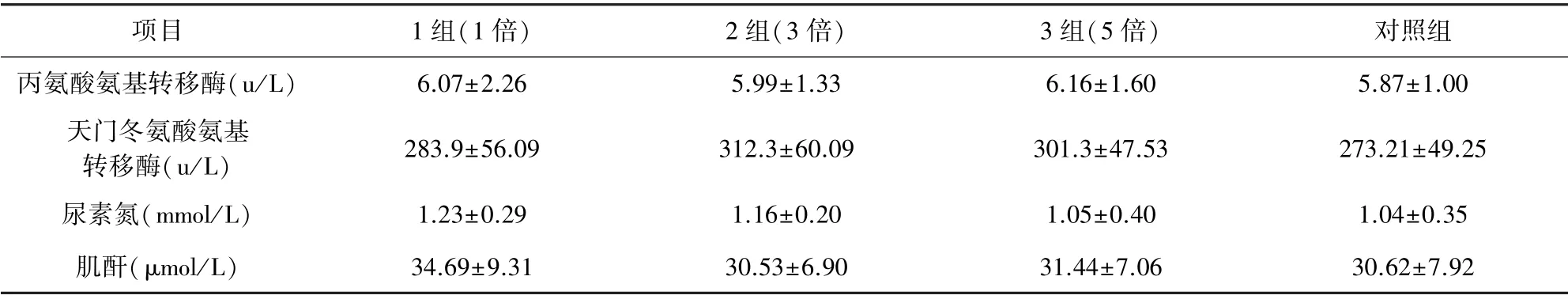
表3 对血液生化指标的影响( ±SD)Tab 3 The influence on blood biochemical indexes
2.5 大体剖检变化 试验结束时对各组雏鸡进行剖检观察。结果发现,各组鸡的脏器颜色,形状,大小、位置等均未见异常变化。
2.6 主要脏器病理组织切片观察 在进行上述剖检检查时,采集各组鸡的心、肝、脾、肾等实质器官,制作石蜡切片,进行组织结构的显微观察。结果发现,各组织器官的细胞轮廓完整,排列有序;胞质丰满,细胞核结构清晰,符合正常组织形态和结构特点,说明柴黄口服液对所采集组织无毒性作用(图1~图4)。
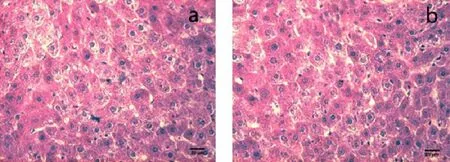
图1 肝脏组织切片显微结构Fig 1 Microstructure of liver tissue slices
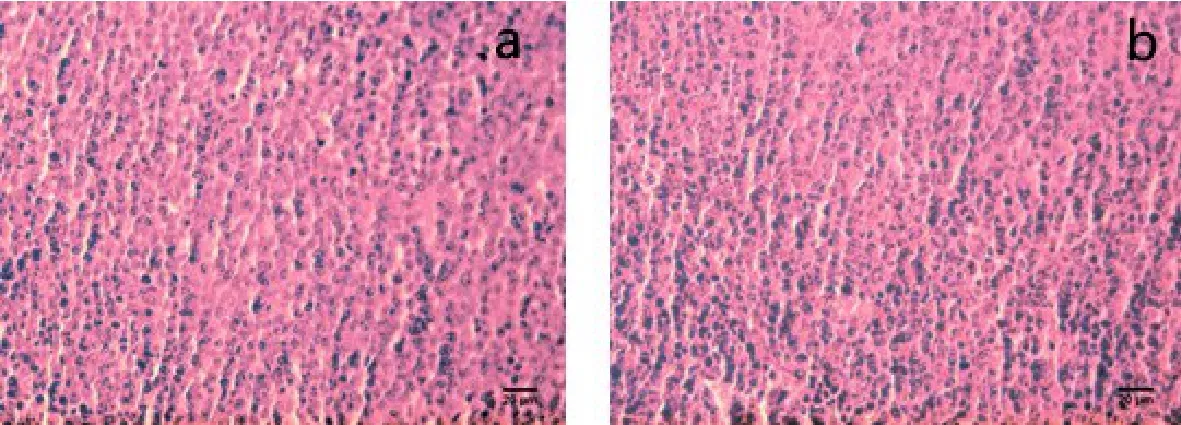
图2 脾脏组织切片显微结构Fig 2 Microstructure of splenic tissue section

图3 脾脏组织切片显微结构Fig 3 Microstructure of splenic tissue section
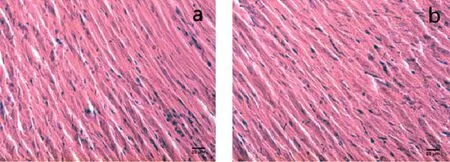
图4 心脏组织切片显微结构Fig 4 Microstructure of cardiac tissue slices
3 讨论与结论
中兽医学认为,鸡群长时间处于高温、高湿的环境中,热邪极易侵袭机体,引起机体发热。柴黄口服液由柴胡和黄芩配伍组成,方中柴胡可泻半表半里之表热[5],黄芩可泻半表半里之里热[6-7];柴胡升清阳,黄芩降浊火。二药相合,升清降浊,调和表里,和解少阳,清少阳之邪热。柴胡又长于开郁,黄芩又善于泄热。两药相互为用,既可调肝胆之气机,又可清泄内蕴之热邪[8-10]。
靶动物安全性试验是观察不同剂量受试兽药作用于靶动物后从有效作用到毒性作用,甚至到致死作用的动态变化的过程。该试验旨在考察受试兽药使用于靶动物的安全性及安全剂量范围,为进一步临床试验给药方案的制定提供依据。为观察不同剂量柴黄口服液作用于靶动物后从有效作用到毒性作用的动态变化过程,而进行了本次试验。采用与临床应用相同的给药途径,给药为全程给药。结果发现:柴黄口服液三个剂量组雏鸡状态良好,生长正常,未出现中毒症状及死亡,血液生化生理指标、剖检以及组织显微结构等与对照组相比均无明显差异。只是在42日龄试验结束时,1 倍剂量组和3 倍剂量组肉鸡的体重均显著高于5 倍剂量组和不用药对照组(P<0.05),这种变化并非受试药物柴黄口服液的毒副作用,可能与柴黄口服液能够清解雏鸡脾胃湿热,进一步调动脾胃功能,提高雏鸡采食、消化和吸收有关。而5 倍剂量组却并未提高雏鸡的体重,可能与药物浓度太高,超过柴黄口服液有效药物浓度范围有关。因此,柴黄口服液按照1 倍(1mL/L)、3 倍(3mL/L)、5 倍(5mL/L)推荐剂量,分别连续饮水给药42 d,均对靶动物鸡无明显毒副作用。因此,柴黄口服液在临床上以1mL/L在鸡饮水中混饮是安全的。

