超声分散比浊法处理BACTEC MGIT 960培养阳性的菌液标本用于药物敏感性试验的价值
杨翰 杨静芬 谈小文 李爱芳 崔晓利 康磊 党丽云
近年来,虽然分子生物学药物敏感性试验(简称“药敏试验”)方法发展迅速[1-2],但其检测范围并不能包含所有抗结核药物,并且实验仪器费用昂贵,所以表型药敏试验仍然为大多数结核病实验室应用,以为结核病的临床治疗提供全面的药敏信息。但在日常操作中,BACTEC MGIT 960(简称“MGIT 960”)液体药敏试验因标本菌量的问题,会导致试验结果有一定的报错率;固体药敏试验时,人工磨菌比浊又受人为因素影响较大,这些都对药敏试验结果有一定的影响。笔者使用细菌超声分散计数仪对MGIT 960培养物进行超声分散比浊,分析其在不同药敏试验中的应用价值。
资料和方法
一、研究资料
1.资料收集:搜集2018年1—12月西安市胸科医院经MGIT 960液体分枝杆菌培养阳性的菌液标本,共计1086份(培养阳性的菌液标本来自于临床各类型标本,包含痰液、支气管冲洗液及各类型体液标本等)。其中,818份菌液标本进行MGIT 960 液体药敏试验,包括MGIT 960推荐方法处理的菌液标本(简称“MGIT 960 法标本”)100份、超声分散比浊法处理的菌液标本(简称“超声比浊法标本”)718份;268份菌液标本进行比例法药敏试验,包括传统磨菌法处理的菌液标本(简称“磨菌法标本”)30份、超声比浊法标本238份。
2.仪器与试剂:MGIT 960 液体药敏试验应用MGIT 960试剂盒(批号:804944;BACTECTMMGIT 960操作系统,购自美国BD公司);比例法药敏试验应用分枝杆菌罗氏培养基(培养法;批号:1806181;购自珠海市银科医学工程股份有限公司);细菌超声分散计数仪(型号:BACspreaderTM1100)、比浊管(批号:20180119)、细菌浊度标准液(批号:20180111),均购自广东体必康生物科技有限公司。
二、MGIT 960液体药敏试验(MGIT 960法)
1.MGIT 960法菌液准备[3]:取MGIT 960系统报阳且菌种鉴定为MTB的菌液,以报阳当天算作第0天,如果在第1、2天进行操作,则直接为工作菌液进行药敏试验接种;如果在第3~5天进行操作,则用灭菌生理盐水按照1∶5稀释为工作菌液(1 ml 菌悬液,4 ml生理盐水),然后进行药敏试验接种。
2.超声分散比浊法菌液准备[4]:取MGIT 960系统报阳且菌种鉴定为MTB的菌液,加入2 ml至磨菌管中。工作参数为超声5 s、间隔5 s;持续1 min。超声后记录浊度。本次研究浊度范围为0.4~1.0麦氏单位。将相应的浊度稀释至0.1麦氏单位的工作液[3],然后进行药敏试验接种。
3.含药培养基准备[3]:于MGIT 960试剂盒取5只培养管。第一管标记GC(空白对照),其余4只管分别标记Sm(链霉素)、INH(异烟肼)、RFP(利福平)、EMB(乙胺丁醇)。无菌操作下每管加入0.8 ml增菌剂;4 ml灭菌蒸馏水溶解药物干粉,在相应含药标记管加入100 μl相应药物;对照管内加入0.5 ml 的1∶100倍稀释的工作菌液(0.1 ml菌液,10 ml灭菌生理盐水),其余4管含药培养基加入工作菌液0.5 ml,盖紧螺旋盖并混匀。
4.结果报告:将上述培养管放入MGIT 960系统内培养,等待报告结果。若报告X200则为活菌含量较少;报告X400则为活菌含量较高,杂菌生长,即污染;以上两种结果表示试验失败。仪器正常报告药敏结果则为试验成功。该指标为效果指标,用于判断试验成功与否,而非评价指标的依据。
三、比例法药敏试验
1. 超声分散比浊法菌液准备:取MGIT 960系统报阳且菌种鉴定为MTB的菌液,加入2 ml至磨菌管中,工作参数为超声5 s、间隔5 s;持续1 min。超声后记录浊度。本次研究浊度范围为0.4~1.0麦氏单位。将相应的浊度稀释至0.1麦氏单位的工作液,将工作液取0.1 ml进行1∶10稀释(0.5 ml菌液,4.5 ml灭菌生理盐水)得到10-2菌悬液。将10-2菌悬液按1∶100稀释(0.1 ml菌液,10 ml灭菌生理盐水)得到10-4菌悬液。
2.传统比浊法菌液准备:取MGIT 960系统报阳且菌种鉴定为MTB的菌液,按照《结核病实验室检验规程》[3]进行磨菌操作,与标准比浊管比浊,得到1麦氏单位工作液,将工作液菌悬液按1∶100稀释(0.1 ml菌液,10 ml灭菌生理盐水)得到10-2菌悬液,将10-2菌悬液按1∶100稀释(0.1 ml菌液,10 ml 灭菌生理盐水)得到10-4菌悬液。
3.药敏试验接种:将10-2、10-4菌悬液,分别接种到2支对照培养基及2支相应含药培养基上。恒温培养箱内35~37 ℃,培养4周后进行结果判读[3]。若高稀释度的对照培养基菌落数<20个,则判断为试验失败;对照培养基菌落数≥20个则为试验成功。该指标为效果指标,非评价指标的依据。
四、统计学分析
采用 SPSS 19.0 统计学软件对数据进行分析。与传统菌液标本制备方法比较,分析超声分散比浊法制备菌液标本用于MGIT 960液体药敏试验和比例法药敏试验的效果。计数资料的比较采用χ2检验,以P<0.05为差异有统计学意义。
结 果
一、超声比浊法标本用于液体药敏试验的价值
浊度为0.6~1.0麦氏单位菌液标本进行MGIT 960液体药敏试验报告结果的时间主要集中在8~10 d,而MGIT 960 法标本报告结果时间则较均匀分布在5~14 d。应用MGIT 960 法标本进行MGIT 960液体药敏试验时,系统报告X200的报告率为11.00%(11/100),X400报告率为4.00%(4/100)。应用超声比浊法标本进行MGIT 960液体药敏试验时,不同浊度标本系统X200报告率的差异有统计学意义(χ2=227.78,P<0.01);浊度为0.4和0.5麦氏单位标本系统X200报告率均高于MGIT 960菌液制备法,差异有统计学意义(χ2值分别为27.75和9.12,P值均<0.01);浊度为0.6~1.0麦氏单位标本系统X200报告率均低于MGIT 960菌液制备法,差异有统计学意义(χ2值分别为11.41、9.94、12.43、12.79、11.28,P值均<0.01)。两种方法制备菌液标本系统X400报告率的差异无统计学意义(χ2=8.85,P=0.257)。具体见表1。
二、超声比浊法标本用于比例法药敏试验的价值
进行二线抗结核药物比例法药敏试验时,随着继续增菌天数的增加,应用超声分散比浊法处理的菌液标本达到1麦氏单位浊度工作液的比率高于传统磨菌法处理的菌液标本;增菌6~7 d后,应用超声分散比浊法处理的菌液标本基本可以达到目标浊度,而传统磨菌法处理的标本在增菌第7天时仅有80%达到目标浊度(图1)。应用超声分散比浊法处理的0.4~0.6麦氏单位菌液标本进行比例法药敏试验的成功率分别为4.00%(1/25)、12.50%(3/24)、42.86%(6/14),均明显低于磨菌法标本[83.33%(25/30)],差异有统计学意义(χ2值分别为34.43、26.80、7.51,P值均<0.05);0.7~1.0麦氏单位菌液标本试验成功率分别为82.61%(19/23)、82.69%(43/52)、94.00%(47/50)、96.00%(48/50),与磨菌法标本试验成功率相近,差异无统计学意义(χ2值分别为0.01、0.01、2.37、3.77,P值均>0.05),见图2。
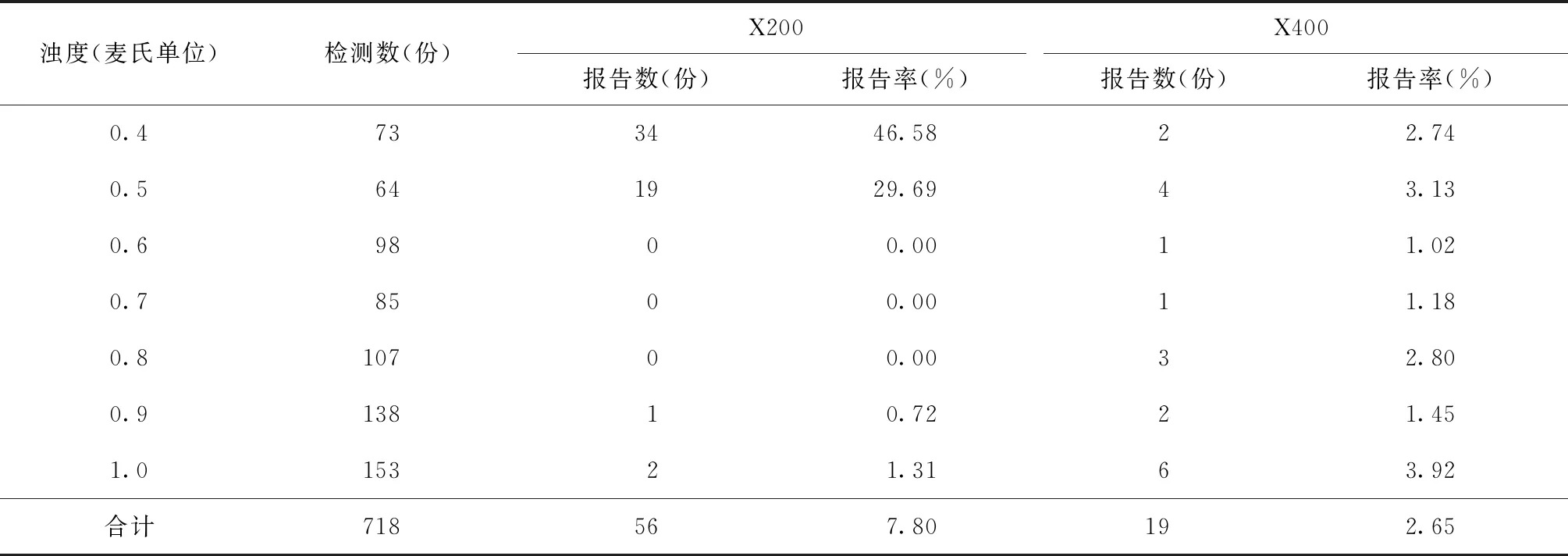
表1 应用超声比浊法制备的不同浊度菌液标本进行MGIT 960液体药敏试验时系统报错情况
注X200表示检测标本活菌含量较少;X400表示检测标本污染

图1 超声分散比浊法和传统磨菌法制备菌液标本达到比例法药敏试验标本目标浊度效果分析图

图2 采用超声比浊法标本和磨菌法标本进行二线抗结核药物比例法药敏试验的效果比较
讨 论
目前,MGIT 960液体培养和药敏试验系统已经常规使用[5]。但在实际应用过程中,MGIT 960药敏试验有一定的报错率,且该方法目前仅针对一线抗结核药物,而针对二线抗结核药物的药敏检测还需应用比例法药敏试验。MGIT 960液体培养物报阳后使用传统磨菌法制备的菌液往往浊度不能达标,需要进一步增菌,从而延长了药敏试验结果报告时间。本次研究显示,应用超声分散比浊法制备菌液标本可以有效解决菌液标本浊度达标的问题。
MGIT 960液体培养时,培养管报阳时管内的菌量是存在差异的,这种差异与每份标本中含菌量有关。菌量较少的标本,培养管内会出现由单个细菌繁殖成的大块索状细菌团,虽然其达到了报阳所需的耗氧量,但实际菌量往往较少,也不容易通过高速旋涡振荡来分散。这部分培养物在进行MGIT 960液体药敏试验时,系统报告X200(对照无生长)的概率很大。本研究结果显示,超声分散比浊法可将索状生长的分枝杆菌有效分散,浊度为0.6~1.0麦氏单位菌液样品系统X200报告率明显低于MGIT 960法制备的菌液样品。虽然报告结果时间固定在8~10 d,但减少了重复试验的几率,对患者治疗及试验成本的节约都具有一定的优势。此外,超声分散比浊法虽然增加了比浊的试验步骤,但只要严格遵守无菌操作,系统报告X400(污染)的概率与MGIT 960法没有太大差异。
在比例法药敏试验中,如果使用传统的磨菌瓶磨菌,因技术限制,需要的菌量大,MGIT 960液体培养报阳后,往往达不到1麦氏单位,需要将培养物继续放在孵育箱内进行增菌。如此,则药敏试验时间就会增加,甚至延长到1周以上,延误了结果的报告时间。MGIT 960液体培养报阳后样品利用超声分散比浊法磨菌,不存在菌液浪费,菌量基本能满足0.7麦氏单位,而0.7~1.0麦氏单位范围内菌液标本进行比例法药敏试验的成功率与传统磨菌法制备标本相近。因此,应用超声分散比浊法处理菌液标品在保证了药敏试验成功率的前提下,可以缩短试验时间。
综上,本次研究结果显示,使用超声分散比浊法制备菌液标本用于MGIT 960液体药敏试验可以减少出错率;用于固体比例法药敏试验可以缩短试验时间。并且,已有研究显示,超声分散比浊法处理菌液标本并不影响MTB菌株活性,对药敏试验的结果无影响[4, 6]。特别强调,本次研究主要探讨效果性指标,并未关注应用超声分散比浊法处理菌液标本对药敏试验准确性和重复性的影响。

