酿造酒中氨基甲酸乙酯的研究进展
林宜锦,欧梦莹,关统伟,*,张习超,尚治豪,李 东,张家旭,赵小林
(1.西华大学微生物研究所,西华大学食品与生物工程学院,四川成都 610039;2.成都蜀之源酒业有限公司,四川成都 611335)
氨基甲酸乙酯(Ethyl Carbamate,EC)又名尿烷,具有一定的抑菌和抗肿瘤活性,在20世纪初期曾被广泛地应用于医药领域[1]。然而,EC在1943年被发现有致癌作用[2],并在随后的小鼠、大鼠、仓鼠及猴子等哺乳动物试验中被证实[3]。EC对哺乳动物的多位点致癌作用引起了人们的高度重视。1974年,国际癌症研究机构(International Agency for Research on Cancer,IARC)将EC列为了2B类致癌物质[4]。此后,又有证据表明EC能够直接导致人类产生肝癌[5],EC的致癌等级因此被提升至2A类[6]。期间,分子生物学技术的发展让EC的致癌机制得到了初步解析。在啮齿动物体内代谢中,EC通过细胞色素P450转化为N-羟基-氨基甲酸乙酯(约占0.1%)和乙烯基-氨基甲酸乙酯(约占0.5%),前者被代谢产生的活性氧簇(ROS)物质可导致Cu2+调控下的DNA损伤,这种损伤多发生于胸腺嘧啶(T)和胞嘧啶(C)的残基上;乙烯基-氨基甲酸乙酯则经过转化加聚物与DNA共价结合而导致细胞癌变[7-8]。近年来,基于公认的动物模型,对EC的致癌作用有了更深入的了解,转录因子STAT3、NF-kB[9-11]及细胞外信号蛋白激酶(ERK)[12]等被证明参与EC诱导的肿瘤的发展。另一方面,EC的毒理学研究也开始转向人体组织或细胞模型。有研究表明,EC可以通过多种途径诱导人体肝癌细胞(HepG2)死亡,包括诱导氧化应激、降低解毒能力、消耗能量、破坏膜完整性、破坏DNA和蛋白质等[13-14]。随着相关研究的进行,EC的安全性可能被重新评估。
由于EC在发酵食品和酿造酒中普遍存在,人体通过日常饮食摄入EC不可避免[15]。根据FAO/WHO食品添加剂联合委员会(JECFA)的数据,人体通过酿造酒摄入EC的平均含量为65 ng·kg-1·d-1,是其他发酵食品和饮品摄入总量的近五倍[16]。有研究表明EC在肝脏清除上可能与乙醇存在复杂的交互作用,不排除乙醇和EC之间具有协同致癌作用[17]。基于上述原因,EC被列为了重点监控对象,加拿大、日本、巴西及欧盟部分国家相继制定了其在酿造酒中的限量标准[18]。在另一方面,科学家们深入探索了EC在酿造酒中的形成机制,确定了EC及其前体物质的来源与转化关系,为发展EC的控制措施奠定了理论基础。目前,物理化学、酶学及代谢工程等手段已经应用于酿造酒生产的各个阶段以控制EC的含量。但鉴于中国尚未建立国家标准对酿造酒中的EC污染进行指导和管控,继续深入针对EC的风险评估、形成机制和控制策略的研究对保障饮酒人群的健康具有重要意义。
1 酿造酒中的EC污染及其风险评估
1.1 酿造酒中EC的污染水平
中国酿造酒的种类繁杂,EC污染在不同酒类的酒精饮料之间存在较大的水平差异(表1)[19-23],参考加拿大制定的EC在酿造酒中的限量标准(葡萄酒30 μg/L,蒸馏酒150 μg/L,水果白兰地400 μg/L,清酒200 μg/L),多数啤酒中的EC含量处在检测限以下,葡萄酒中EC的含量一般低于或接近限值,而很多白酒和黄酒中的EC含量显著高于限值。2015年,卫生部食品安全风险评估中心对我国各地区的890个黄酒样品进行检测分析。结果显示,黄酒中EC的污染水平在6.3~775.8 μg/L(平均为232.9 μg/L),高于烈酒和清酒的限值[23]。另一项针对白酒的检测中,有48.7%的样品中EC的含量高于蒸馏酒中EC的限值(150 μg/L)[24]。
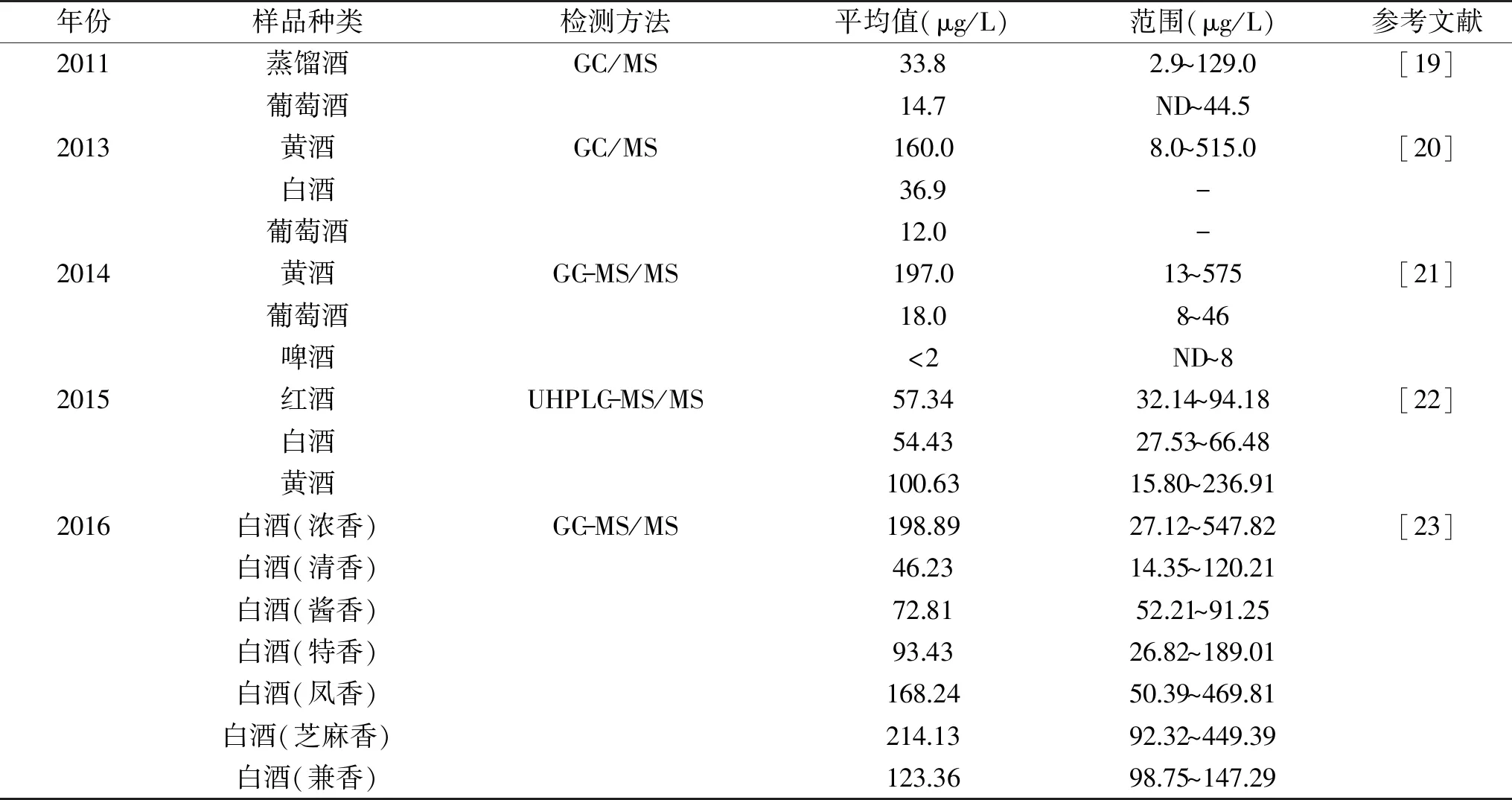
表1 部分酒精饮料中氨基甲酸乙酯含量
此外,EC含量在同类酿造酒中的检测结果也有明显的差异,特别是白酒的酒型众多,EC含量在不同香型(工艺)的白酒中有显著的差异。不同的检测方法如气相色谱-质谱(GC-MS)和高效液相色谱-荧光检测(HPLC-FLD)对检测结果也有一定的影响,一般使用HPLC-FLD方法检测白酒时需要适当调整样品的酒精度以减少EC峰面积上的误差[25]。另外,黄酒的陈贮时间会显著影响EC的检测结果[26]。
1.2 酿造酒中EC的风险评估
目前,膳食EC的摄入风险主要通过欧洲食品安全委员会(EFSA)推荐的暴露边界比(Margin of Exposure,MOE)进行评估,即基准剂量下限值(BMDL)与人群膳食暴露量的比值。一般认为MOE值等于10000是公共卫生风险的阈值,MOE值越小表示致癌风险越大,当该值小于3800则需要考虑采取干预措施[26]。由于黄酒和白酒中的EC含量偏高,同时在消费水平上存在明显的区域和个体差异,它们对饮酒人群的健康威胁要高于普通人群,是风险评估关注的重点。根据第四次和第五次全国总膳食研究(TDS)的数据,2009年人均每日膳食EC摄入估量为8.27 ng/kg BW,高消费人群(P97.5)为45.67 ng/kg BW,低于JECFA建议的每日摄入限值(EDI)80 ng/kg BW,表明中国成年人对EC暴露的风险较低。但是在黄酒消费省份,普通与高消费人群每日黄酒EC的摄入估量分别为290.6和1848.4 ng/kg BW,远高于EDI限值。结合0.3 mg/kg BW的BMDL10值,黄酒EC摄入量的中位数和高消费人群(P97.5)的MOE值分别为3246和162,具有较高的暴露风险[24]。另据国家食品安全风险评估中心对白酒EC摄入的风险评估显示,居民人均每日白酒EC摄入估量为8.09 ng/kg BW,MOE值为37083。白酒饮用人群的人均每日白酒EC摄入估量为159.99 ng/kg BW,MOE值为1875,同样具有较高的暴露风险[27]。
暴露边界比用于评估EC的暴露风险仍有不足之处。一方面,酿造中还有其他已知或未知的致癌物质,定量分析的方法不能排除酒精和其他致癌物质的交互作用[26]。另一方面,基准剂量下限值是由动物实验得到,与人体内的毒代作用有较大的差异,特别是在肺泡和小支气管肿瘤的发生上[28]。而由种族、性别、年龄、遗传、病史、环境、运动及吸烟状态等因素引起的人类个体变异更加难以区分,因此从动物外推到一般人群或特定人群(敏感人群)时就存在很大不确定性[29-30]。尽管如此,保守的评估标准对于公共卫生安全是十分必要的。鉴于目前黄酒和白酒中的EC暴露风险显著高于国内其他酒类,减少饮酒并控制黄酒和白酒中的EC含量就显得尤为重要。
2 酿造酒中氨基甲酸乙酯的形成机制
2.1 EC的前体物质与生成反应
EC的形成和发酵微生物息息有关,其主要前体物质,尿素、瓜氨酸与氨甲酰磷酸均由微生物积累,氰化物和焦磷酸二乙酯则由原料带入并经酶促反应生成[18]。这些前体物质在不同酿造酒中对形成EC的贡献程度有所差异,这取决于发酵微生物的组成体系及其协同代谢过程。
2.1.1 尿素与乙醇反应 在多数酿造中,尿素是形成EC最重要的前体物质之一。尿素由微生物经尿素循环途径生成,并可被进一步分解为氨和二氧化碳。但是微生物对尿素的利用受到氮分解代谢产物抑制(Nitrogen Catabolite Repression,NCR)的调控。在NCR的多级调控中,Gln3p是最多的GATA型调控因子,受到TOR(Target of rapamycin)信号的控制。当环境中存在优选氮源(谷氨酰胺或天冬氨酸),TORC1通过调控Tap42p介导的Sit4p磷酸化酶使Gln3p磷酸化,与阻遏蛋白Ure2p结合形成Gln3p-Ure2p复合体而被留在细胞质中。只有当细胞缺乏氮营养或用雷帕霉素(其受体是TOR蛋白)处理时,Gln3p才能转位到细胞核中,激活参与非优选氮源利用和转运的基因的表达[31-32]。尿素因NCR调控在细胞中大量积累,最终被释放到周围介质中与乙醇反应生成EC。大量研究表明,酵母是尿素产生的主要贡献者,如酱香型白酒与黄酒中的酿酒酵母(Saccharomycescerevisiae)[33]、清香型白酒的异常威克汉逊酵母(Wickerhamomycesanomalus)[34]等。

图1 尿素生成和转运途径[35]
2.1.2 瓜氨酸与乙醇反应 瓜氨酸是形成EC的另一种主要前体物质,特别在葡萄酒及其他果酒之中。瓜氨酸主要由以乳酸菌(Lactic acid bacteria,LAB)为主的细菌通过精氨酸脱亚氨酶途径(Arginine deiminase pathway,ADI)生成[36]。虽然瓜氨酸也是尿素循环的产物之一,但在一株敲除ARG3(编码鸟氨酸转氨基酶,OTC)阻断尿素循环的工程菌中,其产量未见明显减少,说明这是一条次要途径[37]。另外,瓜氨酸向精氨琥珀酸的转化受到pH、氧胁迫和盐浓度等环境因素的限制,这些因素共同造成了瓜氨酸的积累[38-39]。
2.1.3 氨甲酰磷酸与乙醇反应 氨甲酰磷酸主要通过酵母中氨甲酰磷酸合酶和细菌精氨酸脱亚氨基途径产生,但一般不被释放到细胞外,因此大多数情况下被忽略。
2.1.4 其他前体物质与乙醇反应 原料中生氰糖苷酶促(β-葡萄糖苷键)分解或高温裂解生成的氰化物被认为是谷物蒸馏酒中重要的EC前体物质。氰化物在发酵过程中会进一步氧化形成氰酸盐[40],后者在光照、氧气或Cu2+催化下与乙醇生成EC[41]。焦磷酸二乙酯曾作为食品添加剂来抑制有害微生物的生长,它可以与RNA酶活性基团中组氨酸的咪唑环反应而抑制RNA酶的活性,也可以与NH3反应生成EC[42],目前,焦磷酸二乙酯在葡萄酒酿造过程中已经很少使用。
2.2 影响EC生成的环境因素
温度、pH及Cu2+等是EC生成的重要响应因素。如在黄酒的煎酒和贮存过程中,EC含量与温度在一定范围内呈现显著的正相关,与尿素则是负相关[43]。其机理是,在酸性体系中,高温促使尿素分解产生氰酸盐和异氰酸盐,加快与乙醇反应生成EC[44]。瓜氨酸在白酒蒸馏中也有类似的过程[18]。此外,pH对LAB的苹果酸-乳酸发酵(Malolactic fermentation,MLF)途径有重要影响,较低的pH可以抑制一些菌株通过MLF途径利用精氨酸[45]。Cu2+是细胞色素氧化酶的重要辅基[46],也是氰酸盐向EC转化的重要催化剂[41]。在高浓度下,Cu2+还可以催化Fenton反应或与硫醇基团结合产生-OH,胁迫酵母细胞的生长[46]。在酿酒原料中,碱式硫酸铜类杀菌剂残留是Cu2+的主要来源,如波尔多液[CuSO4+Ca(OH)2]被广泛施用在葡萄园中,用于防治霜毒病等葡萄病害[46]。
3 控制EC水平的技术方法
EC及其前体物质形成机制的确定为控制EC的含量提供了基础,得到了许多能够有效降低酿造酒中EC水平的方法,可大致分为改进生产工艺、酶降解和代谢工程三个技术路线。
3.1 改进生产工艺路径
改进生产工艺可以结合原料处理、发酵工艺优化和下游分离等方面进行综合调控。在原料上,通过精制处理或蒸汽清洗去除EC前体物质是常见的方法,其次还可以在原料使用添加催化剂用以催化EC前体物质分解,如氰化物催化剂和铜离子催化剂[47]等。但这些精炼手段很可能会造成营养和风味成分的流失以及铜离子造成的残留和环境污染等问题,因此多作为辅助手段。
EC在酿造过程中的生成受到诸多因素的影响,适当地改进酿造条件可以在一定程度上控制EC的生成。一些添加剂,如没食子酸和原儿茶酸[48]以及磷酸二铵[49]等可以在一定程度上抑制EC的生成。另外,温度调整是控制EC形成的重要手段,在煎酒时采用快速降温或者低温贮存(4 ℃)的方式可以显著降低黄酒中的EC水平[43]。而二次蒸馏[50]、高回流比蒸馏和低温发酵[51]等方式均可以达到控制EC的理想效果。
在酿造酒生产的下游,活性炭或其他特异性吸附材料可被用于去除酒体中的EC,其关键在于要减少对其他风味物质的影响,Park等[52]用活性炭过滤去除了烈酒中45%~47%的EC。进一步探索EC的特异性吸附材料是发展EC控制手段的趋势之一。
3.2 酶降解路径
3.2.1 脲酶 通过直接在酿造酒中添加脲酶(urease)将尿素降解成氨和二氧化碳是控制EC简单而有效的方法,筛选能够生产耐酸和耐乙醇脲酶的菌株曾经一度成为热门课题。1979年,Suzuki等[53]在小鼠肠道中分离得到了产酸性脲酶的发酵乳杆菌(Lactobacillusfermentum),其生产的脲酶最适pH为4.0,可在15 ℃条件下两天内将日本清酒中的尿素降至无法检测的水平(1 ppm)(30 ℃下为15 h)。此后,其他一些具有酸性脲酶生产能力的细菌陆续被筛选出来,如运动节杆菌(Arthrobactermobilis)、肠杆菌属(Enterobactersp.)等[54]。到20世纪90年代后,酸性脲酶已被应用于实际生产,但是受限于酸性脲酶的活性和产量,该方法的成本还未能得到控制。2006年,Fidaleo等[55]建立了葡萄酒中脲酶降解尿素的拟一级动力学模型,并指出了苹果酸和pH是其中最重要的可控变量[56]。最近,有研究将罗伊乳杆菌(Lactobacillusreuteri)CICC6124中的酸性脲酶基因簇转移到乳酸乳球菌(Lactococcuslactis)内构建细胞工厂,在优化条件后,脲酶的产量从1550 U/L提高到了11560 U/L,极大地扩展了脲酶的应用前景[57]。
3.2.2 氨基甲酸酯酶 氨基甲酸酯酶(Urethanase)是能将EC直接分解成乙醇和氨的酰胺类酶。1990年,Kobashi等[58]在小鼠粪便中分离得到了一株柠檬酸杆菌具有生产该酶的能力,但是该菌产生的氨基甲酸酯酶在高浓度乙醇和酸性条件下没有活性,不能用于实际应用。随后发现的一些具有乙醇和酸性环境抗性的氨基甲酸酯酶在其他菌株中被发现,但仍受限于酶的降解活性[59-60]。这个问题直到研究人员在大肠杆菌(Escherichiacoli)中表达外源基因才最终得以解决[44]。另一方面,通过固定化(藻酸钙/壳聚糖)很大程度地提高了产酶菌株对胁迫环境的抗性,提高了降解效率[61]。
3.3 代谢工程路径
该方法是对发酵微生物的代谢路径进行人为改造,减少其代谢终产物中尿素的含量,进而控制EC的水平。目前,有两种代谢调控方法被广泛应用。
3.3.1 尿素生成与代谢调节 在酿酒酵母中,尿素由精氨酸通过精氨酸酶(由CAR1编码)分解精氨酸产生,降低精氨酸酶基因的表达水平可以减少尿素生成(图2)。1990年,Suizu等[62]首先在单倍体酵母菌株中敲除CAR1而使其丧失了精氨酸酶表达能力,该菌的生长和发酵水平和野生型相比没有明显差别,具有工业化应用的潜力。在此基础上,精氨酸酶缺陷的二倍体纯合子(car1/car1)酵母[63-65]也被成功构建。除了基因工程手段外,乙基甲磺酸酯(Ethyl Methanesulfonate,EMS)也作为诱变剂用于获得car1突变体,经过诱变得到的突变体菌株也能达到类似效果[66]。此外,反义RNA和RNA干扰技术也逐渐被用于抑制酿酒酵母CAR1的表达[67]。在野生型酵母(CAR1/CAR1)的污染问题上,编码蛋白毒素和抗体的dsRNA质粒已被开发用于杀死野生型[68]。
目前,酿酒酵母精氨酸酶表达活性的缺失尚不能完全阻断尿素和EC的产生,而精氨酸在发酵液中大量积累则会引起流体动力学和酒体风味的变化。为了缓解这一矛盾,研究人员进一步提出通过基因工程手段让酵母细胞增强对尿素的代谢分解作用。该方法共涉及三个基因的改造,其中DUR1,2(编码尿素酰胺酶)与尿素的转运和代谢有关,DUR3(编码尿素转运蛋白)与尿素的跨膜运输有关(图2)。2006年,Coulon等[69]将DUR1,2通过酿酒酵母PGK1表达系统整合到了工业葡萄酒酵母(UC Davis 522)UPA3基因座中,获得了基因型、表型和转录组几乎等同于亲本的工程菌,使葡萄酒中的EC含量降低了89.1%。该方法也在成功应用于清酒中[70]。进一步地,李晓明等[71]在酿酒酵母N85中过量表达DUR1,2(N85DUR1,2)的基础上敲除CAR1构建了工程菌N85DUR1,2-c,让EC的控制效果得到进一步提升。在另一方面,DUR3的过量表达能够促进非尿素降解型酵母从胞外重新吸收尿素,同样达到降低发酵环境中尿素含量的目的[72-73]。
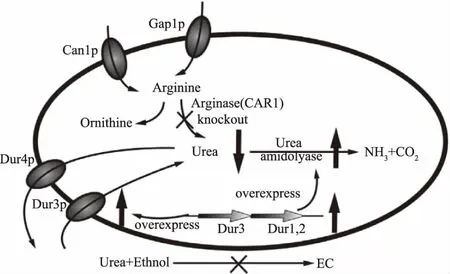
图2 两种代谢工程技术抑制尿素的积累[43]
除了转录水平调节外,Dur3p的泛素化修饰对尿素转运也有显著影响,张鹏等[35]通过定点突变将酿酒酵母Dur3p中两个潜在的泛素化位点——赖氨酸残基K556和K571突变为精氨酸作为替代。相对于Dur3p,突变菌Dur3pK556R在添加尿素和谷氨酰胺的YNB培养基中泛素化水平相对降低了20.1%,对应的,尿素和EC含量在黄酒模拟发酵中分别降低了41.3%和55.4%。
3.3.2 NCR调节 如前文所述,尿素的分解代谢受到NCR的限制,抑制NCR正调控因子(Gln3p和Gln1p)核定位信号(Nuclear Location Sequence,NLS)的中磷酸化和负调控因子Ure2p的表达,可使优质氮源对酵母DUR1,2和DUR3的表达抑制降至最低。赵新睿等[74]通过突变酿酒酵母中NLS的磷酸化位点并敲除了URE2基因,让酿酒酵母中DUR1,2和DUR3的表达得到显著激活。
代谢工程方法对控制葡萄酒、清酒及黄酒中的EC含量有很大助益,但并不适用于发酵体系异常复杂的酒类,如白酒。不过,有新的研究发现白酒发酵过程的乳杆菌能够通过ADI途径与酵母竞争性地降解精氨酸[75-76],一些芽孢杆菌已被开发用于控制白酒发酵中的EC产生。
4 总结与展望
目前,已有大量的调查研究表明人类的全因死亡率与酒精摄入量密切相关。尽管酿造酒中的乙醛是引起癌症的主要物质,在对EC致癌风险的评估中也无法排除其与EC的交互作用,但EC毒理学研究的现有成果已经可以说明EC对人体的致癌作用是不可忽视的。因此,过去人们也致力于研究EC在酿造酒中的形成机制以及对应的控制措施。但至今为止,能够应用于实际生产中的控制措施仍然有限。对于那些会引起酒体风味以及营养成分发生改变的控制措施,还需要结合实际的生产过程进行反复验证才能达到理想的平衡效果。而基因工程手段在与发酵食品有关的应用上需要慎重,可以考虑在发酵过程利用体系中的内源微生物来降解的EC前体物质,特别是对复杂微生物体系的白酒而言。总而言之,中国酿造酒中的EC含量高于风险阈值的情况常有发生,需要针对EC的控制措施做更多地深入研究。另一方面,酿造酒中EC的超标现状与缺少国家标准的指导不无关系,随着人们对EC致癌风险的认知逐步加深,建立相关标准已经势在必行。

