镉和铅联合作用对黑腹果蝇发育及抗氧化的影响
王博,张春红,林欣大
1. 浙江中医药大学中医药科学院,浙江 杭州 310053;2. 中国计量大学生命科学学院,浙江 杭州 310018
Cd2+和Pb2+作为环境中主要的重金属污染物,它们广泛存在于农作物及地下水中且蓄积性强(He et al.,2013)。二者常通过消化及呼吸系统进入人体,并在肝脏及肾脏中积累,引起肺部、肾脏和心血管系统病变(Roggeman et al.,2014;Llobet et al.,2013)。大约 95%的 Pb2+沉积于骨骼中,可引起血红蛋白紊乱并损伤神经系统、肾脏以及生殖器官,并诱发心血管、神经、生殖以及消化系统疾病的产生(Madsen et al.,2013;Wang et al.,2012;Xu et al.,2016;Chandler et al.,2016)。生物体持续暴露在Cd2+污染环境中会导致其在体内积累,并影响发育、生存及繁殖力(Annabi et al.,2012;Rudel et al.,2013;Nawab et al.,2015)。
MTNs蛋白包含的巯基基团,能与重金属结合从而达到解毒作用(Li et al.,2011;Chiaverini et al.,2010;Koivula et al.,2010)。体内实验表明,Cd2+结合MTNs蛋白并以非毒性形态沉积(Jensen et al.,2010;Yang et al.,2011)。过去有研究表明,抗氧化作用在长期 Cd2+诱导的肝脏及肾脏毒性疾病中扮演着重要角色(Li et al.,2011)。研究发现在Cd2+积累组织中MTNs表达量很高(Xu et al.,2016;Jihen et al.,2009;Liu et al.,2009),MTNs作为活性氧清除剂可清除生物体内活性氧自由基(ROS)(Li et al.,2011;Sabolić et al.,2010),当 MTNs蛋白缺失时重金属对生物体带来的毒性作用可能会进一步增强。Pb2+在生物体内以磷酸氢盐的形式存在,它对巯基基团具有高度亲和性。生物体内积累的Pb2+能够抑制生物体生长并提高致死率,对 DNA造成氧化损伤,通过促进 ROS的形成破坏脂质和蛋白质结构(Lin et al.,2015;Miranda et al.,2012;Pan et al.,2011)。当给小鼠饲喂含 Pb2+溶液后,Pb2+能直接降低红细胞中的血铜蛋白超氧化物歧化酶SOD活性(Lee et al.,2011)。此外Pb2+能通过前氧化损伤以及打破细胞抗氧化平衡最终引起机体氧化损伤(Jin et al.,2013)。Gsts(glutathione S-transferase,GST)是一系列能够保护血红蛋白因过氧化氢和 ROS造成氧化损伤的酶,它们能够结合包括重金属离子在内的外部有毒化合物,通过将其从生物体内排除,达到中和、解毒和保护机体免受氧化性损伤的作用(郑双艳等,2019)。
Cd2+和Pb2+在环境中通常以复杂化合物形式存在,尽管这两种重金属对生物体中具有不同影响且各自具有其特有的毒作用机制,然而当它们同时存在于机体内常会表现出拮抗或协同叠加两种不同效应。例如当小鼠在二者的共同作用下,相比单独暴露于同等浓度的Cd2+或Pb2+中反而表现出较低毒性(Ge et al.,2011;Xu et al.,2012)。研究小鼠发现肾脏中存在的Cd2+能有效降低Pb2+的毒性,并减少主要功能性酶的活性(Chiaverini et al.,2010)。二者联合后对肝脏的氧化损伤相比同样浓度的Cd2+单独存在下反而更低,即这两种重金属在小鼠中发挥了拮抗作用(Chereddy et al.,2011;Karwowska et al.,2012;Alslaibi et al.,2014)。然而有时Cd2+和Pb2+却表现出协同叠加效应,例如二者联合作用后,能显著破坏小鼠睾丸支持细胞线粒体,从而对细胞结构完整性造成影响;此外二者联合还能显著降低小鼠大脑干重,引起大脑氧化损伤,二者通过联合胁迫作用使得毒性作用大大加强(Garcia et al.,2004;Antonio et al.,2003;Bizarro et al.,2013;Mahaffey et al.,1977;Zhang et al.,2009)。
黑腹果蝇(Drosophila melanogaster)作为模式生物基因被研究得最为透彻,其短暂的生命周期和大量的基因工具使得研究更方便,它的基因与人类许多疾病基因具有同源性(万永奇等,2016),因此在本研究中,对果蝇分别饲喂 Cd2+、Pb2+和Cd2++Pb2+,并通过测定其化蛹率和羽化率、抗氧化性、MTNs和Gst基因的表达水平,从而探究重金属Cd2+和Pb2+及二者联合对黑腹果蝇的作用效果,以此揭示二者的毒作用机理,为进一步研究及评估Cd2+和Pb2+的毒性机理提供一定的理论依据。
1 材料和方法
1.1 实验动物
野生型黑腹果蝇(Oregon R,OR),培养温度为 25 ℃,相对湿度为60%,光周期为昼∶夜=14∶10。基础培养基配方:每100 mL水中包含11.3%玉米粉,1%琼脂,8.6%蔗糖,1%酵母和 1%丙酸,培养基pH为5.5。葡萄汁培养基配方:每30 mL水中包含蔗糖2.2 g,琼脂1.4 g,冰醋酸1 mL,葡萄汁10 mL。
1.2 方法
1.2.1 Cd2+/Pb2+处理
称取CdCl2和Pb(NO3)2粉末,分别配制成浓度为 0.5 mol·L-1和 3 mmol·L-1的母液,用移液器吸取不同体积母液,将 Cd2+/Pb2+或 Cd2++Pb2+母液溶解在标准玉米糊培养基中,根据课题组先前的预实验结果,分别配制 0.05、0.1、0.3、0.5 mmol·L-1的Cd2+处理食物(下文简写为Cd0.05、Cd0.1、Cd0.03和 Cd0.5),0.2、0.5、1.5、2.9 mmol·L-1的 Pb2+处理食物(下文简写为Pb0.2、Pb0.5、Pb1.5和Pb2.9),以及 0.05 mmol·L-1Cd2++0.2 mmol·L-1Pb2+,0.1 mmol·L-1Cd2++0.5 mmol·L-1Pb2+,0.3 mmol·L-1Cd2++1.5 mmol·L-1Pb2+, 0.5 mmol·L-1Cd2++2.9 mmol·L-1Pb2+的 Cd2++Pb2+联合处理食物(下文简写为 Cd0.05+Pb0.2、Cd0.1+Pb0.5、Cd0.03+Pb1.5和Cd0.5+Pb2.9)。对照组为不含Cd2+/Pb2+的标准培养基(下文简写为CK)。将果蝇成虫放置在葡萄汁培养基中过夜产卵,收集培养基中孵化8 h内的1龄幼虫,转移至基础培养基以及包含不同浓度Cd2+/Pb2+的培养基中进行培养。
1.2.2 原子吸收实验
收集 Cd2+/Pb2+处理组和对照组中羽化 3 d成虫,通过原子吸收光谱仪(PerkinElmer700,USA)测定果蝇中Cd2+/Pb2+含量。用去离子水漂洗果蝇虫体,每次5 min,共3次。之后用63%的浓HNO3和 30% H2O2对果蝇进行微波消解,消解温度为37 ℃,消解时间2 h。每组实验包含雌雄果蝇成虫各5只,共设置3个重复。测定Cd2+和Pb2+的条件如下:
Cd2+(Flame:C2H2∶O2=17 L·min-1∶2 L·min-1;slit:0.7 nm;Light energy:39;Micro-current:4 mA;Wavelength:228.3;Light:C-HCL;Lamp:Cd2+);
Pb2+(Flame:C2H2∶O2=17 L·min-1∶2 L·min-1;slit:0.7 nm;Light energy:58;Micro-current:10 mA;Wavelength:283.3;Light:C-HCL;Lamp:Pb2+)。
1.2.3 化蛹和羽化率试验
将 1龄幼虫从葡萄汁培养基中转移至不同Cd2+/Pb2+处理以及对照培养基中,每日观察果蝇的化蛹情况并记录羽化数量,计算化蛹率和羽化率。试验共设置 4组重复,每个重复包含20只果蝇。
1.2.4 超氧化物歧化酶(SOD)活性、过氧化氢酶(CAT)活性和丙二醛(MDA)含量测定
取 20只果蝇成虫研磨制成组织匀浆,根据Bradford法测定蛋白质浓度。采用试剂盒(南京建成生物工程有限公司)上的方法测定 SOD、CAT活性以及MDA含量。每一组设置10个重复。酶活性计算方式如下:
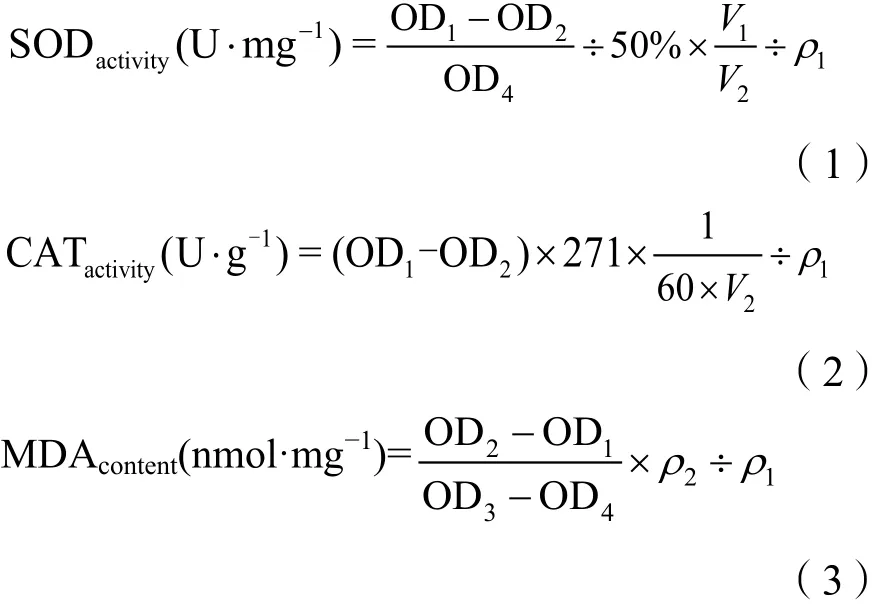
式中,OD为样品在可见分光光度计550 nm处的吸光度,OD1为对照OD值,OD2为测定OD值,OD3为标准OD值,OD4为空白OD值;V1为反应液总体积;V2为取样量;ρ1为待测样本蛋白浓度,mg·mL-1;ρ2 为标准品浓度,10 nmol·mL-1。
1.2.5 QRT-PCR
通过黑腹果蝇基因组数据库(http://flybase.org/),采用 BLAST的方法筛选出MTN及其他基因序列,并根据以上查找的序列设计用于荧光定量PCR的引物(表1)。根据说明书上的方法采用RNAiso Plus试剂盒(Takara,Dalian,China)提取CK及Cd0.5+Pb2.9处理组7日及28日龄成虫总 RNA,以 RNA为模板采用SuperScriptTM II RTase(TaKaRa,Dalian,China)试剂盒反转录cDNA。通过荧光定量PCR和相对定量2-△△Ct法检测不同基因在不同时间段的相对表达量(Livak et al.,2001)。PCR 程序为第一阶段95 ℃预变性1 min;第二阶段95 ℃保持10 s,60 ℃保持25 s,45个循环。
1.2.6 统计分析
运用 Excel对以上各实验数据进行整理及作图。运用SPSS对 SOD、CAT、MDA和荧光定量PCR数据进行单因素方差分析(One-way ANOVA)以及LSD多重比较,采用独立方差t检验分析重金属含量数据。
2 结果与分析
2.1 果蝇中Cd2+/ Pb2+含量
由图1可知,在单独Cd2+和Pb2+处理下,随着培养基中Cd2+/Pb2+浓度的上升果蝇体内Cd2+及Pb2+含量随之上升。例如Cd0.05处理下果蝇体内平均Cd2+积累量为0.02 μg左右,然而在Cd0.5处理下,果蝇体内Cd2+积累量上升至0.2 μg左右;同样地,在Pb0.2处理下果蝇体内Pb2+含量约为0.15 μg,当Pb2.9处理下果蝇体内Pb2+积累量上升至0.7 μg左右。由此表明,果蝇中Cd2+和Pb2+的积累量具有剂量依赖性。此外当同时加入Cd2+和Pb2+后,果蝇中Cd2+和Pb2+积累量均高于单独Cd2+或Pb2+处理。例如在Cd0.05+Pb0.2处理下,较单独Cd0.05处理,Cd2+积累量从0.02 μg上升至0.3 μg左右;较单独Pb0.2 处理,Pb2+积累量从 0.15 μg 上升至 0.3 μg 左右。其他各浓度处理下规律相似,即二者以协同方式相互促进积累。
2.2 镉和铅对果蝇化蛹率和羽化率的影响
为了研究果蝇体内积累的Cd2+和Pb2+是否影响其发育,测定了果蝇的化蛹率和羽化率。结果表明,相比CK、Cd0.05和Cd0.1处理组,Cd0.3和Cd0.5处理下化蛹率从90%左右下降至70%左右,羽化率则从85%下降至70%以下。各浓度Pb处理下化蛹率和羽化率较CK均有所下降,在Pb1.5和Pb2.9处理下,化蛹率和羽化率甚至均降低至50%左右。在 Cd0.05+Pb0.2处理下,果蝇化蛹率和羽化率和CK相比均无显著性差异,甚至高于 Pb0.2处理。然而在 Cd0.1+Pb0.5、Cd0.3+Pb1.5和 Cd0.5+Pb2.9的联合处理下,化蛹率和羽化率较单独 Cd2+/Pb2+处理显著下降(P<0.05),化蛹率从 90%分别下降至 70%、60%和 50%左右,羽化率从 85%下降至64%、49%和 28%(P<0.05)(图 2)。
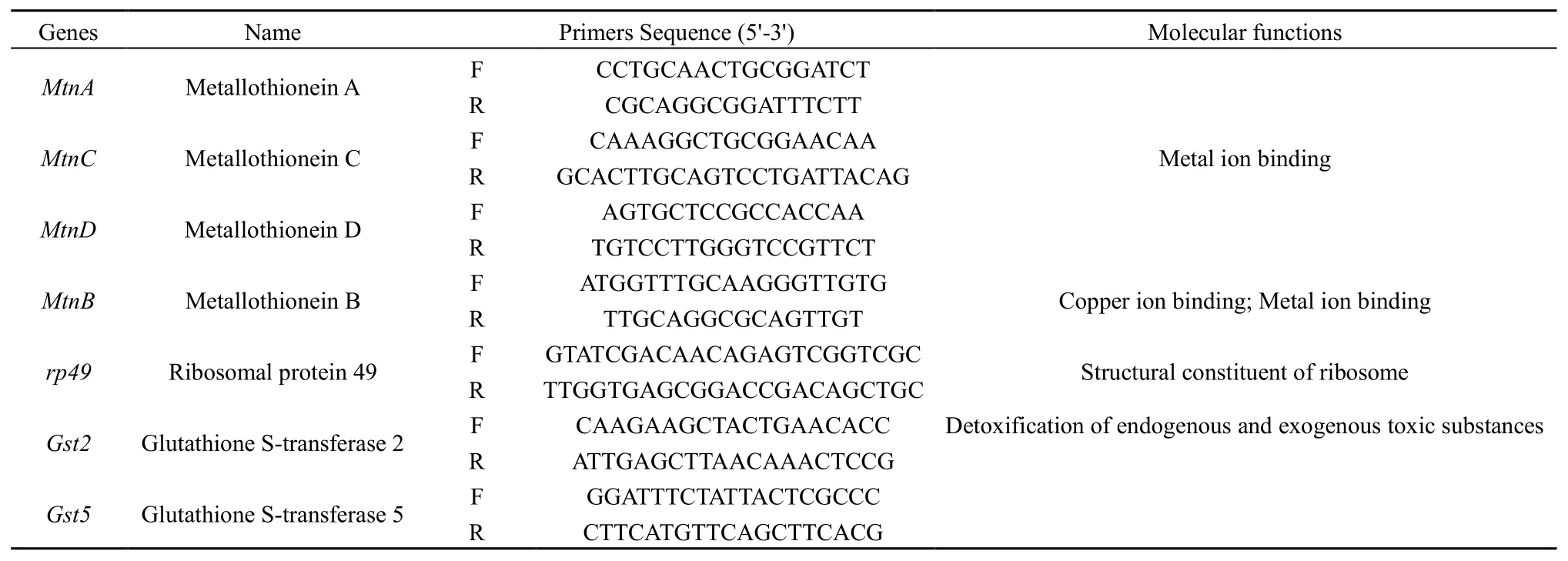
表1 荧光定量PCR引物Table 1 Primers for QRT-PCR
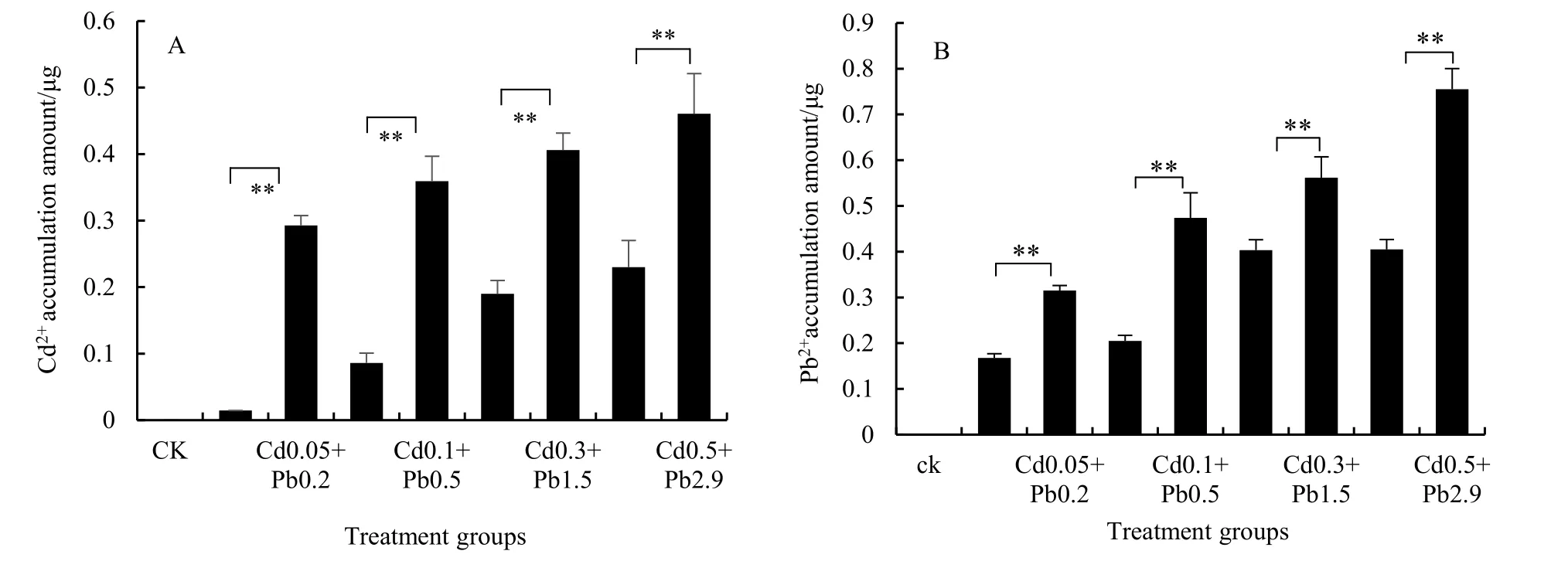
图1 不同处理组中果蝇Cd2+/Pb2+积累量Fig. 1 Accumulation amount of Cd2+/Pb2+ in Drosophila melanogaster in different treatments
2.3 Cd2+/Pb2+对SOD、CAT活性及MDA含量的影响
图 3表明,在 Pb2+及 Cd2+和 Pb2+组合处理下CAT活性较Cd2+显著增加;此外Cd2+和Pb2+表现为协同作用,二者共同处理下 CAT活性均高于单独Pb2+/Cd2+处理。例如在 Pb2.9处理下 CAT活性为0.26 U·g-1,Cd0.5 处理下 CAT 活性低至 0.15 U·g-1,而Cd0.5+Pb2.9处理下CAT活性高达0.4 U·g-1。类似地,Cd2+处理下SOD活性最低,Pb2+处理次之,Cd2+和Pb2+表现出最高的SOD活性。CK组下SOD活性为112 U·mg-1,而Cd0.05处理下SOD反而上升至 128 U·mg-1,而 Cd0.1、Cd0.3和 Cd0.5下 SOD活性均降至90 U·mg-1以下。Pb0.2处理下SOD下降为91.5 U·mg-1,其余Pb2+处理下SOD活性均高于Cd2+。Cd0.05+Pb0.2和Cd0.3+Pb1.5处理下SOD活性最低;但在Cd0.5+Pb2.9联合处理下,SOD活性显著上升122.5 U·mg-1。在Cd0.05+Pb0.2联合处理下,MDA含量高于单独Cd0.05和Pb0.2处理,为1.14 nmol·mg-1,相比之下Cd0.05和Pb0.2处理下 MDA 含 量 仅 为 0.56 nmol·mg-1和 0.62 nmol·mg-1。然而Cd0.1+Pb0.5处理下 MDA 为 0.79 nmol·mg-1,反而比 Pb0.5 处理下的 0.93 nmol·mg-1更低;Cd0.5+Pb2.9处理下 MDA含量为 0.81 nmol·mg-1,同样低于单独 Cd0.5处理下的 1.25 nmol·mg-1(图 3)。
2.4 Cd2+/Pb2+对MTNs和Gsts表达水平的影响
由于在有限的时间段内不能明显地观察到重金属处理效果,而果蝇在长时间处理下又不能良好生长,因此根据之前的实验结果,在 Cd0.5+Pb2.9联合处理下,选取7日和28日龄的果蝇成虫通过荧光定量PCR检测MTNs和Gsts的表达水平。结果表明(图4),7日龄成虫中,Cd2+/Pb2+以及二者共同处理下,MTNB和MTND水平较对照组表达量显著上升(P<0.05)。在 Cd0.5处理下,MTNB和MTND较CK表达量分别提高1400倍和600倍左右;在Cd0.5+Pb2.9处理下,MTNB和MTND较CK表达量分别提高4000倍和1600倍左右,即Cd2+和 Pb2+联合处理上调 MTNs表达水平的效果高于Cd2+/Pb2+单独处理。在 28日龄成虫中,MTNB和MTND表达量较7日龄成虫低,在Cd0.5+Pb2.9处理下MTNB和MTND仅为CK的130倍和120倍。在7日龄成虫中,Cd0.5和Cd0.5+Pb2.9处理下,MTNA、MTNC、Gst2和Gst5表达量同样显著上升(P<0.05),为CK的20-50倍;单独Pb2.9处理对各基因的表达量没有影响。在28日龄成虫中,3组处理下MTNA、MTNC、Gst2和Gst5表达量较对照均显著上升(P<0.05),为CK的20-90倍。
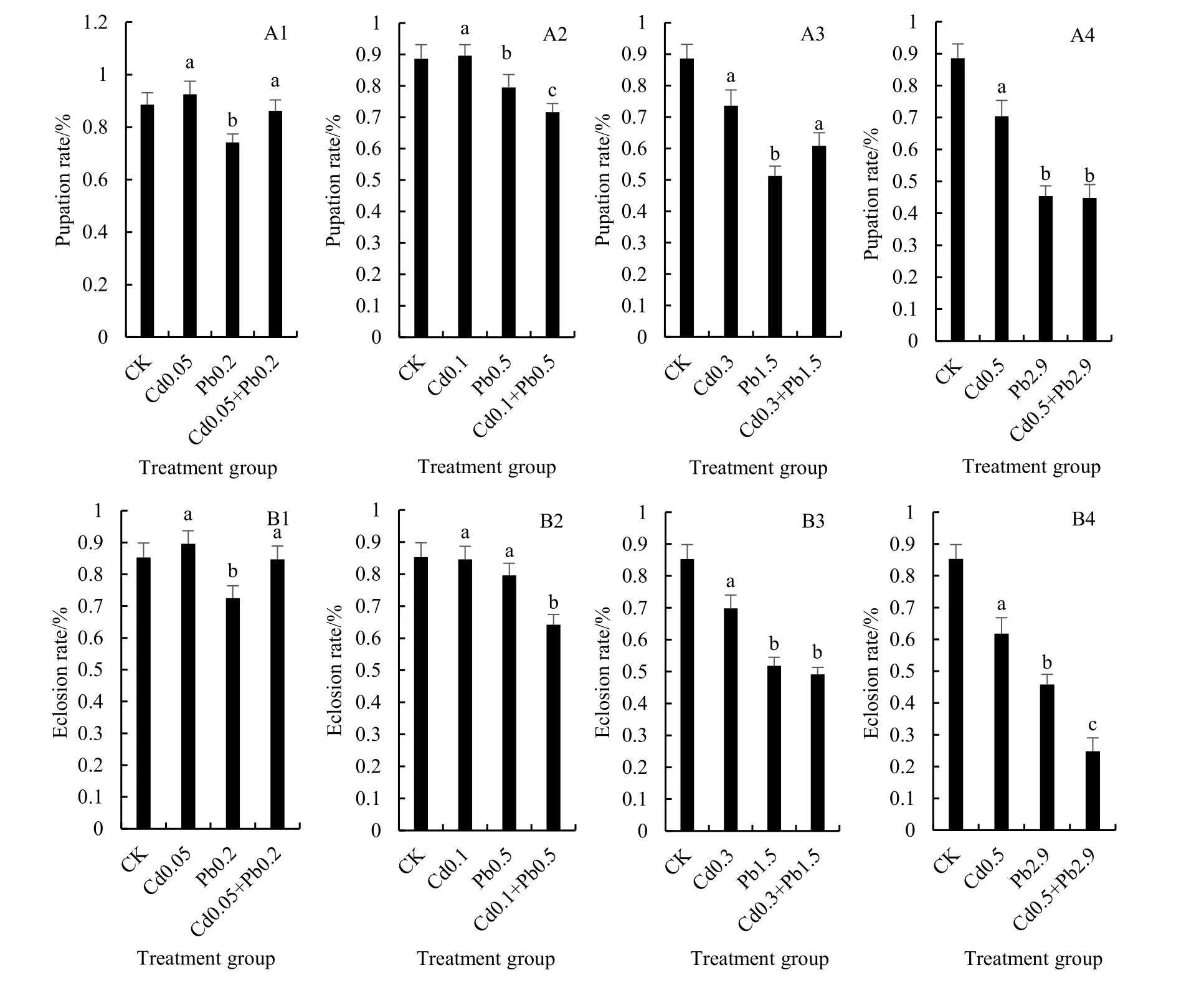
图2 Cd2+/Pb2+处理下果蝇的化蛹率(A)和羽化率(B)Fig. 2 The pupation (A) and eclosion (B) rates of Drosophila after treatment with Cd2+/Pb2+
3 讨论
本研究结果表明,Cd2+/Pb2+的积累量具有剂量依赖性。并且当果蝇饲养在同时包含 Cd2+和 Pb2+的培养基中,其体内Cd2+或者Pb2+的吸收量更高。这暗示在果蝇体内二者的积累具有相互促进的协同作用。然而研究小鼠肺组织发现,重金属的组合反而减少了Pb2+的吸收(Fortoul et al.,2005),这是由于 Cd2+/Pb2+的吸入引起了非髂细支气管细胞和纤毛细胞数量的下降,导致支气管上皮形态发生改变,致使Pb2+浓度反而下降。由于本研究中果蝇依赖取食积累重金属,而小鼠则通过呼吸积累重金属,因此推断造成以上结果差异的原因可能是昆虫和哺乳动物在重金属吸收和应答方面存在差异。
低浓度的Cd2+促进果蝇生长,这可能是因为低浓度的 Cd2+激活了保护果蝇免受外界损伤的相关酶系。然而高浓度的Cd2+抑制果蝇生长,这可能是由于自我保护能力不足以抵抗外界高浓度重金属的毒害作用。高浓度Pb2+对果蝇的生长表现出抑制作用,但是低剂量组对果蝇的影响微乎其微。Cd0.1+Pb0.5、Cd0.3+Pb1.5和 Cd0.5+Pb2.9联合处理均抑制果蝇生长,且二者联合作用较单独Cd2+/Pb2+处理下化蛹率和羽化率显著下降,即两种重金属具有协同作用。此外对于果蝇个体,无论是Cd2+或 Pb2+单独处理,或是 Cd2++Pb2+共同处理,Cd2+都扮演着主要作用。过去有研究表明 Cd2+与Pb2+能显著影响怀孕小鼠肝糖原含量和支气管上皮细胞形态,并且这种影响主要是Cd2+介导的,这与Cd2+扮演着主要作用的结果相一致(Pillai et al.,2005)。
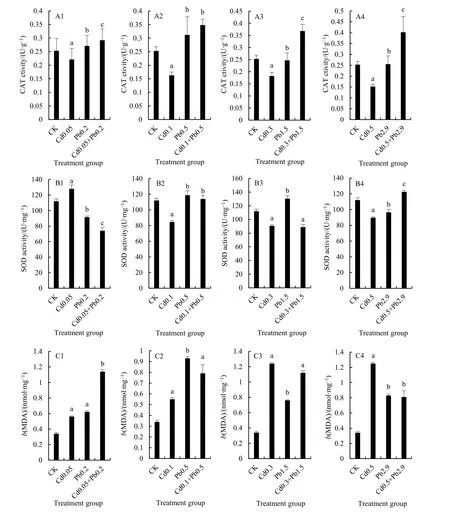
图3 不同处理下的CAT(A)、SOD(B)活性和MDA(C)含量Fig. 3 The CAT (A), SOD (B) activity and MDA (C) contents with different treatment
生物体消除活性氧自由基是一个动态平衡的过程。本研究测定了氧化氢酶CAT、超氧化物歧化酶SOD的酶活性,以及自由基产物MDA的动态变化,用于评估Cd2+和Pb2+对果蝇抗氧化能力的影响。结果表明Cd2+和Pb2+在果蝇抗氧化能力方面具有剂量依赖性,并且二者之间表现出了拮抗特性(Rani et al.,2014)。
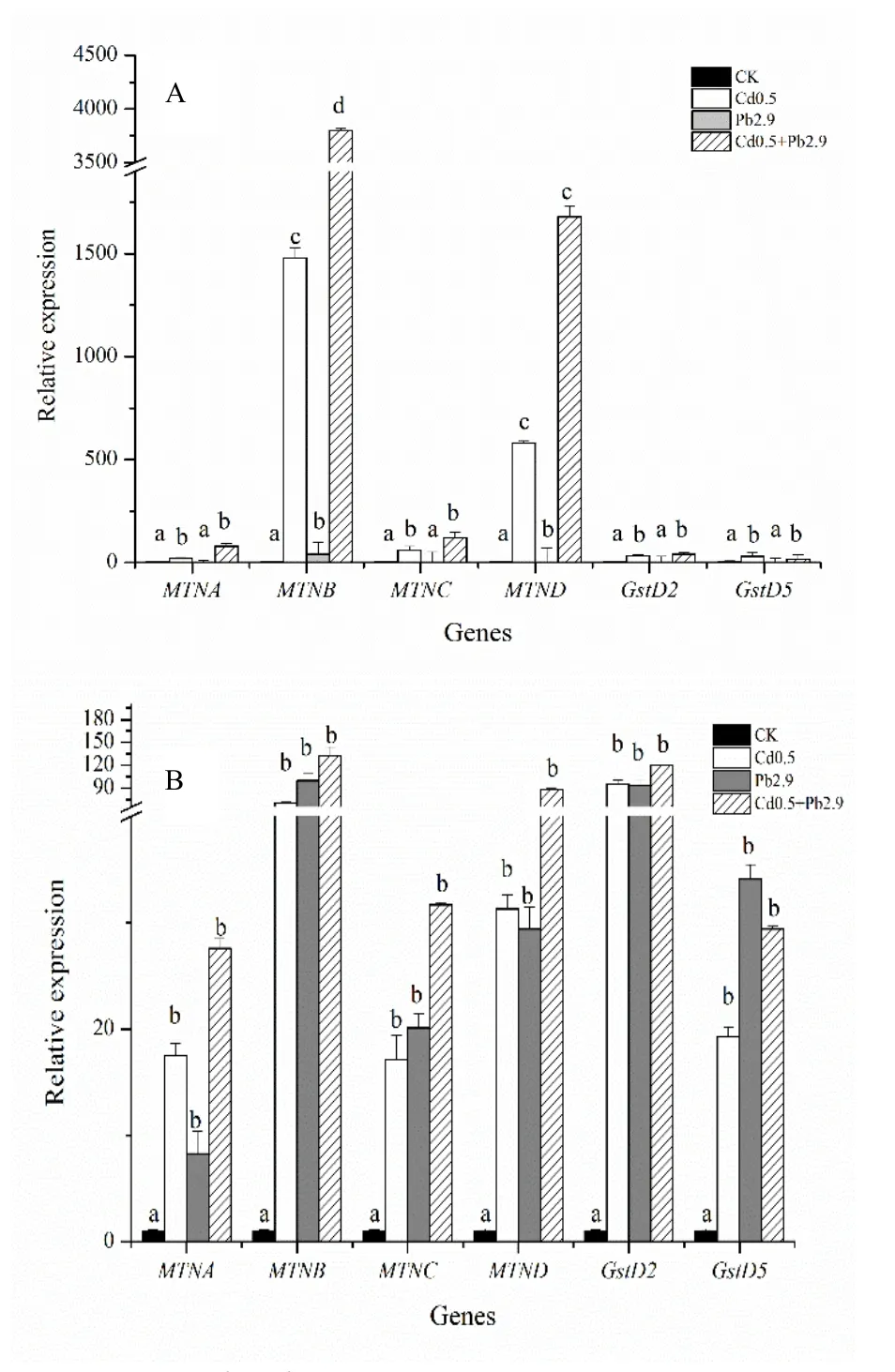
图4 在Cd2+/Pb2+作用下与重金属解毒相关基因的表达谱Fig. 4 The effects of Cd2+/Pb2+ on the expression profiles of detoxifying genes
果蝇在低浓度的 Cd2+处理下较对照组具有较高的SOD活性,然而MDA含量依然维持在较低水平。作为对重金属的反应,生物体通过清除体内自由基以缓解Cd2+带来的氧化损伤,并且这种手段对于保护机体是足够的。然而果蝇经低浓度的 Cd2+处理后,相对对照组发育周期显著降低,且化蛹和羽化率显著上升。此结果表明,清除氧化损伤的系统在低浓度的Cd2+刺激下被激活,用于降低氧化损伤,并且促进了果蝇生长发育,随着Cd2+浓度上升,SOD及CAT活性降低,MDA含量显著上升,导致氧化损伤加剧,并导致抗氧化能力达到极限且不足以清除体内自由基,最终延缓果蝇的生长和发育(Xia et al.,2016)。
当饲喂低浓度 Pb2+后,CAT和 SOD活性及MDA含量显著上升,这表明在低浓度Pb2+环境下,机体可提升抗氧化能力用于应对Pb2+的毒害作用。然而,Pb2+是脂质过氧化物 MDA的诱导物,由于有限的抗氧化能力不足以保护机体免受氧化损伤最终随着Pb2+浓度的上升MDA含量也随之增加。机体内抗氧化系统是动态变化的,为了应对活性氧自由基,过度增加的Pb2+由于超过了其自我保护能力范围,引起果蝇生长力的降低。
Cd2+和 Pb2+能够对小鼠大脑的氧化损伤起到协同促进作用,然而在小鼠肝脏中却发现了拮抗影响(Massó et al.,2007)。本研究发现当 Cd2+和 Pb2+协同作用于果蝇,随着重金属浓度的增加MDA含量同样增加。此外CAT活性的增加同样关系到清除活性氧自由基的功能。本研究发现果蝇针对不同剂量的重金属浓度及组合方式具有不同的应答方式,这种方式是动态变化的,而不是简单的拮抗或协同作用。
重金属能够诱导 MTNs的表达,研究表明MTNs能在痕量重金属刺激下发生改变,通过形成复合物以及其他手段来缓解重金属的毒性(Chandler et al.,2016;Yang et al.,2011;Sabolić et al.,2010;Valko et al.,2005)。本研究中,我们检测了果蝇中一系列MTNs基因的表达水平,研究发现MTNB和MTND在不同浓度的处理组中均有高表达,尤其是在 Cd2+和 Pb2+共同处理组中。有报道表明MTNB对Cd2+极为敏感,MTND和MTNB有着同样功能(Chiaverini et al.,2010)。研究 MTNB的启动子,发现Cd2+可作为MTNB的启动子诱导其表达(Egli et al.,2010)。MTNs的高表达对于缓解Cd2+毒性作用具有重要作用。
在Cd2+处理下,GstD2和GstD5在成虫阶段的第7天和第28天上调。在单独的Cd0.05,Pb1.5以及Cd0.05+Pb0.2处理组下,7日龄成虫阶段MTNB和MTNC以及MTND表达水平高于28日龄成虫,导致了对不同 Cd2+和 Pb2+的应答反应。低浓度的Cd2+能够激活机体内排毒机理,增加 SOD和 CAT活性,加强解毒基因的表达,例如MTNA、MTNB、MTNC、MTND、GstD2和GstD5。然而Cd2+需在高浓度水平下才能激活此能力。两种重金属在低剂量协同作用下可被果蝇机体吸收,并刺激和重金属解毒相关基因表达量的上升从而缓解重金属对果蝇生长产生的副作用。
4 结论
(1)果蝇中Cd2+和Pb2+含量随着培养基中重金属浓度的上升而增加,Cd2++Pb2+联合处理后 Cd2+和Pb2+积累量较单独加入Cd2+或Pb2+均有所上升,二者具有协同吸收效应。
(2)低浓度的 Cd2+促进果蝇发育,高浓度的Cd2+抑制其发育;高浓度的Pb2+会抑制其发育。Cd2+和Pb2+的联合处理抑制果蝇的发育,抑制作用随着Cd2+/Pb2+浓度的增加而增强。
(3)Cd2+/Pb2+联合处理较单独Cd2+/Pb2+处理显著提高CAT活性,Cd0.5+Pb2.9引起SOD活性显著上升,Cd0.05+Pb0.2处理较单独Cd0.05或Pb0.2处理显著提升MDA含量。
(4)Cd2+/Pb2+处理下MTNs和Gsts表达水平显著升高。

