异甘草酸镁注射液预防血液肿瘤化疗相关肝损伤多中心临床协作研究*
李国辉,陈任安,王文清,秦炜炜,赵万红,姚亚洲,张启科,张亚莉,黄国强,田培军,张福林,贺鹏程,葛繁梅0,王 一,宋艳萍,耿 惠,王存邦,王景昌,刘 利△
1.空军军医大学唐都医院(西安710038);2.西安交通大学第二附属医院(西安710004);3. 陕西省宝鸡市中心医院(宝鸡721008);4.甘肃省人民医院(兰州730000);5. 陕西省咸阳市中心医院(咸阳712000);6. 陕西省汉中市中心医院(汉中 723000);7. 陕西省安康市中心医院(安康725000);8. 陕西省延安市人民医院(延安716000);9.西安交通大学第一附属医院(西安 710061);10.延安大学附属医院(延安716000);11.陕西省人民医院(西安710068);12.西安市中心医院(西安710004);13.青海大学附属医院(西宁810001);14.兰州战区陆军总院(兰州730050);15.解放军第三医院(宝鸡721004)
肝脏作为药物代谢的主要器官,特别容易受到化疗药物的损伤,导致药物性肝损伤(Drug-induced liver injury,DILI)。据WHO统计,DILI已经成为全球肝病死亡原因的第5位。对于血液肿瘤患者,DILI已成为我们日常工作必须面对的问题。然后,目前需要大样本的数据反映国内血液肿瘤化疗药物DILI的临床发生情况,并研究异甘草酸镁对不同化疗药物引起DILI的治疗作用,指导临床规范用药。为此,我们设计了异甘草酸镁防治恶性血液疾病化疗肝损伤的多中心的临床研究,现将结果报告如下。
资料与方法
1 一般资料 本研究采用多中心前瞻性、开放、观察性研究设计,主要指标为观察肝功能正常患者化疗后肝损伤发生率和肝功能异常患者肝损伤程度,次要观察指标为异甘草酸镁用药的安全性。病例入选标准:①年龄大于18岁; ②住院且接受化疗的恶性肿瘤患者;③要求化疗方案:含蒽环类药物的方案,每周期剂量≥20mg/m2;或含鬼臼类药物的方案,每周期剂量≥60mg/m2;或含铂类药物的方案,每周期剂量≥80mg/m2;或含环磷酰胺类药物,每周期剂量≥400mg/m2;或含阿糖胞苷类的方案,每周期剂量≥10mg/m2;或含甲氨蝶呤类的方案,每周期剂量≥200mg/m2;或含长春新碱类的方案,每周期剂量≥1.4mg/m2;或含高三尖酯碱类的方案,每周期剂量≥2.5mg/m2;或含门冬酰胺霉类的方案,每周期剂量≥10000U/m2;④机体状况ECOG评分0~2分;⑤血清总胆红素≤1.5×μmol/L;ALT、AST≤2.5U/L;三大常规(血、尿和大便粪)、肾功能和心电图基本正常;⑥预计生存期≥3个月。排除标准:①1周内应用过或正在应用其他甘草酸静脉制剂的患者;②严重的心脏病、肝肾疾病及其他严重器质性病变的患者;③哺乳期和妊娠期妇女;对甘草酸类等防止肝损伤药物有过敏史者;④正在参加其他药物临床研究者。剔除标准:①不符合入选标准者或符合排除标准者;②异甘草酸镁使用﹤7d或每天使用﹤200mg。中止标准:退出研究是指已入选的受试者,在研究过程中出现了不宜继续进行研究的情况,由研究者决定中止或者受试者要求退出本研究。
2 治疗方法 每例受试者完成1个化疗疗程的治疗观察。化疗开始前1d给予200mg的异甘草酸镁注射液(正大天晴药业集团股份有限公司生产)静脉滴注,1次/d,连续用药至1个化疗疗程结束后,异甘草酸镁注射液用药须≥7d(至少不少于5d)。
3 评价指标
3.1 有效性评价:主要是肝功能生化指标,肝功能(ALT、AST、T-BIL、D-BIL、ALP和GGT):用药前3 d内、用药1周后或出院前检查1次,共2次。评价应用化疗药物后肝损伤的发生率。
3.2 安全性评价;根据NCI-CTCAE 4.0版标准,严密观察化疗前、后实验室检查结果正常或异常的变化情况,判断该改变与异甘草酸镁注射液和(或)化疗药物的关系。
4 统计学方法 遵循意向性治疗原则(Intention to treat,ITT),包括至少使用过1次研究用药的受试者全部纳入全分析集(Full analysis sets,FAS)分析;按照方案的要求使用了研究用药、没有使用违禁药物、并且无严重违反方案的受试者归入符合方案集(Per-protocol sets,PPS)分析;使用过试验药品并至少有1次安全性评价记录的病例即纳入安全性分析集(Safety set)分析;而脱落定义为任何原因致受试者不能完成方案和要求的随访,不能够进行有效性和安全性评价者。
本研究的主要分析为肝功能异常率的差异性检验,化疗前后肝功能异常率及安全性比较采用配对t检验。不同化疗药物对肝功能的影响比较采用Fisher’s精确概率法。两组间比较,所有假设检验采用双侧检验(Two-side test),以P<0.05为差异有统计学意义。
结 果
1 患者一般情况 全国共15家医院参与本研究,共入组1567例接受化疗的恶性血液病患者;有56例未按照研究方案的要求用药,无法进行有效性评价,故纳入FAS分析的为1511例。其中急性髓系白血病552例,急性淋巴细胞白血病115例,慢性粒细胞白血病73例,慢性淋巴细胞白血病24例,淋巴瘤580例,多发性骨髓瘤113例,骨髓增生异常综合征38例,其它16例。男性833例,女性678例,中位年龄49岁,异甘草酸镁中位输注7d(8.09±2.29d)。化疗方案中共包含62种化疗药物,其中应用阿糖胞苷792例,环磷酰胺 325例,吡柔比星221例,甲氨蝶呤199例,伊达比星181例,长春新碱143例,地塞米松142例,三氧化二砷114例,依托泊苷111例,阿克拉霉素 98例,米托蒽醌91例,高三尖杉酯碱90例,醋酸泼尼松75例,福达拉滨71例,培门冬酶69例,地西他滨54例。其他应用例数较少的化疗药物还有阿霉素、表阿霉素、多柔比星、柔红霉素、长春地辛、长春瑞滨、博来霉素、氮烯咪胺、异环磷酰胺等。
2 异甘草酸镁的预防效果 对1511患者化疗前后肝功能进行分析,化疗后ALT、AST、T-BIL、D-BIL、ALP及GGT较化疗前均无增高,反而明显降低,见表1。化疗前ALT、AST、T-BIL、T-BIL、ALP、GGT正常的患者分别为969例、1151例、928例、1181,1394,1158例,化疗过程部分患者出现不同程度肝损伤,其中T-BIL异常率最高,为15.19%,其它指标异常率分别为3.2%、1.56%、6.01%、6.13%、1.01%,见表2。化疗前肝功能异常的患者,化疗后肝功能较前好转,化疗前后肝功能指标改善有统计学差异,见表3。

表1 1511例患者化疗前后肝功能指标分析
3 异甘草酸镁预防肝功能损伤的亚组分析 不同药物是否会影响异甘草酸镁的保肝效果,我们对肝功能正常的患者化疗后肝脏的情况进行亚组分析。即便在输注异甘草酸镁的情况下,三氧化二砷仍造成AST、ALP异常率达4.85%及6.78%,而VP16化疗后15.46%患者GGT增高,单项肝功能的异常率均明显高于其它药物,差异均有统计学意义,见表2。
4 安全性分析 使用异甘草酸镁对药物性肝损伤进行防治,在治疗前后患者的肾功能指标、电解质、血压等比较,均没有统计学差异,见表4。

表2 不同化疗药物对肝功能指标的影响[%(例/n)]
续表

D-BIL异常率(%)P值 GGT异常率(%)P值ALP异常率(%)P值全部患者6.01(71/1181)-6.13(71/1158)-1.01(14/1394)-阿糖胞苷6.89(43/624)0.225.21(31/595)0.220.80(6/748)0.434环磷酰胺4.74(12/253)0.3755.91(15/254)10.35(1/289)0.324吡柔比星6.5(13/200)0.7446.60(13/197)0.7451.21(3/247)0.724甲氨蝶呤4.29(7/163)0.3793.03(5/165)0.081.03(2/194)1伊达比星8.55(13/152)0.1986.20(8/129)11.70(3/176)0.405长春新碱4.81(13/270)0.3851.34(4/298)<0.0010.31(1/323)0.21三氧化二砷6.06(6/99)11.82(2/110)0.0576.78(4/59)0.002依托泊苷5.17(3/58)115.46(15/97)<0.0010(0/94)0.617
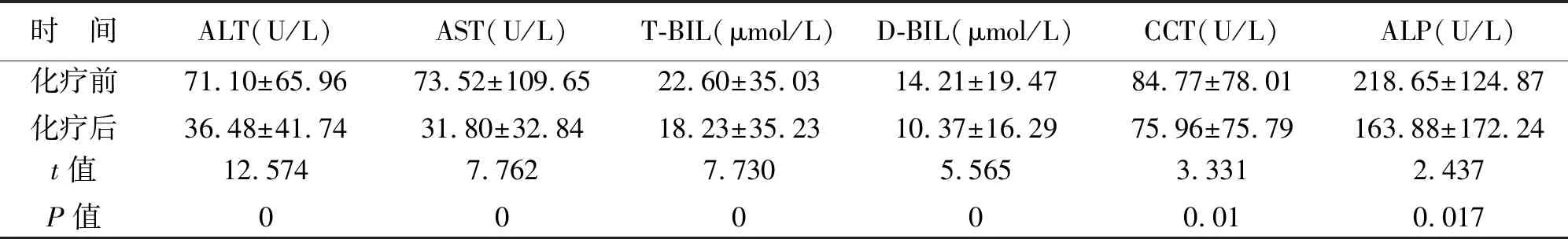
表3 化疗前肝功能异常患者肝功能指标分析
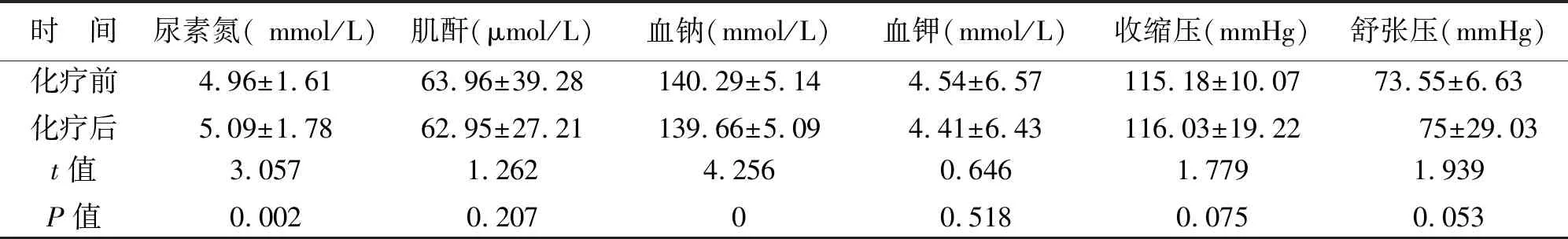
表4 异甘草酸镁安全性评价
讨 论
据WHO统计,随着化学药品的广泛应用,DILI逐年增多,已高居肝病死亡原因的第5位[1]。化疗是血液肿瘤的主要治疗手段,但一项来自国内的研究发现,抗肿瘤药物也是导致DILI的主要原因,占15.3%,位居第3位[2]。多数化疗药物可能导致急性DILI,肝损伤一旦发生,将会影响疗效,并可能危及生命,化疗可能导致的DILI成为血液科医生化疗前必须评估的问题。
异甘草酸镁是第四代甘草酸制剂,具有强效、亲脂、作用迅速、半衰期长等特点,它可调节由炎性刺激诱导的PLA2/AA、NF-κB及MAPK/JNK/STAT3通路中的炎性因子活性,调控关键炎性反应信号在起始阶段的代谢水平,从而抑制多种病因介导的炎性反应。研究证明,异甘草酸镁能有效预防及治疗多种实体肿瘤化疗药物导致的DILI[3-4],已被《药物性肝损伤诊治指南》IA类推荐治疗ALT明显增高的急性肝细胞型或混合型DILI[5]。血液肿瘤化疗药物剂量往往远大于实体肿瘤,化疗后DILI的风险更高,迄今我们并没有看到异甘草酸镁防治血液肿瘤化疗后肝损伤的多中心研究,本研究通过更广泛的人群观察、评价了异甘草酸镁的疗效。
既往研究中发现,抗肿瘤化疗相关肝损伤发生率高达62.63%[4],所以所有患者均应用异甘草酸镁,未设置空白对照组。在本研究中,化疗前肝功能正常的患者,化疗后整体肝功能指标较前并无增高,证实异甘草酸镁对化疗后肝损伤有较好的预防作用。化疗前肝功能正常的患者中,T-BIL异常率稍高,但ALT、AST、T-BIL、D-BIL、ALP及GGT异常率均较低,也低于文献报道,这可能提示血液肿瘤化疗后更容易出现胆汁淤积型DILI[4,6]。肝功能异常的患者多随着化疗药物的停用而逐渐改善。化疗前已出现肝损伤的患者,化疗后肝功能指标均明显改善,提示异甘草酸镁对化疗后肝损伤有较好的治疗作用。
本研究中,阿糖胞苷是应用最广泛的化疗药物,文献报道白血病应用阿糖胞苷化疗后DILI发生率高达37%~85%。Zimmerman HJ等[7]发现,阿糖胞苷的肝脏毒性具有剂量限制性,例如小剂量时AST异常率为5%~10%,而大剂量时达22%~75%。在本研究中阿糖胞苷导致的DILI发生率远低于国内外报道,除了异甘草酸镁的作用,阿糖胞苷每日剂量从20mg至12g,也是导致本研究中DILI发生率较低的原因。我们发现不同化疗药物导致DILI的发生率并无明显差异,可能与化疗方案中往往包含多个药物,难以评价具体是由哪种药物造成的肝损伤。恶性肿瘤患者化疗时,除可因化疗药物的直接细胞毒作用和药物代谢后造成肝细胞超负荷导致肝损伤外,还可因原发病、化疗后骨髓抑制期发生的各种感染以及随之应用的各种抗生素导致肝损伤。血清ALT、ALP、GGT和T-BIL 等改变是目前判断是否有肝损伤和诊断DILI 的主要实验室指标,相对而言三氧化二砷造成AST、ALP异常率较高,但该指标特异性均不高,血清ALT 的上升较AST 对诊断DILI 意义可能更大[8]。
综上所述,异甘草酸镁注射液与化疗药物同时应用,能够防治血液肿瘤化疗药物相关性肝损伤,明显降低其发生率。本研究仅关注了临床上最常应用的数种化疗药物,但异甘草酸镁在防治新的化疗药物、分子靶向药物和免疫抑制剂引起的肝损伤效果如何,如何优化异甘草酸镁的疗程、剂量等尚需进一步探索。

