跗骨窦切口钢板内固定联合经皮置钉技术微创治疗Sanders II、III 型跟骨骨折
赵训明 廖全明 王克军 裴洪 陈顺广刘盖为
跟骨骨折是创伤骨科常见疾病,其发生率占全身骨折的2%,是最常见的跗骨骨折,约占所有跗骨骨折的60%,其中有75%跟骨骨折为关节内骨折[1]。患者以具有劳动能力的青壮年为主,如功能恢复不佳,将会对社会经济带来影响[2]。目前,对累及跟骨关节面并移位的骨折最常用且有效的治疗方法是切开复位内固定术[2-3]。
跟骨Sanders II、III 型骨折为关节内骨折,一般需要手术治疗[4]。其中,最经典的方法是跟骨外侧扩大“L”形切口切开复位内固定术[1]。因该术式能很好的暴露骨折及关节面,并能直接复位,曾一度被认为治疗跟骨关节内骨折的标准术式[5]。然而,跟骨局部软组织覆盖质量差,尤其对局部软组织损伤严重的患者,该术式会带来诸如切口裂开、边缘坏死、切口感染等,且并发症高达15%~20%[5-6]。为了避免上述并发症,许多微创技术被开发出来,其中,跗骨窦切口联合经皮置钉技术具有切口小、可以暴露跟骨关节面,能完成跟骨重建的同时减少伤口并发症的发生率,但该技术单纯使用螺钉,仅能点对点固定,无法对跟骨进行侧方加压,难以恢复跟骨的宽度,不能坚强固定,适应范围窄[2]。对本院2016 年5 月至2017 年12 月采用跗骨窦切口钢板内固定联合经皮置钉技术治疗的Sanders Ⅱ或Ⅲ型跟骨骨折进行回顾性分析,目的是:评价该术式治疗跟骨骨折的术后疗效;总结该术式的适应证及局限性。现总结如下。
1 资料与方法
1.1 一般资料
1.2 术前准备
入院后给予支具或者石膏外固定,积极完善相关术前常规检查,测量Böhler 角和Gissane 角。同时给予消肿治疗,包括患肢抬高、冰敷、静脉使用消肿药物等。根据Caprini风险评分决定是否给予皮下注射低分子肝素预防静脉血栓形成治疗。待软组织肿胀消退后再进行手术。术前12 h 停用抗凝药,术前30 min 给予抗生素静脉滴注。
1.3 手术方法
所有患者均采用连硬外麻醉,麻醉成功后,大腿中上段置气压止血带,取患者健侧卧位,双侧跟骨骨折取患者俯卧位。常规消毒,铺巾,驱血,止血带加压。自外踝尖下1 cm向第4 跖骨基底连线做切口至跟骰关节面,锐性分离,勿进行皮瓣内剥离,注意保护腓肠神经,适当清理跗骨窦内软组织,显露距下关节面,贴跟骨骨膜做全层皮瓣剥离,显露跟骨外侧壁,翻开跟骨外侧壁骨折块,用克氏针撬起塌陷的关节面骨块并临时固定,恢复距下关节面的平整,用一枚克氏针固定载距突。在跟骨结节下钻入1 枚斯氏针,钻入的过程中多次抖动骨折块,恢复骨折块解剖位置,并撬拨跟骨恢复高度,外翻斯氏针纠正内翻,挤压跟骨外侧壁恢复跟骨宽度,复位外侧壁骨块,2 枚2.0 mm 克氏针临时固定维持跟骨宽度。C 臂透视跟骨轴、侧位,确认Böhler 角、Gissane角及跟骨高度、宽度、长度复位满意后挑选2 块相同的跟骨解剖锁定钢板,将1 块钢板从切口插入平放于跟骨外侧,确保钢板各螺钉孔位于跟骨体内。能够从跗骨窦切口内置钉的,直接拧入导向器置入锁定螺钉固定,不能从跗骨窦切口内置钉的,皮肤外侧重叠放置另一块钢板,应用经皮置钉技术置钉。固定完成后再次C 臂透视确认,冲洗伤口,逐层关闭伤口,放置皮片引流,敷料包扎。
1.4 术后处理
因有内固定置入,术后24 h 内使用抗生素。术后常规冰敷、抬高患肢以减少肿胀。术后24 h 拔除引流片,进行踝关节及足趾关节屈伸活动锻炼。根据Caprini 风险评分决定是否给予抗凝治疗。出院之前行跟骨侧轴位X 线片复查。2 周左右视切口愈合情况拆线。6 周后部分负重活动。术后3 个月根据影像学结果决定完全负重时间。
术后3 个月、1 年随访并记录相应结果。
1.5 临床评价
1.5.1 影像学评价
术前和术后3 个月随访时行跟骨侧轴位X 线片检查,测量Böhler 角和Gissane 角。
1.5.2 功能评价
末次随访时依照Maryland 足功能评分系统对患足进行功能评价。优:90 ~100 分;良:75 ~89 分;中:50 ~74 分;差:<50 分。
1.6 统计学分析
采用SPSS 20.0 软件进行统计学分析。数值变量资料采用均数±标准差表示,手术前后的比较采用配对t 检验,P<0.05为差异有统计学意义。
2 结果
2.1 一般结果
所有患者手术均由同一组医师完成,手术时间50~75min,平均62.83 min;手术切口长度4 ~6 cm,平均5.2 cm。所有患者均获得10 ~13 个月(平均11.8 个月)随访。
2.2 影像学结果

表1 手术前后Böhler 角和Gissane 角的比较
2.3 疗效结果
所有患者无骨折不愈合,愈合时间3 ~6 个月,平均4.4 个月,无感染、皮肤坏死发生。根据Manyland 跟骨评分系统评分,优13 例(56.5%),良8 例(34.8%),可2 例(8.7%),优良率为91.3%。腓肠神经损伤2 例。目前为止,无患者接受距下关节融合术。
典型病例:患者,男,45 岁,见图1。
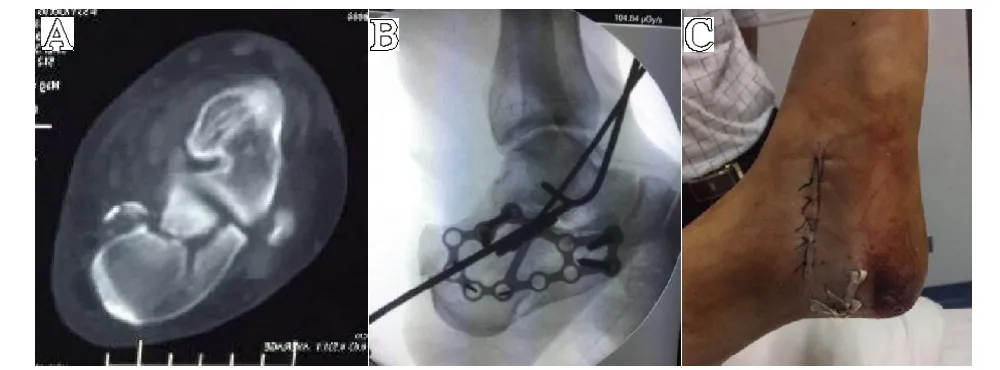
图1 A.右跟骨骨折(Sanders IIA 型);B.术中用斯氏针撬拨并临时固定,术中透视跟骨Böhler 角、Gissane 角及高度基本恢复;C.术后跗骨窦切口及经皮置钉切口
3 讨论
3.1 该术式的优点及临床疗效评价
目前对有移位跟骨骨折,特别是Sanders II 或Ⅲ型跟骨骨折多主张进行手术治疗[2]。目前,常用的术式是跟骨外侧扩大“L”形切口切开复位内固定术。但该术式软组织并发症多,为了降低软组织相关并发症,报道了多种微创技术[1],包括经皮撬拨复位石膏外固定、外固定架固定、经皮球囊扩张复位骨水泥注入术、跗骨窦切口钢板内固定联合经皮置钉技术[5]。据报道[5],跗骨窦切口钢板内固定联合经皮置钉技术能有效治疗Sanders II 和Ⅲ型跟骨骨折,还能有效减少软组织并发症。跗骨窦切口具有切口小、创伤小的优点,通过跗骨窦切口置入内固定联合经皮置钉技术,可更进一步避免切口过长,避免切口过度牵拉,保护软组织血供,使软组织损伤更小,术后疼痛更轻,可避免软组织恢复慢、软组织坏死、切口感染、裂开等术后软组织相关并发症。本组优良率达91.3%,且无伤口感染、皮肤坏死等软组织并发症发生。
关节内移位的跟骨骨折,手术的关键是复位关节面解剖结构,即恢复Böhler 角和Gissane 角以及跟骨长度、宽度、高度[7]。跟骨骨折术后的外形,特别是Böhler 角和Gissane 角,对跟骨功能预后判定特别重要,与跟骨功能恢复呈正相关[8]。故本研究中采用Böhler 角和Gissane 角为观察值。跗骨窦切口可以良好暴露距下关节面、外侧壁及外侧骨折块[5],有利于复位,恢复良好Böhler 角和Gissane 角。本组中,术后Böhler角和Gissane 角较术前都有很大的改善,与跗骨窦切口能良好暴露距下关节面有关。跗骨窦切口还可以暴露跟骨外侧壁,打开跟骨外侧壁,可了解跟骨体的复位情况,结合斯氏针顶撬和牵引技术,可复位跟骨的长度、宽度及高度。复位后通过跗骨窦入路置入传统解剖型锁定跟骨钢板,联合跟骨外侧经皮置钉技术,保护跟骨外侧软组织的同时保证了良好的跟骨骨折固定效果。本研究中,采用Maryland 评分来定量评价跟骨功能恢复情况,优良率达91.3%,说明经跗骨窦切口联合经皮置钉技术治疗SandersⅡ、Ⅲ型骨折可以取得满意的临床效果。
3.2 注意事项
本研究中有2 例出现腓肠神经损伤,需术中加以保护,避免过度牵拉,切口避免过于斜向外下,观察3 个月后神经症状明显改善。
跟骨Sanders Ⅳ型骨折,术中难以达到解剖复位,预后差,本研究未纳入Sanders Ⅳ型患者,该术式是否适应,需要进一步研究。目前认为跗骨窦切口联合经皮置钉技术治疗最佳手术适应证为SandersⅡ、Ⅲ型跟骨骨折,也缺乏对Sanders Ⅳ型的报告。有报道[9]建议一期在跗骨窦入路下尽可能复位距下关节面、跟骨关节面,减低创伤性关节炎发生率,如发生创伤性关节炎等功能障碍,亦可通过跗骨窦入路行距下关节融合术。
据报道,跗骨窦切口还具有手术时间短、术中出血量少、住院时间短、减低距下关节僵硬、提高患者满意度等优点[5,10]。建议绝大多数有明显移位的关节内跟骨骨折应采用跗骨窦小切口入路进行治疗[7]。但因微创切口没有外侧“L”形切口暴露充分,对习惯于“L”形切口的手术医师具有一定的挑战性,术前要充分了解骨折移位方向及骨折类型,手术技巧上也有一定的要求,术中透视的次数会增加。

