姜枣祛寒颗粒质量标准研究
宿曼筠,王友兰,吴爱英
(山东省青岛市食品药品检验研究院,山东 青岛 266071)
姜枣祛寒颗粒由干姜和大枣组方,功效为发散祛寒、和胃温中,用于风寒感冒、胃寒疼痛。现行标准收载于《卫生部药品标准·中药成方制剂(第二册)》[1],其中仅有干姜对照药材的鉴别,且涉及挥发性较大的有害试剂苯及易制毒试剂乙醚。为了更全面地控制该制剂的内在质量,本研究中增加了6-姜辣素对照品及大枣对照药材的薄层色谱(TLC)鉴别,并采用高效液相色谱(HPLC)法对干姜的有效成分6-姜辣素进行了方法学考察和含量测定。现报道如下。
1 仪器与试药
1.1 仪器
LC-20AT型高效液相色谱仪(日本岛津公司);BP211D型电子天平(德国Sartorius公司);Auto Science AS10200BT型超声波清洗器(杭州汇尔仪器设备有限公司);ZF7-C型三用紫外分析仪(上海康华生化仪器制造有限公司);Si60型硅胶板默克化工技术<上海>有限公司,批号为HC39961356,规格为10 cm×20 cm)。
1.2 试药
6-姜辣素对照品(批号为111833-201303),干姜对照药材(批号为120942-201510),大枣对照药材(批号为121040-201408),均购自中国食品药品检定研究院;姜枣祛寒颗粒(厂家HRSJ、厂家SXHK、厂家ZTJD,共11批,规格为每袋15 g);甲醇、乙腈均为色谱纯,其余试剂均为分析纯,水为娃哈哈纯净水。
2 方法与结果
2.1 TLC 鉴别
干姜:取本品5 g,研细,加二氯甲烷-甲醇(2∶1)20 mL,超声处理15 min,滤过,滤液浓缩至干,加甲醇1 mL使溶解,作为供试品溶液。另取干姜对照药材0.5 g,同法制备对照药材溶液。再取6-姜辣素对照品,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。按处方比例和制法制得不含干姜的样品,按供试品溶液制备方法制得干姜阴性对照溶液。照2015年版《中国药典(四部)》通则0502薄层色谱法试验,分别吸取上述溶液各 5 μL,分别点于同一硅胶 G薄层板上,以石油醚(60~90℃)-乙酸乙酯 -甲醇-冰醋酸(20∶3∶2∶0.4)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,105℃加热至斑点显色清晰,分别置日光及紫外光(365 nm)下检视。供试品溶液色谱中,在与对照药材溶液色谱和对照品溶液色谱相应位置上,显相同颜色的斑点或荧光斑点,且阴性对照无干扰。结果见图1。
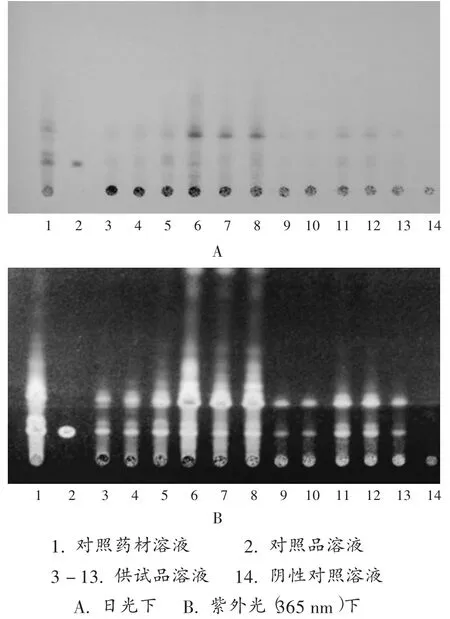
图1 干姜薄层色谱图
大枣:取大枣对照药材1 g,加水50 mL,煎煮1 h,实时补充减失的水分,滤过,滤液蒸干,残渣加二氯甲烷-甲醇(2∶1)20 mL,按干姜鉴别项下供试品溶液制备方法制成对照药材溶液。按处方比例和工艺制得不含干姜的样品,按干姜鉴别项下供试品溶液制备方法制得大枣阴性对照溶液。照2015年版《中国药典(四部)》通则0502中TLC法试验,吸取上述溶液各2 μL,分别点于同一硅胶G薄层板上,以正丁醇-冰醋酸-水(4∶1∶1)为展开剂,展开,取出,晾干,喷以茚三酮试液,105℃加热至斑点显色清晰。供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色的斑点,且阴性对照无干扰。结果见图2。
2.2 含量测定
2.2.1 色谱条件与系统适用性试验
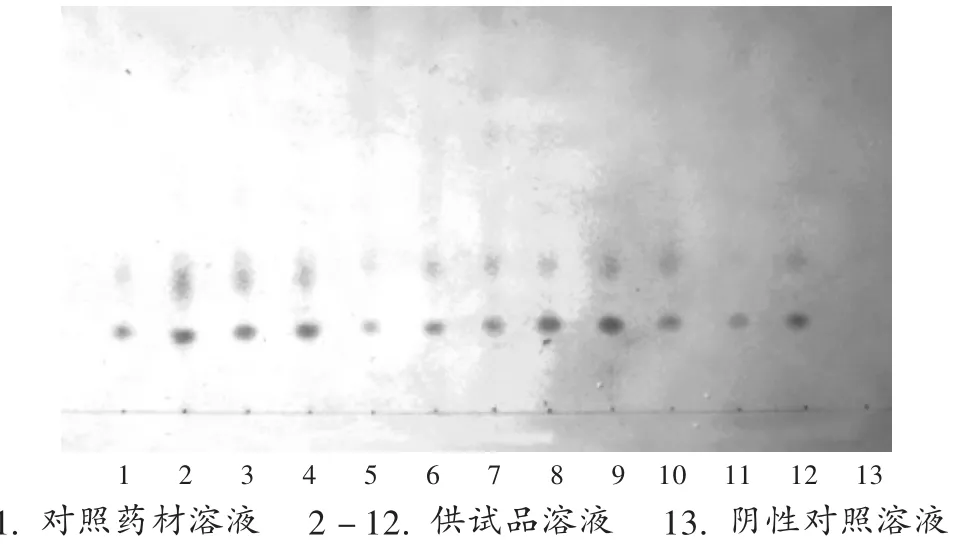
图2 大枣薄层色谱图
色谱柱:Accurasil C18柱(250 mm ×4.6 mm,5 μm);流动相:乙腈 -甲醇 -0.1%磷酸溶液(40∶5∶55);检测波长:280nm;流速:1.0mL/min;柱温:35℃;进样量:10μL。理论板数按6-姜辣素峰计应不低于5 000。
2.2.2 溶液制备
对照品溶液:取6-姜辣素对照品适量,精密称定,加甲醇超声溶解并定容至刻度,混匀,作为对照品贮备液,精密量取1 mL,置10 mL容量瓶中,加甲醇定容至刻度,混匀,即得。
供试品溶液:取样品10袋,倾出内容物,研细,取5g,精密称定,置具塞锥形瓶中,精密加入70%乙醇20 mL,称定质量,超声处理(功率为100 W,频率为40 kHz)20 min,放冷,再称定质量,用70%乙醇补足减失的质量,摇匀,滤过,取续滤液,即得。
阴性对照溶液:按处方比例及工艺配制缺干姜的阴性制剂,按供试品溶液制备方法制备,即得。
2.2.3 方法学考察
专属性试验:取对照品溶液、供试品溶液和阴性对照溶液各10 μL,按拟订色谱条件进样测定。结果在对照品溶液色谱峰相应的保留时间处,阴性对照溶液无色谱峰出现,说明阴性对照无干扰。结果见图3。
线性关系考察:分别精密吸取上述对照品溶液(质量浓度为 0.023 1 g/L)2,5,10,15,25 μL,按拟订色谱条件进样测定,以进样量(X,μg)为横坐标、峰面积积分值(Y)为纵坐标进行线性回归,得6-姜辣素回归方程Y=585 443X-1 194.4,r=1(n=5)。结果表明,6-姜辣素进样量在46~578 ng范围内与峰面积积分值线性关系良好。

图3 高效液相色谱图
精密度试验:精密吸取上述对照品溶液10 μL,按拟订色谱条件重复进样6次,测定峰面积积分值。结果的RSD为0.30%(n=6),表明仪器精密度良好。
稳定性试验:取样品(批号为150108)适量,依法制备供试品溶液,分别于 0,2,8,12,24 h 时进样分析,测定峰面积积分值。结果的RSD为0.38%(n=5),表明供试品溶液在24 h内稳定性良好。
重复性试验:取样品(批号为150108),依法制备供试品溶液,按拟订色谱条件重复进样6次,测定。结果平均含量为每袋 1.40 mg,RSD为 1.40%(n=6),表明方法重复性良好。
加样回收试验:取已知含量的样品(批号为150108),研细,称取约 2.50 g,共 6 份,精密称定,精密加入对照品溶液(质量浓度为 0.011 5 g/L)20 mL,依法制备供试品溶液,按拟订色谱条件进样分析,计算加样回收率。结果见表1。
2.2.4 耐用性试验
流动相比例考察:以乙腈-甲醇-0.1%磷酸溶液为流动相,对流动相的比例稍加调整,进行分析。结果见表2。可见,流动相中乙腈用量减少,6-姜辣素的保留时间有所延长,含量未发生变化,流动相组成比例的适量变化不影响结果。

表2 流动相比例考察结果(n=2)
色谱柱考察:选用3种不同的色谱柱,按拟订色谱条件进样分析,测定6-姜辣素的峰面积。结果6-姜辣素平均含量为每袋 1.42 mg,RSD为 0.70% (n=2),表明不同色谱柱对结果影响较小。
2.2.5 样品含量测定
2.2.2项下方法制备供试品溶液,依法进样测定,记录峰面积并计算其含量。结果见表4。
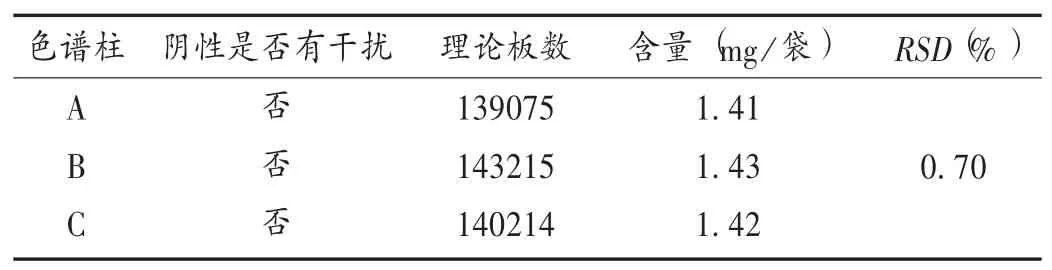
表3 色谱柱耐用性试验结果(n=2)
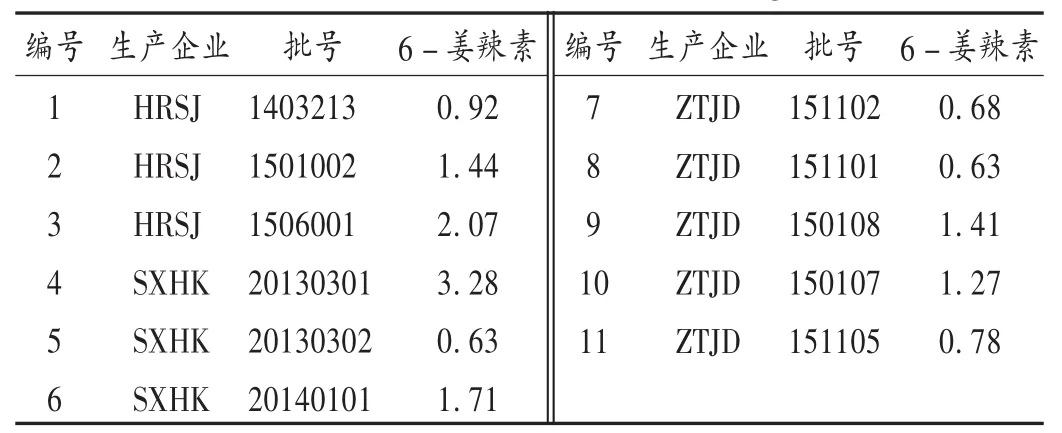
表4 各批样品的含量测定结果(mg/袋)
3 讨论
3.1 干姜定性鉴别的修订
原标准[1]中提取溶剂乙醚属易制毒试剂,改用二氯甲烷-甲醇(2∶1)提取溶剂毒性较小,且可同时适用于干姜和大枣的鉴别,既简化了操作步骤,又节约了溶剂,因此选用此系统为提取溶剂。原标准使用1 g对照药材,供试品取样量折算干姜的用量约为0.4 g,结合试验验证结果,将干姜对照药材的用量由原标准的1 g改为0.5 g。原标准及2015年版《中国药典(一部)》干姜药材TLC展开剂[2]14使用了毒性较大的苯和三氯甲烷有机试剂,为了遵循绿色环保的理念,经试验比较多个展开系统,以石油醚(60~90℃)-乙酸乙酯-甲醇-冰醋酸(20 ∶3 ∶2 ∶0.4)为展开剂分离效果良好、试剂毒性较小,随行阴性样品无干扰,故选用此展开剂系统。本研究中对方法的耐用性进行了考察,使用3种不同品牌的硅胶板展开:Si60(默克化工技术有限公司,批号为HC39961356,规格为10cm×20cm);硅胶G板(青岛海洋化工厂分厂,批号为20161220,规格为200mm×100mm);自制硅胶G薄层板,取硅胶G(青岛海洋化工厂,化学纯,批号为20161220)加0.5%羧甲基纤维素钠溶液调配,用手动铺板器铺成厚度为0.25 mm的薄层板,室温晾干,110℃活化1 h,置硅胶干燥器中备用。供试品溶液色谱中,在与对照药材溶液和对照品溶液色谱相应位置上,显相同颜色的斑点或荧光斑点,说明方法的专属性、耐用性较好。
3.2 大枣定性鉴别考察
尝试采用2015年版《中国药典(一部)》大枣药材TLC鉴别方法[2]22发现,本制剂中的阴性对照有干扰;由于大枣中主要含有多糖[3]等成分,对供试品的提取方法进行了更换溶剂及水解[4-7]等多次试验,发现供试品溶液不稳定且阴性对照仍有干扰。大枣中含有齐墩果酸等多种有机酸与多种氨基酸类成分[3],结合本制剂的工艺,经过多方试验,最终选用正丁醇-醋酸-水系统[8]作为展开剂,茚三酮试液为显色剂,显色斑点清晰,稳定性与重复性均良好,阴性无干扰。本研究中对方法的耐用性进行了考察,在上述3种不同硅胶板展开后,供试品溶液色谱中,在与对照药材溶液色谱相应位置上,显相同颜色的斑点,说明方法专属性、耐用性好。
3.3 6-姜辣素含量测定条件选择
干姜中最主要的辛辣成分为姜辣素,以6-姜辣素含量最大[9]。参考 2015 年版《中国药典 (一部 )》干姜项下的含量测定项,对处方中干姜的6-姜辣素的含量采用HPLC法进行考察。本研究中对提取溶剂和提取时间进行了考察,试验结果表明,70%乙醇超声提取20 min即可完全提取;并考察了甲醇 - 水(62 ∶38)[10]、甲醇 -水(55 ∶45)[11]和乙腈 -甲醇 -水(40 ∶5 ∶55)3 种流动相,结果发现,6-姜辣素的峰型有拖尾现象,对流动性稍加改进,采用乙腈-甲醇-0.1%磷酸溶液(40∶5∶55)流动相,峰型较好,拖尾因子为 1.0。

