大孔吸附树脂分离纯化薰衣草中迷迭香酸
熊天真, 管政兵, 廖祥儒, 蔡宇杰
(江南大学 工业生物技术教育部重点实验室,江苏 无锡 214122)
迷迭香酸在许多种植物中均有分布,主要分布于唇形科、紫草科和伞形科植物[1]。袁干军等采用大孔吸附树脂的方法从迷迭香中分离得到迷迭香酸[2],欧余航等也从九节茶浸膏中分离得到迷迭香酸[3]。迷迭香酸有预防许多疾病的发生、保护心脑血管循环系统[4]、抗氧化[5]、抗癌[6]、抗炎、抗过敏[7]等生理作用,在食品、化妆品、医药等方面有着广阔的应用前景。目前薰衣草中含有迷迭香酸已有文献报道[8-9],但是对薰衣草中迷迭香酸的提取与纯化工艺还鲜有报道。因此,对薰衣草中迷迭香酸纯化工艺进行研究,能够为生产迷迭香酸带来新途径。
大孔吸附树脂是一类不含交换基团且具有大孔网状结构和较大比表面积的高分子吸附树脂,能够选择性吸附水溶液中的物质[10]。大孔吸附树脂应用于很多种天然产物的分离[11-12]。因为可重复使用且价格低廉的大孔吸附树脂能够使天然产物得到高效分离,使其非常适合应用于工业化生产[13-14]。为此,作者采用大孔吸附树脂法对薰衣草中迷迭香酸分离纯化工艺进行研究,为开发利用薰衣草资源提供理论基础。
1 材料与方法
1.1 实验材料
于春季在江苏省无锡市采集的薰衣草样品进行实验。
1.2 实验方法
1.2.1 薰衣草中迷迭香酸的粗提取 薰衣草经过60%乙醇溶液于70℃振荡水浴12 h。将提取液用滤纸过滤,取滤液用旋转蒸发仪蒸发出乙醇,然后用蒸馏水稀释,此样品溶液用于大孔吸附树脂静态吸附及解吸性能考察。
1.2.2 大孔吸附树脂的预处理 先用5%HCl水溶液浸泡12 h,再用去离子水洗至中性。用95%乙醇浸泡12 h,用去离子水洗至无醇味为止。然后用5%NaOH浸泡12 h,用水洗至中性,备用。
1.2.3 液相检测方法 色谱柱:LaChrom C18柱(4.6 mm×250 mm,5 μm);流动相 A 和 B:分别是乙腈和甲酸溶液(0.1%);流量:1 mL/min;检测波长:280 nm;柱温:35 ℃;进样体积:10 μL。
1.2.4 对照品溶液的制备 精密称取迷迭香酸标准品25 mg置于25 mL容量瓶中,加入50%甲醇溶解并定容至刻度,得到1 mg/mL的迷迭香酸对照品溶液。
1.2.5 不同类型大孔树脂性能的比较 准确称取预处理后的大孔树脂2 g,置于50 mL三角瓶中,加入20 mL迷迭香酸粗提液,于30℃、100 r/min水浴振荡吸附24 h,取上清液进样测定迷迭香酸质量浓度。将吸干表面水分的大孔吸附树脂置于50 mL三角瓶中,加入20 mL体积分数95%的乙醇。于30℃、100 r/min水浴振荡24 h,用高效液相色谱法测定洗脱液中迷迭香酸质量浓度,分别计算各种树脂的吸附率及解析率。
1.2.6 大孔树脂的装柱处理 经预处理后的大孔吸附树脂湿法装入Φ2.0 cm×50 cm具活塞层析柱,装填高度17 cm,柱体积为40 mL。
1.2.7 迷迭香酸质量浓度的测定 收集迷迭香酸提取液和纯化液,经旋转蒸发仪减压浓缩至无醇味。将浓缩物冷冻成冰块后,进行真空冷冻干燥。称取适量的冷冻干燥物加水定容至50 mL,进样测定迷迭香酸含量。最后计算迷迭香酸纯度。
1.2.8 静态吸附动力学曲线的测定 准确称取LX-60干树脂2 g,置于50 mL三角瓶,再加入20 mL迷迭香酸粗提液,30℃、100 r/min水浴振荡。每隔20 min取样测定含量,以时间和迷迭香酸的吸附量作图绘制吸附动力学曲线。
1.2.9 静态吸附等温线的测定 分别量取4、8、12、16、20 mL迷迭香酸溶液,用体积分数60%乙醇分别稀释至20 mL,配置成不同质量浓度的迷迭香酸溶液,再分别加入2 g LX-60树脂,于30℃、100 r/min水浴振荡12 h,进样测定含量。以吸附平衡时迷迭香酸质量浓度与吸附量作图绘制吸附等温线。
2 结果与分析
2.1 迷迭香酸标准曲线的绘制
精密吸取迷迭香酸对照品溶液 (质量浓度为1 mg/mL)0.5、1、2、4、6、8 mL 定容至 10 mL,分别配置成 0.05、0.1、0.2、0.4、0.6、0.8 mg/mL 的迷迭香酸溶液。样品处理后,进高效液相色谱测质量浓度,考察迷迭香酸出峰面积与对照品溶液质量浓度的关系,见图1。可得线性回归方程为y=0.000 000 06x+0.018 05,R2=0.999 6,迷迭香酸质量浓度在0.05~1 mg/mL呈良好的线性关系。

图1 迷迭香酸标准曲线Fig.1 Standard curve of rosmarinic acid
2.2 大孔吸附树脂静态吸附与解吸性能考察
由表1可见,吸附率比较高的有非极性树脂LX-60、X-5、LX-17、LSA-21, 均可达到 50%以上,这与迷迭香酸分子中的苯环能够和吸附树脂本身的苯环之间形成疏水作用及电子堆积力有关,还与这几种树脂相对较大的孔径及比表面积有关。同时极性树脂D3520、NKA-C也能够达到一定的吸附效果。可能由于迷迭香酸为极性化合物,且其分子结构中带有四个酚羟基(见图2),形成氢键的能力较强,因此很容易被极性树脂所吸附。树脂对迷迭香酸的吸附是多种方面综合作用的结果,只要有合适的孔径与比表面积,极性或非极性的树脂均可达到很好的分离效果[15]。

表1 不同型号的大孔吸附树脂吸附和解吸能力测定结果Table 1 Adsorption and desorption abilities of macroporous resins
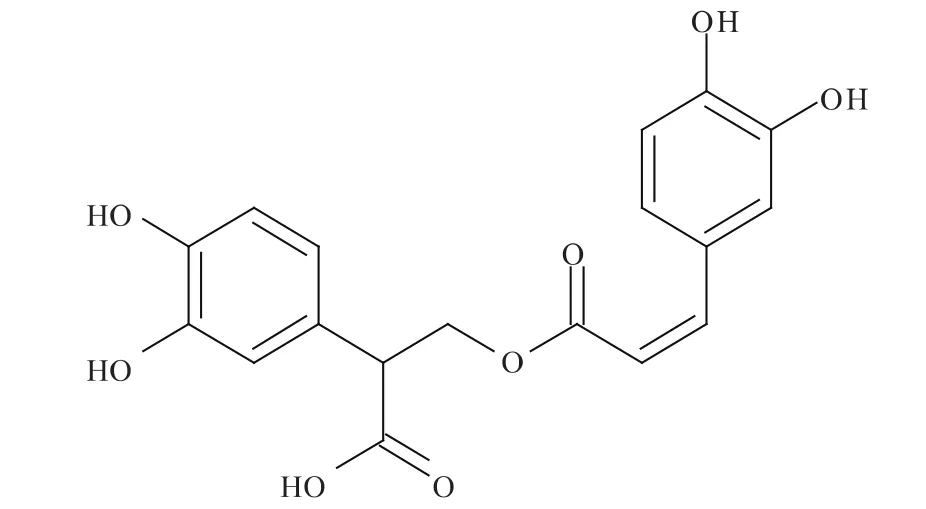
图2 迷迭香酸分子式Fig.2 Structure of rosmarinic acid
实验中筛选出最佳的树脂为LX-60大孔吸附树脂,其吸附率及解析率较为理想,是分离薰衣草中迷迭香酸的合适树脂。虽然LX-17、NKA-C、D4020解析率较高,但是其吸附率低,无法满足迷迭香酸的纯化要求。综合考虑,选择LX-60作为吸附树脂,故以下实验重点考察LX-60大孔树脂对薰衣草粗提液中迷迭香酸的纯化条件。
2.3 LX-60静态吸附动力学曲线及吸附等温线的绘制
LX-60大孔吸附树脂在80 min时,几乎能够达到吸附平衡。80 min以后吸附量几乎不再增加,见图3。在30℃自然pH下,此种树脂的最大吸附量可以达到4.98 mg/g。这种能够在短时间内达到吸附平衡点的性质,使其非常适合应用于工业化生产。
从迷迭香酸吸附等温线见图4。随着迷迭香酸质量浓度的增加,LX-60树脂对迷迭香酸的吸附量增加。当迷迭香酸质量浓度达到1.62 mg/mL时,吸附量开始平缓。原因可能因为树脂对迷迭香酸的吸附要达到固液相平衡,质量浓度高有助于树脂吸附。

图3 LX-60静态吸附动力学曲线Fig.3 Static absorption kinetics curve of LX-60

图4 LX-60静态吸附等温线Fig.4 Static absorption isotherm of LX-60
2.4 LX-60树脂动态吸附曲线
用LX-60树脂湿法装柱,将迷迭香酸质量浓度为0.42 mg/mL的料液上样进行动态吸附,以40 mL为一个柱体积,以1 mL/min的流速上柱,直到树脂吸附饱和为止。以一个柱体积为单位收集流出液,进样测定流出液中迷迭香酸的质量浓度,见图5。
从图5可以看出,该树脂可处理17倍柱体积的迷迭香酸溶液。树脂床共吸附迷迭香酸283.9 mg,湿态树脂对迷迭香酸的吸附量为7.09 mg/mL。
2.5 进样液pH对吸附率的影响
在不同的pH下进行吸附实验,结果见图6。迷迭香酸提取液pH 1~2时,LX-60树脂对迷迭香酸的吸附量差别不大;当pH 2~5时,树脂对迷迭香酸的吸附量逐渐减少。因此,选择进样液的pH为2较合适。原因可能是由于迷迭香酸作为多羟基的酚酸类物质,为酸性,在酸性的条件下容易被吸附。在酸性条件下,迷迭香酸能够以分子的形式存在,疏水性增强,树脂对其吸附也会相应的增强。在碱性条件下,迷迭香酸以离子的形式存在,不易被吸附。

图6 进样液pH对吸附率的影响Fig.6 Relation between pH and adsorption rate
2.6 进样液质量浓度对吸附效果的影响
将不同质量浓度的迷迭香酸溶液进行动态吸附实验,结果见图7。可以看出,当迷迭香酸质量浓度小于2.12 mg/mL时。随着样品质量浓度的增加,迷迭香酸的吸附率基本保持不变。当迷迭香酸的质量浓度大于2.12 mg/mL时,随着质量浓度的增加,迷迭香酸的吸附率下降,但是其下降的幅度不会很大。当上样质量浓度过高时,吸附率会下降很多,可能是由于提取液粘度过大,对树脂的粘附性过强,不容易被洗脱下来。这样会影响分离。根据实验结果,上样液的质量浓度为2.12 mg/mL左右为宜。

图7 进样液质量浓度对吸附率的影响Fig.7 Effect of concentration on adsorption rate
2.7 吸附流速对吸附效果的影响
将迷迭香酸溶液分别以 1、2、3、4、5、6 mL/min的吸附流速上柱。由图8可以看出,随着吸附流速的加快,迷迭香酸泄漏率增大。如果流速过慢,吸附时间会相应增加,延长了生产周期,提高了成本。如果流速过快,树脂吸附量下降严重。吸附流速影响溶质向树脂表面扩散的能力,从而决定了吸附效果。流速太快,溶质不能够很好的扩散到树脂内表面,从而不会被吸附,就会发生泄漏,造成迷迭香酸的流失。流速为1~2 mL/min时泄漏率差别不大。综合考虑,吸附流速为2 mL/min为宜。

图8 吸附流速对吸附率的影响Fig.8 Effect of adsorption flow rate on adsorption rate
2.8 乙醇体积分数对洗脱效果的影响
LX-60树脂是一种非极性大孔吸附树脂,依次用不同体积分数的乙醇溶液进行洗脱。将一定体积分数的迷迭香酸溶液上柱,达到吸附饱和后,用2 BV的去离子水洗去原液。在流速2 mL/min下,分别用体积分数10%、20%、40%、60%、80%、95%乙醇洗脱, 洗脱结果见图9。
由图9可以看出,40%乙醇洗脱效果最好,其洗脱峰集中,对称性良好。80%乙醇洗脱拖尾严重;而20%乙醇洗脱不太集中;10%乙醇几乎不能洗脱迷迭香酸。因此,40%乙醇为最佳洗脱溶剂。

图9 不同体积分数乙醇对迷迭香酸洗脱效果的影响Fig.9 Elution effect on rosmarinic acid with different concentration ethanol
2.9 洗脱流速对洗脱效果的影响
将一定质量浓度的迷迭香酸溶液吸附在树脂柱上,在 1、2、3、4、5、6 mL/min 不同流速下,用 40%乙醇洗脱,收集4个柱床体积的40%乙醇洗脱液,结果见图10。
由图10可以看出,洗脱流速对洗脱效果有一定的影响。当洗脱流速在1~2 mL/min时,迷迭香酸的质量浓度几乎不变;当洗脱流速大于3 mL/min时,迷迭香酸质量浓度大幅度下降。结果表明:洗脱流速越慢,洗脱效果越好,但太慢又会使工作周期延长。综合考虑,洗脱流速2 mL/min为最佳。

图10 洗脱流速对迷迭香酸洗脱效果的影响Fig.10 Effect of elution flow rate on desorption rate
2.1 0 LX-60树脂再生能力的考察
准确称取LX-60树脂2 g,预处理后重复多次静态吸附、洗脱实验,对树脂的再生能力进行考察,结果见图11。
由图11可以看出,随着使用次数的增加,树脂的分离效果逐渐变差。综合分析生产成本与分离效果,确定最佳再生周期为4次。

图11 LX-60树脂的再生周期Fig.11 Regeneration cycle of LX-60 macroreticular resin
2.1 1 最佳工艺条件的验证实验
将制备的迷迭香酸提取液配成质量浓度为2.15 mg/mL左右的迷迭香酸水溶液,调节其pH为2,在2 mL/min流速下,加入到LX-60树脂层析柱中。用水洗去未被吸附的原液,再用40%乙醇以2 mL/min的速度洗脱,收集4个柱体积洗脱液,减压浓缩除去溶剂,冷冻干燥得到迷迭香酸产品。测定得,迷迭香酸纯度为15.6%,其纯度提高了42倍,产品得率为86.79%。
图12为迷迭香酸标准品的高效液相色谱图。由图可知,迷迭香酸的出峰时间为12 min左右。图13为大孔吸附树脂纯化前的样品液相色谱图,可见12 min之前的杂质较多。图14为纯化后的色谱图,可见除杂效果明显。LX-60树脂具有工业化应用的潜力。

图12 迷迭香酸标准品高效液相色谱图Fig.12 HPLC chromatogram of standard rosemarinic acid

图13 处理前样品高效液相色谱图Fig.13 HPLC of non-purified sample

图14 处理后样品高效液相色谱图Fig.14 HPLC of purified sample
3 结语
大孔吸附树脂具有吸附容量大、选择性好、解吸条件温和、容易再生处理、较长使用周期、节约费用等众多优点,现已大量用于环保、化工、医药和食品工业[16]。
通过研究大孔吸附树脂对薰衣草中迷迭香酸的吸附和解吸性能,确定了LX-60树脂作为最佳树脂。其吸附率为71.48%,解吸率为94.92%。其吸附率大且容易解吸,能够满足实验的要求,较适合于薰衣草中迷迭香酸的纯化。
经过纯化后,迷迭香酸纯度达到15.6%,仍然存在纯度不高的问题,分析可能是由于提取物中的酚酸类化合物结构复杂、衍生物较多。因此,可以考虑在利用大孔吸附树脂进行纯化之前,选用合适的溶剂进行萃取或使用絮凝剂对多聚物进行絮凝来除去一部分杂质,提高薰衣草提取液中迷迭香酸的纯度[17]。

