瘢痕子宫妊娠人工流产术后大出血治疗
姜家英 刘 红
陕西省安康市中医医院(725000)
瘢痕子宫妊娠(CSP)是处理难度较大的异常妊娠,易引起晚期子宫破裂和阴道大出血,甚至危及产妇生命[1]。CSP的发生率较低不足0.05%,在有≥1次剖宫产史妇女中的发病率6.1%[2]。目前,临床对CSP尚无统一治疗标准,多根据患者的孕周、临床表现、严重程度、生育意愿及子宫肌层缺损情况等个体化治疗,但仍有部分患者治疗后出现阴道大出血或持续出血[3]。本研究回顾分析了CSP流产术后阴道大出血临床资料,探讨其危险因素、临床治疗方法及临床效果。
1 对象与方法
1.1 研究对象
回顾性收集2010年1月-2018年5月本院行人工流产术或清宫术后发生阴道出血的CSP患者102例临床资料。纳入标准:①具有停经史,经尿妊娠试验及血β人绒毛膜促性腺激素(β-hCG)检查呈阳性;②具有子宫下段横切口剖宫产手术史;③超声检查符合[4];④终止妊娠前未能明确排除CSP而导致阴道出血,或术中发现为CSP但术后仍发生阴道出血者,根据WHO产后出血定义(产后24h内出血量≥500ml)将术后6h内出血量≥500ml界定为术后阴道大出血。排除标准:①合并心、脑、肝、肺、肾等重要脏器功能障碍;②严重凝血功能障碍;③其他原因导致阴道不规则出血。所有患者均签署知情同意书,研究获得医院伦理委员会审核批准。
1.2 治疗方法
所有患者根据出血情况采取不同的治疗方法,治疗前明确无相关禁忌证。
1.2.1大出血组(36例)术中或术后6h内出血量≥500ml者。①子宫动脉栓塞(UAE)治疗:28例(77.8%)行急诊UAE紧急止血,其中5例止血成功后血β-hCG水平持续下降(术后3d下降50%)且宫内包块直径较小(<25mm),未采取其他杀胚药物辅助治疗;8例止血后因血β-hCG水平未能明显下降或者升高,且宫内包块直径较小(<25mm),超声提示子宫瘢痕肌层厚度≥3mm,心管搏动且血流信号丰富,予以甲氨蝶呤(MTX)单次肌内注射(50mg/次)并口服米非司酮(25mg/次),2次/d,连续服用5d,如β-hCG下降不理想(<30%)则于7d后再行第2疗程服药;8例UAE止血后由于瘢痕局部血流信号不丰富、子宫瘢痕肌层厚度≥3.5mm且宫内包块直径>35mm,在超声引导下清宫或宫腔镜下清宫,活动出血点采取电凝止血;7例UAE止血后因瘢痕局部血流信号丰富、子宫瘢痕肌层厚度<3.5mm且宫内包块直径>35mm,采取腹腔镜(6例)或开腹(1例)瘢痕妊娠物清除修补术。②宫腔填塞:5例(13.9%)直接清宫或UAE联合清宫术后阴道大出血,予以舌下含服米索前列醇、应用缩宫素,经阴道宫腔填塞纱条止血。③子宫切除:3例(8.3%)出血量达1700~3000ml,常规止血无效,紧急输血治疗,实施子宫次全切除或全切除术治疗,经术后病理检查证实为CSP。
1.2.2少量出血组(66例)中或术后6h内出血量<500ml,且出血持续时间10d~3个月者。①保守治疗:31例无明显腹痛症状,经超声检查提示子宫瘢痕肌层厚度≥2mm但宫内包块直径<25mm,采取药物保守治疗,即MTX单次肌内注射(50mg/次),并口服米非司酮(25mg/次),2次/d,连续服用5d,如β-hCG下降不理想(<30%)则于7d后再行第2疗程服药。②手术治疗:19例无明显腹痛,瘢痕局部血流信号丰富、子宫瘢痕肌层厚度<3.5mm且宫内包块直径>30mm,采取宫腔镜下电切术清除妊娠组织,或在超声引导下清宫术;16例瘢痕局部血流信号丰富、子宫瘢痕肌层厚度<3.5mm且宫内包块直径>35mm,实施腹腔镜或开腹瘢痕妊娠物清除修补术,术后定期复查观察瘢痕局部子宫内膜修复情况。
1.3 观察指标
记录患者的年龄、孕产次、剖宫产史、流产史、孕周、超声特征、治疗方法、治疗结局及出血情况。
1.4 统计学分析
2 结果
2.1 两组临床特征比较
大出血组与少量出血组年龄、孕产次、剖宫产次数、距前次剖宫产时间、血β-hCG比较无差异(P>0.05);孕周、孕周>8周率、包块直径、包块直径>60mm及子宫瘢痕肌层厚度大出血组均高于少量出血组(P<0.05)。见表1。
2.2 阴道大出血的危险因素分析
logistic回归分析模型显示,孕周>8周、包块直径>60mm是阴道大出血的独立危险因素(P<0.05)。见表2。
2.3 治疗结局情况
月经恢复正常时间和首次月经经期大出血组均长于少量出血组(P<0.05);少量出血组中手术治疗患者各指标均短于保守治疗患者(P<0.05)。见表3。
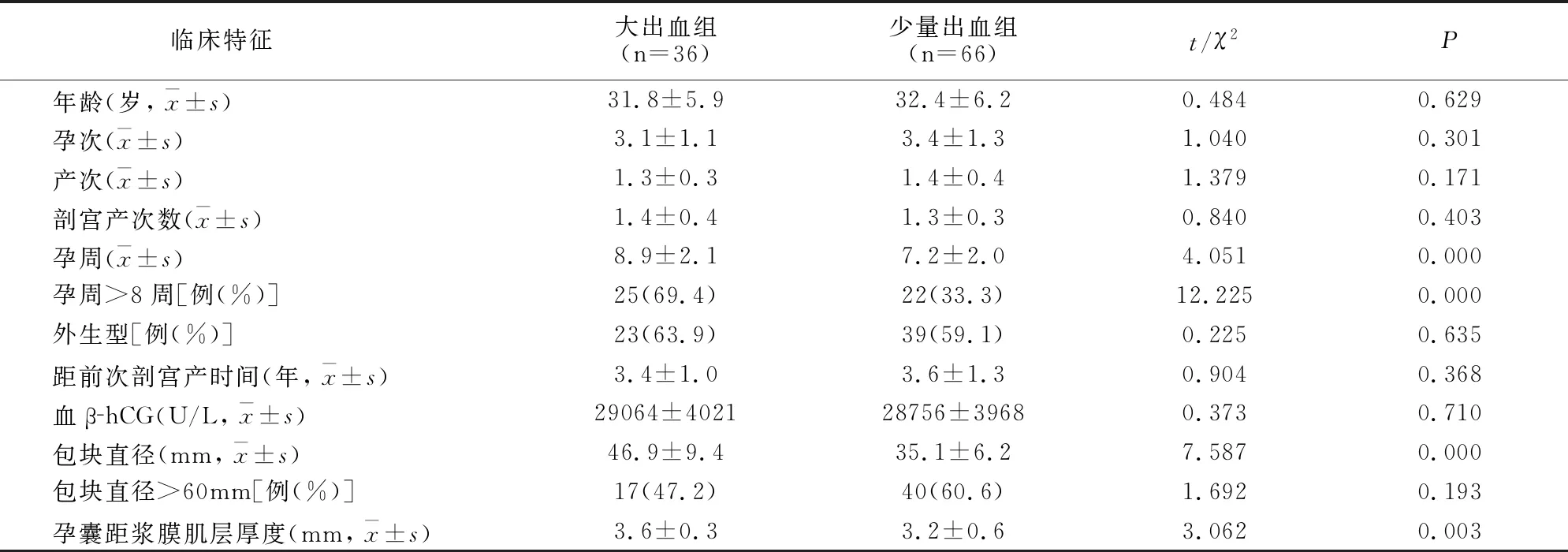
表1 两组临床特征比较

表2 阴道大出血的危险因素分析
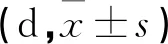
表3 各组治疗结局情况
*大出血组与少量出血组比较#保守治疗与手术治疗比较P<0.05
2.5 安全性评价
102例均无药物或造影剂过敏发生,无感染事件,行清宫术者均无膀胱损伤、子宫穿孔病例。大出血组中,UAE治疗后下肢静脉血栓形成1例(予以抗凝治疗后好转),发热11例、臀部或下肢疼痛5例; MTX用药后恶心(呕吐)2例;治疗后3个月发生子宫憩室7例(19.4%)。少量出血组中,MTX用药后恶心(呕吐)4例;治疗后3个月子宫憩室15例(22.7%)。腹痛、发热、恶心(呕吐)等均经对症治疗在3d左右缓解。
3 讨论
近年来随着子宫保守性手术及剖宫产人数的增加,CSP发病率呈现逐年升高趋势[1]。CSP的发生机制尚未完全阐明,多认为由于剖宫产术后或子宫保守性手术后子宫宫腔侧壁愈合不良,局部形成微小瘢痕缺损或裂隙,再次妊娠时孕囊种植于该部位而引起[5]。因CSP早期临床表现缺乏特异性,往往发生误诊或漏诊,容易发生盲目流产术,而由于孕囊种植部位子宫肌层较为薄弱甚至缺失,局部子宫壁弹性降低,盲目手术极易发生大出血甚至子宫破裂穿孔。而妊娠进展亦可发生子宫破裂大出血,甚至切除子宫或危及生命[6]。近年来超声检查成为诊断CSP的首选方法。张淋淋等[7]研究显示,病灶直径、分型、瘢痕局部残留基层厚度及血流信号分级是CSP大出血的独立危险因素。但本研究结果与之有一定差异,大出血组与少量出血组均以外生型为主,组间并无差异,仅在孕周、孕囊直径及孕囊距浆膜肌层厚度方面有差异。考虑为本组病例均为确诊后实施流产手术,诊断孕周相对较早有关。回归分析显示,孕周>8周和包块直径>60mm是阴道大出血的独立危险因素,考虑因素:①孕<8周是不良妊娠诊断及干预的最佳时期,对CSP而言如>8周行流产手术风险增大,治疗时更易发生大出血。②CSP患者病灶局部的蜕膜组织较缺乏,而绒毛组织逐渐侵袭肌层,随着孕周的增加肌层组织的逐步收缩力降低,并伴有不同程度的血管新生,尤其当包块直径较大时,病灶破裂的风险增加,更易发生大出血[8]。因此,在临床中如遇孕周>8周、巨大包块(直径>60mm)者术前应充分告知其出血风险并强化围手术期管理,最大限度降低严重并发症发生风险。
目前,CSP的临床治疗方法主要可分为药物治疗(MTX、MF等)、局部治疗(UAE、UACE等)和手术治疗(清宫术、开腹或腹腔镜下瘢痕妊娠组织清除修补术、子宫全切除术或此券切除术)三类,具体方案应根据患者的具体情况选择[4]。MTX、MF等对无明显腹痛症状、无子宫破裂征象、子宫瘢痕肌层厚度≥2mm、包块体积>20mm、出血行或尚未行介入治疗的CSP者均有一定疗效[9]。本研究中少量阴道出血者采取MTX+MF药物保守治疗后控制出血。但药物治疗疗程较长,仍具有出血停止后再出血或阴道流血时间长等问题,故建议用于少量出血(<500ml)或大出血UAE治疗的辅助用药。
UAE对具有生育要求的患者是一种较理想保守治疗措施[10]。将MTX与UAE联合的方案即UACE,术中通过局部灌注小剂量MTX序贯双侧子宫动脉栓塞促使孕囊缺血、坏死而终止妊娠[11]。UACE可单独或与其他疗法联用,对CSP严重阴道出血者有良好疗效,疗效优于全身MTX化疗[12]。但也有研究显示,对于胚胎植入较深或持续出血CSP患者,有63.2%后续仍需接受清宫术[13]。本研究中28例紧急行UAE治疗,5例止血成功,未再添加任何杀胚药物辅助治疗;8例由于病灶残留及β-hCG下降不理想,但病灶较小且血流丰富,辅助应用MTX+MF治疗控制;8例因病灶残留且病灶体积相对较大、瘢痕肌层较厚,考虑药物干预可能效果不理想而补充清宫术后成功止血;7例由于因病灶残留且病灶体积相对较大,但瘢痕肌层较薄,未免再次出血,采取经腹妊娠组织清除修补术后成功止血。另外,5例由于未明确CSP情况下直接清宫或在明确诊断后实施UAE联合清宫术后发生大出血,采取药物辅助宫腔纱条填塞成功止血,避免了二次手术。
手术处理CSP的选择仍需结合患者的宫腔包块体积、子宫瘢痕肌层厚度、局部血流情况、阴道出血量、β-hCG水平及患者的生命体征变化。鉴于CSP具有较高的大出血发生风险,临床多不考虑单独清宫治疗,有文献[14]显示, 76%的CSP患者在清宫术后需要联合全身MTX化疗或补充行开腹或腹腔镜异位妊娠病灶切除术,少数患者还可能切除子宫。为降低清宫术中出血风险以及术后并发症,临床多推荐预防性实施UAE或UACE联合超声引导下清宫术治疗CSP[15]。但目前多用于孕周<8周且包块直径<3cm CSP患者。有研究显示,对孕周≤7周的CSP患者实施UAE联合清宫术安全可行,而对孕周>8周及包块直径>6cm者则有较高的大出血发生风险[16]。Wang等[3]研究亦显示,外生型CSP患者在使用UAE联合清宫术后仍有一定的子宫破裂及阴道大出血发生风险。此外,UAE价格较贵,对医师技术有一定要求,只能在有条件的医院实施。也有学者提出,微创技术宫腔镜下妊娠组织电切术能够清晰地探查子宫形态、瘢痕局部血流状况及孕囊情况等,准确清除孕囊组织,减少损伤,术中应用电凝止血可降低大出血发生风险或减少出血量[17]。而对于出血量较大病情危急者,子宫次(全)切除术可作为最终补充治疗手段。本研究中,3例因出血量较大、病情危急且常规止血措施无效,果断采取子宫切除,成功挽救了患者生命。而在少量出血组中,由于残余包块较大,接受了二次手术治疗。
分析各组治疗结局显示,大出血患者采取UAE或宫腔填塞治疗多可快速有效控制出血,但在包块消失及月经恢复方面仍不及少量出血者。而在少量出血者中,保守治疗的止血速度及恢复速度不及手术治疗。鉴于药物副反应及手术创伤等因素,根据治疗经验认为:对包块体积较小(<25mm)、瘢痕肌层较厚(≥3mm)的少量出血者,考虑以MTX等药物保守治疗;如包块体积较大(≥30mm)且瘢痕肌层较厚(≥3mm)且局部血流不丰富者,MTX化疗可能效果不佳,可考虑手术治疗,且尽量以微创、操作简便的术式为主。但如果瘢痕肌层较薄,清宫术可能再发大出血甚至子宫破裂、穿孔,为保留患者的生育功能,可考虑经腹瘢痕妊娠物清除修补术;而对怀疑或急诊剖腹探查显示瘢痕妊娠局部胎盘大部分植入、出血量较大且难以纠正,应考虑次全(全)子宫切除以挽救患者生命[18-19]。此外,对于因未明确诊断为CSP而终止妊娠导致大出血患者,可考虑行UAE或UACE控制出血,密切监测β-hCG水平变化,超声监测子宫瘢痕肌层厚度及宫内包块大小情况,以便采取进一步治疗。
综上所述,为预防未明确排除CSP而盲目人工流产或清宫,对具有剖宫产史者,再次妊娠后应完善阴道超声等检查尽早确诊CSP。孕周>8周、巨大包块(直径>60mm)的CSP是大出血高危患者,应根据患者的生命体征、孕囊情况尤其是局部血流状况等采取个体化治疗措施,UAE可作为紧急止血的首要手段,药物、宫腔镜或超声引导下清宫、经腹瘢痕妊娠物清除修补术可作为辅助或补充措施,必要时可采取子宫次全或全切除术。但本研究样本较小,随访时间尚短,具体方案选择及其指征、长期预后还有待进一步研究加以完善。

