烷基化果胶凝胶性质的研究
郭晓娟 贺小红 刘成梅 梁瑞红 陈 军
(南昌大学食品科学与技术国家重点实验室 南昌330047)
果胶是一种天然多糖,按分子结构可分为同型聚半乳糖醛酸、鼠李半乳糖醛酸聚糖I 型、鼠李半乳糖醛酸聚糖II 型3 类[1]。由于其具有良好的凝胶性、乳化性、增稠性及稳定性等,在食品工业中常被用作食品添加剂。然而,果胶固有的一些缺陷,限制了其在一些特定领域的应用[2]。例如:高甲氧基果胶在形成凝胶时需要使用大量的糖(55%~75%),导致这些产品不利于糖尿病患者食用;果胶在溶解过程中容易结块,从而阻碍其有效溶解;果胶的高水溶性限制了其在载药体系中的应用。
果胶修饰可以改善果胶的一些功能和理化性质,因此越来越受到人们的关注。果胶分子主链上含有大量的羟基和羧基,这为果胶的修饰和改性提供了无限可能。目前应用比较广泛的果胶修饰方法包括取代法、链延伸法及降解法等[2]。其中,烷基化修饰是取代法的一种,它主要是将烷基链通过酯键引入果胶的羧基上。甲基化是引入碳链最短的烷基化修饰,其方法多种多样并已趋于成熟。基于甲基化的方法,也可以将更长的碳链引入果胶中,一般通过TBA 果胶盐与相应的卤代烷反应,过程如图1所示[2]。Houzelle 等[3-4]采用该方法将C12、C16和C18链引入到果胶分子中,发现其衍生物的疏水性和黏性大大提高。本课题组前期将C6、C12和C18链引入果胶中,制备了不同取代度和不同链长的烷基化果胶,发现果胶的结构、特性黏度及乳化性质发生极大改变,并且这些性质受取代度和链长的影响[5]。然而,目前对烷基化果胶凝胶性质的研究鲜有报道。本文将C6、C12和C18链引入果胶中,制备不同链长和不同取代度的烷基化果胶,研究蔗糖含量、pH 值及钙离子浓度对所制烷基化果胶凝胶性质的影响。
1 材料与方法
1.1 材料与试剂
柑橘果胶,中国上海Sigma Aldrich 公司;溴代己烷、溴代十二烷、溴代十八烷、己醇、十二醇、十八醇、十二烷、环戊烷、四丁基氢氧化铵(TBA+OH-)(25%水溶液),阿拉丁试剂(上海)有限公司;其它试剂均为国产分析纯级。
1.2 仪器与设备

图1 烷基化反应过程[2]Fig.1 Alkylation of pectin with alkyl halide[2]
Agilent6890 气相色谱仪,美国安捷伦公司;FE 20 pH 计,瑞士梅特勒-托利多有限公司;X85-2S 型恒温磁力搅拌器,上海梅颖浦仪器仪表制造有限公司;HH-S26 恒温水浴锅,金坛市梅香仪器有限公司;MCR302 流变仪,奥地利Anton Paar 公司;TA.XTplus 质地分析仪,美国TA 公司;Nicolet 5700 傅里叶红外光谱仪,美国Thermo 公司。
1.3 试验方法
1.3.1 烷基化果胶的制备 参照Liang 等[5]的方法并加以改进,具体步骤:配制20 mg/mL 的果胶溶液,用TBA+OH-中和至pH=7,冻干。配制20 mg/mL 的TBA 果胶盐溶液 (溶于二甲基亚砜DMSO中),然后加入不同摩尔质量的溴代己烷、溴代十二烷和溴代十八烷,50 ℃下搅拌反应24 h。在超纯水中透析7 d 除去DMSO,将透析液与氯化钠(1 mol/L 溶于70%乙醇溶液中) 在4 ℃下反应24 h。将反应后的产物抽滤,先用80%的酸化乙醇和75%的乙醇清洗,之后用无水乙醇清洗,直至没有氯离子存在(用硝酸银检测),最后用无水丙酮清洗,常温、常压下干燥。
1.3.2 烷基化产物取代度的测定 用气相色谱法(GC)测定衍生物的取代度[6],色谱条件:色谱柱HP-5;进样温度280 ℃;检测器FID 温度280 ℃;载气流速2.5 mL/min;进样量2 μL;分流比1∶10。程序升温条件:己醇:从60 ℃以10 ℃/min 升温至200 ℃,在90 ℃和150 ℃各保持1 min,200 ℃保持5 min;十二醇:从60 ℃以15 ℃/min 升温至230℃,在200 ℃和230 ℃各保持3 min;十八醇:从60℃以20 ℃/min 升温至290 ℃,在200 ℃和290 ℃分别保持1 min 和2 min。
(1)标准曲线的绘制:内标液的配制:将内标物十二烷溶于环戊烷中,定容,使质量浓度为1 mg/mL。
标准液的配制:将己醇、十二醇或十八醇溶于甲醇中,定容,得质量浓度为2 mg/mL 的标准液。
将标准液分别稀释至0.2,0.4,0.6,0.8,1,1.2 mg/mL。吸取1 mL 稀释后的标准液与2 mL 内标液混合均匀后,过滤膜进样。以标准样品的峰面积/内标物的峰面积为纵坐标,标准样品的质量为横坐标,绘制己醇、十二醇和十八醇的标准曲线,线性回归。
(2)样品取代度的测定:100 mg 的烷基化果胶溶于10 mL 水中,搅拌至完全溶解,然后加入0.4 mol/L 的NaOH 反应4 h。加入内标液,持续剧烈搅拌,4 800 r/min 离心15 min 后,取上层有机相过滤膜进样,与标准曲线对照得到对应的己醇、十二醇或十八醇量。取代度(DS)计算公式如下:

使用PCnSx来命名烷基化果胶,其中P 代表果胶,Cn代表共价连接的长链烷基(n=6,12 或18),x代表取代度DS 值。
1.3.3 原果胶及烷基化果胶凝胶溶液的制备 称取一定质量的原果胶及烷基化果胶,分别溶于新配制的不同pH 值的柠檬酸缓冲液(0.1 mol/L),搅拌至溶解,最终质量浓度为7.5 mg/mL,备用。在果胶溶液中分别加入不同质量的蔗糖和不同体积的氯化钙溶液(0.1 g/mL),搅拌均匀。凝胶溶液配制方案具体如表1所示。
1.3.4 原果胶和烷基化果胶凝胶的流变性质 参照Evageliou 等[7]方法并做修改,研究果胶凝胶的流变性质,将1.3.3 中的样品加到流变仪的样品台上,采用直径为50 mm 的1°锥板,平衡5 min 后,从25 ℃以8 ℃/min 的速度升温至80 ℃,停留5 min 后,再以5 ℃/min 的速度降至4 ℃。测定降温过程中存储模量(G′)的变化。本文还考察了钙离子加入后果胶凝胶的G′随频率的变化,样品在4℃下保持10 min 后进行频率扫描,扫描范围为0.1~100 rad/s(在线性黏弹区内),应变力为3%。

表1 原果胶及烷基化果胶凝胶溶液的配制Table1 Preparation of gel solutions of original pectin and alkylated pectins
1.3.5 原果胶及烷基化果胶凝胶的质构特性 将果胶溶液置于恒温水浴锅中预热至80 ℃,然后加入不同质量的蔗糖和不同体积的氯化钙溶液(0.1 g/mL),搅拌均匀,然后放入4 ℃恒温冰箱中12 h,待凝胶形成[8]。利用质地分析仪进行质构性质测定,采用P36 探头,穿刺速度为1 mm/s,穿刺深度为3 mm,第1 次穿刺过程中探头所受的最大应力即为凝胶强度。试验重复3 次,取平均值。
1.3.6 FT-IR 光谱分析 将果胶钙凝胶进行冻干,冻干后的样品与一定量的KBr 粉末一起研磨至粉状压片。用Nicolet 5700 傅里叶红外光谱仪记录样品4 000~400 cm-1频率范围内的光谱图[9]。
2 结果与分析
2.1 烷基化果胶的制备

图2 烷基化果胶经过皂化后的代表性GC 图谱Fig.2 Representive gas chromatograms of alkylated pectin after saponification
通过气相测定烷基化产物的取代度,结果图2所示。本试验成功制备了烷基化果胶PC6S1.35,PC6S2.90,PC6S4.53,PC12S2.90 和PC18S2.90,其果胶与相应溴代烷的摩尔比分别为1∶0.1,1∶0.3,1∶1,1∶0.13 和1∶0.17。可以将产物分为具有相同链长不同取代度和相同取代度不同链长的两组,分 别 命 名 为PC6S1.35,PC6S2.90,PC6S4.53和PC6S2.90,PC12S2.90,PC18S2.90。
2.2 蔗糖含量对烷基化果胶凝胶性质的影响
本文考察了蔗糖含量对原果胶及烷基化果胶凝胶流变性质(图3)及质构特性(图4)的影响。流变储能模量(G′)又称弹性模量,指材料在发生形变时由于弹性形变(可逆)而储存能量的大小。G′能较好的反应凝胶体系的形成过程,可衡量果胶凝胶结构的弹性与强度,其值越大则弹性和强度越大[10],因此本文主要考察G′的变化。结果表明,在降温过程中,G′随着温度的降低而升高,这可能是随着温度的降低,分子间热运动缩减,有利于分子内和分子间氢键的形成,模量逐渐升高[11]。所有果胶凝胶G′随着蔗糖含量的升高而升高。蔗糖可以与果胶竞争水分从而使果胶分子间相互靠近,促进凝胶形成。因此蔗糖含量越高,果胶越容易形成凝胶,其凝胶强度也越高。质构数据显示,果胶的凝胶强度随着蔗糖含量的升高而升高,与流变结果一致。当糖浓度为65%时,原果胶,PC6S1.35,PC6S2.90,PC6S4.53,PC12S2.90和PC18S2.90凝 胶 强 度 分 别为42.95,32.35,53.5,75.0,78.3,82.1 g,即当糖浓度一定时,烷基化果胶的凝胶强度随着取代度和链长的增加而增强,且较高取代度和较长链长的烷基化果胶凝胶强度高于原果胶。
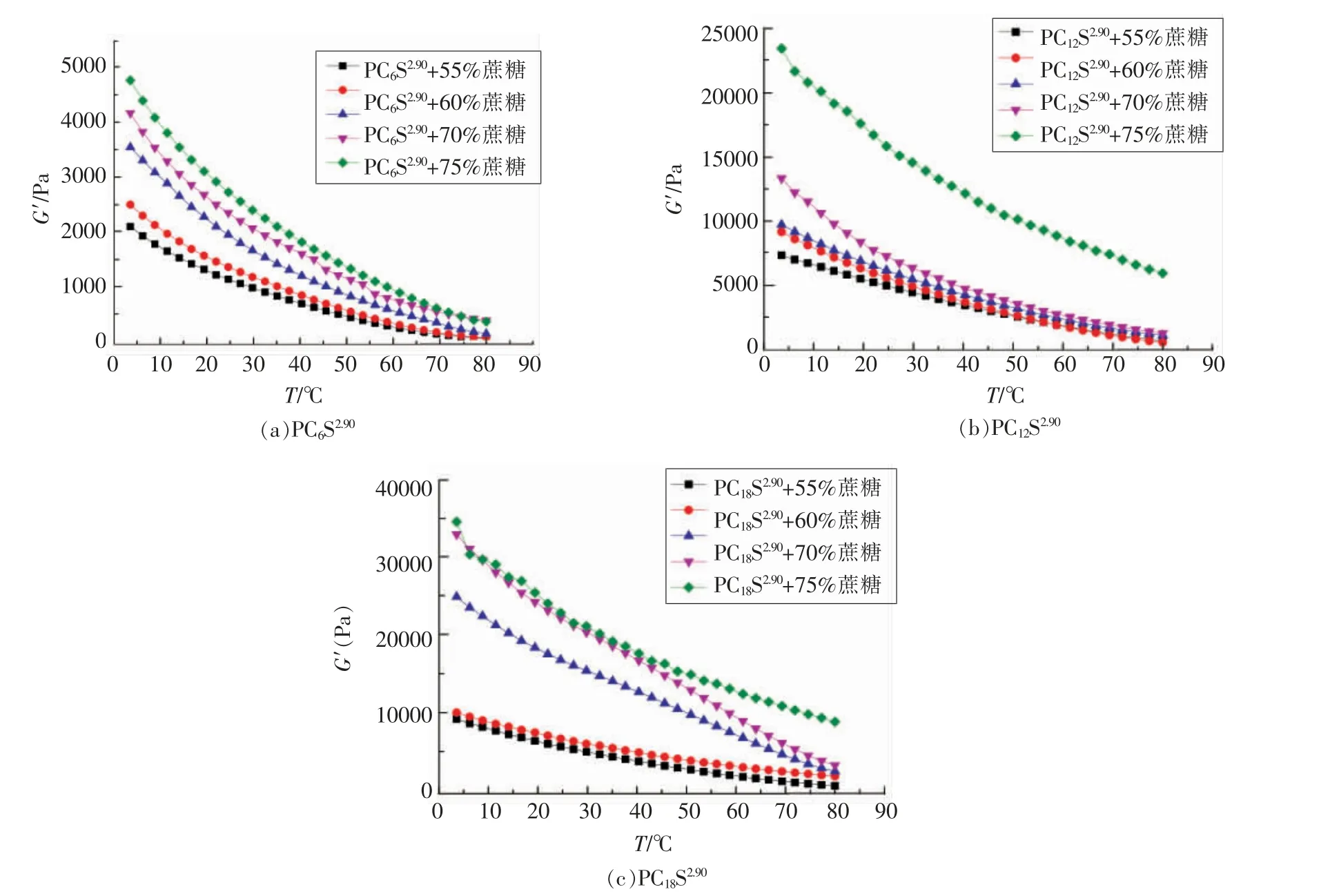
图3 蔗糖含量对烷基化果胶的凝胶储能模量(G′)的影响Fig.3 Effect of sucrose content on the G′ of alkylated pectin gel

图4 蔗糖含量对原果胶及烷基化果胶凝胶强度的影响Fig.4 Effect of sucrose content on the gel strength of original pectin and alkylated pectin
2.3 pH 值对烷基化果胶凝胶性质的影响
高甲氧基果胶只有在适当的酸性条件下才能形成凝胶,因此本文还考察了pH 值对原果胶和烷基化果胶凝胶流变(图5)和质构(图6)性质的影响。结果表明,所有果胶凝胶的G′随pH 值的降低而增加。通常,果胶主链上的羧基以一定量的不带电荷的COOH 和带负电荷的COO-存在于溶液中,果胶分子上的COO-越多,分子间的相互排斥越强,果胶分子间越不容易相互靠近,凝胶就越难形成。适当降低pH 值,果胶分子上带电荷的COO-减少,当带电荷总数降低到某一值的时候,凝胶开始形成,且随着体系pH 值的继续下降凝胶强度增强。质构数据显示,果胶的凝胶强度随着pH 值的降低而增大,这与流变结果一致。当pH 值为3时,原 果 胶,PC6S1.35,PC6S2.90,PC6S4.53,PC12S2.90和PC18S2.90凝 胶 强 度 分 别 为37.0,29.4,48.9,59.7,63.8,77.5 g,即当pH 值一定时,烷基化果胶的凝胶强度随着取代度和链长的增加而增强,且较高取代度和较长链长的烷基化果胶凝胶强度高于原果胶。

图5 pH 值对烷基化果胶的凝胶储能模量(G′)的影响Fig.5 Effect of pH value on the G′ of alkylated pectin gel
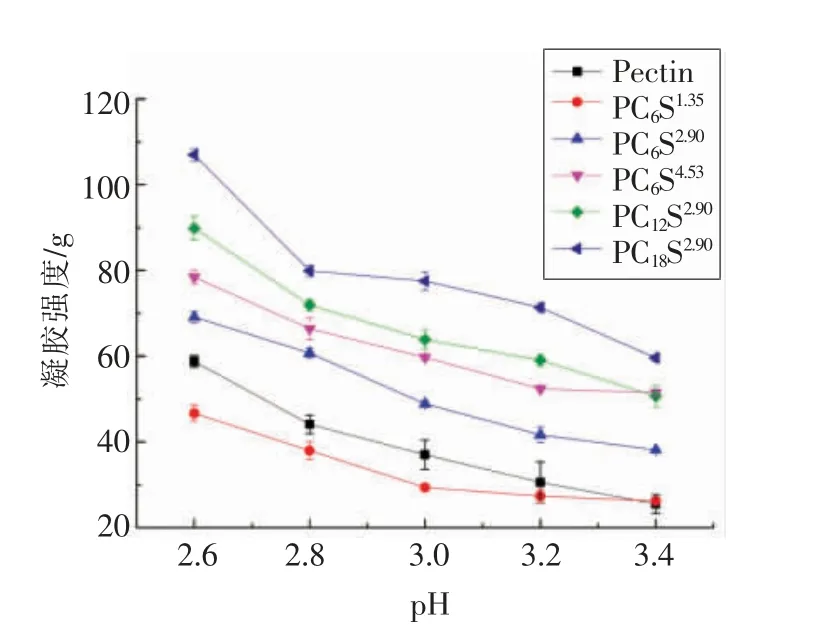
图6 pH 值对原果胶及烷基化果胶凝胶强度的影响Fig.6 Effect of pH value on the gel strength of original pectin and alkylated pectin
2.4 钙离子浓度对烷基化果胶凝胶性质的影响
2.4.1 流变性质及质构特性 研究表明钙离子浓度对高甲氧基果胶的凝胶性质会产生影响,因此本文继续考察了钙离子浓度对原果胶和烷基化果胶凝胶流变(图7)和质构(图8)性质的影响。随着钙离子浓度的增加,所有果胶凝胶的G′增大。这可能是由于钙离子的加入会影响凝胶形成过程中的动力学行为[12],会使未酯化的羧基基团参与到凝胶形成过程中,使凝胶强度增强。质构数据显示,果胶的凝胶强度随着钙离子浓度的增加而增大,这与流变结果一致。当钙离子浓度为0.15%时,原果胶,PC6S1.35,PC6S2.90,PC6S4.53,PC12S2.90和PC18S2.90凝 胶 强度分别为60.6,50.3,61.8,73.7,88.5,111.4 g,即当钙离子浓度一定时,烷基化果胶的凝胶强度随着取代度和链长的增加而增强,且较高取代度和较长链长的烷基化果胶凝胶强度高于原果胶。
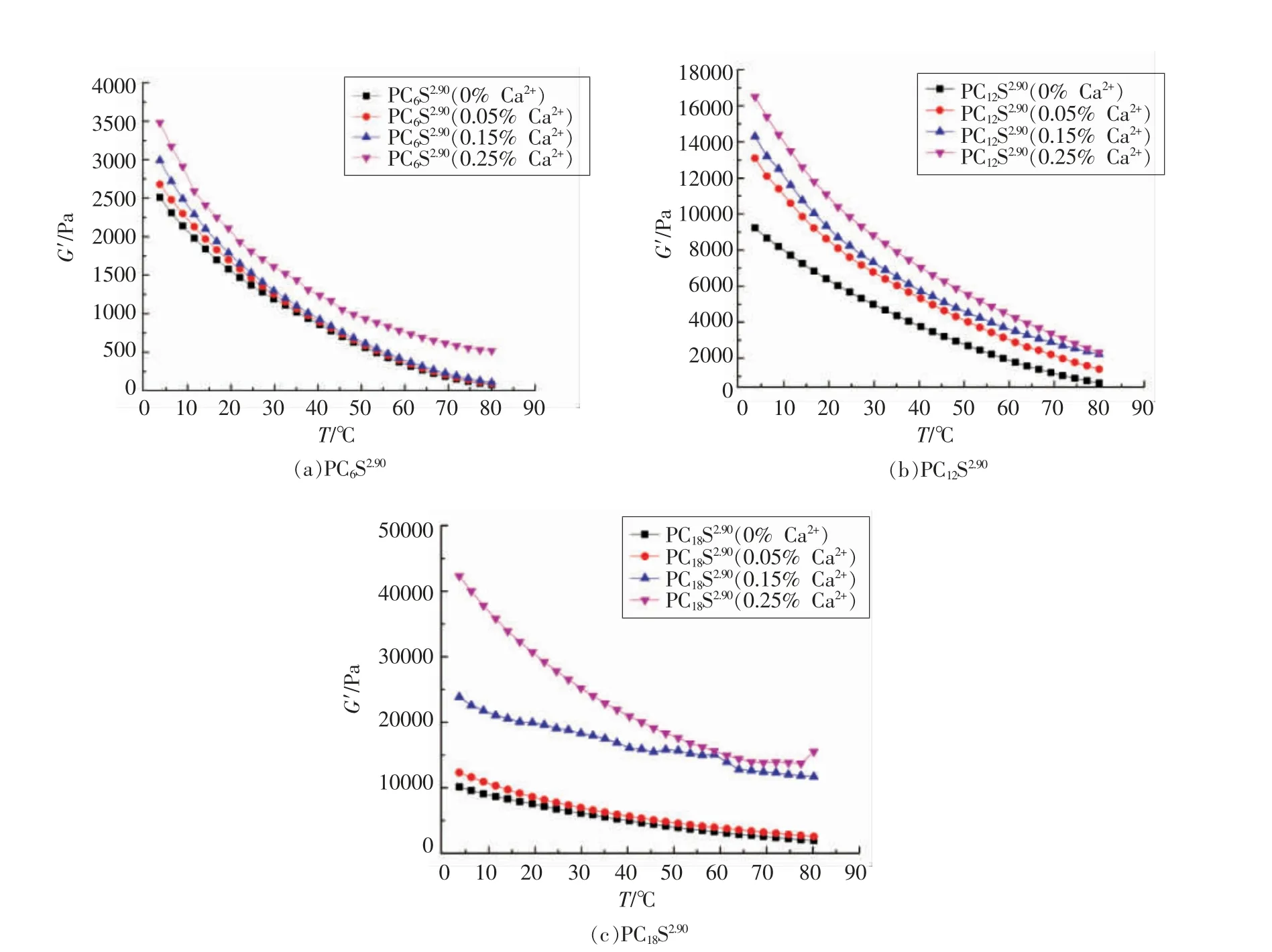
图7 钙离子浓度对烷基化果胶的凝胶储能模量(G′)的影响Fig.7 Effect of Ca2+ content on the G′ of alkylated pectin gel

图8 钙离子浓度对原果胶及烷基化果胶凝胶强度的影响Fig.8 Effect of Ca2+ concentration on the gel strength of original pectin and alkylated pectin
图9显示,在钙离子存在下,频率变化对原果胶及烷基化果胶凝胶体系G′的影响。从图中可以看出,在低频区,G′随着频率的升高而缓慢增加,显示了典型的黏弹性材料的性质[13]。当频率继续增加,出现两种现象:①钙离子浓度较低时,频率增加到一定程度,原果胶以及较低取代度的C6-烷基化果胶(PC6S1.35、PC6S2.90)G′陡然下降,说明这些果胶样品与钙离子配比形成的凝胶体系结构松散,在高频时结构容易被破坏;而最高取代度的C6-烷基化果胶 (PC6S4.53)、C12-及C18-烷基化果胶G′依然继续增加,这可能与这些烷基化果胶样品的取代度和链长有关。最高取代度的C6-烷基化果胶其疏水相互作用较其它两个低取代度的C6-烷基化果胶强,网状结构可能更稳定;C12、C18烷基链的疏水作用更强,且链内连接可能较C6-烷基化果胶更稳定[11],因此在高频区不易被破坏。②当钙离子浓度较高时(0.25%),所有果胶的G′都随频率的升高而增加,说明适当浓度的钙离子可以增强果胶凝胶的网状结构。因此,提高取代度和取代基的碳链长度以及钙离子浓度均可以提高烷基化果胶的凝胶稳定性。
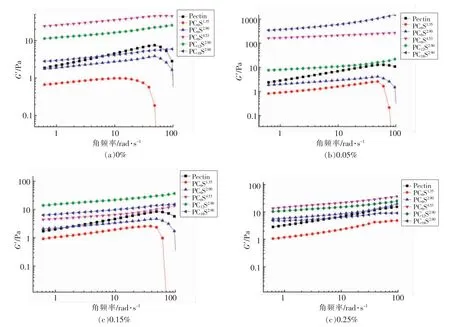
图9 频率对果胶凝胶体系G′的影响Fig.9 Effect of angular frequency on the G′ of pectin gels
2.4.2 FT-IR 分析 以PC12S2.90为例,钙离子浓度对果胶凝胶的红外结构影响如图10 所示。可以把图谱分为3 部分:第1 部分(3 500~1 800 cm-1)范围内出现2 个吸收峰,3 450 cm-1(由O-H 振动吸收引起)和2 950 cm-1(由CH、CH2和CH3引起的C-H 振动);第2 部分(1 800~1 500 cm-1)也出现2个峰,1 740 cm-1(COOCH3及COOH 的振动吸收峰)和1 620 cm-1(COO-的振动吸收峰);第3 部分(低于1 500 cm-1) 为C-C,C-O-C 和C-OH 振动吸收峰。从图10 中可见随着钙离子浓度的增加,1 620 cm-1处COO-的振动吸收峰发生红移并且强度增强。Assifaoui 等[14]也发现与钙离子结合后,果胶COO-的吸收峰向高波数移动且吸收峰强度增强。钙离子可与果胶的羧酸基团络合,改变了果胶官能团之间的相互作用,从而形成更稳定的结构[15],这与果胶凝胶的“蛋盒”结构相符。

图10 PC12S2.90 凝胶的红外光谱图Fig.10 FT-IR spectra of PC12S2.90 gel
3 结论
原果胶及烷基化果胶的凝胶强度随着蔗糖含量及钙离子浓度的增加而增强,随着pH 值的降低而增强。当凝胶条件相同时,烷基化果胶的凝胶强度随着取代度和链长的增加而增强,且较高取代度和较长链长的烷基化果胶凝胶强度高于原果胶。提高取代度、取代基的碳链长度以及钙离子浓度均可以提高烷基化果胶的凝胶稳定性。另外,钙离子浓度的增加会使红外吸收峰红移并使吸收峰强度变大,这可能是由于钙与果胶的羧酸基团发生了络合。
——中核工程创新驱动改革,奋力打造核工程产业链“链长”

