铁催化的N-烷基化反应研究进展
步亚楠
(温州大学化学与材料工程学院,浙江 温州 325035)
含氮化合物在生物活性分子和药物中广泛存在。其中,氮杂环骨架是天然产物和药物(如抗病毒、抗惊厥、抗溃疡、抗炎)中的重要结构单元[1-5](如图 1)。因此,N-烷基化反应是药物分子合成中一类重要的反应。通过N-烷基化直接构建含氮化合物是较为高效的合成策略。传统直接构建C-N 键的烷基化反应有Ullmann-Goldberg 偶联反应、Hoffmann反应和Buchwald Hartwig 反应等[6-8],但是这些反应通常原子经济性较差,反应条件较为苛刻,而且常受限于具有特定官能团的底物(如芳基卤化物)[9,10]。因此,发展新的N-烷基化策略对方法学研究和药物开发设计都具有重要作用,亟待探究。
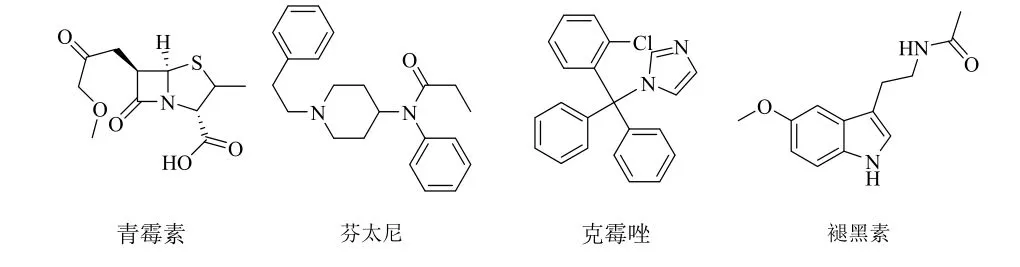
图1 含氮杂环骨架的药物分子
烷基化反应是将烷基从一个化合物转移到另一个化合物上的过程。烷基基团可以通过烷基碳正离子、自由基、碳负离子或卡宾等形式参与反应[11-14],提供烷基基团的化合物被称为烷基化试剂。本文主要讨论了以醇、羧酸等为烷基化试剂,铁催化N-烷基化反应的研究进展。
近年来,常见以贵金属为主的过渡金属配合物催化的N-烷基化反应[15-17]。铁属于廉价金属,作为催化剂具有高效性、低毒性、可回收性等优点,常用于催化各类反应。因此将铁催化应用于N-烷基化反应可以降低反应成本,更加绿色经济,是一类值得引起重视的研究方向。本文主要从以下几方面进行简要综述。
1 伯胺的N-烷基化反应
Qu 等报道了一种由铁催化的,通过借氢策略(Borrowing Hydrogen Transfer)实现的N-烷基化反应[18]。FeCl2与三齿配体配位,通过生成铁的氢化物促进伯醇氧化为相应的醛,然后在碱的作用下与胺生成亚胺中间体,随后亚胺与铁的氢化物通过氢转移得到仲胺。不同取代基的苯胺都能发生反应,均有较好收率(图2)。

图2 铁借借氢策略催化伯芳胺的N-烷基化反应
Saito 等报道了一种利用苄醇作为烷基化试剂,实现芳胺N-烷基化的新策略[19]。与上述报道的常见于过渡金属催化胺与饱和醇烷基化反应的借氢转移策略(BHT)不同,该课题组通过采用不同的醇类进行交叉实验验证反应机理,得到的结果为氘完全转移到了苄基的位置,这与其他过渡金属催化反应的D-H 交换形成对比,从而证明该反应不是以借氢转移策略进行的(图 3)。
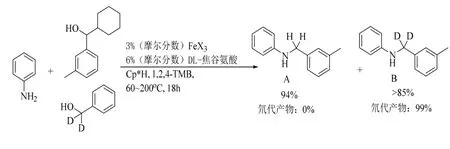
图3 铁/氨基酸催化胺与醇的N-烷基化反应
Liu 课题组报道了一种以Fe(OTf)2作为催化剂,联吡啶为配体的反应体系,催化胺基磺酸酯sp3C-H键的N-烷基化反应。以较好的收率得到了一系列的氮杂噻唑烷[20]。并通过一锅法合成了多巴胺拮抗剂、乙酰胆碱受体激动剂等一系列具有重要生物学意义的氮杂噻唑烷(图4)。
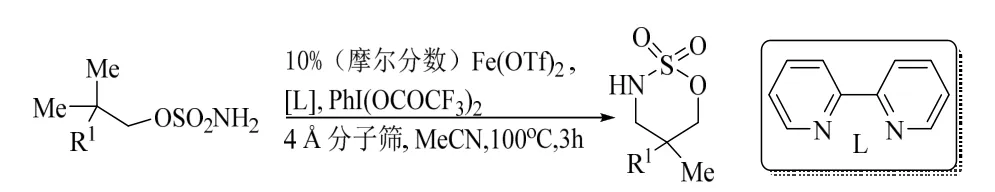
图4 铁催化胺基磺酸酯sp3C-H 键的N-烷基化反应
2 仲胺的N-烷基化反应
Maurya 课题组报道了一种利用FeBr2催化的仲芳胺与醇之间N-烷基化反应的新策略[21],并提出了一种新颖的反应机理:通过碳正离子中间体实现N-烷基化。苄醇在FeBr2和KHSO4的作用下生成醚,该醚在FeBr2的作用下生成瞬时的碳正离子,同时由亲核试剂胺进攻碳正离子,最后得到目标产物。该方法可以兼容伯、仲、杂环胺与芳基、烯丙基和杂环的醇N-烷基化,底物范围广泛(图5)。

图5 铁借碳正离子途径催化仲芳胺的N-烷基化反应
Barta 等报道了一种由铁催化的将苄醇转化为苄胺的重要策略[22]。虽然过渡金属通过借氢策略催化合成胺的报道屡见不鲜,但这是利用铁催化通过借氢策略将苄醇与胺直接偶联得到多种取代的苄基仲、叔胺的首次报道,并且还取得了从中等到优异的收率,值得一提的是该报道还提供了一锅法合成手性叔胺和二醇依次功能化的新策略(图6)。

图6 铁催化苄醇、仲胺制备苄胺的合成策略
Xia 等报道了一种铁催化仲胺的N-烷基化反应[23]。在该反应体系中,使用已商业化生产的三苯基膦为配体,廉价金属铁为催化剂,CO2为烷基化试剂,并且底物范围广泛,收率良好,为仲胺的N-烷基化提供了一种绿色经济可持续发展的合成策略(图7)。

图7 铁催化仲胺的N-甲基化、N-甲酰化反应
He 等报道了一种利用铁催化的以羧酸为烷基试剂、苯基硅烷为还原剂的合成策略,将多种伯、仲芳胺转化为芳基叔胺[24]。该反应由仲胺与羧酸缩合生成中间体酰胺,随后酰胺被还原,将仲芳胺转化为芳基叔胺。但是不排除有少量羧酸被还原为醛,胺与醛反应生成亚胺,亚胺被还原得到叔芳胺。该方法为以各类苯胺为底物制备N-烷基化苯胺提供了一种收率优良,绿色经济的反应策略。(图 8)

图8 铁催化仲胺、羧酸的还原性N-烷基化反应
3 酰胺的N-烷基化反应
3.1 酰胺的N-烷基化反应
Zhao 等报道了一种利用FeCl2作为催化剂、NBS 作为氧化剂的反应体系,用于催化sp3C-H 键的酰胺化反应[25]。该催化体系(FeCl2/NBS)不仅易于制备,而且绿色经济。在FeCl2、NBS 作用下酰胺与金属离子发生质子交换,随后与苄基的C-H 键反应,得到目标产物。反应收率从中等到良好,为sp3C-H 键的酰胺化提供了新策略(图9)。

图9 铁催化sp3C-H 键的酰胺化反应
3.2 磺胺的N-烷基化反应
Deng 等报道了利用FeCl2/K2CO3催化磺胺与苄醇的N-烷基化反应策略[26]。该反应通过借氢策略实现N-烷基化反应,并且通过XPS 分析佐证了Fe(II)和Fe(0)之间可能存在的催化循环。同时考察了底物范围,发现不同官能团的脂肪族磺胺与苄醇反应都能得到优异的收率,且副产物只有水。(图 10)

图10 铁催化磺酰胺与苄醇的N-烷基化反应
4 其他反应
4.1 环胺的N-烷基化反应
Barta 等报道了一种利用铁催化来构建N-取代环胺的新策略[27]。首先通过α-氨基酸脱羧得到N-取代环胺,随后N-取代环胺通过N-烷基化反应得到新的N-取代环胺。该反应体系以脯氨酸为底物,可以兼容各类苯甲醇,以中等至优异的产率合成多种五元和六元N-烷基化杂环(图11)。
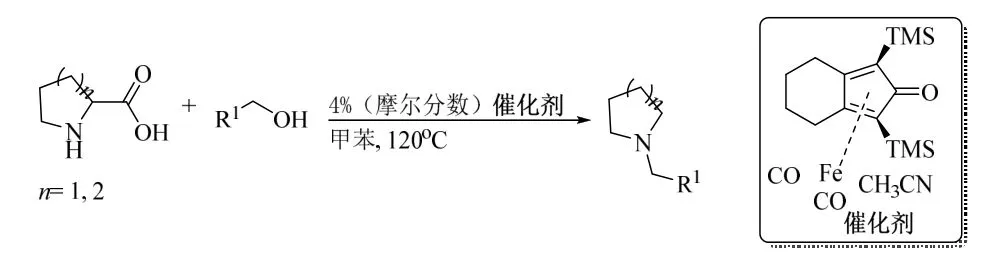
图11 铁催化环状α-氨基酸的脱羧N-烷基化反应
4.2 氨的N-烷基化反应
Shi 等通过设计一种对于空气和湿度稳定的新催化剂NiCuFeOx,为胺或氨与醇的N-烷基化反应提供了一种符合绿色化学要求、具有原子经济性的新策略[28]。在不需要加入碱和有机配体的情况下,共合成了113 个不同结构的伯、仲、叔胺产物,分离收率最高达98%。同时还尝试了吗啉与苄醇的N-烷基化反应,收率可达98%。这个反应还被用于合成一种基于哌嗪结构的用于治疗帕金森氏症的药物——吡喃地尔。该催化剂的主要优点是它可以多次使用而不失活,而且由于它具有磁性,因此很容易从反应介质中分离,便于回收(图12)。

图12 铁催化氨的N-烷基化反应
5 结语
本文主要讨论了铁催化的以醇、羧酸等为烷基化试剂的N-烷基化反应。通过利用铁催化具有低毒性,易获得,易回收,可重复利用等优点,与传统的构成C-N 键的方法相比,本文所论述的这些反应大多数都遵循绿色化学原理,具有较高的原子经济性、广泛的底物范围、较好的官能团耐受性。因此,铁催化N-烷基化反应在构建C-N 键中具有重要作用。

